Реакции ионного обмена. Условия их необратимости
В растворах электролитов реакции протекают между ионами.
Реакции ионного обмена — окислительно-восстановительная реакция, которая идет в направлении связывания ионов, но при которой не происходит изменения степеней окисления.
Условия течения реакций в растворах электролитов до конца:
1) в результате реакции выпадает осадок:
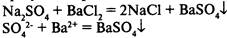
2) в результате реакции выделяется газ:
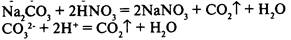
3) в результате реакции образуется малодиссоциирующее вещество:
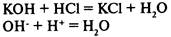
Ионный обмен – это процесс, в результате которого ионы, находящиеся в твердой фазе. обмениваются с ионами, находящимися в растворе. Нерастворимое твердое вещество может представлять собой какой-либо природный материал либо синтетическую смолу. Природные материалы, используемые для ионного обмена, включают цеолиты (комплексные алюмосиликаты натрия) и глауконитовый песок.
На поверхности этих твердых веществ имеются электрически заряженные центры, расположенные на более или менее регулярном расстоянии друг от друга. Эти центры удерживают на себе простые ионы с зарядами противоположного знака. Именно эти ионы обмениваются с другими ионами, содержащимися в растворе.
Катионообменники. Катионообменные материалы состоят из трех частей:
1) основная масса, или скелет, обычно обозначаемый символом R–;
2) активные центры (такие группы, как — 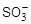 либо —
либо — 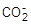 );
);
3) катионы, подлежащие обмену (обычно это ионы Н+ или Н3О+).
Когда твердый катионообменник приходит в соприкосновение с раствором, в котором содержатся какие-либо ионы, между ними устанавливается равновесие. Например,
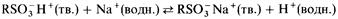
Если первоначально раствор содержит, например, хлорид натрия, то ионы натрия обмениваются с ионами водорода и из нижней части колонки вытекает разбавленный раствор соляной кислоты.
Ионообменный материал можно регенерировать (восстанавливать), промывая колонку разбавленной соляной кислотой. Это приводит к смещению влево рассматриваемого равновесия, в результате чего ионы натрия замещаются ионами водорода.
Анионообменники. Анионообменник удаляет из раствора анионы. Типичным примером анионного обмена является следующее равновесие:
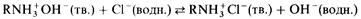
Для регенерации анионообменника может использоваться какое-либо основание, например раствор гидроксида натрия. Это сдвигает указанное равновесие влево.
1. Если образуется осадок (¯) (смотри таблицу растворимости)
Pb(NO3)2 + 2KI ® PbI2¯ + 2KNO3
Pb2+ + 2I- ® PbI2¯
2. Если выделяется газ ()
Na2CO3 + H2SO4 ® Na2SO4 + H2O + CO2
CO32- + 2H+ ® H2O + CO2
3. Если образуется малодиссоциированное вещество (H2O)
Ca(OH)2 + 2HNO3 ® Ca(NO3)2 + 2H2O
H+ + OH- ® H2O
4. Если образуются комплексные соединения (малодиссоциированные комплексные ионы)
CuSO4 • 5H2O + 4NH3 ® [Cu(NH3)4]SO4 + 5H2O
Cu2+ + 4NH3 ® [Cu(NH3)4]2+
В тех случаях, когда нет ионов, которые могут связываться между собой с образованием осадка, газа, малодиссоциированных соединений (H2O) или комплексных ионов реакции обмена обратимы «.
ВОПРОС №32
Важнейшие классы неорганических соединений
К важнейшим классам неорганических соединений относятся оксиды, кислоты, основания и соли.
Оксиды — это сложные вещества, состоящие из двух видов химических элементов, одним из которых является кислород. Оксиды делятся на кислотные (в основном оксиды неметаллов) и основные (оксиды многих металлов). Кислотные оксиды реагируют с щелочами, в результате чего образуется соль. Соли также образуются в результате взаимодействия основного оксида с кислотой.
Основания — это сложные вещества, состоящие из атомов металла и гидроксогрупп (OH). Гидроксогруппа имеет валентность I, поэтому их количество в основании определяется валентностью металла. Например, NaOH — здесь одна гидроксогруппа, так как валентность натрия I. Ca(OH)2 — здесь валентность металла равна II, следовательно, к нему присоединяются две гидроксогруппы.
Основания, которые растворяются в воде, называются щелочами. Их можно получить при взаимодействии металла или его оксида с водой. Щелочи образуют наиболее активные металлы.
Все основания реагируют с кислотами с образованием соли и воды. Эта реакция называется реакцией нейтрализации.
Кислоты — это сложные вещества, состоящие из атомов водорода, которые могут замещаться на металл, и кислотных остатков. Кислотные остатки большинства кислот содержат атомы кислорода и другого какого-либо неметалла. Например, H2SO4, HNO3, H3PO4, H2CO3. Однако есть бескислородные кислоты — HCl, H2S, HBr.
Соли — это сложные вещества, состоящие из атомов металлов и кислотных остатков. Например, NaCl, CaCl2, K2SO4, CuSO4 и т. д. Соли можно рассматривать как результат замещения атомов водорода в кислоте на металл. Соли вступают в реакции обмена с другими солями, растворами кислот и щелочей. Более активный металл вытесняет из соли менее активный.
Из одних классов веществ в результате химических взаимодействий можно получать другие классы. Таким образом, говорят, что классы химических соединений генетически взаимосвязаны между собой.
В химии все многообразие неорганических веществ: принято разделять на две группы – простые и сложные. Простые вещества подразделяются на металлы и неметаллы. А сложные – на производные от простых, образованные путем их взаимодействия с кислородом, водой и между собой. Эту классификацию неорганических веществ в виде схемы изображают следующим образом:
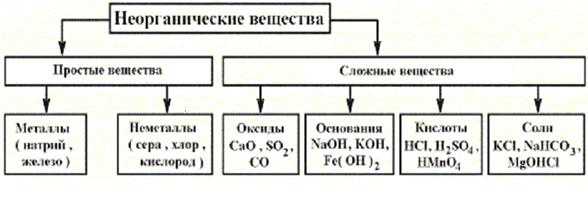
Рис. 2.1. Классификация неорганических соединений.
Классификация реакций в неорганической химии. В неорганической химии различают реакции: 1)соединения, 2)разложения (и те и другие могут быть окислительно-восстановительными реакциями, а могут и не быть таковыми), 3)обмена, 4)замещения, которые всегда являются окислительно-восстановительными. Схемы реакций и примеры даны в таблице 2.1.
Таблица 2.1
Классификация реакций
| Тип реакции | Схема реакции | Примеры реакций |
| Соединение | А +В = АВ | 1) Ca0 + Cl20= Ca2+Cl2- (ОВР) 2) CaO + CO2 = CaCO3 |
| Разложение | АВ = А + В | 1) 2Ag2O = 4Ag +O2 (ОВР) 2) Cu(OH)2 = CuO + H2O |
| Обмен | AB +CD=AD + CB | BaCl2 + Na2SO4 = BaSO4↓ +2NaCl |
| Замещение | AB + C = CB + A | Zn + Pb(NO3)2 = Pb + Zn(NO3)2 (ОВР) |
Рассмотрим получение и свойства наиболее важных классов неорганических соединений.
ОКСИДЫ (окислы) - сложные вещества, состоящие из двух элементов, одним из которых является кислород в степени окисления, равной -2. Общая формула любого оксида - ЭхОу-2. Различают солеобразующие (основные: Li2O, CaO, MgO ,FeO; амфотерные: ZnO, Al2O3, SnO2, Cr2O3, Fe2O3; кислотные: B2O3 , SO3 , CO2, P2O5 Mn2O7) и несолеобразующие: N2O, NO, CO оксиды. Элементы с переменной степенью окисления образуют несколько оксидов (MnO, MnO2, Mn2O7, NO, N2O3, NO2, N2O5). В высшем оксиде, как правило, элемент находится в степени окисления, равной номеру группы.
По современной международной номенклатуре названия оксидов составляют следующим образом: слово «оксид», далее русское название элемента в родительном падеже, степень окисления элемента (если она переменна). Например: FeO – оксид железа (II), P2O5 – оксид фосфора (V).
Основные оксиды это те, которым соответствуют гидроксиды – основания. Основными называют оксиды, взаимодействующие с кислотами с образованием соли и воды. Основные оксиды образуются только металлами в степени окисления +1,+2 (иногда +3), например: BaO, SrO, FeO, MnO, CrO, Li2O, Bi2O3, Ag2O.
Получение основных оксидов:
1) Окисление металлов при нагревании в атмосфере кислорода:
2Mg+O2=2MgO;
2Cu+O2=2CuO.
Свойства основных оксидов. Большинство основных оксидов представляет собой твердые кристаллические вещества ионного характера; в узлах кристаллической решетки расположены ионы металлов, достаточно прочно связанные с ионами O2-, поэтому оксиды типичных металлов обладают высокими температурами плавления и кипения.
Отметим одну характерную для оксидов особенность. Близость ионных радиусов многих ионов металлов приводит к тому, что в кристаллической решетке оксидов часть ионов одного металла может быть заменена на ионы другого металла. Это приводит к тому, что для оксидов часто не выполняется закон постоянства состава, и могут существовать смешанные оксиды переменного состава.
Кислотные оксиды - оксиды, которые при взаимодействии с основаниями образуют соль и воду. Кислотным оксидам соответствуют гидроксиды – кислоты. Кислотные оксиды – это оксиды неметаллов в различных степенях окисления, либо оксиды металлов в высокой степени окисления (+4 и выше). Примеры: SO2, SO3, Cl2O7, Mn2O7, CrO3.
Химическая связь в кислотных оксидах – ковалентная полярная. При обычных условиях кислотные оксиды неметаллов могут быть газообразными (CO2, SO2), жидкими (N2O3, Cl2O7), твердыми (P2O5, SiO2).
Получение кислотных оксидов.
1) Окисление неметаллов:
S+O2=SO2
2) Окисление сульфидов:
2ZnS+3O2=2ZnO+2SO2
Амфотерные оксиды взаимодействуют и с кислотами и со щелочами, проявляя свойства кислотных и основных оксидов. Им соответствуют амфотерные гидроксиды. Все они твердые вещества, нерастворимые в воде. Примеры амфотерных оксидов: ZnO, BeO, SnO, PbO, Al2O3, Cr2O3, Sb2O3, MnO2.
Свойства амфотерных оксидов.
Амфотерные оксиды реагируют с кислотами как основные:
Al2O3+6HCl=2AlCl3+3H2O,
а со щелочами – как кислотные. Состав продуктов реакции зависит от условий. При сплавлении:
ZnO+2NaOH=Na2ZnO2+H2O;
Цинкат натрия
В растворе щелочи образуется растворимая комплексная соль, содержащая гидроксокомплексный ион:
ZnO+2NaOH+H2O=Na2[Zn(OH)4]
Тетрагидроксоцинкат натрия
Несолеобразующие оксиды – это оксиды неметаллов, которым не соответствуют гидроксиды и соли. Примеры: CO, N2O, NO, SiO.
Оксиды широко распространены в природе. Так вода – самый распространенный оксид покрывает 71% поверхности планеты. Оксид кремния (IV) в виде 400 разновидностей кварца составляет 12% от массы земной коры. Оксид углерода (IV) (углекислый газ) содержится в атмосфере - 0,03% по объему, а также в природных водах. Важнейшие руды: гематит, магнетит, бурый железняк состоят из различных оксидов железа. Бокситы содержат оксид алюминия, и т.д.
ОСНОВАНИЯ – сложные вещества, в которых на атом металла приходится одна или несколько гидроксогрупп ОН-. Степень окисления атомов металла обычно +1, +2 (реже +3). Общая формула оснований Ме(ОН)х, где х – число гидроксогрупп – кислотность основания. (МеОН – однокислотное, Ме(ОН)2 – двухкислотное , Ме(ОН)3 – трехкислотное основание).
Названия основаниям дают следующим образом: «гидроксид», затем русское название металла в родительном падеже, а в скобках римскими цифрами – степень окисления, если она переменная. Например: KOH –гидроксид калия, Ni(OH)2 – гидроксид никеля(II).
При обычных условиях основания – твердые вещества, кроме гидроксида аммония – водного раствора аммиака NH4OH (NH4+ - ион аммония, входящий в состав солей аммония).
Классификация оснований. В зависимости от отношения к воде основания делятся на растворимые (щелочи) и нерастворимые. К растворимым основаниям - щелочам относятся только гидроксиды щелочных и щелочноземельных металлов (LiOH, NaOH, KOH, CsOH, RbOH, FrOH, Ca(OH)2, Sr(OH)2, Ba(OH)2, Ra(OH)2) а также водный раствор аммиака. Все остальные основания практически нерастворимы в воде.
С точки зрения теории электролитической диссоциации основания – электролиты, диссоциирующие в водном растворе с образованием в качестве анионов только гидроксид-ионов:
Ме(ОН)х Û Мех+ + хОН-.
Наличие в растворе ионов гидроксида определяют с помощью индикаторов: лакмуса (синий), фенолфталеина (малиновый), метилоранжа (желтый). Нерастворимые основания не меняют окраски индикаторов.
ВОПРОС №33
Классификации:
Все неорганические соединения делятся на две большие группы:
- Простые вещества — состоят из атомов одного элемента;
- Сложные вещества — состоят из атомов двух или более элементов.
Простые вещества по химическим свойствам делятся на:
- металлы
- неметаллы
- амфотерные простые вещества
- благородные газы
Сложные вещества по химическим свойствам делятся на:
- оксиды:
- осно́вные оксиды
- кислотные оксиды
- амфотерные оксиды
- двойные оксиды
- несолеобразующие оксиды
- Гидроксиды;
- основания
- кислоты
- амфотерные гидроксиды
- соли:
- средние соли
- кислые соли
- осно́вные соли
- двойные и/или комплексные соли
бинарные соединения:
- бескислородные кислоты
- бескислородные соли
- прочие бинарные соединения
Неорганические вещества, содержащие углерод:
Данные вещества традиционно относятся к области неорганической химии:
- Карбонаты
- Карбиды
- Цианиды
- Оксиды углерода
- Цианаты
- Неорганические тиоцианаты (роданиды)
- Селеноцианаты
- Карбонилы металлов
Металлы - группа элементов, в виде простых веществ, обладающих характерными металлическими свойствами, такими, как высокие тепло- и электропроводность, положительный температурный коэффициент сопротивления, высокая пластичность и металлический блеск.
Характерные свойства металлов
- Металлический блеск
- Хорошая электропроводность
- Возможность лёгкой механической
- Высокая плотность
- Высокая температура плавления (исключения: ртуть, галлий и щелочные металлы)
- Большая теплопроводность
В реакциях чаще всего являются восстановителями окислительно-восстановительных реакциях в водных растворах.
Неметаллы — химические элементы с типично неметаллическими свойствами, которые занимают правый верхний угол Периодической системы.
Характерной особенностью неметаллов является большее (по сравнению с металлами) число электронов на внешнем энергетическом уровне их атомов. Это определяет их большую способность к присоединению дополнительных электронов, и проявлению более высокой окислительной активности, чем у металлов.
Неметаллы имеют высокие значения сродства к электрону, большую электроотрицательность и высокий окислительно-восстановительный потенциал.
В периодической системе элементов Д.И.Менделеева металлы расположены в левом нижнем углу от диагонали B–At.
В металлах связь металлическая и металлическая кристаллическая решётка чем объясняются физические свойства металлов.
Для главных подгрупп: чем левее и ниже металл, тем большую химическую активность он проявляет. В периодах металлические свойства убывают, а в группах усиливаются (с увеличением порядкового номера), так как изменяется радиус атома.
Для металлов характерны общие физические свойства:
1) твёрдость; 2) электро и теплопровдность; 3) непрозрачность; 4) металлический блеск;
5) ковкость или пластичность (объяснение – металлическая кристаллическая решётка).
ВОПРОС №34
Дата добавления: 2019-07-15; просмотров: 4746; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
