Обратимые и необратимые процессы. Энтропия. Второй закон термодинамики.
1. Обратимым термодинамическим процессом называется термодинамический процесс, допускающий возможность возвращения системы в первоначальное состояние без того, чтобы в окружающей среде остались какие-либо изменения.
Необходимым и достаточным условием обратимости термодинамического процесса является его равновесность.
2. Необратимым термодинамическим процессом называется термодинамический процесс, не допускающий возможности возвращения системы в первоначальное состояние без того, чтобы в окружающей среде остались какие-либо изменения.
Все реальные процессы протекают с конечной скоростью. Они сопровождаются трением, диффузией и теплообменом при конечной разности между температурами системы и внешней среды. Следовательно, все они неравновесны и необратимы.
3. Всякий необратимый процесс в одном направлений (прямом) протекает самопроизвольно, а для осуществления его в обратном направлении так, чтобы система вернулась в первоначальное состояние, требуется компенсирующий процесс во внешних телах, в результате которого состояния этих тел .оказываются отличными от первоначальных. Например, процесс выравнивания температур двух соприкасающихся различно нагретых тел идет самопроизвольно, т. е. не связан с необходимостью одновременного существования каких-либо процессов в других (внешних), телах. Однако для осуществления обратного процесса увеличения разности температур тел до первоначальной нужны компенсирующие процессы во внешних телах, обусловливающие, например, работу холодильной машины.
Второй закон термодинамики связан с понятием энтропии, являющейся мерой хаоса (или мерой порядка). Второй закон термодинамики гласит, что для вселенной в целом энтропия возрастает.
Существует два классических определения второго закона термодинамики :
● Кельвина и Планка
Не существует циклического процесса, который извлекает количество теплоты из резервуара при определенной температуре и полностью превращает эту теплоту в работу. (Невозможно построить периодически действующую машину, которая не производит ничего другого, кроме поднятия груза и охлаждения резервуара теплоты)
● Клаузиуса
Не существует процесса, единственным результатом которого является передача количества теплоты от менее нагретого тела к более нагретому. (Невозможен круговой процесс, единственным результатом которого было бы производство работы за счет охлаждения теплового резервуара)
Энтропия порождается всеми процессами, она связана с потерей системы способности совершать работу. Рост энтропии - стихийный процесс. Если объем и энергия системы постоянны, то любое измение в системе увеличивает энтропию. Если же объем или энергия системы меняются, энтропия системы уменьшается. Однако, энтропия вселенной при этом не уменьшается.
Для того, чтобы энергию можно было использовать, в системе должны быть области с высоким и низким уровнями энергии. Полезная работа производится в результате передачи энергии от области с высоким уровнем энергии к области с низким уровнем энергии.
● 100% энергии не может быть преобразовано в работу
● Энтропия может вырабатываться, но не может быть уничтожена
Энтропия определяется как :
S=H/T
S = энтропия (кДж/кг*К)
H = энтальпия (кДж/кг)
T = абсолютная температура (K)
Изменение энтропии системы вызвано изменением содержания темпла в ней. Изменение энтропии равно изменению темпла системы деленной на среднюю абсолютную температуру ( Ta):
dS = dH / Ta
Тепловые двигатели. Цикл Карно и его КПД для идеального газа
https://tehtab.ru/Guide/GuidePhysics/GuidePhysicsHeatAndTemperature/Thermodynamics/TheSecondLawOfThermodynamics/
Эффективность теплового двигателя: Эффективность теплового двигателя, действующего между двумя энергетическими уровнями , определена в пересчете на абсолютные температуры
η = ( Th - Tc ) / Th = 1 - Tc / Th
η = эффективность
Th = верхняя граница температуры (K)
Tc = нижняя граница температуры (K)
Для того, чтобы достичь максимальной эффективности Tc должна быть настолько низкой, насколько это возможно. Чтобы эффект был 100% -м, Tc должна равнятся 0 по шкале Кельвина. Практически это невозможно, поэтому эффективность всегда меньше 1 (менее 100%).
● Изменение энтропии > 0
Необратимый процесс
● Изменение энтропии= 0
Двусторонний процесс (обратимый)
● Изменение энтропии < 0
Невозможный процесс (неосуществимый)
Энтропия определяет относительную способность одной системы влиять на другую. Когда энергия двигается к нижнему энергетическому уровню, где уменьшается возможность влияния на окружающую среду, энтропия увеличивается.
Определение энтропии
Энтропия определяется как :
S = H / T
S = энтропия (кДж/кг*К)
H = энтальпия (кДж/кг)
T = абсолютная температура (K)
Изменение энтропии системы вызвано изменением содержания темпла в ней. Изменение энтропии равно изменению темпла системы деленной на среднюю абсолютную температуру ( Ta):
dS = dH / Ta
Сумма значений (H / T) для каждого полного цикла Карно равна 0. Это происходит из-за того, что каждому положительному H противостоит отрицательное значение H.
Тепловой цикл Карно
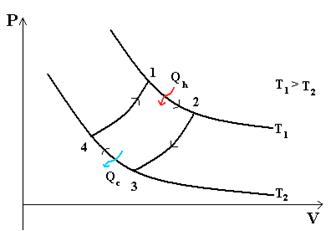
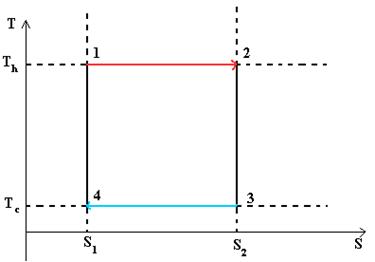
Цикл Карно— идеальный термодинамический цикл.
В тепловом двигателе, газ (реверсивно) нагревается (reversibly heated), а затем охлаждается. Модель цика следующая: Положение 1 --(изотермическое расширение) --> Положение 2 --( адиабатическое расширение) --> Положение 3 --(изотермическое сжатие) --> Положение 4 --(адиабатическое сжатие) --> Положение 1
Дата добавления: 2019-02-22; просмотров: 573; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
