Практичне заняття 9 Зрівнювання рівнянь окисно-відновних реакцій
Мета –сформувати вміння зрівнювати рівняння окисно-відновних реакцій методом електронного балансу.
Підготовка до заняття
| Що необхідно зробити | | Що необхідно знати і вміти | |
| - повторити правила визначення ступеня окиснення елементів у сполуках, типи окисно-відновних реакцій | - визначати окисники та відновники, процеси окиснення та відновлення, складати схеми цих процесів | ||
| - повторити (вивчити) правила методу електронного балансу | - розставляти коефіцієнти в рівняннях окисно-відновних реакцій методом електронного балансу | ||
| - ознайомитися з алгоритмами і прикладами виконання типових завдань; - обдумати відповіді на запропоновані до заняття запитання; - виконати домашні завдання (1 у переліку завдань), переглянути завдання (2-4), які будуть розглядатися під час практичного заняття | - виконувати типові завдання | ||
Запитання до практичного заняття
1 Охарактеризуйте метод електронного балансу.
2 На яких припущеннях ґрунтується метод електронного балансу?
Завдання
1 Розставте коефіцієнти у схемах рівнянь хімічних реакцій методом електронного балансу, визначте тип ОВР:
а)  ;
;
б)  ;
;
в)  ;
;
г) 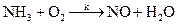 ;
;
д)  ;
;
е)  ;
;
ж)  ;
;
з)  ;
;
и)  ;
;
к)  ;
;
л) 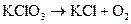 ;
;
м)  ;
;
н)  ;
;
о)  ;
;
п)  ;
;
р)  ;
;
с)  .
.
2 Розставте коефіцієнти у схемах рівнянь хімічних реакцій методом електронного балансу, визначте тип ОВР:
а)  ;
;
б)  ;
;
в) 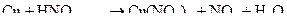 ;
;
г)  ;
;
д)  ;
;
е)  ;
;
ж)  ;
;
з)  ;
;
и)  ;
;
к)  ;
;
л)  ;
;
м)  .
.
3 Розставте коефіцієнти методом електронного балансу у схемах рівнянь хімічних реакцій, в яких три елементи змінюють свій ступінь окиснення:
а)  ;
;
б)  ;
;
в)  ;
;
г)  .
.
4 Розставте коефіцієнти методом електронного балансу у схемах рівнянь хімічних реакцій, в яких беруть участь органічні речовини.
а)  ;
;
б)  ;
;
в) 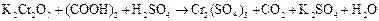 .
.
Практичне заняття 10 Електроліз
Мета – сформувати уявлення про процеси, які відбуваються під час електролізу
Підготовка до заняття
| Що необхідно зробити | | Що необхідно знати і вміти | |
| 1 | 2 | ||
| - вивчити визначення поняття «електроліз»; вивчити правила електролізу (катодного відновлення та анодного окиснення) | - вміти складати схеми катодного та анодного процесів і сумарне рівняння електролізу розплавів лугів та солей, розчинів | ||
| - вивчити закони Фарадея | - знати рівняння, які характеризують закони Фарадея, пояснювати фізичний зміст сталої Фарадея; проводити розрахунки за законом Фарадея | ||
| - ознайомитися з застосуванням електролізу у промисловості | - пояснювати застосування електролізу для добування речовин, отримання гальванічного покриття, електрохімічного захисту металів | ||
| 1 | 2 | ||
| - ознайомитися з алгоритмами і прикладами виконання типових завдань; - обдумати відповіді на запропоновані до заняття запитання; - виконати домашні завдання (1-5 у переліку завдань), переглянути завдання (6-13), які будуть розглядатися під час практичного заняття | - виконувати типові завдання | ||
Дата добавления: 2019-02-13; просмотров: 123; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!


