СИЛЬНЫЕ ЭЛЕКТРОЛИТЫ. ВЫЧИСЛЕНИЕ СТЕПЕНИ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ
Примеры решения задач
Пример 1.
Раствор, содержащий 8г NaOH в 1000 г H2O, кипит при 100,184 ºС. Определите изотонический коэффициент (i) (для воды Kэ=0,516 ºС).
Решение:
Второй закон Рауля для растворов электролитов выражается уравнением
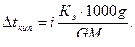 , где g – масса растворенного вещества (г); G - масса растворителя (г); Мr – молекулярная масса растворенного вещества.
, где g – масса растворенного вещества (г); G - масса растворителя (г); Мr – молекулярная масса растворенного вещества.
Молярная масса NaOH равна 40,0. Изотонический коэффициент равен
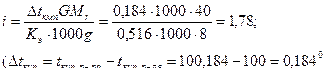
Пример 2. Изотонический коэффициент 0,2 н. раствора нитрата кальция равен 2,48. Вычислите кажущуюся степень диссоциации этого электролита.
Решение:
В случае сильных электролитов кажущуюся степень диссоциации определяют экспериментально, она всегда меньше истинной степени диссоциации, которая близка к единице. Степень диссоциации и изотонический коэффициент электролита связаны между собой соотношением
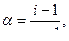
где n- число ионов, образующихся при диссоциации одной молекулы вещества.
При диссоциации Сa(NO3)2 образуется три иона. Кажущаяся степень диссоциации этого электролита равна
 (или 74 %).
(или 74 %).
Пример 3 Давление пара водного раствора NaNO3 (ω=8%) равно 2268,8 Па при 20ºС. Давление паров воды при этой температуре равно 2337,8 Па. Найдите кажущуюся степень диссоциации нитрата натрия в этом растворе.
Решение:
С помощью первого закона Рауля для электролитов 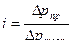 вычисляем значение изотонического коэффициента для NaNO3:
вычисляем значение изотонического коэффициента для NaNO3:
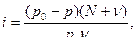 где υ-число молей растворенного вещества; N-число молей растворителя; Р0, Р –давл. паров воды над чистым растворителем и раствором соответственно
где υ-число молей растворенного вещества; N-число молей растворителя; Р0, Р –давл. паров воды над чистым растворителем и раствором соответственно
|
|
|
M (NaNO3) =85,00 г/моль; n= 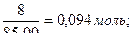
M (H2O)=18,02 г/моль; N= 

Кажущаяся степень диссоциации NaNO3 в этом растворе равна
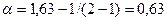 (или 63 %).
(или 63 %).
Пример 4 Вычислить осмотическое давление при 270 С раствора сахара С12Н22О11, один литр которого содержит 91 г растворенного вещества.
Решение:
Росм=См∙RT, где См-молярная концентрация, моль/л; R= 8,31 Дж/моль∙К; Т-температура по Кельвину.
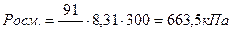
Численное значение R зависит от единиц объема и давления:
Росм кПа; R= 8,31 Дж/моль∙К;
Росм мм Hg ст.; R= 62,32 л∙мм.рт.ст./град. ∙ моль;
Росм. атм.; R= 0,082 л∙атм./град. ∙ моль.
ЗАДАЧИ ДЛЯ САМОСТОЯТЕЛЬНОГО РЕШЕНИЯ
2.1 Степень диссоциации HCl в растворе, содержащем 7,3 г HCl в 200 г воды, равна 78%. Вычислить температуру кипения раствора. Ответ: 100,93ºС.
2.2 Осмотическое давление 0,01 н. раствора KCl при 0ºС равно 0,44 атм. Вычислить степень диссоциации KCl в растворе. Ответ: 96%
2.3 Температура кипения раствора, содержащего 9,09 г KNO3 в 100 г воды, равна 100,80ºС. Вычислить степень диссоциации KNO3 в растворе . Ответ: 70%
2.4 Раствор, содержащий 3,00 г MgCl2 в 125 г воды, замерзает при – 1,23ºС. Вычислить степень диссоциации MgCl2 в растворе. Ответ: 81%
|
|
|
2.5 Осмотическое давление при 0º С раствора, содержащего 0,050 г KNO3 в 100 мл раствора, равно 166,6 мм рт. ст. Вычислить степень диссоциации KNO3 в растворе. Ответ: 95%
2.6 Раствор, содержащий 0,636 г Na2CO3 в120 г воды, замерзает при – 0,225ºС. Вычислить степень диссоциации Na2CO3 в растворе. Ответ: 0,7
2.7 5%-ный раствор KOH кипит при 100,86ºС. Вычислить степень диссоциации KOH в растворе. Ответ: 0,75
2.8 Степень диссоциации MgCl2 в растворе, содержащем 0,25 моль MgCl2 в 1000 г воды, равна 0,84. Во сколько раз понижение температуры замерзания этого раствора больше понижения температуры замерзания эквимолярного раствора неэлектролита? Ответ: 2,68
2.9 Степень диссоциации HCl в 0,02 М растворе равна 0,922. Вычислить осмотическое давление раствора при 0ºС. Ответ: 87,17 Кпа.
2.10 Степень диссоциации HBr в 0,05 н. растворе равна 0,889. Вычислить осмотическое давление раствора при 20ºС. Ответ: 300 кПа.
2.11 Степень диссоциации KCl в растворе, содержащем 0,02 моль KCl в 10л воды, равна 0,969. Вычислить осмотическое давление раствора при 18ºС. Ответ: 9,52 кПа.
2.12 Степень диссоциации K2SO4 в растворе, содержащем 0,026 моль K2SO4 в 50,0 г воды, равна 53%. Вычислить повышение температуры кипения раствора. Ответ: 0,555ºС.
|
|
|
2.13 Степень диссоциации Na2CO3 в растворе, содержащем 0,01 моль Na2CO3 в 200г воды, равна 0,70. Вычислить температуру замерзания раствора. Ответ: - 0,22ºС
2.14 Степень диссоциации CaCl2 в растворе, содержащем 0,666 г CaCl2в 125 г воды, равна 75%. Вычислить температуру замерзания раствора. Ответ: - 0,22ºС
2.15 Раствор KIO3, в 500 мл которого содержится 5,35 г соли, оказывает при 17,5ºС осмотическое давление, равное 2,18 атм.
2.16 В каком объеме раствора должен быть растворен 1 моль сахара, чтобы раствор был изотоничен с 0,1 н. раствором LiCl, кажущаяся степень диссоциации которого в растворе равна 0,9? Ответ: 5,26 л.
2.17 Вычислить молярность раствора некоторого неэлектролита, изотоничного 0,05 н. раствору Pb(NO3)2. Кажущаяся степень диссоциации соли в растворе 0,72. Ответ: 0,061 моль/л.
2.18 Вычислить давление пара 10%-ного раствора Ba(NO3)2 при 28ºС. Давление пара воды при той же температуре составляет 28,35 мм рт. ст. Кажущаяся степень диссоциации соли 0,575. Ответ: 27,89 мм рт. ст.
2.19 Давление пара раствора, содержащего 16,72 Ca(NO3)2 в 250 г воды, составляет 14,28 мм рт. ст. при 17ºС. Вычислить кажущуюся степень диссоциации соли, если известно, что давление пара воды при той же температуре составляет 14,53 мм рт. ст. Ответ: 0,69.
2.20 Давление пара 4%-ного раствора KCl составляет 17,23 мм рт. ст. Вычислить осмотическое давление раствора при 20ºС, если плотность его равна 1,026. Ответ: 23,5 атм.
|
|
|
2.21 Раствор содержащий 33,2 г Ba(NO3)2 в 300 г воды, кипит при 100,466ºС. Вычислить кажущуюся степень диссоциации соли в растворе. Ответ: 0,56
2.22 Раствор KNO3, содержащий 8,44% соли, показывает прирост температуры кипения на 0,797º по сравнению с температурой кипения воды. Вычислить кажущуюся степень диссоциации соли в растворе. Ответ: 0,68
2.23 Кажущаяся степень диссоциации соли в 3,2%-ном растворе KCl составляет 0,68. Вычислить температуру кипения раствора. Ответ: 100,387ºС.
2.24 Давление пара раствора, приготовленного из 0,408 моля Ca(NO3)2 и 1000 г воды, равно 746,9 мм рт. ст. при 100ºС. Вычислить, при какой температуре давление пара раствора достигнет 760 мм рт. ст. и раствор закипит. Ответ: 100,506ºС.
2.25 Раствор содержит 3,38% нитрата кальция, кажущаяся степень диссоциации которого составляет 0,65. Вычислить: а)величину осмотическое давление раствора при 0ºС, приняв плотность его равной 1,01; б)температуру кипения раствора. Ответ: а)10,72 атм; б)100,255ºС.
2.26 Если растворить 55,8 г ZnCl2 в 5кг воды, получится раствор, кристаллизующийся при -0,385ºС. Вычислить кажущуюся степень диссоциации соли в растворе. Ответ: 0,765.
2.27 Вычислить кажущуюся степень диссоциации CaCl2 в растворе, содержащем 0,0995 моля CaCl2 в 500г воды. Температура кристаллизации такого раствора -0,740ºС. Ответ: 0,50.
2.28 Если растворить 25,5 г BaCl2 в 750 г воды, то получится раствор, кристаллизующийся при -0,756ºС. Вычислить кажущуюся степень диссоциации соли в растворе. Ответ: 0,74.
2.29 Какова температура кристаллизации раствора, содержащего 84,9 г NaNO3 в 1000 г воды? Давление пара раствора составляет 17,02 мм рт. ст., а давление пара воды при той же температуре -17,54 мм рт. ст. Ответ: -3,16ºС.
2.30 Вычислить осмотическое давление при 18,5ºС раствора, в 5 л которого содержится 62,4 г CuSO4 · 5H2O. Кажущаяся степень диссоциации соли в растворе 0,38. Ответ: 1,65 атм.
ПРОИЗВЕДЕНИЕ РАСТВОРИМОСТИ
Примеры решения задач
Пример 1. Растворимость гидроксида магния Mg(OH)2 при 18 оС равна
1,7∙10 –4 моль/л. Найти ПР(Mg(OH)2) при этой температуре.
Решение: При растворении каждого моля Mg(OH)2 в раствор переходит 1 моль ионов Mg+2 и 2 моль ионов ОН–.
Mg(OH)2 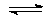 Mg2+ + 2 OH–
Mg2+ + 2 OH–
Следовательно, в насыщенном растворе Mg(OH)2
[Mg2+] = 1,7∙10-4 моль/л; [OH–] = 3,4∙10– 4 моль/л.
Отсюда 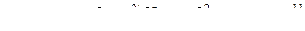 .
.
Пример 2. 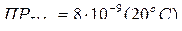 . Вычислить растворимость соли (в моль/л и в г/л) при указанной температуре.
. Вычислить растворимость соли (в моль/л и в г/л) при указанной температуре.
Решение: Обозначим растворимость соли через s (моль/л). Тогда в насыщенном растворе PbI2 cодержится s моль/л ионов Pb2+ и 2s моль/л ионов I–.
PbI2  Pb+2+2I–
Pb+2+2I–
s s 2s
ПР=[Pb2+][I–]2 = 4s3
 ;
; 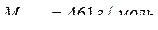 .
.
Растворимость PbI2, выраженная в г/л, (m = ν∙M) составляет 1,3∙10-3∙461 = 0,6 г/л.
Пример 3. Во сколько раз растворимость CaC2O4 в 0,1 М растворе (NH4)2C2O4 меньше, чем в воде?
Решение: Вычислим растворимость CaC2O4 в воде. Пусть концентрация соли в растворе будет s (моль/л), поэтому можем записать

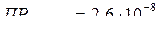
Отсюда,

Найдем растворимость этой соли в 0,1 М растворе (NH4)2C2O4; обозначим её через s′. Концентрация ионов Ca2+ в насыщенном растворе тоже будет s′, а концентрация [C2O42–] составит (0,1+s′), т.к. s′<<0,1, то можно считать, что [C2O42–] = 0,1моль/л. Тогда 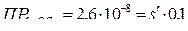 ; s′=2,6∙10–7 моль/л. Следовательно, в присутствии (NH4)2C2O4 растворимость СaC2O4 уменьшилась в
; s′=2,6∙10–7 моль/л. Следовательно, в присутствии (NH4)2C2O4 растворимость СaC2O4 уменьшилась в 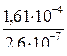 =620 раз.
=620 раз.
Пример 4. Смешаны равные объемы 0,02 н. растворов CaCl2 и Na2SO4; образуется ли осадок CaSO4?
Решение: Найдем произведение концентраций ионов Ca+2 и SO42– и сравним его с  . Условием выпадения осадка является [Ca2+][SO42–] >
. Условием выпадения осадка является [Ca2+][SO42–] > 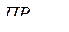 .
.
Исходные молярные концентрации растворов CaCl2 и Na2SO4 одинаковы и равны 0,01 моль/л, т.к. при смешении исходных растворов общий объем раствора вдвое больше, то концентрация каждого из ионов вдвое уменьшается вдвое по сравнению с исходными. [Ca2+] = [SO42–] = 5∙10–3. Находим [Ca2+][SO42–] = 2,5∙10–5
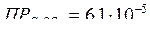
2,5∙10-5 <6,1∙10-5.
Поэтому осадок не образуется.
Дата добавления: 2018-11-24; просмотров: 1153; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
