Характерные химические свойства простых веществ – металлов. Общие способы получения металлов. Коррозия металлов
Примеры заданий
Базовый уровень сложности
1. В порядке усиления металлических свойств химические элементы расположены в ряду
| 1) | Na – K – Cu – Rb | 3) | Al – Mg – Na – Li |
| 2) | Mg – Ca – Sr – Rb | 4) | Ca – K – Rb – Sr |
2. Наиболее активному металлу соответствует электронная конфигурация его атомов
| 1) | 1s22s22p63s1 | 3) | 1s22s22p63s23p1 |
| 2) | 1s22s22p63s2 | 4) | 1s22s22p63s23p64s1 |
3. Восстановительные свойства металлов увеличиваются в ряду
| 1) | Mg – Sr – Ca | 3) | Al – Mg – Be |
| 2) | Na – K – Rb | 4) | Mg – Na – Li |
4. Восстановительные свойства металлов уменьшаются в ряду
| 1) | Cu – K – Na | 3) | Sr – Ca – Mg |
| 2) | Al – Mg – Be | 4) | K – Rb – Sr |
5. С кислородом непосредственно не взаимодействует
| 1) | медь | 2) | ртуть | 3) | барий | 4) | Серебро |
6. Пероксид металла образуется при взаимодействии кислорода с
| 1) | цинком | 2) | литием | 3) | натрием | 4) | Алюминием |
7. В перечне металлов
| А) | Цинк |
| Б) | Ртуть |
| В) | Алюминий |
| Г) | Железо |
| Д) | Медь |
| Е) | Висмут |
водород вытесняют из раствора разбавленной серной кислоты
| 1) | АГЕ | 2) | ВГД | 3) | ВДЕ | 4) | АВГ |
8. Железо окисляется до степени окисления +2 под действием
| 1) | фтора | 2) | хлора | 3) | брома | 4) | Йода |
9. Никель вытесняет металл из раствора соли
| 1) | CoSO4 | 2) | Zn(NO3)2 | 3) | MgSO4 | 4) | CuCl2 |
10. Цинк вытесняет металл из растворов обеих солей, содержащихся в группе
| 1) | хлорид кальция и сульфат марганца (II) |
| 2) | сульфат меди(II) и сульфат алюминия |
| 3) | нитрат кобальта(II) и сульфат магния |
| 4) | нитрат меди (II) и хлорид никеля(II) |
|
|
|
11. Металл можно вытеснить из раствора соли в результате взаимодействия между
| 1) | AlCl3(р-р) и Mg |
| 2) | MnSO4(р-р) и Na |
| 3) | ZnSO4(р-р) и Al |
| 4) | CuSO4(р-р) и Ag |
12. С концентрированной азотной кислотой при комнатной температуре взаимодействует
| 1) | Аl | 2) | Cr | 3) | Au | 4) | Сu |
13. Водород выделяется в результате взаимодействия между
| 1) | соляной кислотой и медью |
| 2) | цинком и раствором гидроксида натрия |
| 3) | серебром и концентрированной серной кислотой |
| 4) | цинком и концентрированной азотной кислотой |
14. И цинк, и алюминий способны вступать во взаимодействие с выделением водорода с
| 1) | концентрированной азотной кислотой |
| 2) | разбавленной азотной кислотой |
| 3) | раствором гидроксида калия |
| 4) | концентрированной серной кислотой |
15. С образованием щелочи с водой взаимодействует
| 1) | железо | 2) | хром | 3) | калий | 4) | Магний |
16. При комнатной температуре медь может вступать во взаимодействие с
| 1) | разбавленным раствором серной кислоты |
| 2) | Азотом |
| 3) | раствором нитрата ртути(II) |
| 4) | раствором гидроксида калия |
|
|
|
17. При комнатной температуре серебро может вступать во взаимодействие с
| 1) | соляной кислотой |
| 2) | азотной кислотой |
| 3) | раствором нитрата меди(II) |
| 4) | раствором гидроксида натрия |
18. Какие из приведенных утверждений о металлах и их свойствах верны?
А. В природе все металлы встречаются в самородном состоянии.
Б. Атомы металлов способны только отдавать валентные электроны.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
19. Коррозия конструкций, изготовленных из сплава железа, будет наибольшей в среде электролита, содержащего
| 1) | кислород в кислой среде при высокой температуре |
| 2) | водород в кислой среде при низкой температуре |
| 3) | кислород в щелочной среде при низкой температуре |
| 4) | водород в щелочной среде при высокой температуре |
20. Коррозия детали, изготовленной из железного сплава, будет наибольшей при помещении ее в воду
| 1) | насыщенную кислородом |
| 2) | насыщенную смесью кислорода и углекислого газа |
| 3) | содержащую уротропин |
| 4) | Дистиллированную |
21. Какие из приведенных утверждений о коррозии металлов верны?
|
|
|
А. Химическая коррозия металлов происходит в не проводящей электрический ток среде.
Б. Для протекторной защиты металлической конструкции от коррозии к ней присоединяют кусок менее активного металла.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
22. Какие из приведенных утверждений о коррозии металлов верны?
А. Важнейшими окислителями в процессеэлектрохимической коррозии являются растворенный кислород и катионы водорода.
Б. Присоединение металлической конструкции к катоду внешнего источника тока исключает возможность ее анодного разрушения.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
23. Какие из приведенных утверждений о коррозии металлов верны?
А. Коррозия является окислительно-восстановительным процессом.
Б. Уменьшению скорости коррозии способствует деаэрация электролита или среды, в которой находится защищаемая металлическая конструкция.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
24. Какие из приведенных утверждений о коррозии металлов верны?
|
|
|
А. При соприкосновении двух металлов электрохимической коррозии подвергается менее активный металл.
Б. Уменьшению скорости коррозии способствует увеличение кислотности внешней среды.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
25. Какие из приведенных утверждений о способах получения металлов верны?
А. Сущность металлургических процессов заключается в восстановлении ионов металла с помощью различных восстановителей.
Б. Щелочные металлы можно получить путем электролиза водных растворов их солей.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
26. Какие из приведенных утверждений о способах получения металлов верны?
А. Для восстановления активных металлов из их оксидов можно использовать водород.
Б. Для очистки некоторых металлов (меди, никеля, свинца) от примесей используют электролиз с растворимым анодом.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
27. Какие из приведенных утверждений о d-элементах верны?
А. Валентные электроны атомов d-элементов находятся на s-орбитали внешнего уровня и d-орбиталях предвнешнего.
Б. Большинство соединений d-элементов окрашено.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
28. Какие из приведенных утверждений о серебре и его соединениях верны?
А. Для серебра наиболее характерна степень окисления +1.
Б. Аммиачный раствор оксида серебра взаимодействует с ацетиленом.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
29. Какие из приведенных утверждений о ртути и ее соединениях верны?
А. Ртуть – единственный жидкий при обычных условиях металл.
Б. Ртуть и ее растворимые соли чрезвычайно ядовиты.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
30. Какие из приведенных утверждений о хроме и его соединениях верны?
А. Электронная конфигурация внешнего и предвнешнего уровней атома хрома 3s23p63d44s2.
Б. Соединения хрома(VI) являются сильными окислителями.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
31. Какие из приведенных утверждений о марганце и его соединениях верны?
А. В соединениях марганец проявляет степени окисления от +2 до +7.
Б. Оксид марганца(VII) и соответствующий ему гидроксид проявляют кислотные свойства.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
32. Какие из приведенных утверждений о железе и его соединениях верны?
А. Для железа наиболее устойчива степень окисления +3.
Б. Соединения железа(II) и железа(III) проявляют окислительно-восстановительную двойственность.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
Повышенный уровень сложности
33. Водород выделяется при взаимодействии
| 1) | цинка и азотной кислоты |
| 2) | магния и соляной кислоты |
| 3) | алюминия и раствора гидроксида натрия |
| 4) | меди и раствора серной кислоты |
| 5) | меди и концентрированной серной кислоты |
| 6) | железа и разбавленной серной кислоты |
34. Водород не выделяется при взаимодействии
| 1) | хрома и разбавленной азотной кислоты |
| 2) | магния и концентрированной серной кислоты |
| 3) | цинка и раствора гидроксида натрия |
| 4) | серебра и азотной кислоты |
| 5) | алюминия и разбавленной серной кислоты |
| 6) | цинка и воды |
35. Вытеснение металла из раствора соли возможно в результате взаимодействия между
| 1) | Na и MgSO4(р-р) |
| 2) | Mg и FeCl2(р-р) |
| 3) | Fe и Zn(NO3)2(р-р) |
| 4) | Cu и AgNO3(р-р) |
| 5) | Ag и CoCl2(р-р) |
| 6) | Zn и NiSO4(р-р) |
36. С образованием щелочи протекают реакции между водой и
| 1) | Цинком | 4) | Магнием |
| 2) | Натрием | 5) | Калием |
| 3) | Барием | 6) | Железом |
37. При комнатной температуре железо не взаимодействует с
| 1) | раствором сульфата меди(II) |
| 2) | соляной кислотой |
| 3) | Серой |
| 4) | концентрированной серной кислотой |
| 5) | водой в присутствии кислорода |
| 6) | концентрированной азотной кислотой |
38. Литий взаимодействует с
| 1) | Азотом | 4) | Толуолом |
| 2) | Водородом | 5) | Кислородом |
| 3) | Метаном | 6) | гексаном |
39. Магний взаимодействует с
| 1) | 1,2-дихлорэтаном | 4) | Пропаном |
| 2) | Хлором | 5) | карбонатом кальция |
| 3) | гидроксидом натрия | 6) | муравьиной кислотой |
40. Хром взаимодействует с
| 1) | гидроксидом меди(II) |
| 2) | разбавленной серной кислотой |
| 3) | соляной кислотой |
| 4) | Этанолом |
| 5) | оксидом алюминия |
| 6) | раствором хлорида меди(II) |
41. Установите соответствие между реагирующими веществами и газообразным продуктом, который выделяется в результате их взаимодействия.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ГАЗООБРАЗНЫЙ ПРОДУКТ | |||||
| А) | Cu + HNO3(конц.) → | 1) | H2 | |||
| Б) | Cu + HNO3(разб.) → | 2) | NO | |||
| В) | Zn + H2SO4(разб.) → | 3) | N2 | |||
| Г) | Ag + H2SO4(конц.) | 4) | NO2 | |||
|
| 5) | H2S | ||||
|
| 6) | SO2 | ||||
| А | Б | В | Г | |||
|
|
|
| ||||
42. Установите соответствие между реагирующими веществами и газообразным продуктом, который выделяется в результате их взаимодействия.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ГАЗООБРАЗНЫЙ ПРОДУКТ | |||||
| А) | Ag + HNO3(конц.) → | 1) | N2 | |||
| Б) | Ag + HNO3(разб.) → | 2) | NO | |||
| В) | Fe + H2SO4(разб.) → | 3) | NO2 | |||
| Г) | Fe + H2SO4(конц.) | 4) 5) 6) | H2 SO2 H2S | |||
|
| ||||||
|
| ||||||
| А | Б | В | Г | |||
|
|
|
| ||||
43. Электролиз водного раствора соли можно использовать для получения
| 1) | Калия | 4) | Кальция |
| 2) | Никеля | 5) | Марганца |
| 3) | Олова | 6) | Алюминия |
44. Установите соответствие между металлом и способом его электролитического получения.
| МЕТАЛЛ | ЭЛЕКТРОЛИЗ | |||||
| А) | Калий | 1) | водного раствора солей | |||
| Б) | Кальций | 2) | расплава галогенида | |||
| В) | Серебро | 3) | водного раствора гидроксида | |||
| Г) | Кадмий | 4) | расплава нитрата | |||
|
| 5) | раствора глинозема в расплавленном криолите | ||||
| А | Б | В | Г | |||
|
|
| |||||
45. Установите соответствие между металлом и способом его электролитического получения.
| МЕТАЛЛ | ЭЛЕКТРОЛИЗ | |||||
| А) | Натрий | 1) | водного раствора солей | |||
| Б) | Медь | 2) | расплава поваренной соли | |||
| В) | Алюминий | 3) | водного раствора гидроксида | |||
| Г) | Никель | 4) | расплава нитрата | |||
|
| 5) | раствора глинозема в расплавленном криолите | ||||
| А | Б | В | Г | |||
|
|
| |||||
46. Железо массой 11,2 г полностью прореагировало с избытком соляной кислоты. Объем (н.у.) газа, выделившегося в результате реакции, составил _________ л. (Запишите число с точностью до сотых.)
47. Натрий массой 0,92 г полностью прореагировал с водой. Объем (н.у.) газа, выделившегося в результате реакции, составил _________ л. (Запишите число с точностью до тысячных.)
48. Сплав цинка и меди массой 10 г обработали избытком соляной кислоты. В результате реакции выделилось 2,24 л (н.у.) газа. Массовая доля меди в сплаве равна _________ %. (Запишите число с точностью до целых.)
49. Смесь железной и медной стружки массой 15 г обработали избытком концентрированной азотной кислоты на холоду. В результате реакции выделилось 6,72 л (н.у.) газа. Массовая доля железа в смеси равна _________ %. (Запишите число с точностью до целых.)
50. Смесь алюминиевой и медной стружки массой 20 г обработали избытком раствора щелочи. В результате реакции выделилось 6,72 л (н.у.) газа. Массовая доля меди в смеси равна _________ %. (Запишите число с точностью до целых.)
51. Сплав магния и цинка массой 8,9 г обработали избытком соляной кислоты. В результате реакции выделилось 4,48 л (н.у.) газа. Массовая доля цинка в сплаве равна _________ %. (Запишите число с точностью до целых.)
52. Железную пластинку массой 10 г поместили в раствор сульфата меди(II). После окончания реакции масса пластинки составила 10,8 г. Масса железа, вступившего в реакцию, равна _________ г. (Запишите число с точностью до десятых.)
53. Цинковую пластинку массой 15 г поместили в раствор сульфата железа(II). После окончания реакции масса пластинки составила 13,2 г. Масса железа, выделившегося на пластинке, равна _________ г. (Запишите число с точностью до десятых.)
54. Медную пластинку массой 20 г поместили в раствор нитрата серебра. После окончания реакции масса пластинки составила 21,52 г. Масса нитрата серебра, вступившего в реакцию, равна _________ г. (Запишите число с точностью до десятых.)
55. Алюминиевую пластинку массой 12 г поместили в раствор сульфата цинка. После окончания реакции масса пластинки составила 13,41 г. Масса образовавшегося в результате реакции сульфата алюминия равна _________ г. (Запишите число с точностью до десятых.)
Высокий уровень сложности
56. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
NaCl → Na 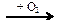 X1
X1 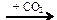 X2
X2 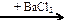 X3 → NaOH
X3 → NaOH
Укажите условия протекания реакций.
57. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Са 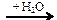 X1
X1  X2 → CaCO3 → CaO
X2 → CaCO3 → CaO  X3
X3
Укажите условия протекания реакций.
58. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Al2O3 → Al 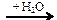 X1
X1 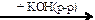 X2
X2 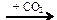 X1
X1 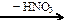 X3
X3
Укажите условия протекания реакций.
59. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Ag → AgNO3 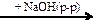 X1
X1 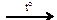 X2 → X1
X2 → X1  X3
X3
Укажите условия протекания реакций.
60. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Fe  X1
X1 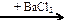 X2
X2  X3
X3 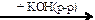 X4
X4 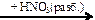 X5
X5
Укажите условия протекания реакций.
61. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Cr 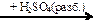 X1
X1 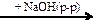 X2
X2  X3
X3  X4
X4 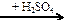 X5
X5
Укажите условия протекания реакций.
Вариант 1
1. В порядке уменьшения металлических свойств простые вещества-металлы расположены в ряду
| 1) | Mg – Be – Li | 3) | Cs – Rb – Sr |
| 2) | Sc – Rb – K | 4) | Li – Na – K |
2. Между собой не взаимодействуют
| 1) | Zn и H2O | 3) | Ag и O2 |
| 2) | Mg и HCl | 4) | Fe и AgNO3 (р-р) |
3. Железо вытесняет металл из растворов обеих солей, содержащихся в группе
| 1) | нитрат цинка и сульфат никеля(II) |
| 2) | сульфат меди(II) и нитрат серебра |
| 3) | нитрат марганца(II) и сульфат алюминия |
| 4) | хлорид магния и хлорид кобальта(II) |
4. Водород выделяется в результате взаимодействия между
| 1) | Al и HNO3(конц.) |
| 2) | Al и H2SO4(конц.) |
| 3) | Al и HNO3(разб.) |
| 4) | Al и H2SO4(разб.) |
5. И медь, и цинк способны вступать во взаимодействие с
| 1) | соляной кислотой |
| 2) | разбавленной серной кислотой |
| 3) | раствором гидроксида калия |
| 4) | концентрированной серной кислотой |
6. Без нагревания с водой взаимодействует
| 1) | натрий | 2) | марганец | 3) | хром | 4) | Олово |
7. Медь может вступать во взаимодействие с водным раствором
| 1) | гидроксида натрия | 3) | серной кислоты |
| 2) | хлорида цинка | 4) | нитрата серебра |
8. Какие из приведенных утверждений о металлах и их свойствах верны?
А. Все металлы при комнатной температуре находятся в твердом агрегатном состоянии.
Б. Металлы в химических реакциях могут быть как окислителями, так и восстановителями.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
9. Скорость коррозии железа будет наибольшей при его контакте с
| 1) | алюминием | 2) | Хромом | 3) | кобальтом | 4) | Медью |
10. Какие из приведенных утверждений о щелочных металлах верны?
А. Щелочные металлы проявляют во всех соединениях степень окисления +1.
Б. Щелочные металлы получают путем электролиза растворов их хлоридов.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
11. Какие из приведенных утверждений о меди верны?
А. Электронная конфигурация внешнего уровня атома меди в невозбужденном состоянии 4s2.
Б. Медь взаимодействует как с разбавленной, так и с концентрированной серной кислотой.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
12. Натрий взаимодействует с
| 1) | Бензолом | 4) | Ацетиленом |
| 2) | Этаном | 5) | Бромом |
| 3) | Этанолом | 6) | гидроксидом калия |
13. Цинк взаимодействует с
| 1) | раствором гидроксида натрия | 4) | Кислородом |
| 2) | Толуолом | 5) | оксидом алюминия |
| 3) | 1,2-дибромпропаном | 6) | сульфатом калия |
14. Установите соответствие между реагирующими веществами и газообразным продуктом, который выделяется в результате их взаимодействия.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ГАЗООБРАЗНЫЙ ПРОДУКТ | |||||
| А) | Na + H2O → | 1) | N2O | |||
| Б) | Zn + NaOH + H2O → | 2) | NO2 | |||
| В) | Mg + H2SO4(разб.) → | 3) | N2 | |||
| Г) | Сu + HNO3(конц.) → | 4) | SO2 | |||
|
| 5) | H2 | ||||
|
| 6) | О2 | ||||
| А | Б | В | Г | |||
|
|
|
| ||||
15. Установите соответствие между металлом и способом его электролитического получения.
| МЕТАЛЛ | ЭЛЕКТРОЛИЗ | |||||
| А) | Ртуть | 1) | водного раствора солей | |||
| Б) | Алюминий | 2) | расплава хлорида | |||
| В) | Литий | 3) | водного раствора гидроксида | |||
| Г) | Железо | 4) | расплава нитрата | |||
|
| 5) | раствора глинозема в расплавленном криолите | ||||
| А | Б | В | Г | |||
|
|
| |||||
16. Серебро массой 5,4 г полностью растворили в концентрированной азотной кислоте. Объем (н.у.) газа, выделившегося в результате реакции, составил _________ л. (Запишите число с точностью до сотых.)
17. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Zn → Zn(NO3)2 → Zn(OH)2 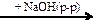 X1
X1 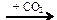 X2
X2 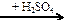 X3
X3
Укажите условия протекания реакций.
Вариант 2
1. Наименее активному металлу соответствует электронная конфигурация его атомов
| 1) | 1s22s22p63s23p64s2 | 3) | 1s22s22p63s2 |
| 2) | 1s22s22p63s1 | 4) | 1s22s22p63s23p1 |
2. С соляной кислотой взаимодействует каждый из трех металлов группы
| 1) | цинк, магний, серебро |
| 2) | железо, марганец, никель |
| 3) | алюминий, хром, медь |
| 4) | магний, висмут, ртуть |
3. Хром вытесняет металл из растворов обеих солей, содержащихся в группе
| 1) | хлорид меди(II) и нитрат никеля(II) |
| 2) | нитрат железа(II) и хлорид магния |
| 3) | сульфат марганца(II) и сульфат натрия |
| 4) | хлорид цинка и хлорид бария |
4. Водород выделяется в результате взаимодействия между
| 1) | Mg и HNO3(конц.) |
| 2) | Cu и H2SO4(конц.) |
| 3) | Zn и HNO3(разб.) |
| 4) | Fe и H2SO4(разб.) |
5. И медь, и серебро способны реагировать с
| 1) | соляной кислотой |
| 2) | разбавленной серной кислотой |
| 3) | раствором нитрата железа(II) |
| 4) | концентрированной азотной кислотой |
6. Продуктами взаимодействия натрия с водой являются
| 1) | Na2O и H2 | 3) | NaOH и H2 |
| 2) | NaH и O2 | 4) | NaOH и O2 |
7. Железо окисляется до степени окисления +2 под действием
| 1) | фтора | 2) | Хлора | 3) | брома | 4) | Серы |
8. Какие из приведенных утверждений о металлах и их свойствах верны?
А. Металлы характеризуются низкими значениями электроотрицательности.
Б. Все металлы взаимодействуют с кислородом при комнатной температуре.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
9. Для защиты железных конструкций от коррозии на ней следует укрепить пластинку из
| 1) | цинка | 2) | Никеля | 3) | олова | 4) | Меди |
10. Какие из приведенных утверждений об алюминии и его соединениях верны?
А. Алюминий проявляет сильные восстановительные свойства.
Б. Оксид и гидроксид алюминия обладают амфотерными свойствами.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
11. Какие из приведенных утверждений о цинке и его соединениях верны?
А. Цинк встречается в природе в самородном состоянии.
Б. Оксид и гидроксид цинка обладают амфотерными свойствами.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
12. Калий взаимодействует с
| 1) | Бензолом | 4) | Бутаном |
| 2) | Хлорэтаном | 5) | гидроксидом натрия |
| 3) | Фенолом | 6) | Серой |
13. Медь взаимодействует с
| 1) | Кислородом |
| 2) | разбавленной серной кислотой |
| 3) | разбавленной азотной кислотой |
| 4) | Водой |
| 5) | Хлором |
| 6) | гидроксидом кальция |
14. Установите соответствие между реагирующими веществами и газообразным продуктом, который выделяется в результате их взаимодействия.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ГАЗООБРАЗНЫЙ ПРОДУКТ | |||||
| А) | Вa + H2O → | 1) | Cl2 | |||
| Б) | Al + KOH + H2O → | 2) | О2 | |||
| В) | Cu + HNO3(разб.) → | 3) | N2 | |||
| Г) | Ag + HNO3(конц.) → | 4) | NO | |||
|
| 5) | NO2 | ||||
|
| 6) | H2 | ||||
| А | Б | В | Г | |||
|
|
|
| ||||
15. Установите соответствие между металлом и способом его электролитического получения.
| МЕТАЛЛ | ЭЛЕКТРОЛИЗ | |||||
| А) | Барий | 1) | водного раствора гидроксида | |||
| Б) | Серебро | 2) | водного раствора солей | |||
| В) | Цезий | 3) | расплава нитрата | |||
| Г) | Хром | 4) | расплава галогенидов | |||
|
| 5) | раствора глинозема в расплавленном криолите | ||||
| А | Б | В | Г | |||
|
|
| |||||
16. При полном растворении меди в разбавленной азотной кислоте выделилось 4,48 л газа (н.у.). Масса меди, вступившей в реакцию, равна _________ г. (Запишите число с точностью до десятых.)
17. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Fe  X1
X1  X2
X2 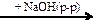 X3
X3 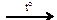 X4 → Fe
X4 → Fe
Укажите условия протекания реакций.
Дата добавления: 2018-11-24; просмотров: 3694; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!