Характерные химические свойства простых веществ – неметаллов. Водородные соединения неметаллов. Характерные химические свойства оксидов неметаллов и соответствующих им гидроксидов
Примеры заданий
Базовый уровень сложности
1. Аллотропия характерна для
| 1) | кислорода | 2) | фтора | 3) | азота | 4) | водорода |
2. Аллотропия не характерна для
| 1) | углерода | 2) | азота | 3) | кислорода | 4) | серы |
3. Молекулярную кристаллическую решетку имеет
| 1) | графит | 2) | кремний | 3) | бор | 4) | йод |
4. Атомную кристаллическую решетку имеет
| 1) | кислород | 3) | белый фосфор |
| 2) | алмаз | 4) | бром |
5. Окислительные свойства наиболее ярко выражены у
| 1) | F2 | 2) | Сl2 | 3) | Br2 | 4) | I2 |
6. Восстановительные свойства наиболее ярко выражены у
| 1) | хлора | 2) | серы | 3) | фосфора | 4) | углерода |
7. Окислительные свойства сера проявляет при взаимодействии с
| 1) | кислородом | 2) | хлором | 3) | фтором | 4) | водородом |
8. Окислительные свойства углерод проявляет при взаимодействии с
| 1) | кислородом | 2) | водородом | 3) | серой | 4) | фтором |
9. Окислительные свойства углерод проявляет при взаимодействии с
| 1) | оксидом алюминия | 3) | азотной кислотой |
| 2) | углекислым газом | 4) | кальцием |
10. Окислительные свойства кремний проявляет при взаимодействии с
| 1) | кислородом | 2) | углеродом | 3) | магнием | 4) | азотом |
11. Окислительные свойства фосфор проявляет при взаимодействии с
| 1) | хлором | 2) | кислородом | 3) | серой | 4) | магнием |
12. Окислительные свойства водород проявляет при взаимодействии с
|
|
|
| 1) | бромом | 2) | кислородом | 3) | углеродом | 4) | калием |
13. Восстановительные свойства водород проявляет при взаимодействии с
| 1) | оксидом меди (II) | 3) | алюминием |
| 2) | натрием | 4) | кальцием |
14. Восстановительные свойства сера проявляет при взаимодействии с
| 1) | кислородом | 2) | водородом | 3) | натрием | 4) | углеродом |
15. Восстановительные свойства углерод проявляет при взаимодействии с
| 1) | водородом | 2) | кислородом | 3) | кремнием | 4) | кальцием |
16. Восстановительные свойства азот проявляет при взаимодействии с
| 1) | кислородом | 2) | водородом | 3) | магнием | 4) | углеродом |
17. И углерод, и сера проявляют окислительные свойства при взаимодействии с
| 1) | кислородом | 3) | фтором |
| 2) | водородом | 4) | азотной кислотой |
18. Восстановительные свойства не способен проявлять
| 1) | фтор | 2) | водород | 3) | азот | 4) | углерод |
19. При комнатной температуре азот реагирует с
| 1) | кислородом | 3) | кальцием |
| 2) | литием | 4) | водородом |
20. При комнатной температуре сера реагирует с
| 1) | кислородом |
| 2) | водородом |
| 3) | концентрированной азотной кислотой |
| 4) | ртутью |
|
|
|
21. Фосфор образует соединения, в которых его степень окисления равна – 3, при взаимодействии с каждым из двух веществ
| 1) | хлором и концентрированной серной кислотой |
| 2) | кальцием и натрием |
| 3) | концентрированной азотной кислотой и серой |
| 4) | магнием и кислородом |
22. Йод образует соединения, в которых его степень окисления равна – 1, при взаимодействии с каждым из двух веществ
| 1) | водородом и хлорной кислотой |
| 2) | алюминием и азотной кислотой |
| 3) | кальцием и сероводородом |
| 4) | хлором и магнием |
23. Какие из приведенных утверждений о галогенах верны?
А. Электронная конфигурация внешнего электронного уровня атомов галогенов ns2np5.
Б. С щелочными металлами галогены образуют соединения с ионным типом связи.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
24. Какие из приведенных утверждений о фторе верны?
А. Высшая степень окисления фтора равна + 7.
Б. В химических реакциях фтор может проявлять только окислительные свойства.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
25. Какие из приведенных утверждений о сере и ее свойствах верны?
|
|
|
А. На внешнем электроном уровне атома серы в невозбужденном состоянии содержится два неспаренных электрона.
Б. В реакциях с металлами сера проявляет окислительные свойства.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
26. Какие из приведенных утверждений об азоте и его свойствах верны?
А. Высшая валентность азота равна V.
Б. Азот образует очень прочную, достаточно инертную двухатомную молекулу.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
27. Какие из приведенных утверждений о фосфоре и его свойствах верны?
А. Белый фосфор образует молекулярную кристаллическую решетку.
Б. Наиболее устойчивая степень окисления фосфора равна + 5.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
28. Какие из приведенных утверждений об углероде и его свойствах верны?
А. Углерод образует несколько простых веществ.
Б. Для углерода наиболее характерны окислительные свойства.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
|
|
|
29. Какие из приведенных утверждений о кремнии и его свойствах верны?
А. Кристаллическая решетка кремния подобна кристаллической решетке алмаза.
Б. Кремний широко используется в полупроводниковой технике.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
30. Наиболее слабой кислотой является
| 1) | HF | 2) | HCl | 3) | HBr | 4) | HI |
31. Восстановительные свойства не проявляет
| 1) | HF | 2) | HCl | 3) | HBr | 4) | HI |
32. Наиболее сильные окислительные свойства проявляет
| 1) | HClO | 2) | HClO2 | 3) | HClO3 | 4) | HClO4 |
33. Наиболее сильные кислотные свойства проявляет
| 1) | HClO | 2) | HClO2 | 3) | HСlO3 | 4) | HClO4 |
34. Наиболее слабые кислотные свойства проявляет
| 1) | H3РO4 | 2) | H3AsO4 | 3) | H2SeO4 | 4) | HClO4 |
35. C водой не взаимодействует
| 1) | CO2 | 2) | SO2 | 3) | SeO2 | 4) | SiO2 |
36. Оксид кремния(IV) не взаимодействует с
| 1) | oксидом серы(VI) | 3) | гидроксидом натрия |
| 2) | углеродом | 4) | плавиковой кислотой |
37. Между собой взаимодействуют
| 1) | SO2 и H2S | 3) | P2O5 и HNO3 |
| 2) | CO2 и SO3 | 4) | SiO2 и H2O |
38. Между собой не взаимодействуют
| 1) | N2O5 и H2SO4 | 3) | P2O5 и KOH |
| 2) | CO2 и СaO | 4) | SO2 и H2O |
39. Оксид серы (VI) взаимодействует с каждым из трех веществ
| 1) | H2O, CO2, NaOH |
| 2) | H2O, MgO, HNO3 |
| 3) | CaO, KOH, H2O |
| 4) | Ca(OH)2, SiO2, BaO |
40. Oксид фосфора(V) взаимодействует с каждым из двух веществ
| 1) | серной кислотой и гидроксидом кальция |
| 2) | водой и оксидом натрия |
| 3) | оксидом серы(VI) и оксидом кальция |
| 4) | азотной кислотой и углекислым газом |
41. И с оксидом кремния(IV), и с оксидом серы(VI) взаимодействует каждое из трех веществ
| 1) | H2O, Li2O, NaOH |
| 2) | CO2, CaO, H2SO4 |
| 3) | Na2O, KOH, СаO |
| 4) | HNO3, P2O5, BaO |
42. Между собой взаимодействуют
| 1) | H2SO4 и P2O5 | 3) | H2SO4 и H2CO3 |
| 2) | конц. H2SO4 и Au | 4) | конц. H2SO4 и H2S |
43. Соляная кислота взаимодействует с
| 1) | NaHCO3 | 2) | Ag | 3) | SiO2 | 4) | H2S |
44. Соляная кислота не взаимодействует с
| 1) | Zn | 2) | Au | 3) | K2SO3 | 4) | FeS |
45. Азотная кислота не взаимодействует с
| 1) | H2S | 2) | Pt | 3) | Ag | 4) | CaСO3 |
Повышенный уровень сложности
46. Оксид кремния(IV) взаимодействует с
| 1) | углеродом |
| 2) | соляной кислотой |
| 3) | плавиковой кислотой |
| 4) | oксидом азота(V) |
| 5) | карбонатом кальция |
| 6) | кислородом |
47. Оксид серы(IV) взаимодействует с
| 1) | сероводородом |
| 2) | концентрированной серной кислотой |
| 3) | кислородом |
| 4) | азотом |
| 5) | азотной кислотой |
| 6) | оксидом углерода(IV) |
48. Оксид фосфора(V) взаимодействует с
| 1) | водой |
| 2) | оксидом кремния (IV) |
| 3) | углекислым газом |
| 4) | раствором гидроксида калия |
| 5) | оксидом магния |
| 6) | кислородом |
49. Оксид серы(VI) взаимодействует с
| 1) | кислородом |
| 2) | водой |
| 3) | углекислым газом |
| 4) | гидроксидом натрия |
| 5) | оксидом кальция |
| 6) | азотной кислотой |
50. Плавиковая (фтороводородная) кислота взаимодействует с
| 1) | сульфатом натрия |
| 2) | кислородом |
| 3) | oксидом кремния(IV) |
| 4) | гидроксидом кальция |
| 5) | оксидом бария |
| 6) | ортофосфорной кислотой |
51. Аммиак взаимодействует с
| 1) | азотной кислотой |
| 2) | водородом |
| 3) | медью |
| 4) | оксидом меди(II) |
| 5) | гидроксидом меди(II) |
| 6) | гидроксидом калия |
52. Установите соответствие между реагирующими веществами и продуктами их взаимодействия.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ПРОДУКТЫ ВЗАИМОДЕЙСТВИЯ | |||||
| А) | CO2(избыт.) + Ca(OH)2 → | 1) | СаСО3 | |||
| Б) | CO2 + Ca(ОH)2(избыт.) → | 2) | СаСО3 + H2 | |||
| В) | CO2 + CaO → | 3) | СаСО3 + H2O | |||
| Г) | СО2 + СаСО3 + Н2О → | 4) | Са(НСО3)2 | |||
|
| 5) | Са(НСО3)2 + H2 | ||||
|
| 6) | Са(НСО3)2 + H2O | ||||
| А | Б | В | Г | |||
|
|
|
| ||||
53. Установите соответствие между реагирующими веществами и продуктами их взаимодействия.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ПРОДУКТЫ ВЗАИМОДЕЙСТВИЯ | |||||
| А) | SO2 + Ba(ОH)2(избыт.) → | 1) | BаSО3 | |||
| Б) | SO2(избыт.) + Ba(OH)2 → | 2) | BаSО4 | |||
| В) | SO2 + BaO → | 3) | BаSО3 + H2O | |||
| Г) | SO3 + BaO → | 4) | BаSО4 + H2O | |||
|
| 5) | Bа(НSО3)2 + H2O | ||||
|
| 6) | Bа(НSО3)2 | ||||
| А | Б | В | Г | |||
|
|
|
| ||||
54. Установите соответствие между реагирующими веществами и продуктами их взаимодействия.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ПРОДУКТЫ ВЗАИМОДЕЙСТВИЯ | |||||
| А) | NO2 + NaОH → | 1) | N2O | |||
| Б) | N2O5 + NaOH → | 2) | N2O3 | |||
| В) | N2O3 + NaOH → | 3) | NaNO2 + H2O | |||
| Г) | NO + NO2 → | 4) | NaNO3 + H2O | |||
|
| 5) | NaNO2 + NaNO3 + H2O | ||||
|
| 6) | NH4NO3 + H2O | ||||
| А | Б | В | Г | |||
|
|
|
| ||||
55. Установите соответствие между реагирующими веществами и продуктами их взаимодействия.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ПРОДУКТЫ ВЗАИМОДЕЙСТВИЯ | |||||
| А) | NO2 + H2O → | 1) | SO3 + N2O4 | |||
| Б) | NO2 + H2O | 2) | SO3 + NO | |||
| В) | NO2 + O2 + H2O → | 3) | HNO3 | |||
| Г) | NO2 + SO2 → | 4) | HNO2 + NO | |||
|
| 5) | HNO3 + NO | ||||
|
| 6) | HNO2 + HNO3 | ||||
| А | Б | В | Г | |||
|
|
|
| ||||
56. Установите соответствие между реагирующими веществами и продуктами их взаимодействия.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ПРОДУКТЫ ВЗАИМОДЕЙСТВИЯ | |||||
| А) | HNO3(разб.) + Ag → | 1) | AgNO3 + H2 | |||
| Б) | HNO3(конц.) + Ag → | 2) | AgNO3 + NO + H2O | |||
| В) | HNO3(разб.) + Al(ОН)3 → | 3) | AgNO3 + NO2 + H2O | |||
| Г) | HNO3(конц.) + Al | 4) | Al(NO3)3 + NH4NO3 + H2O | |||
|
| 5) | Al(NO3)3 + NO2 + H2O | ||||
|
| 6) | Al(NO3)3 + H2О | ||||
| А | Б | В | Г | |||
|
|
|
| ||||
57. Установите соответствие между реагирующими веществами и продуктами их взаимодействия.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ПРОДУКТЫ ВЗАИМОДЕЙСТВИЯ | |||||
| А) | HNO3(разб.) + FeO → | 1) | Fe(NO3)2 + H2O | |||
| Б) | HNO3(конц.) + Fe3O4 → | 2) | Fe(NO3)3 + H2O | |||
| В) | HNO3(разб.) + Fe(OH)2 → | 3) | Fe(NO3)2 + NO + H2O | |||
| Г) | HNO3(конц.) + Fe(OH)3 → | 4) | Fe(NO3)3 + NO + H2O | |||
|
| 5) | Fe(NO3)2 + NO2 + H2O | ||||
|
| 6) | Fe(NO3)3 + NO2 + H2O | ||||
| А | Б | В | Г | |||
|
|
|
| ||||
58. Установите соответствие между схемой реакции и формулой недостающего в ней вещества.
| СХЕМА РЕАКЦИИ | ФОРМУЛА ВЕЩЕСТВА | ||||||
| А) | Cr + … | 1) | H2SO4(разб.) | ||||
| Б) | Cr + … | 2) | H2SO4(конц.) | ||||
| В) | CrO + … → CrSO4 + H2O | 3) | Cr(NO3)2 | ||||
| Г) | CrO + HNO3(конц.) → … + NO2 + H2O | 4) | Cr(NO3)3 | ||||
|
| 5) | HNO3(разб.) | |||||
|
| 6) | HNO3(конц.) | |||||
| А | Б | В | Г | ||||
|
|
|
| |||||
59. Установите соответствие между схемой реакции и формулой недостающего в ней вещества.
| СХЕМА РЕАКЦИИ | ФОРМУЛА ВЕЩЕСТВА | ||||||
| А) | Mg2Si + H2O → Mg(OH)2 +… | 1) | Si | ||||
| Б) | SiH4 + O2 → … + H2O | 2) | H2 | ||||
| В) | Si + NaOH + H2O → Na2SiO3 + … | 3) | H2SiO3 | ||||
| Г) | SiCl4 + H2 → … + HCl | 4) | SiO2 | ||||
|
| 5) | SiH4 | |||||
| А | Б | В | Г | ||||
|
|
|
| |||||
60. Объем оксида углерода(II), который можно сжечь в кислороде объемом 35 л (н.у.), равен _________ л. (Запишите число с точностью до целых.)
61. Объем оксида серы(IV), который может вступить во взаимодействие с кислородом объемом 40 л (н.у.), равен _________ л. (Запишите число с точностью до целых.)
62. Масса воды, образующейся при сгорании 15 л (н.у.) водорода в 15 л (н.у.) кислорода, равна _________ г. (Запишите число с точностью до целых.)
63. Объем аммиака (н.у.), образующегося при взаимодействии 60 л (н.у.) водорода с 40 л (н.у.) азота, равен _________ л. (Запишите число с точностью до целых.)
64. Объем сернистого газа (н.у.), образующегося при сгорании 6,4 г серы в 10 л (н.у.) кислорода, равен _________ л. (Запишите число с точностью до сотых.)
65. Объем хлороводорода (н.у.), образующегося при взаимодействии 15 л (н.у.) водорода с 20 л (н.у.) хлора, равен _________ л. (Запишите число с точностью до целых.)
66. Объем воздуха (н.у.), необходимый для полного сгорания 36 г углерода, равен _________ л. (Запишите число с точностью до целых.)
67. Объем воздуха (н.у.), необходимый для полного сгорания 20 л (н.у.) сероводорода, равен _________ л. (Запишите число с точностью до целых.)
68. Объем газа (н.у.), выделившегося при взаимодействии 12,8 г меди с избытком концентрированной азотной кислоты, равен _________ л. (Запишите число с точностью до сотых.)
69. Объем газа (н.у.), выделившегося при взаимодействии 32,4 г серебра с избытком разбавленной азотной кислоты, равен _________ л. (Запишите число с точностью до сотых.)
70. 16 г оксида серы(VI) растворили в 150 мл воды. Массовая доля кислоты в полученном растворе равна _________ %. (Запишите число с точностью до десятых.)
71. 14,2 г оксида фосфора(V) растворили в 200 мл воды. Массовая доля кислоты в полученном растворе равна _________ %. (Запишите число с точностью до десятых.)
72. 44,8 л аммиака (н.у.) растворили в 1 л воды. Массовая доля аммиака в растворе равна _________ %. (Запишите число с точностью до сотых.)
73. В 140 г 20%-ного раствора серной кислоты растворили 10 г оксида серы(VI). Массовая доля серной кислоты в полученном растворе равна _________ %. (Запишите число с точностью до десятых.)
74. В 200 г 10%-ного раствора ортофосфорной кислоты растворили 14,2 г оксида фосфора(V). Массовая доля ортофосфорной кислоты в полученном растворе равна _________ %. (Запишите число с точностью до десятых.)
75. В 120 г 10%-ного раствора аммиака растворили 28 л аммиака (н.у.). Массовая доля аммиака в полученном растворе равна _________ %. (Запишите число с точностью до десятых.)
Высокий уровень сложности
76. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
HNO3(конц.)  X1
X1  X2
X2  X3
X3  X4
X4 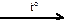 X3
X3
77. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
P  X1
X1  X2
X2  X3 → P
X3 → P 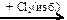 X4
X4
Укажите условия протекания реакций.
78. Сернистый газ, полученный в результате полного сгорания 2,24 л (н.у.) сероводорода, пропустили через 218,6 мл 18,3%-ный раствор гидроксида натрия (плотность 1,20 г/мл). Определите массовые доли веществ в полученном растворе.
79. Хлор, полученный в результате взаимодействия 31,6 г перманганата калия с избытком концентрированной соляной кислоты, пропустили через горячий 16,26%-ный раствор гидроксида калия объемом 359,4 мл (плотность 1,15 г/мл). Определите массовые доли веществ в растворе после окончания реакции.
80. Хлороводород, выделившийся при нагревании 2,34 г хлорида натрия с избытком концентрированной серной кислоты, пропустили через 204 г 5,00%-ного раствора нитрата серебра. Определите массу выпавшего осадка и массовые доли веществ в растворе над осадком
81. Водород объемом 3,36 л (н.у.) пропустили над нагретой серой массой 6,4 г. Полученный в результате реакции газ пропустили через 67,97%-ный раствор азотной кислоты объемом 100 мл (плотность 1,40 г/мл). Определить массовые доли веществ в полученном растворе.
Вариант 1
1. И азот, и фосфор проявляют восстановительные свойства при взаимодействии с
| 1) | кальцием |
| 2) | водородом |
| 3) | кислородом |
| 4) | натрием |
2. И бром, и водород способны реагировать с
| 1) | гидроксидом калия | 3) | натрием |
| 2) | водой | 4) | соляной кислотой |
3. Сера образует соединения, в которых ее степень окисления равна – 2, при взаимодействии с каждым из двух веществ
| 1) | магнием и водородом |
| 2) | калием и кислородом |
| 3) | хлором и гидроксидом натрия |
| 4) | азотной кислотой и кальцием |
4. Какие из приведенных утверждений о водороде верны?
А. Водород является самым распространенным химическим элементов во Вселенной.
Б. В химических реакциях водород способен проявлять как окислительную, так и восстановительную способность.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
5. Какие из приведенных утверждений об элементах подгруппы кислорода верны?
А. Высшая степень окисления всех элементов подгруппы кислорода равна +6.
Б. Все элементы подгруппы кислорода являются типичными неметаллами.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
6. Наиболее сильные кислотные свойства проявляет
| 1) | H2O | 2) | H2S | 3) | H2Se | 4) | H2Te |
7. Наиболее сильные кислотные свойства проявляет
| 1) | H2SO3 | 2) | H2SO4 | 3) | H2SeO3 | 4) | H2SeO4 |
8. Оксид кремния(IV) взаимодействует с каждым из трех веществ
| 1) | H2O, O2, NaOH |
| 2) | K2CO3, CaO, HNO3 |
| 3) | C, KOH, SO2 |
| 4) | HF, Mg, CaCO3 |
9. Концентрированная азотная кислота взаимодействует с
| 1) | конц. HСl | 2) | NaHSO4 | 3) | Au | 4) | SiO2 |
10. И с соляной, и с азотной кислотой взаимодействует каждое из трех веществ
| 1) | Ag, NaHCO3, NaOH |
| 2) | P2O5, CaO, H2S |
| 3) | K2O, Cu(OH)2, Mg |
| 4) | Na2SO3, Au, BaO |
11. Какие из приведенных утверждений о неметаллах и свойствах их соединений верны?
А. Неметаллы способны к образованию как кислотных, так и основных оксидов.
Б. Водородные соединения неметаллов имеют молекулярное строение.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
12. Оксид углерода(II) взаимодействует с
| 1) | хлором |
| 2) | oксидом железа(III) |
| 3) | карбонатом кальция |
| 4) | соляной кислотой |
| 5) | кислородом |
| 6) | раствором гидроксида калия |
13. Хлороводородная кислота взаимодействует с
| 1) | золотом |
| 2) | цинком |
| 3) | oксидом углерода(IV) |
| 4) | сульфидом железа(II) |
| 5) | нитратом серебра |
| 6) | сероводородом |
14. Установите соответствие между реагирующими веществами и продуктами их взаимодействия.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ПРОДУКТЫ ВЗАИМОДЕЙСТВИЯ | |||||
| А) | HNO3(конц.) + P → | 1) | P2O3 + NH3 + H2O | |||
| Б) | HNO3(конц.) + PH3 → | 2) | H3PO4 + NO2 + H2O | |||
| В) | HNO3(конц.) + S → | 3) | SO2 + NH4NO3 + H2O | |||
| Г) | HNO3(конц.) + H2S → | 4) | H2SO4 + NO2 + H2O | |||
| А | Б | В | Г | |||
|
|
|
| ||||
15. Установите соответствие между схемой реакции и формулой недостающего в ней вещества.
| СХЕМА РЕАКЦИИ | ФОРМУЛА ВЕЩЕСТВА | ||||||
| А) | C + … | 1) | H2SO4(разб.) | ||||
| Б) | S + … | 2) | H2SO4(конц.) | ||||
| В) | I2 + SO2 + H2O → … + H2SO4 | 3) | H2SO3 | ||||
| Г) | I2 + HNO3 → … + NO + H2O | 4) | SO3 | ||||
|
| 5) | HI | |||||
|
| 6) | HIO3 | |||||
| А | Б | В | Г | ||||
|
|
|
| |||||
16. Объем углекислого газа (н.у.), выделившегося при взаимодействии 20 г карбоната кальция с избытком соляной кислоты, равен _________ л. (Запишите число с точностью до сотых.)
17. В 150 мл 20%-ного раствора серной кислоты (плотность 1,14 г/мл) растворили 4,0 г оксида серы(VI). К полученному раствору добавили 100 мл 18%-ного раствора хлорида бария (плотность 1,18 г/мл). Определите массу выпавшего осадка и массовые доли веществ в растворе над осадком.
18. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
H2S  X1
X1 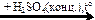 X2
X2  X3
X3  X4
X4  X5
X5
Вариант 2
1. И водород, и углерод проявляют окислительные свойства при взаимодействии с
| 1) | oксидом железа(III) |
| 2) | кальцием |
| 3) | кислородом |
| 4) | фтором |
2. И хлор, и йод способны реагировать с
| 1) | бромидом натрия | 3) | азотом |
| 2) | гидроксидом натрия | 4) | кислородом |
3. Азот образует соединения, в которых его степень окисления равна – 3, при взаимодействии с каждым из двух веществ
| 1) | водородом и магнием |
| 2) | водородом и кислородом |
| 3) | фтором и натрием |
| 4) | алюминием и кислородом |
4. Какие из приведенных утверждений о кислороде и его свойствах верны?
А. В свободном состоянии кислород способен существовать в виде двух аллотропных модификаций.
Б. Кислород взаимодействует с галогенами с образованием оксидов.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
5. Какие из приведенных утверждений об элементах подгруппы углерода верны?
А. Все элементы подгруппы углерода являются неметаллами.
Б. Восстановительная активность элементов подгруппы углерода уменьшается с увеличением заряда ядра их атомов.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
6. Кислотные свойства не проявляет
| 1) | HF | 2) | HBr | 3) | H2Se | 4) | CH4 |
7. Наиболее сильные кислотные свойства проявляет
| 1) | H2SO3 | 2) | H2SO4 | 3) | HBrO3 | 4) | HClO4 |
8. Oксид серы(IV) взаимодействует с каждым из трех веществ
| 1) | O2, H2S, Сa(OH)2 |
| 2) | CO2, H2SO4, H2O |
| 3) | CaO, KOH, SiO2 |
| 4) | HCl, ZnO, CaSiO3 |
9. Cерная кислота не взаимодействует с
| 1) | Mg | 2) | CuO | 3) | Na2CO3 | 4) | СO2 |
10. И с хлороводородной, и с серной кислотой взаимодействует каждое из трех веществ
| 1) | Ag, BaCl2, NaOH |
| 2) | K2CO3, Mg(OH)2, Zn |
| 3) | Ca(NO3)2, BaO, H2S |
| 4) | Na3PO4, SO2, BaO |
11. Какие из приведенных утверждений о соединениях неметаллов верны?
А. Летучие водородные соединения, образованные химическими элементами IVА группы, проявляют основные свойства.
Б. Оксиды и кислоты, в которых атом неметалла проявляет промежуточную степень окисления, обладают окислительно-восстановительной двойственностью.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
12. Оксид углерода(IV) взаимодействует с
| 1) | оксидом лития |
| 2) | концентрированной азотной кислотой |
| 3) | раствором карбоната натрия |
| 4) | магнием |
| 5) | кислородом |
| 6) | оксидом фосфора(V) |
13. Сероводород взаимодействует с
| 1) | оксидом серы(IV) |
| 2) | раствором сульфата меди(II) |
| 3) | азотной кислотой |
| 4) | соляной кислотой |
| 5) | раствором бромида натрия |
| 6) | азотом |
14. Установите соответствие между реагирующими веществами и продуктами их взаимодействия.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ПРОДУКТЫ ВЗАИМОДЕЙСТВИЯ | |||||
| А) | H2SO4(разб.) + Cu(OH)2 → | 1) | СuSO4 + H2O | |||
| Б) | H2SO4(конц.) + Cu | 2) | СuSO4 + H2 | |||
| В) | H2SO4(разб.) + CuО → | 3) | CuSO4 + SO2 + H2O | |||
| Г) | SO3 + Cu(OH)2 → | 4) | CuSO4 | |||
|
| 5) | CuO + H2O | ||||
| А | Б | В | Г | |||
|
|
|
| ||||
15. Установите соответствие между схемой реакции и формулой недостающего в ней вещества.
| СХЕМА РЕАКЦИИ | ФОРМУЛА ВЕЩЕСТВА | ||||||
| А) | Cl2 + … → NaCl + NaClO + H2O | 1) | NaOH(гор.) | ||||
| Б) | Сl2 + … → NaCl + NaClO3 + H2O | 2) | NaOH(хол.) | ||||
| В) | H2S + SO2 → H2O + … | 3) | H2SO4 | ||||
| Г) | … + H2SO4 → S + I2 + H2O | 4) | S | ||||
|
| 5) | HI | |||||
|
| 6) | HIO3 | |||||
| А | Б | В | Г | ||||
|
|
|
| |||||
16. Объем сероводорода (н.у.), выделившегося при взаимодействии 4,4 г сульфида железа(II) с избытком соляной кислоты, равен _________ л. (Запишите число с точностью до сотых.)
17. Сероводород, полученный в результате взаимодействия между сульфидом железа(II) массой 8,8 г и раствором соляной кислоты объемом 75 мл с массовой долей НСl 20% (плотность 1,14 г/мл), пропустили через раствор сульфата меди(II) массой 150 г с массовой долей соли 16%. Определите массовую долю серной кислоты в полученном растворе.
18. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
С 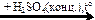 X1
X1  X2
X2 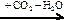 X3 → X1 → C
X3 → X1 → C
Укажите условия протекания реакций.
Дата добавления: 2018-11-24; просмотров: 2960; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!


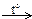 Cr(NO3)3 + NO2 + H2O
Cr(NO3)3 + NO2 + H2O