Равновесия в растворах электролитов
Электролитами называют вещества, расплавы и растворы которых проводят электрический ток. Неэлектролиты электрический ток не проводят. Электролиты делят на две большие группы: cильные и слабые. Сильные электролиты в растворах ионизированы полностью
КА 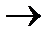 К
К  + А
+ А 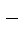 ; HNO
; HNO 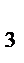
 H
H  + NO
+ NO 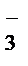 ,
,
а слабые – частично
KA 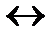 К
К  + А
+ А 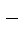 ; CH
; CH  COOH
COOH  H
H 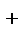 + CH
+ CH 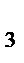 COO
COO 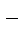 .
.
Количественными характеристиками процесса диссоциации слабого электролита являются степень диссоциации  и константа диссоциации К
и константа диссоциации К 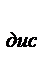
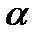 =
= 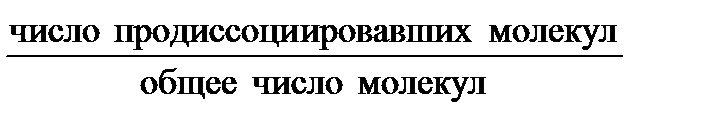 , (0≤
, (0≤  ≤1); К
≤1); К 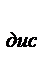 =
= 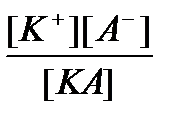 .
.
Cвязь между степенью диссоциации и константой диссоциации описывается уравнением Оствальда: К 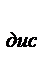 =
=  ,
,
где С – молярная концентрация электролита, моль/л.
Для очень слабых электролитов уравнение преобразуется в более простое К 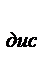 =
= 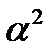 С, откуда
С, откуда 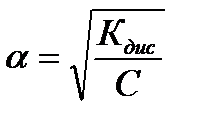 .
.
В растворах электролитов существует взаимное влияние ионов: одноименные по заряду ионы отталкиваются, а разноименные – притягиваются. В результате часть ионов оказывается в связанном состоянии. Это приводит к изменению свойств растворов, уменьшению концентрации кинетически самостоятельных частиц, как бы к снижению диссоциации электролита. Для количественного определения этого влияния используют величину ионной силы раствора (I):
I = 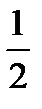 (C
(C 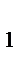 z
z  + C
+ C  z
z 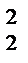 + … + C
+ … + C 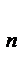 z
z  ),
), 
где С 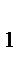 ,C
,C  , …, C
, …, C 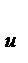 - молярные концентрации ионов в растворе, моль/л; z
- молярные концентрации ионов в растворе, моль/л; z  ,z
,z  ,…,z
,…,z 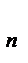 - заряды ионов, соответственно.
- заряды ионов, соответственно.
Ионная сила является аддитивной величиной, т.е. каждый электролит вносит свой вклад в величину I независимо от других.
|
|
|
Для каждого иона определенному значению ионной силы соответствует свой коэффициент активности f, который показывает, какая часть ионов от их общего числа находится в активном, т. е. несвязанном состоянии.
Состав растворов электролитов часто характеризуют эффективной концентрацией, называемой активностью (а). Активность связана с молярной концентрацией соотношением: a = f C. При уменьшении концентрации коэффициент активности f стремится к единице и, следовательно, активность практически равна молярной концентрации.
В растворах слабых электролитов, где значение ионной силы низкое, и для разбавленных растворов сильных электролитов, можно принять а = С.
Пример 1. Рассчитать, как изменится рН раствора гидроксида натрия с молярной концентрацией 0,05 моль/л при введении в него 0,05 моль/л хлорида натрия.
Решение:
а) Находим рН раствора чистой щелочи. Согласно уравнению диссоциации NaOH  Na
Na  + OH
+ OH 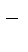 C
C  = C
= C  = 0,05 моль/л.
= 0,05 моль/л.
Ионная сила данного раствора:
I =  .
.
По таблице находим коэффициент активности для однозарядных ионов
f = 0,85. Тогда, а 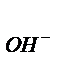 = f
= f 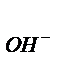 C
C 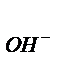 = 0,85∙0,05 = 0,0425 моль/л и
= 0,85∙0,05 = 0,0425 моль/л и
рОН = - lg a 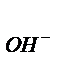 = - lg 0,0425 = 1,37, pH = 14 – pOH = 14 – 1,37 = 12,63.
= - lg 0,0425 = 1,37, pH = 14 – pOH = 14 – 1,37 = 12,63.
|
|
|
б) Рассчитаем рН после добавления в раствор щелочи соли хлорида натрия. Хлорид натрия диссоциирует полностью NaCl 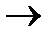 Na
Na 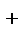 + Cl
+ Cl 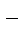 ,
,
давая в раствор 0,05 моль/л ионов Na 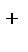 и 0,05 моль/л ионов Cl
и 0,05 моль/л ионов Cl 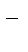 . Следовательно, ионная сила такого раствора станет равной 0,1.
. Следовательно, ионная сила такого раствора станет равной 0,1.
I = 
При такой ионной силе f  = 0,8 (см. таблицу).
= 0,8 (см. таблицу).
рOН = - lg a 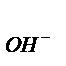 = - lg 0,8∙0,05 = - lg 0,04 =1,4; pH = 14 – pOH = 14 – 1,4 = 12,6
= - lg 0,8∙0,05 = - lg 0,04 =1,4; pH = 14 – pOH = 14 – 1,4 = 12,6
Таким образом, рН уменьшится с 12,63 до 12,6.
Ответ: рН уменьшится с 12,63 до 12,6
Пример 2. Вычислить концентрацию ионов водорода Н 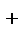 и степень диссоциации уксусной кислоты в растворе с молярной концентрацией эквивалента кислоты 0,001 моль/л.
и степень диссоциации уксусной кислоты в растворе с молярной концентрацией эквивалента кислоты 0,001 моль/л.
Решение: Уксусная кислота - слабый электролит
СH 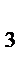 COOH
COOH  H
H 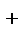 + CH
+ CH 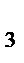 COO
COO 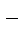 .
.
C  =
= 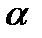 C
C  ,
, 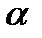 =
= 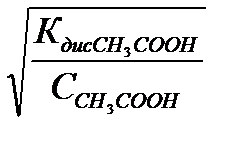 , K
, K  = 1,8∙10
= 1,8∙10 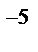 ,
,
 =
=  = 0,134, C
= 0,134, C  = 0,134∙0,001 = 1,34∙10
= 0,134∙0,001 = 1,34∙10 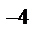 моль/л.
моль/л.
Ответ: C  = 1,34∙10
= 1,34∙10 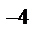 моль/л.;
моль/л.; 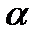 = 0,134
= 0,134
Пример 3. Выпадет ли осадок при смешивании равных объемов сульфата марганца с С(MnSO 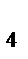 ) = 0,01 моль/л и раствора сульфида аммония с С((NH
) = 0,01 моль/л и раствора сульфида аммония с С((NH 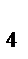 )
) 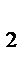 S) = 0,02 моль/л?
S) = 0,02 моль/л?
Решение : MnSO 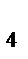 + (NH
+ (NH 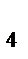 )
) 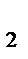 S = MnS
S = MnS  + (NH
+ (NH  )
) 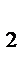 SO
SO 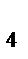
Осадок будет образовываться только в том случае, если [Mn 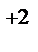 ]∙[S
]∙[S 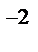 ] > ПР
] > ПР 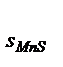 .
.
При сливании равных объемов растворов концентрации уменьшились вдвое, т.е. концентрация сульфата марганца стала 0,005 моль/л, а концентрация сульфида аммония – 0, 01 моль/л.
|
|
|
MnSO 
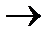 Mn
Mn 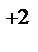 +SO
+SO  , (NH
, (NH 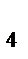 )
) 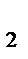 S
S  2NH
2NH 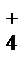 + S
+ S 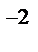 ,
,
[Mn 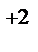 ] = [MnSO
] = [MnSO  ] = 0,005 моль/л, [S
] = 0,005 моль/л, [S 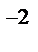 ] = [(NH
] = [(NH 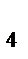 )
) 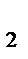 S] = 0,01 моль/л,
S] = 0,01 моль/л,
[Mn 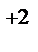 ]∙[S
]∙[S 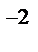 ] = 0,005∙0,01 = 5∙10
] = 0,005∙0,01 = 5∙10 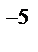 , ПР
, ПР 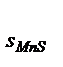 = 1,1∙10
= 1,1∙10  (cправочная величина ),
(cправочная величина ),
[Mn 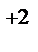 ]∙[S
]∙[S 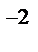 ] > ПР
] > ПР 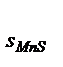 , осадок будет выпадать.
, осадок будет выпадать.
Ответ: осадок будет выпадать
Пример 4. Можно ли приготовить раствор гидроксида кальция с молярной концентрацией 0,002 моль/л?
Решение: Определим молярную концентрацию ионов в заданном растворе из уравнения диссоциации Ca(OH) 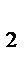
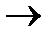 Ca
Ca 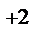 + 2OH
+ 2OH  ,
,
[Ca+2] = C  = 2∙10
= 2∙10 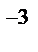 моль/л, [OH-1] = 2С
моль/л, [OH-1] = 2С 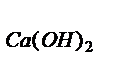 = 2∙2∙10
= 2∙2∙10  = 4∙10
= 4∙10  моль/л,
моль/л,
[Ca+2][OH-1]2 = 2∙10-3(4∙10-3)2 =32∙10-9 =3,2∙10-8
Полученная величина произведения концентраций меньше справочного значения константы растворимости ( K 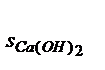 = 6 ∙10-6) следовательно, вещество растворится полностью и раствор с концентрацией (Са(ОН)
= 6 ∙10-6) следовательно, вещество растворится полностью и раствор с концентрацией (Са(ОН) 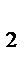 ) равной 0,002 моль/л приготовить можно.
) равной 0,002 моль/л приготовить можно.
Ответ: можно
Ответ: среда кислая, рН = 3,57
Задания для самостоятельного решения:
Написать уравнение гидролиза соли, по всем возможным ступеням и выражение для констант гидролиза по этим ступеням. Рассчитать рН раствора соли, учитывая только первую ступень гидролиза (концентрация соли указана в столбце 4а). Указать реакцию среды раствора. Определить, как будет изменяться рН раствора при нагревании и почему?
|
|
|
|
| формула вещества | Концентрация соли, моль/л | ||||
| 1 | 2 | 3 | 4 |
| ||
| 1 | NaOH | H2SO3 | AgCl | MnI2 | 0,06 | |
| 2 | HCl | NH4OH | PbSO4 | Zn(NO3)2 | 0,01 | |
| 3 | LiOH | H2CO3 | CdS | FeCl3 | 0,04 | |
| 4 | HNO3 | HNO2 | CaF2 | КCN | 0,007 | |
| 5 | HBr | H3BO3 | Ag2S | NaHCO3 | 0,05 | |
| 6 | KOH | H2Se | BaSO4 | CuBr2 | 0,001 | |
| 7 | H2SO4 | NH4OH | PbCl2 | (NH4)2SO4 | 0,005 | |
| 8 | HClO4 | HClO | ZnS | Na2S | 0,03 | |
| 9 | Ba(OH)2 | H3PO4 | PbI2 | Ni(NO3)2 | 0,004 | |
| 10 | RbOH | H2S | Ag3PO4 | K2SiO3 | 0,7 | |
| 11 | HNO3 | HCOOH | Fe2S3 | NH4Cl | 0,002 | |
| 12 | HI | H2SiO3 | Cu2S | Na3PO4 | 0,06 | |

Дата добавления: 2018-11-24; просмотров: 326; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
