Опыт 1. Электролиз раствора иодида калия
В U-образную трубку налить приблизительно до половины раствора иодида калия. Вставить в оба колена трубки угольные электроды и подключить прибор к источнику постоянного электрического тока. Наблюдать окрашивание раствора у анода и выделение газа на катоде. Отключить ток и прибавить 2-3 капли раствора фенолфталеина в катодное пространство. Что наблюдается?
Требования к результатам опыта:
1. Составить схему электролиза водного растворов иодида калия. Написать уравнения электродных и суммарной реакций. Указать продукты электролиза.
2. Какое вещество обусловливает окраску индикатора? Указать рН раствора.
Опыт 2. Электролиз раствора сульфата натрия
В U-образную трубку налить раствор сульфата натрия. Погрузить электроды, включить ток и наблюдать выделение пузырьков газа на электродах. Через 1-2 мин отключить ток и добавить в оба колена трубки по несколько капель раствора лакмуса. В какие цвета окрашивается лакмус?
Требования к результатам опыта:
1. Составить схему электролиза водного раствора сульфата натрия. Написать уравнения электродных и суммарной реакций. Указать продукты электролиза.
2. Указать вещества, которые образуются у катода и анода и изменяют окраску индикатора. Каково значение рН в анодном и катодном пространстве?
Опыт 3. Электролиз раствора сульфата меди
Налить в U-образную трубку раствор сульфата меди. Пользуясь угольными электродами, пропускать ток в течение 4-5 мин. Что выделяется на электродах?
Требования к результатам опыта:
1. Составить схему электролиза водного раствора CuSO4. Написать уравнения электродных и суммарной реакций. Указать продукты электролиза.
2. Назвать вещество, которое образуется у анода (в анодном пространстве) и указать рН среды.
Опыт 4. Электролиз с растворимым анодом
Присоединить электрод с отложившейся в предыдущем опыте медью к положительному полюсу источника тока, а другой электрод – к отрицательному полюсу, пропускать электрический ток. Наблюдать растворение меди с анода и выделение ее на катоде.
Требование к результатам опыта:
Составить схему электролиза раствора сульфата меди с медным анодом. Написать уравнения электродных реакций.
Примеры решения задач
Пример 13.1. Сколько граммов никеля выделится на катоде при пропускании через раствор сернокислого никеля NiSO4 тока силой 5 А в течение 10 мин? Привести схемы электродных процессов, протекающих при электролизе с инертным анодом. Определить продукты электролиза.
Решение. В водном растворе сульфат никеля (II) диссоциирует: NiSO4 = Ni2+ + SO42–. Стандартный электродный потенциал никеля (–0,250 В) выше значения потенциала восстановления ионов водорода из воды (–0,41 В). Поэтому на катоде будет происходить разряд ионов Ni2+ и выделение металлического никеля. При электролизе сернокислых солей на инертном аноде происходит электрохимическое окисление воды с выделением кислорода.
Катод (−) Ni2+, Н2О Анод (+) SO42–, Н2О
На катоде: Ni2+ + 2ē = Ni На аноде: 2Н2О – 4ē = 4Н+ + О2
Продукты электролиза – Ni и О2,
У анода: 4Н+ + 2SO42– = 2Н2SO4
Масса вещества, выделившегося на электроде при электролизе, определяется по законам Фарадея, математическое выражение которых имеет вид:
m = 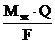 , (1)
, (1)
где m – масса вещества, выделившегося на электроде, г; М эк – молярная масса эквивалентов этого вещества, г/моль; Q – количество электричества, прошедшего через электролит, Кл; F – постоянная Фарадея, равная 96500 Кл/моль∙экв.
Q = I ∙ t, где I – сила тока, А; t – время, электролиза, с. Подставляя в формулу (1) вместо Q его значение, получаем m 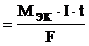
Молярная масса эквивалентов никеля (молярная масса атомов никеля – 58,71 г/моль) равняется 58,71 / 2 = 29,36 г/моль. Подставляя это значение, а также силу тока и время электролиза (в секундах) в формулу m 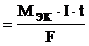 , получаем искомую массу никеля: m = (29,36 × 5 × 600) / 96500 = 0,91 г.
, получаем искомую массу никеля: m = (29,36 × 5 × 600) / 96500 = 0,91 г.
Пример 13.2. Сколько времени нужно пропускать через раствор кислоты ток силой 10 А, чтобы получить 5,6 л водорода (при н.у.)?
Решение. Продукт электролиза представляет собой газообразное вещество, поэтому для решения воспользуемся уравнением V газа 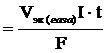 .
.
Так как 1 моль эквивалентов водорода занимает при нормальных условиях объем 11,2 л, то искомое количество времени прохождения тока: t 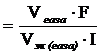 =
= 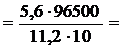 4825 c =1ч 20мин 25с.
4825 c =1ч 20мин 25с.
Пример 13.3. При проведении электролиза водного раствора хлорида двухвалентного металла затрачено 3561 Кл электричества. В результате процесса на катоде выделилось 2,19 г этого металла. Определить металл, водный раствор хлорида которого подвергли электролизу. Привести схему электродных процессов. Определить продукты электролиза.
Решение.Находим молярную массу эквивалентов металла: Мэк 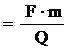
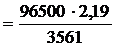 = 59,347 г/моль. Умножая эту величину на 2 (валентность металла) получаем 118,69 г/моль, что соответствует молярной массе атомов олова. Следовательно, электролизу подвергли раствор SnCl2. В водном растворе хлорид олова (II) диссоциирует: SnС12 = Sn2+ + 2С1–. Стандартный электродный потенциал олова (II) (–0,136 В) существенно выше значения потенциала восстановления ионов водорода из воды (–0,41 В). Поэтому на катоде будет происходить разряд ионов Sn2+ и выделение металлического олова. На аноде будут окисляться анионы хлора.
= 59,347 г/моль. Умножая эту величину на 2 (валентность металла) получаем 118,69 г/моль, что соответствует молярной массе атомов олова. Следовательно, электролизу подвергли раствор SnCl2. В водном растворе хлорид олова (II) диссоциирует: SnС12 = Sn2+ + 2С1–. Стандартный электродный потенциал олова (II) (–0,136 В) существенно выше значения потенциала восстановления ионов водорода из воды (–0,41 В). Поэтому на катоде будет происходить разряд ионов Sn2+ и выделение металлического олова. На аноде будут окисляться анионы хлора.
Катод (−) Sn2+, Н2О Анод (+) С1–, Н2О
Катодный процесс: Sn2+ + 2ē = Sn Анодный процесс: 2С1– –2ē = С12
Продукты электролиза – Sn и С12.
Пример 13.4.При электролизе раствора CuSO4 на угольном аноде выделилось 350 мл кислорода при нормальных условиях. Сколько граммов меди выделилось на катоде? Привести уравнения электродных процессов, определить продукты электролиза.
Решение. В водном растворе сульфат меди (II) диссоциирует по схеме: CuSO4 = Cu2+ + SO42−. Электродный потенциал меди (+0,337 В) значительно больше потенциала восстановления ионов водорода из воды (–0,41 В). Поэтому на катоде происходит процесс восстановления ионов Cu2+. При электролизе водных растворов сульфат-анионы не окисляются на аноде. На нем происходит окисление воды.
Катод () − Cu2+, Н2О Анод (+) SO42–, Н2О
На катоде: Cu2+ + 2ē = Сu На аноде: 2Н2О – 4ē = 4Н+ + О2.
Продукты электролиза – Сu и О2.
У анода: 4Н+ + 2SO42– = 2Н2SO4
Один моль эквивалентов кислорода при н.у. занимает объем 5,6 л. Следовательно, 350 мл составляют 0,35 / 5,6 = 0,0625 моль. Столько же молей эквивалентов выделилось на катоде. Отсюда, масса меди
m = 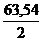 × 0,0625 = 1,98 г.
× 0,0625 = 1,98 г.
Пример 13.5.Будут ли, и в какой последовательности, восстанавливаться на катоде одновременно присутствующие в растворе (в равных концентрациях) ионы А13+, Ni2+, Sn2+, Au3+ и Mg2+? Напряжение достаточно для выделения любого металла.
Решение. На катоде сначала восстанавливаются катионы, имеющие большее значение электродного потенциала (таблица стандартных элекродных потенциалов). Поэтому, в первую очередь, на катоде будут восстанавливаться ионы Au3+ (+1,498 В), далее Sn2+ (–0,136 В) и, наконец, Ni2+ (–0,250 В). Ионы А13+ (–1,662 В) и Mg2+ (–2,363 В), имеющие значения электродного потенциала значительно отрицательнее потенциала восстановления ионов Н+ из воды
(–0,41 В), при электролизе водных растворов не восстанавливаются на катоде. При электролизе их солей протекает восстановление молекул воды:
2Н2О + 2ē = Н2 + 2ОН–.
Задачи
№ 13.1. Водный раствор, содержащий смесь нитратов серебра, калия, цинка с одинаковыми концентрациями, подвергли электролизу. Указать значение молярной массы вещества, которое будет восстанавливаться на катоде в первую очередь. Привести уравнения электродных процессов, происходящих на графитовых электродах для всех солей.
№ 13.2. При электролизе водных растворов каких из приведенных ниже веществ на катоде выделяется только металл: хлорид бария, хлорид меди (II), иодид калия, нитрат серебра, сульфид натрия? Привести соответствующие уравнения электродных процессов.
№ 13.3. При электролизе водных растворов каких из приведенных ниже веществ на катоде выделяется только водород: хлорид калия, хлорид никеля (II), бромид кальция, нитрат серебра, иодид натрия? Привести соответствующие уравнения электродных процессов.
№ 13.4. Среди приведенных ниже соединений указать вещества, продукты электролиза которых одинаковы как для растворов, так и для расплавов: фторид серебра, хлорид меди (II), иодид калия, гидроксид натрия. Привести соответствующие уравнения электродных процессов.
№ 13.5. Сколько граммов меди выделилось на катоде при электролизе раствора CuSO4 в течение 40 мин при силе тока 1,2 А? Привести уравнения электродных процессов. (Ответ: 0,948 г).
№ 13.6. Для выделения 1,75 г некоторого металла из раствора его соли потребовалось пропускать ток силой 1,8 А в течение 1,5 ч. Вычислить молярную массу эквивалентов металла. (Ответ: 17,37 г/моль).
№ 13.7. При электролизе раствора CuCl2 на аноде выделилось 560 мл газа (условия нормальные). Найти массу меди, выделившейся на катоде. Привести уравнения электродных процессов. (Ответ: 1,59 г).
№ 13.8.При электролизе в течение 1 ч водного раствора нитрата висмута Bi(NO3)3 на катоде выделилось 14 г висмута. Выход по току составляет 94 %. Вычислить силу тока. (Ответ: 5,73 А).
№ 13.9.Через электролизеры с водными растворами нитрата ртути (II) и нитрата серебра пропустили одинаковое количество электричества. При этом выделилась ртуть массой 401,2 г. Чему равна масса выделившегося серебра? Привести уравнения электродных процессов. (Ответ: 432 г).
№ 13.10.При электролизе водного раствора SnCl2 на аноде выделилось
4,48 л хлора (условия нормальные). Найти массу выделившегося на катоде олова. Привести уравнения электродных процессов. (Ответ: 23,74 г).
№ 13.11.Сколько минут следует пропускать ток силой 0,5 А через раствор нитрата серебра для выделения 0,27 г серебра? Привести уравнения электродных процессов. (Ответ: 8 мин).
№ 13.12. При какой силе тока можно получить на катоде 0,5 г никеля, подвергая электролизу раствор сульфата никеля в течение 25 мин? (Ответ: 1,1 А).
№ 13.13.Раствор содержит ионы Fe3+, Cu2+, Sn2+ в одинаковой концентрации. В какой последовательности эти ионы будут выделяться при электролизе, если напряжение достаточно для выделения любого металла? Ответ обосновать.
№ 13.14.При электролизе раствора AgNO3 в течение 50 мин при силе тока
3 А на катоде выделилось 9,6 г серебра. Определить выход серебра в процентах от теоретически возможного. Привести уравнения электродных процессов. (Ответ: 95,4 %).
№ 13.15.Какие вещества и в каком объеме можно получить при нормальных условиях на нерастворимом аноде при электролизе водного раствора КОН, если пропустить ток силой 13,4 А в течение 2 ч? Привести уравнения электродных процессов. (Ответ: 1,2 л; 5,6 л).
№ 13.16.Сколько времени потребуется для выделения на катоде 4 г вещества при электролизе расплава хлорида кальция при токе силой 1А? Привести уравнения электродных процессов. (Ответ: 5,36 ч).
№ 13.17. Через водный раствор сульфата цинка пропущено 8407 Кл электричества. При этом на катоде выделилось 1,9 г цинка. Рассчитать катодный выход цинка по току. Привести уравнения электродных процессов.
(Ответ: 67 %).
№ 13.18.Вычислить объем кислорода (нормальные условия), выделившегося у анода при электролизе водного раствора сульфата меди, если сила тока составляла 5 А, а продолжительность электролиза 1 ч. (Ответ: 1,04 л).
№ 13.19.Вычислить количество электричества, которое необходимо пропустить через раствор хлорида натрия, чтобы получить 1 т гидроксида натрия. Привести схемы электродных процессов. (Ответ: 2412,5×109 Кл).
№ 13.20. При электролизе водного раствора СuCl2 с медным анодом масса анода уменьшилась на 1,4 г. Определить расход электричества при этом, если выход по току составляет 73 %. Составить уравнения электродных процессов, определить продукты электролиза. (Ответ: 5825 Кл).
Лабораторная работа 14
Химические свойства металлов
Цель работы: изучить химические свойства металлов научиться составлять уравнения реакций взаимодействия металлов с водой, кислотами, щелочами.
Задание: провести реакции взаимодействия металлов с водой, щелочами, разбавленными и концентрированными растворами серной и азотной кислот. Выполнить требования к результатам опытов, оформить отчет, решить задачу.
Теоретическое введение
 |
Металлы, имея низкие потенциалы ионизации, легко отдают валентные электроны и образуют положительно заряженные ионы:
M − nē = Mn+ .
Поэтому металлы в химических реакциях являются восстановителями и способны взаимодействовать с различными веществами − окислителями.
Рассмотрим некоторые типичные случаи такого взаимодействия.
1. Металлы высокой химической активности могут разлагать воду с вытеснением водорода при комнатных температурах:
2K + 2H2O = 2KOH + H2
2. С кислотами металлы реагируют различно в зависимости от активности самого металла и окислительных свойств кислоты:
– В разбавленной серной кислоте и в растворах галогеноводородов окислителем является ион H+, поэтому в них растворяются металлы, стоящие в ряду напряжений до водорода:
Cd + H2SO4 (разб.) = CdSO4 + H2
Ni + 2HCl = NiCl2 + H2
– Концентрированная серная кислота является окислителем за счет иона SO42− и может при нагревании окислять металлы, стоящие в ряду напряжений после водорода. Продукты ее восстановления могут быть различными в зависимости от активности металла. При взаимодействии с малоактивными металлами кислота восстанавливается до SO2.
Hg + 2H2SO4 (конц.) = HgSO4 + SO2 + 2H2O
При взаимодействии с более активными металлами продуктами восстановления могут быть как SO2, так и свободная сера и сероводород.
4Mg + 5H2SO4 (конц.) = 4MgSO4 + H2S + 4H2O
В этих реакциях часть молекул серной кислоты играют роль среды.
– Азотная кислота является сильнейшим окислителем за счет иона NO3−. Продукты восстановления различны и зависят от концентрации кислоты и активности металла:
HNO3 → NO2 → NO → N2O → N2 → NH4NO3
При реакциях с концентрированной кислотой чаще всего выделяется NO2. При взаимодействии разбавленной азотной кислоты с малоактивными металлами выделяется NO. В случае более активных металлов выделяется N2O. Сильно разбавленная азотная кислота взаимодействует с активными металлами с образованием иона аммония, дающего с кислотой нитрат аммония.
Ag + 2HNO3 (конц.) = AgNO3 + NO2 + H2O
3Ag + 4HNO3 (разб.) = 3AgNO3 + NO + H2O
4Mg + 10HNO3 (разб.) = 4Mg(NO3)2 + N2O + 5H2O
4Ca + 10HNO3 (оч. разб.) = 4Ca(NO3)2 + NH4NO3 + 3H2O
3. Со щелочами реагируют металлы, дающие амфотерные гидроксиды, а также металлы, обладающие высокими степенями окисления в присутствии сильных окислителей:
Be + 2NaOH + 2H2O = Na2[Be(OH)4] + H2
2Mo + 4KOH + 3O2  2K2MoO4 + 2H2O
2K2MoO4 + 2H2O
Выполнение работы
Опыт 1. Взаимодействие металлов с водой
В кристаллизатор с водой добавить несколько капель фенолфталеина. Пинцетом достать кусочек натрия (или кальция) из склянки, где он хранится под слоем керосина, и высушить его фильтровальной бумагой. Ножом отрезать небольшую часть (размером со спичечную головку) и пинцетом перенести в кристаллизатор с водой. Что наблюдается?
Требования к результатам опыта:
1. Составить уравнение реакции взаимодействия натрия с водой.
2. Сделать вывод, какие металлы взаимодействуют с водой.
Опыт 2. Действие разбавленной и концентрированной серной кислоты на металлы
В три пробирки налить по 2-3 мл разбавленной серной кислоты и опустить в одну из них кусочек железа, в другую – цинка, в третью – меди. Какие металлы реагируют с кислотами?
(Проводить под тягой!) В две пробирки налить по 2-3 мл концентрированной серной кислоты. В одну из них опустить кусочек цинка, в другую – кусочек меди. Обе пробирки слегка нагреть. Наблюдать выделение серы и по запаху определить выделяющийся газ в первой пробирке. Какой газ выделяется во второй пробирке?
Требования к результатам опыта:
1. Составить уравнения реакций взаимодействия металлов с разбавленной серной кислотой.
2. Сделать вывод, какие металлы взаимодействуют с разбавленной серной и соляной кислотами.
3. Составить уравнения реакций взаимодействия цинка и меди с концентрированной серной кислотой.
4. Сформулировать правило взаимодействия металлов с концентрированной H2SO4.
Опыт 3. Действие разбавленной и концентрированной азотной кислоты на металлы
(Проводить под тягой!) В две пробирки налить по 2-3 мл разбавленной азотной кислоты и опустить в одну из них кусочек цинка, в другую – кусочек меди. Слегка нагреть обе пробирки. Наблюдать выделение газа.
(Проводить под тягой!) В две пробирки налить по 2-3 мл концентрированной азотной кислоты и опустить в одну из них кусочек цинка, в другую – кусочек меди. Какой газ выделяется?
Требования к результатам опыта:
1. Составить уравнения реакций взаимодействия цинка и меди с разбавленной азотной кислотой.
2. Составить уравнения реакций взаимодействия цинка и меди с концентрированной азотной кислотой.
3. Сформулировать правило взаимодействия металлов с концентрированной и разбавленной HNO3.
Дата добавления: 2018-06-27; просмотров: 1068; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
