Классификация желудочно-кишечных кровотечений по степени
Кровопотери.
Степень кровопотери (три степени). Оценивается на основании:
1) данных анамнеза (в т.ч. расспрос родственников и т.д.)
2) окраски кожных покровов, зевота, сонливость
3) показателей гемодинамики (АД, ЧСС, ЦВД, реовазография)
4) показателей красной крови ( информативны в стадии аутогемодилюции)
5) измерения дефицита глобулярного объема (методы разведения, радиоизотопный и др.)
| Степень 1 — легкая кровопотеря | Общее состояние больного удовлетворительное. Число сердечных сокращений от 80 до 100 в 1 мин. АД в пределах нормы. ЦВД — 5—15 см вод. ст. Диурез не снижен. Содержание гемоглобина не менее 100 г/л Дефицит ОЦК до 20% |
| Степень 2 — средняя кровопотеря | Общее состояние больного средней тяжести Тахикардия до 110 ударов в 1 мин Систолическое АД не ниже 90 мм рт. ст. ЦВД меньше 5 см вод. ст. Умеренное снижение диуреза. Содержание гемоглобина не менее 80 г/л Дефицит ОЦК — 20—29%. |
| Степень 3 — тяжелая кровопотеря | Общее состояние больного тяжелое, сознание спутанное, дезориентация, при продолжающемся кровотечении могут быть полная потеря сознания и кома. Тахикардия более 110 ударов в 1 мин Систолическое АД ниже 90 мм рт. ст ЦВД — 0. Олигурия, метаболический ацидоз, содержание гемоглобина менее 80 г/л дефицит ОЦК 30% и более |
Эндоскопический гемостаз при желудочно-кишечном кровотечении.
Методы эндоскопического гемостаза
|
|
|
| Методы | Тип | Основной механизм действия |
| Термические | Электрокоагуляция Термокаутеризация Лазерная фотокоагуляция Аргоноплазменная коагуляция. | Тромбоз сосуда в зоне кровотечения |
| Инъекционные | Адреналин Алкоголь. Склерозанты Цианакрилаты Тромбин Фибриновый клей | Вазоконстрикция Химическая коагуляция + дегидратация Клеевая пломбировка Клеевая пломбировка |
| Механические | Клипирование. Лигирование | Лигирование сосуда и источника желудочно-кишечного кровотечения |
Термокаутеризация (прижигание или тепловая коагуляция) многими специалистами рассматривается как метод выбора для проведения эндоскопического гемостаза.
В отличие от диатермокоагуляции действующим началом термокаутеризации является не электрический ток, а разогреваемый им до температуры свыше 100°С рабочий наконечник термозонда. С помощью такого «мини-паяльника» осуществляются прижигающее и, как результат, гемостатическое воздействие на кровоточащий или тромбированный сосуд.
Благодаря тому, что наконечник термозонда покрыт тефлоновым слоем, он меньше пригорает к кровяному сгустку. Одновременно сохраняются все положительные свойства контактного метода. Подаваемая под давлением струя жидкости одновременно охлаждает зонд и смывает с источника кровотечения накопившуюся кровь, обеспечивая более выгодные условия для каутеризации.
|
|
|
При остановке продолжающегося кровотечения наконечник зонда целесообразно прижимать непосредственно к кровоточащему сосуду, прекратив таким образом временно кровотечение, а затем приступать к нагреву рабочей головки термозонда.
При остановке продолжающегося кровотечения применяется достаточно большое количество теплоты — 20—30 Дж. Для коагуляции тромбированных сосудов и создания более прочного коагулята воздействуют более низкими параметрами энергии — 10—20 Дж.
Степень нагрева термозонда легко дозируется и регулируется; при соблюдении элементарных правил работы он не вызывает глубоких ожогов и успешно используется практически при всех видах неварикозных гастродуоденальных кровотечений.
Лазерная фотокоагуляция источника кровотечения, пережив этап повального увлечения и обнадеживающего энтузиазма, в последние годы практически отошла на второй план.
В большинстве клинических ситуаций лазерная фотокоагуляция уступила место аналогичным по эффективности, но значительно менее дорогим и громоздким, зато более простым в исполнении и безопасным как для пациента, так и для медицинского персонала методам эндоскопического гемостаза.
|
|
|
Одним из важнейших преимуществ метода аргоноплазменной коагуляции состоит в том, что он является бесконтактным, а следовательно, лишенным побочных эффектов в виде рецидива кровотечения вследствие отрыва тромба-сгустка.
Аргоноплазменную коагуляцию можно использовать для гемостаза в труднодоступных участках за счет сродства аргоновой плазмы к зонам высокой электропроводимости (жидкая кровь и свежие тромбы) и режима работы путем «стекания за угол».
Немаловажен и тот факт,что методика практически не обладает эффектом -«минус тканью. Аргоноплазменная коагуляция минимально испаряет и повреждает ткани и не «выжигает» углубление в источнике кровотечения, а формирует плотный защитный слой, как бы заваривая его.
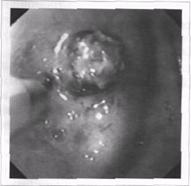 Рис. Аргоноплазменная коагуляция источника кровотечения: Исходный вид язвенного дефекта в луковице двенадцатиперстной кишки с крупным тромбированным сосудом.
Рис. Аргоноплазменная коагуляция источника кровотечения: Исходный вид язвенного дефекта в луковице двенадцатиперстной кишки с крупным тромбированным сосудом.
Коагулирующий эффект аргоновой плазмы легко дозируется. Она не обладает выраженным термическим воздействием на глубокие слои кишечной стенки: проникновение аргоновой плазмы вглубь ткани составляет не более 2-3 мм. Следовательно, аргоновая плазма безопасна и не вызывает перфорации органов.
|
|
|
Первые клинические опыты показали, что использование аргоновой плазмы особенно эффективно при кровотечениях из сосудистых пороков развития, таких, как поражения Дьелафуа, телеангиэктазии, когда необходимо обеспечить мощный гемостатический эффект и чрезмерно не разрушить слизистую оболочку. Однако аргоноплазменная коагуляция находит все более широкое применение при кровотечениях язвенной этиологии и опухолях.
Инъекционные методы гемостаза широко используются в клинической практике. Механическое сдавление сосудов раствором жидкости в сочетании с местным гемостатическим склерозирующим действием практически всегда приводит к временной остановке кровотечения или по крайней мере к уменьшению его интенсивности. Это обстоятельство в ряде случаев позволяет применять инъекционные методы в качестве самостоятельных либо в комбинации с другими методами эндоскопического гемостаза.
Дата добавления: 2018-06-01; просмотров: 200; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
