Ацетиленовые углеводороды, алкины
Общие сведения, номенклатура ацетиленовых углеводородов
Ацетиленовые углеводороды – это ненасыщенные углеводороды, имеющие в своем составе одну тройную связь. Тройная связь – это сочетание одной s- и двух p-связей. Общая формула алкинов -СnH2n-2 . По систематической номенклатуре ацетиленовые углеводороды называют, заменяя в названиях суффикс -ан в предельных углеводородах на суффикс -ин. Для алкинов характерна изомерия углеродного скелета, изомерия положения кратной связи. Пространственная изомерия не характерна.
Таблица 6. Гомологический ряд ацетиленовых углеводородов
| Предельные углеводороды | Ацетиленовые углеводороды |
| Метан СН4 | - |
| Этан С2Н6 | Этин (ацетилен) С2Н2 |
| Пропан С3Н8 | Пропин С3Н4 |
| Бутан С4Н10 | Бутин С4Н6 |
| Пентан С5Н12 | Пентин С5Н8 |
| Гексан С6Н14 | Гексин С6Н10 |
| и.т.д. | и.т.д. |
Физические свойства алкинов
В нормальных условиях: С2-С4 – газы; С5 –С16 – жидкости; С17 и более – твердые вещества. Температуры кипения алкинов выше, чем у соответствующих алканов. Растворимость в воде незначительна, немного выше, чем у алканов и алкенов, но все равно очень мала. Растворимость в неполярных органических растворителях высокая. На основе алкинов производят много различных соединений, имеющих широкое применение в промышленности. Например, получают изопрен – исходное соединения для производства изопренового каучука. Ацетилен используют для сварки металлов, т.к. процесс его горения весьма экзотермичный.
Получение алкинов
1. Отщепление 2-х молекул галогенводорода от дигалогенааконов, которые находятся либо у соседних атомов углерода или у одного. Отщепление происходит под воздействием спиртового раствора щелочи:
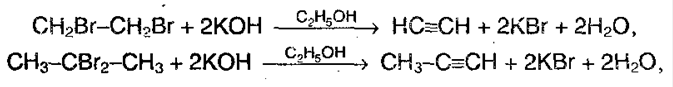
2. Действие галогеналканов на соли ацетиленовых углевородородов:

3. Крекинг метана и его гомологов:
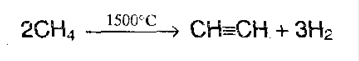


4. Реакции дегидрирования алканов и алкенов:
CH3-CH3 → СH≡CH + 2H2;
CH2 = CH2 → СH≡CH + H2.
5. Ацетилен получают в лаборатории:

Химические свойства ацетиленовых углеводородов
Химические свойства алкинов объясняет наличие тройной связи в молекуле алкина. Типичная реакция для алкинов – реакция присоединения, которая протекает в 2 стадии. На первой происходит присоединение и образование двойной связи, а на второй – присоединение к двойной связи. Реакция у алкинов протекает медленнее, чем и алкенов, т.к. электронная плотность тройной связи «размазана» более компактно, чем у алкенов, и поэтому менее доступна для реагентов.
1. Галогенирование. Алкины также, как алкены, обесцвечивают бромную воду, поэтому эта реакция является качественной и для алкинов. Галогены присоединяются к алкинам в 2 стадии:

2. Гидрогалогенирование. Галогенводороды присоединяются к тройной связи несколько труднее, чем к двойной. Для ускорения (активации) процесса используют сильную кислоту Льюиса – AlCl3. Из ацетилена при таких условиях можно получить винилхлорид, который идет на производства полимера – поливинилхлорида, имеющего важнейшее значение в промышлености:

Если же галогенводород в избытке, то реакция (особенно у несимметричных алкинов) идет по правилу Марковникова:
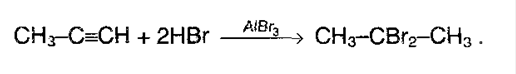
3. Гидратация. Реакция протекает только в присутствии солей ртути (II) в качестве катализатора:

Только ацетилен превращается в альдегид, его гомологи - в кетоны. Реакция протекает по правилу В.В. Марковникова:

Эта реакция носит названия – реакции М.Г. Кучерова.
4. Гидрирование. Протекает в две стадии под действием катализаторов (Ni, Pt, Pd):

5. Полимеризация. При участии катализаторов алкины могут реагировать друг с другом, причем в зависимости от условий, могут образовываться различные продукты. Например, под воздействием хлорида меди (I) и хлорида аммония:
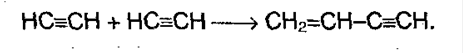
Винилацетилен (полученное соединение) присоединяет хлороводород, образуя хлорпрен, который служит сырьем для получения синтетического каучука:

6. Получение бензола. Если ацетилен пропускать через уголь при 600ºС, получают ароматическое соединение – бензол.
 .
.
Из гомологов ацетилена, получают гомологи бензола:

7. Присоединение циановодородной кислоты:
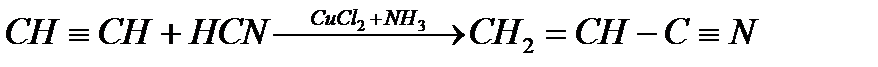
Ацетилен Акрилонитрил
Акрилонитрил – мономер для получения синтетического волокна – полиакрилонитрила.
8. Присоединение спирта (реакция А.Е.Фаворского):

Ацетилен Этиловый спирт Этилвиниловый эфир
9. Реакция окисления.и восстановления. Алкины легко окисляются пер-манганатом калия. Раствор обесцвечивается, т.к. в исходном соединении есть тройная связь. При окислении происходит расщепление тройной связи с образованием карбоновой кислоты:

10. Реакция восстановления.В присутствие металлических катализаторов происходит восстановление водородом:
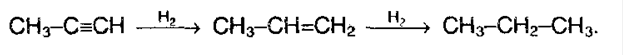
11. Присоединение ацетона. Это реакции, имеющие большое практическое значение. Например, из ацетилена и ацетона можно получить изопрен (реакция Фаворского):

Ацетон Ацетилен

Изопрен
11. Замещение атома водорода при тройной связи. Те алкины, которые имеют концевую тройную связь, могут отщеплять протон под действием сильных кислотных реагентов. Это обусловлено сильной поляризацией связи 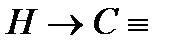 , причиной этого является высокая электроотрицательность атома углерода в состоянии sp- гибридизации. Поэтому алкины образуют ацетилениды:
, причиной этого является высокая электроотрицательность атома углерода в состоянии sp- гибридизации. Поэтому алкины образуют ацетилениды:

Ацетилениды меди и серебра легко образуются и выпадают в осадок (при пропускании ацетилена через аммиачный раствор оксида серебра или хлорида меди). Эти реакции являются качественнымина концевую тройную связь:

Полученные соли легко разлагаются под действием HCl, в результате выделяется исходный алкин, поэтому алкины легко выделить из смеси других углеводородоров:

ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Дата добавления: 2018-05-13; просмотров: 4704; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
