Дослідження аеробного окислення глюкози та альтернативних шляхів обміну моносахаридів.
 1.
1.
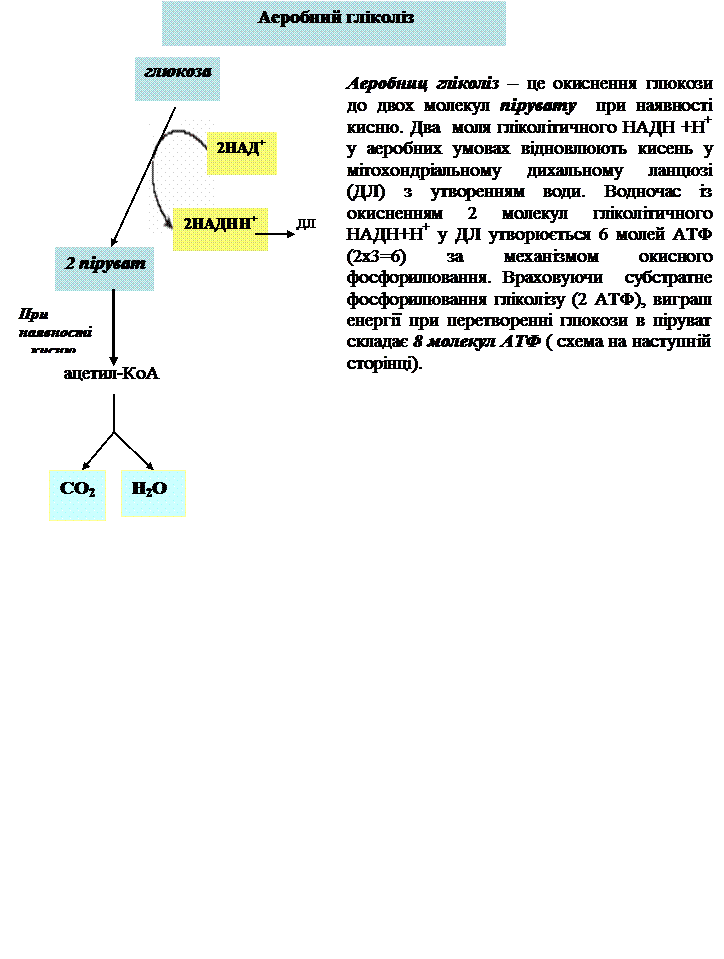
Далі піруват у аеробних умовах окиснюється у ацетил-КоА з утворенням 3 молекул АТФ шляхом окисного фосфорилювання. Ацетил-КоА окиснюється у ЦТК із утворенням СО2, Н2О і 12 молекул АТФ. Таким чином, при окисненні пірувату до вуглекислого газу та води утворюється 15 молекул АТФ. Оскільки з глюкози утворюється 2 моля пірувату, то кількість молекул АТФ буде складати 30 (2х15).
При окисненні глюкози у аеробних умовах до вуглекислого газу та води утворюється 38 молекул АТФ (30+8 =38).
Аеробне окиснення глюкози є значно більше вигідним процесом, тому що глюкоза глюкоза витрачається більш економно (повільно) у порівнянні з анаеробним гліколізом.
Тому при переключенні з анаеробного на аеробний шлях зменшується швидкість витрачання глюкози та припиняється накопичення лактату (ефект Пастера). Молекулярний механізм цього ефекту полягає у конкуренції між диханням і гліколізом за АДФ, необхідним для утворення АТФ.
Окислювальне декарбоксилювання піровиноградної кислоти - це процес відщеплення СО2 від пірувату та перенесення ацетильного залишку на коензим А з наступним утворенням ацетил-КоА. Процес здійснюється за участю мультиферментого піруватдегідрогеназного комплексу.
Комплекс складається з трьох ферментів (Е1 , Е2 , Е3)та п’яти коферментів:
1. Тіамінпірофосфат (ТПФ)
2. Ліпоєва кислота (ЛК)
ФАД
4. НАД+
5. коензим А (HS-КоА)
Е1 –ТПФ: каталізує відщеплення СО2 від пірувату та перенесення гідроксіетильного залишку на ТПФ.
Е2 –ЛК: переносить гідроксіетильний залишок від ТПФ на простетичну групу – ЛК, При цьому дисульфідний зв’язок розривається, а ацетильний залишок і водень приєднуються до ЛК. Далі ацетильный залишок переноситься з ЛК на НSКоАз утворенням ацетил-SКоА, а ЛК відновлюється до дигідро-ЛК.
Е3-ФАД каталізує дегідрування дигідро-ЛК, котра знов окиснюється. Атоми водню відновлюють ФАД. На останній стадії атоми водню переносяться на НАД+ з утворенням НАДН Н+.
Сумарне рівняння аеробного окислення глюкози:
С6Н12О6 + 6О2 ¾¾¾® 6СО2 + 6Н2О.
Крім гліколізу, існує альтернативний метаболічний процес окиснення глюкози. Це процес прямого окиснення глюкози – пентозофосфатний шлях (ПФШ), котрий не пов’язаний безпосередньо з дихальним ланцюгом перенесення електронів та окисним фосфорилюванням. В ньому утворюється інший тип носіїв метаболічної енергії - відновлені коферменти НАДФН+Н+. Вони містять атоми водню окисненої глюкози, котрі далі використовуються у відновних синтезах ліпідів, біохімічно важливого трипептиду глутатіону та інших сполук. Друга функція ПФШ – утворення фосфопентоз, необхідних для синтезу нуклеотидів.
v1 стадія – окисна, в ході якої глюкоза у активній формі (глюкозо-6-фосфат) безпосередньо (прямо) окиснюється, а далі декарбоксилюється (апотомія –відщеплення верхівки (apex) - одного атому вуглуцю у вигляді вуглекислого газу з утворенням фосфопентоз и НАДФН+Н+.
v 2 стадія – неокисна (стадія ізомерних перетворень), під час котрих фосфорибози (6 молекул) знов перетворюються у вихідний глюкозо-6-фосфат (5 молекул).
Сумарне рівняння пентозофосфатного циклу:
глюкозо-6-фосфат + 12 НАДФ+ + 7Н2О
ПФШ активно функціонує в еритроцитах. Біологічна роль цього процесу для еритроцитів полягає в тому, що НАДФН+Н+ використовується в цих клітинах для протидії пероксидному окисненню ненасичених жирних кислот фосфоліпідів мембран еритроцитів, тобто попереджує гемоліз еритроцитів.
При спадковому дефекті пускового ферменту ПФШ – глюкозо-6-фосфат-дегідрогенази спостерігається схильність еритроцитів до гемолізу, особливо при лікуванні деякими лікарськими засобами (сульфаніламідів, аспірину, примахіну - протималярийного препарату).
Ферментативні реакції перетворення фруктози в організмі людини.
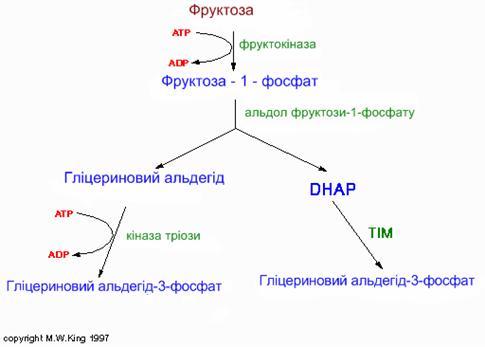
Спадкові ензимопатії обміну фруктози.
Непереносимість фруктози – дефект ферменту фруктозо-1-фосфатальдолази, при цьому накопичується фруктозо-1-фосфат, котрий гальмує розпад глікогену. В результаті виникають фруктоземія, фруктозурія та гіпоглікемія.
Есенціальна фруктоземія – дефект ферменту фруктокінази, що супроводжується підвищенням вмісту фруктози у сечі. Клінічних проявів ця
ензимопатія не має.
Ферментативні реакції перетворення галактози в організмі людини.
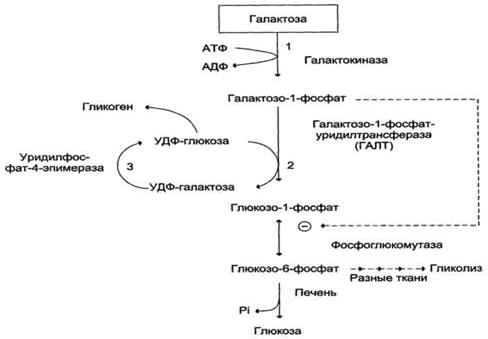
Спадкові ензимопатії обміну галактози.
Галактоземія – дефект ферменту галактозо-1-фосфат-уридил-трансферази, внаслідок якого у крові та внутрішніх органах накопичуються галактоза і галак-тозо-1-фосфат. Клінічні прояви: помутніння кришталику (катарак-та), збільшення печінки, затримка розумового розвитку. Ензимопа-тія з’являється у ранньому віці при споживанні молока.
Дата добавления: 2018-05-12; просмотров: 2740; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
