Особливості використання ферментів як лікарських препаратів
Пепсин, ліпази, амілази, панкреатин – знайшли широке використання при недостатній секреторній функції шлунково-кишкового тракту (замісна терапія). Трипсин використовується для очищення гнійних ран і внутрішньом’язово як протизапальний засіб при остеомієлітах і гайморитах. Фібринолізин використовується як фібринолітичний засіб. Для активації діяльності відповідних ферментів використовуються в клініці коферменти. Так, сульфаніламідні препарати дають позитивний ефект при коковій інфекції. В основі їх дії лежить конкурентне гальмування ферментативної реакції, так як вони є структурними аналогами субстратів, необхідних для життєдіяльності кокових мікроорганізмів. Нікотинова кислота необхідна для життєдіяльності туберкульозних бацил, а її структурний аналог гідразид ізонікотинової кислоти (фтивазид) являється ефективним засобом для лікування туберкульозу.
Дослідження ролі кофакторів та коферментних вітамінів у прояві каталітичної активності ферментів.
Багато ферментів потребують для реалізації своєї каталітичної активності наявності певних низькомолекулярних небілкових сполук – кофакторів. Роль кофакторів можуть відігравати біоорганічні сполуки різної хімічної природи або іони металів( Mg2+ , Ca2+ , Fe3+ -Fe2+ , Cu2+ - Cu1+ та ін.)
Кожний складний фермент в активному центрі має специфічну ділянку для зв’язування коферменту – кофермент.
Усі коферменти можуть бути класифіковані залежно від хімічної природи, типу реакції, яку вони каталізують, класу ферментів, до складу яких вони можуть входити.
Класифікація коферментів за хімічною природою:
1) невітамінні;
2) вітамінні;
3) вітаміноподібні.
До невітамінних коферментів належать: гем, глутатіон, нуклеотиди.
Гем. Структурною основою гему є протопорфірин IX, який складається з 4 пірольних кілець, які з’єднанні метиновими містками. До складу гему входить іон металу зі змінною валентністю (залізо або мідь), тому він може брати участь в окисно-відновних реакціях – віддавати та приймати електрони:
 .
.
Гем, наприклад, входить до складу цитохромів мітохондрій, які транспортують електрони із субстратів на кисень і створюють умови для синтезу АТФ. Крім того, гемвмісними ферментами є каталаза та пероксидаза:
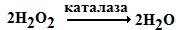
 .
.
Глутатіон – це трипептид, який містить SH-групу (однин з амінокислотних залишків – цистеїн). Ця група може брати участь у транспорті атомів водню і приєднанні молекул субстратів. Саме тому глутатіон входить до складу ферментів антиоксидантної системи клітин (глутатіонредуктаза та глутатіонпероксидаза) та бере участь у реакціях кон’югації при знешкодженні чужорідних сполук (глутатіон-S-трансфераза).
Нуклеотиди (АТФ, ГТФ, УТФ, ЦТФ, ТТФ) беруть участь у транспорті фосфатних груп при утворенні активних форм деяких сполук (глюкозо-6-фосфату, УДФ-глюкуронової кислоти, УДФ-холіну та ін.), які необхідні для синтезу більш складних молекул (глікогену, кон’югатів,фосфоліпідів та ін.).
До вітаміноподібних коферментів належать: ліпоєва кислота, коензим Q, хінонові коферменти, карнітин та ін.
Ліпоєва кислота бере участь у реакціях окисного декар-боксилювання і входить до складу таких мультиферментних комплексів, як піруватдегідрогеназа і α-кетоглутаратдегідро-геназа.
Коензим Q – жиророзчинний кофермент, який може транспортувати електрони та протони і тому бере участь у окисно-відновних реакціях при роботі дихального ланцюга мітохондрій (робота цього ланцюга необхідна для синтезу енергії у клітині).
Хінонові коферменти (топахінон, триптофан-триптофілохінон та ін.) утворюються при конденсації глутамату та тирозину; беруть участь у транспорті атомів водню. Ці коферменти є складовою моноамінооксидази (МАО), гістаміназ тощо.
Карнітин необхідний для транспорту жирних кислот у мітохондрії для подальшого їх окиснення та продукції АТФ.
До вітамінних коферментів належать похідні водороз-чинних вітамінів. У наступній таблиці наведені приклади деяких вітамінів, їх коферментних форм та функція:
Таблиця -Вітамінні коферменти
| Назва вітаміну | Кофермент(и) | Функція |
| В1(тіамін) | ТПФ(тіамінпіро-фосфат) | Транспорт гідроксіалкільних груп |
| В2(рибофлавін) | ФАД, ФМН | Участь в окисно-віднов-них реакціях (транспорт гідроксид-іонів) |
| РР (нікотинова кислота) | НАД, НАДФ | Участь в окисно-віднов-них реакціях (транспорт гідроксид-іонів) |
| Фолева кислота | ТГФК (тетрагід-рофолева кислота) | Транспорт одновуглеце-вих фрагментів (С1-обмін) |
| С (аскорбінова кислота) | Невідомі | Участь в окисно-віднов-них процесах (реакції гідроксилювання, антиоксидантна функція) |
| Пантотенова кислота | Коензим А | Активація і транспорт залишків карбонових кислот |
| В6 (піридоксин) | ПАЛФ, ПАМФ | Транспорт NH2-груп, ре-акції декарбоксилювання |
Класифікація коферментів за механізмом дії:
1) переносники атомів водню, протонів, електронів;
2) переносники окремих хімічних груп.
Таблиця - Класифікація коферментів за механізмом дії з прикладами відповідно до хімічної природи
| Група коферментів | Механізм дії | Хімічна природа коферменту | ||
| Невітамінні | Вітаміно- подібні | Вітамінні | ||
| I | Переносники атомів водню, протонів, електронів | гем, глутатіон | ліпоєва кислота, коензим Q, хінонові коферменти | В2, РР, С |
| II | Переносники окремих хімічних груп | нуклеотиди | карнітин | В1, фолієва кислота, пантоте-нова кислота, В6, Н, В12 |
Дата добавления: 2018-05-12; просмотров: 1048; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
