Определение констант кислотности слабых кислот
Методом рН-метрии
Измерения проводят в разбавленных растворах, принимая коэффициент активности равным единице.
Если не учитывать реакцию автопротолиза воды, то уравнение ионных равновесий в водном растворе слабой одноосновной кислоты будет иметь следующий вид:
HA + H2O = H3O+ + A- x
Константа кислотности выразится как:
 причем [c] = 1 моль/л
причем [c] = 1 моль/л

Если кислота слабая, то 


Отсюда получаем
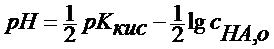
Готовят растворы с разной начальной концентрацией кислоты и измеряют их рН.
Строят график зависимости рН от lg cHA . Из вышеприведенного уравнения следует, что отрезок, отсекаемый прямой на оси ординат равен 1/2рKкис.

Определение константы кислотности потенциометрическим методом
Для одноосновной кислоты
 .
.
Для определения  надо измерить концентрацию ионов гидроксония в растворе с известной концентрацией кислоты. В качестве индикаторного электрода можно использовать стеклянный или хингидронный электрод , например Ag | AgCl | KCl || H3O+, нас.х.г |Pt
надо измерить концентрацию ионов гидроксония в растворе с известной концентрацией кислоты. В качестве индикаторного электрода можно использовать стеклянный или хингидронный электрод , например Ag | AgCl | KCl || H3O+, нас.х.г |Pt
Для получения более точных результатов проводят титрование раствора слабой кислоты раствором NaOH, в ходе титрования измеряют величину ЭДС элемента и рассчитывают рН.
В системе протекают следующие реакции:
H2O + H2O = H3O+ + OH- x1
HA + H2O = H3O+ + A- x2
H3O+ + NaOH = 2 H2O + Na x3
Можно допустить, что x1 << x2 и x1 << x3 .
Балансовые уравнения имеют вид: 
 ;
;
 .
.

Как было показано ранее
|
|
|

Отсюда:
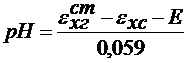


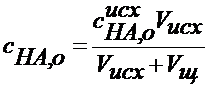



РАЗДЕЛ 3. КИНЕТИЧЕСКИЕ ЗАКОНОМЕРНОСТИ ПРОСТЫХ РЕАКЦИЙ
Химическая кинетика – это наука, изучающая протекание химической реакции или физико – химических процессов во времени, это раздел физической химии, в котором изучается зависимость скорости химической реакции от концентрации реагентов, температуры, свойств среды, излучения и других факторов.
Химическая кинетика позволяет рассчитать время заданной степени превращения вещества и найти наиболее эффективные факторы воздействия на скорость химической реакции.
Классификация химических реакций
С точки зрения кинетики существует несколько принципов классификации химических реакций:
1) по агрегатному состоянию участников реакции все реакции делятся на гомогенные и гетерогенные.
Гомогенные реакции, когда все реактанты находятся в одной фазе. Они бывают:
а) газофазные
б) жидкофазные
в) твердофазные
Гетерогенные реакции, когда участники реакции находятся в разных фазах; реакция протекает на границе раздела фаз
2) по специфике элементарного акта
а) каталитические
б) некаталитические
в) фотохимические
г) электрохимические
д) цепные
3) по числу стадий
|
|
|
а) простые (1 стадия)
б) сложные
4) по обратимости реакций
а) обратимые (двусторонние)
б) необратимые
Реакция считается необратимой, если:
а) в результате реакции образуется газ
HCOOH → H2O + CO2 ↑
б) образуется труднорастворимое соединение
AgNO3 + KJ → AgJ↓ + KNO3
в) образуется малодиссоциируемое соединение
HNO3 + NaOH → NaNO3 + H2O
г) выделяется большое количество тепла
3Fe3O4 + 8Al → 4Al2O3 + 9Fe + ∆H↑
3.2. Элементарные химические реакции
Скорость химических реакций зависит от пути прохождения реакции. Этот путь может быть представлен в виде суммы элементарных химических реакций.
Элементарная реакция – это односторонний процесс превращения одних компонентов в другие. Она является совокупностью однотипных элементарных актов химического превращения. Большинство химических реакций не являются элементарными; они включают в себя несколько элементарных стадий – сложные реакции.
Механизм реакции – это совокупность элементарных стадий.
Реактант – участник химической реакции.
dρnk – бесконечно малое изменение числа молей компонента k в элементарной реакции ρ
Если dρnk > 0 – продукт реакции
dρnk < 0 – исходное вещество
dρnk = 0 – индифферентное вещество
|
|
|
3.3. Скорость химической реакции
Скорость химической реакции – это число однотипных элементарных актов химического превращения, совершающихся в единицу времени в единице объема или на единице поверхности.
Рассмотрим реакцию:

t = 0 
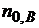

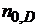 - исходные числа молей
- исходные числа молей
t ≠ 0 nA nB nC nD - текущие числа молей ξ =
(кси) ξ – глубина протекания реакций
ξ 

ξ  (3.1)
(3.1)
dξ  (3.2)
(3.2)
Под скоростью химической реакции понимается производная по времени от глубины протекания реакции.
Wp 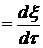 (3.3)
(3.3)
Wp 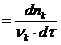 (3.4)
(3.4)
x – плотность глубины реакции, x = 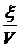
V – объем реакционной системы
x = 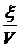 =
=  (3.5)
(3.5)
Wp(V) =  - плотность скорости реакции
- плотность скорости реакции
тогда Wp(V) =  (3.6)
(3.6)
или Wp(V) =  (3.7)
(3.7)
Скорость химической реакции можно определить по изменению концентрации одного из компонентов реакции
|
|
|
W(V) = 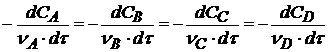 (3.8)
(3.8)
По мере протекания реакции ее скорость будет уменьшаться
Основной постулат Бекетова – Гульдберга – Вааги:
Скорость химической реакции пропорциональна концентрации исходных веществ в степенях, равных их стехиометрическим коэффициентам
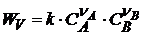 (3.9)
(3.9)
где k – константа скорости реакции
если  , то количественно
, то количественно 
k определяется природой реакции, T и присутствием катализаторов; K называют удельной скоростью. Этот постулат справедлив для простых одностадийных реакций.
Дата добавления: 2018-04-05; просмотров: 895; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
