Окислительно-восстановительные электроды
В электродной реакции участвуют ионы разной степени окисления. О-В электроды состоят из инертного металла, обычно платины и раствора, содержащего ионы разной степени окисления.
Например, Pt| Fe2+, Fe3+ ; Pt |Sn2+ , Sn4+ .
Sn4+ + 2e = Sn2+

В общем виде:
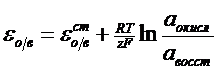
z- число электронов, участвующих в ОВ реакции.
Газовые электроды
Это электроды, у которых в электродной реакции участвует вещество в газообразном состоянии и его ионы, находящиеся в растворе.
Например, водородный электрод 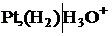
2H3O+ +2e = H2+2H2O

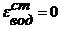
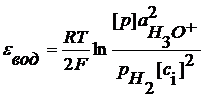
Если давление водорода 1 атм, то 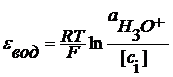
Хлорный электрод Pt (Cl2) | Cl-
Cl2 + 2e = 2Cl-
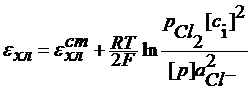
При давлении газообразного хлора 1 атм:
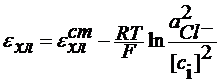
Классификация гальванических элементов
По источнику ЭДС гальванические элементы делятся на химические и концентрационные.
В химических ГЭ источником ЭДС является химическая реакция. В концентрационных ГЭ ЭДС возникает за счет разной концентрации ионов в растворах и вещества на электродах.
И химические и концентрационные ГЭ по наличию или отсутствию диффузионной разности потенциалов ( 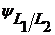 ) делятся на элементы с переносом и элементы без переноса.
) делятся на элементы с переносом и элементы без переноса.
Пример1.
Ag | AgClТВ |KCl || KCl | (Cl2) Pt
Ag – e + Cl- = AgClТВ
Cl2 + 2e = 2Cl-
2 Ag + Cl2+ 2Cl-(лев) = 2AgClтв + 2Cl-(прав)
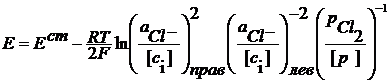
В элементе ЭДС возникает за счет химической реакции и ее величина зависит от активности компонентов, участвующих в ней. В элементе имеется граница раздела между двумя электролитами KCl. Следовательно данный элемент относится к химическим элементам с переносом.
|
|
|
Пример 2
Но если оба электрода поместить в один электролит, то получим элемент
Ag | AgClТВ |KCl | (Cl2) Pt
Ag – e + Cl- = AgClТВ
Cl2 + 2e = 2Cl-
2 Ag + Cl2 = 2AgClтв

В этом элементе нет границы раздела между электролитами, это химический элемент без переноса.
Пример 3.
Zn | ZnSO4 || ZnSO4 | Zn
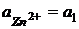
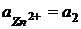
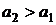
Zn – 2e = Zn2+ 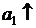
Zn2+ +2e = Zn 
(Zn2+)пр + Zn = (Zn2+)лев + Zn
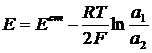
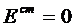
В общем случае

Элемент состоит из одинаковых электродов, различаются только концентрации ионов Zn2+ в растворах - это концентрационный элемент с переносом.
Пример 4
Pt (H2) | HCl (водный раствор) | (H2) Pt
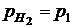

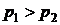
H2 - 2 e + 2H2O = 2H3O+ 
2H3O+ + 2e = H2 +2H2O 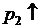
(H2)лев = (H2)прав
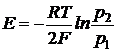 или
или 
Это концентрационный элемент без переноса.
Потенциометрический метод анализа (ПМА)
ПМА основан на зависимости условного электродного потенциала от активности определяемых ионов. В ПМА используются элементы, состоящие из индикаторного электрода и электрода сравнения.
Индикаторный электрод - это электрод, потенциал которого зависит от активности определяемых ионов.
Электрод сравнения - это обычно электрод второго рода, потенциал которого остается постоянным в ходе эксперимента.
|
|
|
Измерение рН растворов
Индикаторный электрод - это электрод, потенциал которого зависит от активности ионов гидроксония.
Это могут быть:
а) водородный электрод
б) хингидронный электрод
в) стеклянный электрод.
Рассмотрим подробнее случаи б) и в)
б). Индикатоный электрод - хингидронный.
Pt | H3O+, нас. хингидроном
Это окислительно-восстановительный электрод.
Хингидрон: C6H4O2× C6H4(OH)2 = C6H4O2+C6H4(OH)2
C6H4O2 + 2e = 2H3O+ = C6H4(OH)2+2H2O
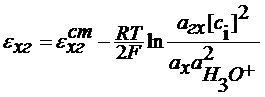
В кислых средах 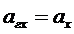

Ag | AgCl | KCl || H3O+, нас.х.г |Pt
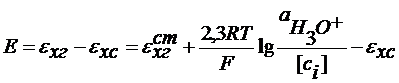
Отсюда:
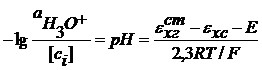
У этого электрода есть и преимущества и недостатки.
В) индикаторный электрод - стеклянный электрод.
В состав стекла входят ионы щелочных металлов.


На поверх. В растворе в растворе на поверхн.
стекла стекла
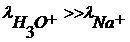 , поэтому поверхность стекла получает избыточный положительный заряд. Образуется скачок потенциала на границе фаз «стекло- раствор». Его величина зависит от концентрации ионов гидроксония в растворе.
, поэтому поверхность стекла получает избыточный положительный заряд. Образуется скачок потенциала на границе фаз «стекло- раствор». Его величина зависит от концентрации ионов гидроксония в растворе.
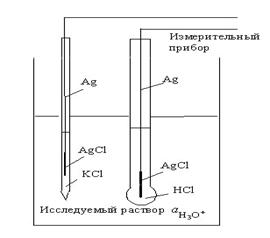
Элемент для измерения рН
Ag | AgCl |KCl || исследуемый раствор, H3O+ HCl |AgCl|Ag
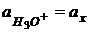
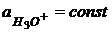

 - этим символом обозначена стеклянная мембрана.
- этим символом обозначена стеклянная мембрана.
Приборы для измерения ЭДС этого элемента, а, следовательно, и величины рН, называются рН-метры.
|
|
|

 - это активность ионов гидроксония в стеклянном электроде.
- это активность ионов гидроксония в стеклянном электроде.
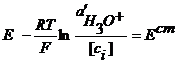
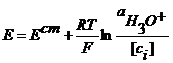
Шкала прибора градуируется в единицах рН с помощью буферных растворов. рН-метр удобен в работе. Позволяет измерять рН в широких пределах. На показания прибора не влияют примеси окислителей и восстановителей.
Дата добавления: 2018-04-05; просмотров: 451; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
