Термодинамика гальванического элемента
Любой самопроизвольный процесс, протекающий при постоянном давлении и температуре, сопровождается уменьшением энергии Гиббса, которое равно максимально полезной работе, электрической работе.
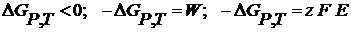 (2.3)
(2.3)
По уравнению Гиббса-Гельмгольца
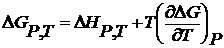 (2.4)
(2.4)
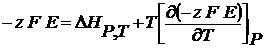
Величины Z и F ≠ f (Т), тогда
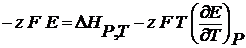 (2.5)
(2.5)
где 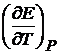 – есть температурный коэффициент Е гальванического элемента, который показывает, как изменяется ЭДС при изменении температуры.
– есть температурный коэффициент Е гальванического элемента, который показывает, как изменяется ЭДС при изменении температуры.
Из уравнения (2.54) можно вычислить тепловой эффект реакции.
 (2.6)
(2.6)
Изменение энтропии в ходе процесса:
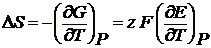 (2.7)
(2.7)
Измерение ЭДС гальванического элемента можно проводить компенсационным методом при любой температуре. С увеличением температуры ЭДС увеличивается нелинейно.
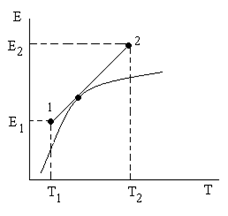
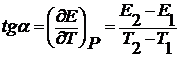 (2.8)
(2.8)
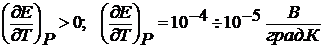
Электрическая работа больше теплового эффекта реакции.
Может быть 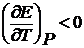 , тогда электрическая работа меньше
, тогда электрическая работа меньше 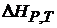
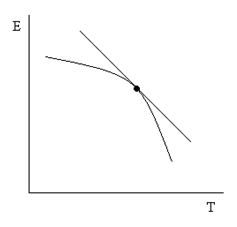 Значения
Значения 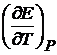 даются в справочниках, но можно определить и экспериментально.
даются в справочниках, но можно определить и экспериментально.
Вывод уравнения Нернста для расчета ЭДС
Гальванического элемента
Изменение энергии Гиббса в ходе химического процесса:
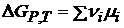
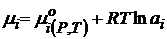 (чаще всего концентрация в С - шкале).
(чаще всего концентрация в С - шкале).
Для газовых электродов:
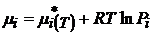
Тогда 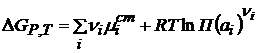
Изменение энергии Гиббса в ходе электрохимической реакции
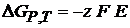
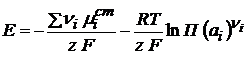 (2.9)
(2.9)
Это постоянная величина при заданных давлении и температуре, она называется стандартная ЭДС гальванического элемента – Е0 и определяется только природой реакции.
|
|
|
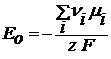 (2.10)
(2.10)
Исходя из изотермы химической реакции, можно записать выражение для Е0:
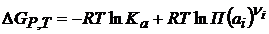
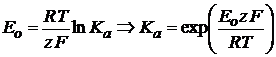 (2.11)
(2.11)
Исходя из этого, можно записать уравнение Нернста для определения ЭДС гальванического элемента:
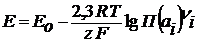 (2.12)
(2.12)
R, T, F не зависят от природы реакции, вводится сonst:
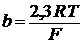 (2.13)
(2.13)
При Т=298 К (250С) 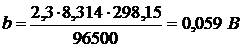
При 293 К  =0,058
=0,058
Выражение для расчета ЭДС примет вид:
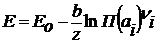 (2.14)
(2.14)
Для гальванического элемента Даниэля-Якоби:
Zn – 2e = Zn2+ (Окисление)
Cu2+ + 2e = Cu0 (восстановление)
Zn + Cu2+ = Cu0 + Zn2+
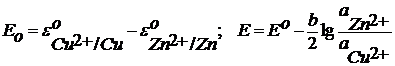
Классификация электродов
Электрод - это часть гальванического элемента, сочетание проводника 1 рода (металла) и проводника 2 рода(электролита). Электроды классифицируются по виду компонентов, участвующих в электродной реакции.
Электроды первого рода
В электродной реакции участвуют металлы и их катионы или металлоиды и их анионы. Электроды 1 рода состоят из металлов, погруженных в раствор их растворимой соли или металлоидов в растворе, содержащих их анионы.
|
|
|
Например:
Ag | AgNO3; Cd | CdSO4.
Сd2+ +2e =Cd
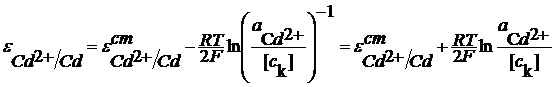
Или в общем виде:
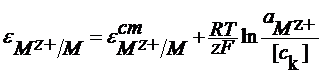
У этих электродов в реакции участвуют катионы и потенциал этих электродов зависит от активности катионов. Такие электроды называют электродами обратимыми по катиону.
Другой пример электродов первого рода:
Se/Se2- Se + 2e = Se2-
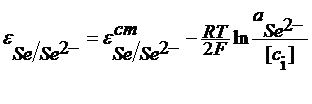
В электродной реакции участвуют анионы и потенциал электрода зависит от активности аниона - это электроды, обратимые относительно аниона.
Электроды второго рода
В электродной реакции участвуют металлы, их труднорастворимые соединения и анионы труднорастворимых соединений. Электроды 2 рода состоят из металла, его труднорастворимого соединения и электролита, содержащего анионы труднорастворимого соединения.
Например, хлорсеребряный электрод
Ag | AgClТВ | KCl
Или каломельный электрод (каломель - это Hg2Cl2)
Hg | Hg2Cl2тв |NaCl
Hg2Cl2тв+2e = 2Hg + 2Cl-
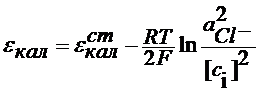
В растворе над осадком Hg2Cl2
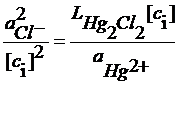
С учетом последнего уравнения
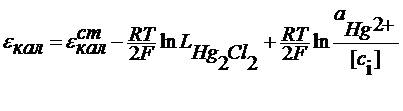
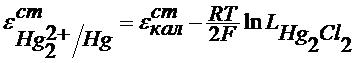
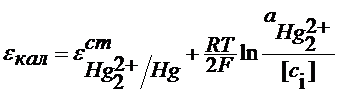
Из сказанного следует, что потенциал электрода 2 рода можно представить и как функцию анионов и как функцию катионов ,т.е. они являются обратимыми по катиону и по аниону. При этом стандартный условный электродный потенциал электрода второго рода связан со стандартным условным электродным потенциалом соответствующего электрода первого рода:
|
|
|
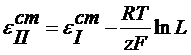
где z - заряд катиона труднорастворимого соединения.
Дата добавления: 2018-04-05; просмотров: 454; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
