Перечислите заболевания, которые можно диагностировать как гетерозиготное носительство с помощью биохимических методов
Биохимические методы играют первоочередную роль в диагностике наследственных нарушений обмена веществ (НБО). Универсальность этих методов позволяет использовать их в дифференциальной диагностике и для выявления гетерозиготного носительства другой моногенной патологии, при которой изменение биохимических показателей является вторичным: например, при прогрессирующей мышечной дистрофии Дюшенна/Бекера (ПМДД/Б) повышается уровень креатин-фосфокиназы (фермент мышц) в крови больных при начальной и развернутой стадии заболевания, а также и у 30% носительниц гена ПМДД/Б.
Раскройте понятие блот-гибридизации или амплификации
Блот-гибридизация— гибридизация рестриктазных фрагментов исследуемой ДНК,
предварительно разделенныхэлектрофоретически и перенесенных на нитроцеллюлозный фильтр при помощи фильтровальной бумаги, соспецифичным нуклеотидным зондом.
Блот-гибридизация - высоко чувствительный метод идентификации специфических последовательностей ДНК.
Перечислите, на чем основаны прямые и косвенные методы ДНК-диагностики.
С помощью прямых методов выявляются нарушения в первичной нуклеотидной последовательности ДНК (мутации и их типы). Прямые методы отличаются точностью, достигающей почти 100 %.
Однако на практике указанные методы могут применяться при определенных условиях: 1) известной цитогенетической локализации гена, ответственного за развитие наследственного заболевания, 2) должен быть клонированным ген заболевания и известна его нуклеотидная последовательность.
Косвенные методы ДНК-диагностики основаны на анализе сцепления с исследуемым геном определенного полиморфного локуса (маркера), с помощью которого можно производить маркировку как мутантных, так и нормальных аллелей и проанализировать их передачу в поколениях, т.е. среди родственников обследуемого лица. Это особенно важно при решении вопроса о пренатальной (дородовой) диагностике наследственного заболевания. При использовании косвенных методов ДНК-диагностики следует помнить — чем теснее сцепление между маркерным локусом и мутантным геном, тем точнее диагноз. Чтобы свести до минимума ошибку диагностики, необходимо по возможности использовать внутригенные маркеры или использовать два маркерных локуса, фланкирующих мутантный аллель.
Охарактеризуйте метод «преимплантационной» диагностики врожденных аномалий.
Преимплантационная диагностика - это исследование молекулы ДНК в клетках зародыша на ранней стадии развития зиготы - стадии бластоциста (6-8 клеток, полученных при оплодотворении invitro - неинвазивный метод) или при помощи маточного лаважа в период 90-130 ч после оплодотворения (инвазивный метод).
Суть этих методов заключается в том, что с помощью микрохирургического вмешательства от зародыша отделяются одна или две клетки для последующего генетического анализа.
Остальные зародышевые клетки замораживаются до окончания анализа. Если в анализируемых клетках исключается наследственная патология, то оставшиеся клетки размораживаются и для них создаются условия, оптимальные для нормального развития, после чего они имплантируются в матку в соответствующий период менструального цикла.
Преимущество этих методов - возможность прервать беременность при обнаружении у зародыша наследственной патологии.
Недостаток этих методов - низкий процент успешных имплантаций (всего 10-20%), а также возможные осложнения в ходе беременности после успешной имплантации зародыша.
С помощью данного метода, например, осуществима диагностика синдрома Марфана, основанная на ПЦР с обратной транскрипцией, позволяющей идентифицировать мутации в гене фибриллина.
Значение расчета повторного генетического риска при моногенных заболеваниях.
Используются теоретические расчеты риска, основанные на генетических закономерностях.
1. Оценка риска при всех типах наследования, когда известны генотипы обоих родителей, несложна, сводится к менделевскому расщеплению
2. При идентификации новой мутации используется популяционные данные о частоте мутирования.
3. Оценка риска при аутосомно-рецессивных заболеваниях, когда известен генотип только одного из супругов. Для расчета используют данные о частоте распространения гетерозигот в популяции.
Формула Харди–Вейнберга:
АА : Аа : аа = р2 : 2pq : q2, гдеpq– частота гетерозигот (2pq≈ 2, т.к.p + q= 1,р≈ 1, аqочень мала),q– частота данного заболевания в популяции (  )
)
4. Оценка генетического риска при неустановленных генотипах родителей – определяют вероятность принадлежности их к различным возможным генотипам, которые могли бы объяснить распределение данного дефекта у детей.
5. Оценка риска при кровно–родственном браке – браке между индивидуумами, которые имеют хотя бы одного общего предка. Имеют значение близко–родственные браки между супругами, имеющих общих предков в трех или четырех поколениях. Мерой родства является коэффициент инбридинга (F).
Формула Райта: А = (½)n–1, гдеn– число ступеней передачи гена от общего предка к ребенку через одного из родителей и возвращаясь обратно через второго – все пути суммируются.
| Характер брака | F |
| 1. Инцестный – между родителями и потомками, сибсами | 
|
| 2. Между дядей (теткой) и племянниками, между полусибсами, дважды двоюродными сибсами | 
|
| 3. Между двоюродными сибсами | 
|
| 4. Между троюродными сибсами | 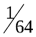
|
| 5. Между двоюродным дядей и племянницей | 
|
Этапы консультирования:
1. Уточнение диагноза наследственного заболевания.
2. Определение прогноза потомства.
3. Заключительный
Риск до 5% – низкий,
до 10% – повышен в некоторой степени,
до 20% – средний,
свыше 20% – высокий.
Дата добавления: 2018-04-05; просмотров: 610; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
