ИЭТ альбумина плазмы крови равна 4,64
Определите знак заряда частиц альбумина в 0,001М растворе HCl.
Укажите направление перемещения частиц альбумина при электрофорезе в данных условиях.
Решение
1.Определим рН в 0,001 М растворе НCl:
рН=-lgC(HCl)=3
2.Так как рН< ИЭТ, частицы альбумина будут заряжены положительно и при электрофорезе будут двигаться к отрицательному электроду (катоду)
3. Напишите схему реакции гидролиза бензилхлорида (фенилхлорметана).
Опишите её механизм.
Укажитенуклеофил, субстрат, уходящую группу.
Объясните причину повышенной устойчивости бензильного катиона.
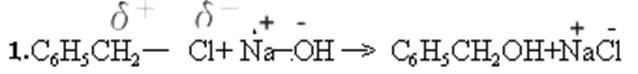
4.Гидролиз бензилхлорида в щелочном водном растворе является реакцией нуклеофильного замещения (Sn). Механизм реакции: замещение нуклеофильное, бимолекулярное, SN2.
Реакция происходит в одну стадию. При этом атака нуклеофила и отщепление уходящей группы происходит одновременно:
C6H5СН2Cl+ -OH → [OH ⋯C6H5СН2⋯Cl]− → C6H5СН2OH + Cl –
5.Нуклеофил - гидроксил-анион-OH ,
субстрат - бензилхлорида, C6H5СН2Cl,
уходящая группа - Cl –
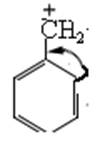
6. Причина повышенной устойчивости бензильного катиона –сопряжение электронной плотности метиленовой группировки СН2 с электронной плотностью бензольного кольца:
Билет 6
Гипо и гипер изотонические р-ры. Понятие об изоосмии. Осмоляльность и осмолярность биологических жидкостей
Изотонические растворы-р-ры, кот имеют осмотическое давление, равное осмотическому давлению жидкостей организма(крови, плазмы, лимфы)
Гипертонический раствор - ра-р с высоким осмотическим давлением. При введении его в организм , в результате разности осмотичесих давление внутри клетки начинается движение воды из клетки, до выравнивания осм. давления. При этом клетки, теряя часть воды, теряют свою фору-происходит плазмолиз. Гипертонич р-ры в медицине исп-ся для снятия отеков,для оттока гноя
Гипотонические растворы-р-ры с низким осмотическим давлением. Если ввести в организм, то жидкость будет проникать внутрь клетки, клетка разбухает и иногда не выдерживает давления и разрывается- происходит гемолиз.
Изоосмия-относительное постоянство осмотического давление в жидких средах и тканях организма, обусловленное поддержанием на данном уровне концентраций содержащихся в них в-в: электролитов, белков и т.д
Осмоляльность-мера способности р-ра создавать осмотическое давление. Осмоляльность биолог жидкостей-важный фактор поддержания гомеостаза всех органов и тканей, а на практике- интегральный показатель водно-солевого обмена, поддерживается по средствам гормона АДГ гипоталамуса
Осмоляльность измеряется мосм/кг H20, и отражает фактическое общее число частиц в 1 кг
Осмолярнгстьизм в мосл/л, определяют химич методами через определение концентрации осмотическиактивных в-в и далее рассчитывают.
Из них, продиктовать, дам знак
Имеются 3 коллоидных раствора: гидроксида железа (III), полученного гидролизом FeCl3, иодида серебра, полученного в избытке КI, и иодида серебра, полученного в избытке AgNO3.
Предложите два варианта взаимной коагуляции.
Объясните, используя формулы мицелл.
Решение
1.Формулы мицелл:
А)гидроксида железа (III), полученного гидролизом FeCl3:
[m Fe(OH)3 *nFeO+*(n-x)Cl-]+x*xCl-,
Положительно заряженный золь
Б)иодида серебра, полученного в избытке КI:
[mAgI *nI-*(n-x) К+]x- *х К+
Отрицательно заряженный золь
в)иодида серебра, полученного в избытке AgNO3:
[mAgI *nAg+*(n-x) NO3-]x+ *х NO3-
Положительно заряженный золь
3.Взаимная коагуляция наблюдается при сливании растворов противоположно заряженных золей., а именно:
- Отрицательно заряженного золя иодида серебра, полученного в избытке КI, и положительно заряженного золя иодида серебра, полученного в избытке AgNO3.;
- Отрицательно заряженного золя иодида серебра, полученного в избытке КI, и положительно заряженного золя гидроксида железа (III), полученного гидролизом FeCl3.
Дата добавления: 2018-02-28; просмотров: 1484; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
