Марганцовка в роли хамелеона
Предварительные сведения. Перманганат калия (KMnO4), в быту на-зываемый марганцовкой, один из самых сильных окислителей. В зависи-мости от среды раствора (кислая, нейтральная или щелочная) марганец восстанавливается до разных степеней окисления (Mn+2, Mn+4, Mn+6).
Порядок выполнения:
1. Налейте в три пробирки по 1 мл раствора перманганата калия KMnO4.
2. Добавьте в первую пробирку - разбавленный раствор серной кислоты H2SO4, во вторую - воду, в третью - концентрированный раствор гидроксида натрия NaOH.
3. Добавьте в каждую пробирку несколько кристаллов сухой соли сульфита натрия Nа2SО3.
Наблюдения:
Как изменилась окраска раствора в каждой пробирке?
1. Отметьте цвет растворов в кислой, нейтральной и щелочной средах.
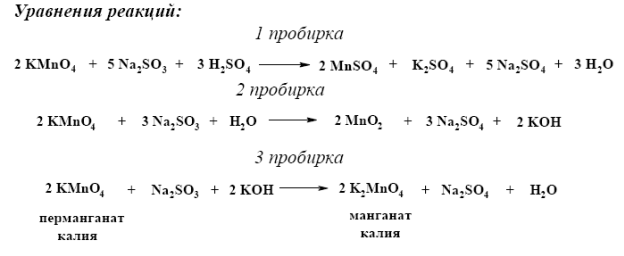
Выводы:
1. Какой тип реакции имеет место в проведенном Вами эксперименте?
2. Как влияет рН среды на состав продуктов восстановления перман-ганат-иона МnО4-?
3. Почему в разных средах происходит изменение окраски перманганат-иона МnО4-?
Дата добавления: 2015-12-17; просмотров: 20; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
