Лекция 5. Осадительное титрование. Требования к реакциям. Индикаторы. Аргентометрия.
2. Цель лекции: Изучить метод осадительного титрования и его классификацию. Рассмотреть индикаторы и кривые осадительного титрования. Изучить методаргентометрии.
3. Тезисы лекции: Осадительное титрование − метод титриметрического анализа, основанный на применении титрантов, образующих с определяемым веществом малорастворимые соединения.
Методы осадительного титрования обычно классифицируют по природе активного реагента, взаимодействующего с определяемыми веществами следующим образом: аргентометрия (AgNО3), тиоцианатометрия (KNCS или NH4NCS), меркурометрия (Нg(NO3)2), гексацианоферратометрия (K4[Fe(CN)6]), сульфатометрия (H2SO4), бариметрия (ВаС12) и др.
В осадительном титровании применяют прямое и обратное титрование.
Кривая осадительного титрования− графическое изображение изменения концентрации определяемого вещества (или титранта) в зависимости от объема прибавленного титранта (или определяемого вещества).
Кривые осадительного титрования строят в координатах рМ−V(Т) или рА−V(T). На величину скачка кривой осадительного титрования влияют концентрация растворов титруемого вещества и титранта, растворимость образующегося при титровании осадка, температура, ионная сила раствора.
В методе осадительного титрования для фиксации ТЭ используют индикаторы следующих типов: осадительные, металлохромные, адсорбционные.
Осадительные индикаторы − такие индикаторы, которые выделяются из раствора в виде осадка в хорошо заметной форме в ТЭ или вблизи ее. Известно небольшое число осадительных индикаторов. Примером осадительных индикаторов может служить хромат калия К2СrO4, используемый для аргентометрического титрования хлорид-ионов нитратом серебра.
|
|
|
Металлохромные индикаторы в осадительном титровании − индикаторы, образующие с титрантом окрашенные комплексы вблизи ТЭ. Например, соль железа (III) - железоаммонийные квасцы NH4Fe(SO4)2•12Н2O.
Адсорбционные индикаторы − такие индикаторы, адсорбция или десорбция которых осадком при осадительном титровании сопровождается изменением окраски в ТЭ или вблизи ее. Индикаторы этого типа органические вещества, которые адсорбируются осадком в ТЭ и окрашивают его. Они являются слабыми протолитами кислотного или основного характера.
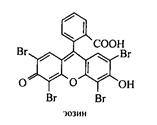
Типичные адсорбционные индикаторы − флуоресцеин и эозин (тетрабромфлуоресцеин):
Флуоресцеин 
Аргентометрия, или аргентометрическое титрование − метод осадительного титрования, основанный на использовании стандартного раствора нитрата серебра AgNО3 в качестве реагента-осадителя. В основе метода лежат осадительные реакции
|
|
|

Титрование проводят обычно в присутствии индикаторов. В качестве основного титранта метода используют стандартный раствор AgNО3, с концентрацией 0,1 и 0,05 моль/л, который стандартизируют по хлориду натрия.
В зависимости от способа проведения титрования и применяемого индикатора различают 4 метода аргентометрического титрования.
1. Метод Гей-Люссака − прямое титрование галогенид-ионов стандартным раствором нитрата серебра без индикаторов. Окончание титрования фиксируют визуально по прекращению образования осадка соли серебра и просветлению раствора. Метод дает очень точные результаты. Требует известного навыка, сравнительно продолжителен.
2. Метод Мора − определение галогенид-ионов прямым титрованием раствором нитрата серебра в присутствии индикатора − раствора хромата калия. Применяется для определения Сl-, Вr-. Однако метод не позволяет определять I- и NCS-, так как при титровании происходит соосаждение хромата калия с осадками AgI или AgNCS. Определению мешают катионы образующие осадки хроматов, а также анионы, дающие осадки солей серебра.
3. Метод Фаянса – Фишера – Ходакова – определение галогенид-ионов прямым титрованием раствором нитрата серебра в присутствии адсорбционных индикаторов − флуоресцеина, эозина и др. Метод позволяет определять хлориды, бромиды, иодиды, цианиды, тиоцианаты.
|
|
|
4. Метод Фольгарда − обратное титрование избытка катионов серебра раствором тиоцианата аммония NH4NCS или калия KNCS в присутствии индикатора − железоаммонийных квасцов NH4Fe(SO4)2•12Н2O. Применяется для определения галогенид-ионов, CN-, SCN-, S2-, СО32-, С2О42- и др.
Из всех методов осадительного титрования аргентометрия − наиболее распространенный в аналитической практике метод. Его используют в анализе как органических, так и неорганических веществ. Аргентометрия применяется для анализа таких фармацевтических препаратов, как NaCl, NaBr, KBr, NaI, KI, спиртовых растворов иода, эфедрина гидрохлорида, галогенпроизводных органических веществ (после перевода галогена в ионогенное состояние, например, нагреванием со щелочью) − бромизовала, карбромала, бромкамфоры. Аргентометрически анализируют барбитураты − производные ди-оксопиримидина. Анализ основан на том, что однозамещенные соли серебра растворимы, а двузамещенные − нерастворимы в воде. В слабо щелочной среде (в присутствии Na2CO3) титруют анализируемый раствор, содержащий определяемый препарат, стандартным 0,1 моль/л раствором нитрата серебра до образования мути, не исчезающей при взбалтывании смеси.
|
|
|
4. Иллюстративный материал:


Рис.1 Кривая титрования 100 мл Рис.2. Cравнение кривых титрования-
0,1моль/л раствора NaСl вания 0,1моль/л растворов КСl, 0,1моль/л раствором AgNO3 KBr, KI 0,1моль/л раствором AgNO3.
5. Литература:
Основная: 1, 2, 3, 4, 5.
Дополнительная: 7, 8.
6. Контрольные вопросы:
· Сущность и классификация методов осадительного титрования.
· Индикаторы осадительного титрования.
· Расчет, построение и анализ кривых осадительного титрования.
· Аргентометрия.
· Тиоцианатометрия.
Дата добавления: 2016-01-05; просмотров: 244; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
