Лекция 4. Применение ЗДМ к кислотно-основным равновесиям. Протолитическая теория растворов. Расчет рН и рОН сильных и слабых кислот и оснований.
2. Цель лекции: Дать понятие о протолитической теории растворов. Рассмотреть применение ЗДМ к кислотно-основным равновесиям.
3. Тезисы лекции: Согласно протолитической теории кислот и основаниий Бренстеда-Лоурикислота является донором протона, а основание − акцептором протона; кислоты и основания существуют как сопряженные пары; протон Н+ в водном растворе не существует, а образует ион Н3О+. Т.о., кислота − это вещество, выделяющее при ионизации протоны, а основание − вещество, присоединяющее протоны.В рамках этой теории кислотами и основаниями могут быть катионы, анионы или нейтральные молекулы. Вещества − переносчики протонов называют протолитами.
Рассмотрим, следуя протолитической теории Бренстеда-Лоури, процесс обратимого перехода одноосновной кислоты в однокислотное основание в растворе:
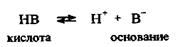 (1.1)
(1.1)
Здесь НВ и В- являются соответственно кислотой и основанием, причем они называются сопряженными кислотой и основанием.
Реакциями протолиза н азывают реакции кислот или оснований с растворителем с участием протонов.
Прототропными называют такие реакции, в которых переносчиками протонов служат не молекулы воды, а частицы других веществ.
Вещества, способные как присоединять, так и отдавать протоны, называются амфолитами. Примерами амфолитов могут служить вода, гидрокарбонат-ион HCO3-.
В самой жидкой воде устанавливается протолитическое равновесие (автопротолиз воды):
|
|
|
 или Н2О ↔ Н+ +ОН- (1.2)
или Н2О ↔ Н+ +ОН- (1.2)
Процесс диссоциации воды описывается константой химического равновесия
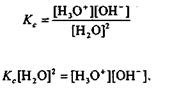 (1.3)
(1.3)
При постоянной температуре константа химического равновесия постоянна: Кс = const. Концентрация воды в чистой воде также постоянна и равна 55,55 моль/л, т. е. [Н2О]2 = const. Произведение Кс[Н2О] = const = Kw. Тогда для автопротолиза воды имеем:
Kw = [Н3О+][ОН-] или Kw = [Н+][ОН-] (1.4)
Величина Kw, называется константа автопротолиза воды или ионное произведение воды. Она постоянна при постоянной температуре. При повышении температуры степень ионизации жидкой воды увеличивается и значение Kw, растет.
В растворах слабых электролитов устанавливается равновесие между ионами и непродиссоциированными молекулами.
Для диссоциации слабой одноосновной кислоты уравнение протолиза имеет вид:
HB + H2O↔B- +H3O+,
тогда истинной термодинамической константой К этого равновесия будет
 (1.5)
(1.5)
Так как a (Н2O) = const, тогда
 (1.6) или
(1.6) или  (1.7)
(1.7)
где все концентрации − равновесные. Здесь величина Ка называется константой кислотной диссоциации или константой кислотности.
Для многих слабых кислот числовые значения Ка очень малы, поэтому вместо величины Ка применяют силовой показатель рКа: рКа = - lg Ka (1.8)
|
|
|
Чем больше Ка (т. е. чем меньше рКа), тем сильнее кислота.
Аналогично из уравнения протолиза основания в воде выводится константа основности. Для ионизации однокислотного слабого основания В в водных растворах можно записать:

Если степень ионизации основания α «1, то за константу данного химического равновесия можно принять концентрационную константу

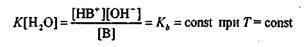
 (1.9)
(1.9)
Величина Кb называется константой диссоциации слабого однокислотного основания или просто константой основностиэтого основания, а величина
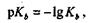 (1.10)
(1.10)
силовым показателем константы основности.
Для воды: pKw = pKa + pKb
4. Иллюстративный материал:
Таблица 1. Истинные термодинамические константы ионизации
некоторых кислот и оснований.
| Константы диссоциации слабых кислот | |||
| Кислота | Ка | рКа = | -lgKa |
| Пероксид водорода Н2О2 | 2,0.10-12 | 11,70 | |
| Сероводородная H2S | K1 = 1,0.10-7 | 6,99 | |
| К2 = 2,5.10-13 | 12,60 | ||
| Синильная HCN | 5,0.10-10 | 9,30 | |
| Угольная Н2СО3 | K1 = 4,5.10-7 | 6,35 | |
| К2 = 4,8.10-11 | 10,32 | ||
| Уксусная СН3СООН | 1,74.10-5 | 4,76 | |
| Константы диссоциации | слабых оснований | ||
| Основание | Кь | рКb= | -lgKb |
| Аммиак NH3*H2О | 1,76.10-5 | 4,755 | |
| Анилин С6Н5NН2 | 4,3.10-10 | 9,37 | |
| Бария гидроксид Ва(ОН)2 | K2 = 2,3.10-1 | 0,64 | |
| Гексаметиленгетрамин (уротропин) | 1,4.10-9 | 8,87 | |
| (CH2)6N4 | |||
| Гидразин N2H4 | 9,3.10-7 | 6,03 | |
| Гидроксиламин NH2OH | 8,9.10-9 | 8,05 | |
| Кальция гидроксид Са(ОН)2 | 4,0.10-2 | 1,40 | |
| Пиридин C6H5N | 1,5.10-9 | 8,82 | |
| Серебра гидроксид AgOH | 5,0.10-3 | 2,30 | |
| Этилендиамин NH2CH2CH2NH2 | К1 = 1,2.10-4 | 3,92 | |
| К2 = 9,8.10-8 | 7,01 |
|
|
|
5. Литература:
Основная: 1, 2, 3, 4, 5.
Дополнительная: 7, 8.
6. Контрольные вопросы:
· Протолитическая теория кислот и оснований Бренстеда-Лоури.
· Другие теории кислот и оснований (Аррениуса, Льюиса, Усановича)
· Константа автопротолиза воды.
· Константы кислотности.
· Константы основности.
· Расчет рН и рОН растворов сильных кислот и оснований.
· Расчет рН и рОН растворов слабых кислот и оснований.
Дата добавления: 2016-01-05; просмотров: 143; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
