Вольтамперная кривая (полярографическая волна)
Поскольку в вольтамперометрии один из электродов не поляризуется и для него потенциал остается постоянным, то подаваемое напряжение на ячейку проявляется в изменении потенциала только рабочего электрода. Если потенциал рабочего электрода измерять относительно потенциала электрода сравнения, условно приняв его потенциал за нуль, то Е = Еа для рабочего микроанода и Е = -Ек для рабочего микрокатода. Таким образом, регистрируемая вольтамперная кривая отражает электрохимический процесс, происходящий только на одном электроде.
Если в растворе присутствуют вещества, способные электрохимически восстанавливаться или окисляться, то при наложении на ячейку линейно изменяющегося напряжения (скорость не превышает 200 мВ/мин) кривая имеет форму волны (в отсутствии электрохимической реакции эта зависимость линейна, как следует из закона Ома). Если построить зависимость силы тока от напряжения, то получим вольтамперную волну (рис. 10).

|
| Рис. 9. Установка для вольтамперметрических измерений. |
при низких значениях потенциала (участок ОА) на рабочем электроде происходила электрохимическая реакция, через ячейку проходит очень незначительный остаточный ток, обусловленный, прежде всего, током заряжения двойного электрического слоя и присутствием в растворе электрохимически более активных, чем анализируемое вещество, примесей, при увеличении потенциала электрохимически активное вещество (деполяризатор) вступает в электрохимическую реакцию на электроде и ток в результате этого возрастает (участок АВ), это так называемый фарадеевский ток.
|
|
|
С ростом потенциала ток возрастает до некоторого предельного значения, оставаясь затем постоянным (участок ВС). Предельный ток обусловлен тем, что в данной области потенциалов практически весь деполяризатор приэлектродного слоя исчерпан в результате электрохимической реакции, а обедненный слой обогатится за счет диффузии деполяризатора из объёма раствора. Скорость диффузии в этих условиях контролирует скорость электрохимического процесса в целом. Такой ток называют предельным или диффузионным. Если из точек А и В провести параллели относительно оси абсцисс, то участок h – высота волны. Если расстояние от А до В разделить пополам и из точки D опустить перпендикуляр, то потенциал в точке К называется потенциалом полуволны (Е½), он равен ½ диффузионного тока.

|
| Рис. 10. Вольтамперная волна. |
Вольтамперограмма содержит ценную аналитическую информацию, потенциал полуволны Е½ является качественной характеристикой деполяризатора, в то время как предельный диффузионный ток линейно связан с концентрацией его в объёме раствора и является количественной характеристикой.
|
|
|
Качественный вольтамперометрический анализ. Качественной характеристикой активного вещества является величина Е½. Для этого определения снимают вольтамперную кривую исследуемого вещества на фоне определяемого электролита в интервале Е от 0 до 2,0 В. Параллельно снимают вольтамперограмму фона (он не должен давать вольтамперной волны), найденные значения сравнивают с табличными.
Однако некоторые ионы восстанавливаются ступенчато, поэтому вместо одной волны может быть две и более волны:
Cu2+ + ē → Cu+ (Е½ = - 0,25 B)
Cu+ + ē → Cu0 (Е½= - 0,54 B)
На кривых различимых качественно только те ионы, Е½ которых отличаются не менее чем на 0,2 В, в противном случае получается одна волна.
Величина Е½ может быть определена графически, как показано на рис. 7, более точно значение Е½ определяют расчетным путем, используя уравнение полярографической волны Гейровского-Ильковича. На участке полярограммы, соответствующем образованию волны, для различных значений Е определяют ток, измеряют значение предельного диффузионного тока I, вычисляют отношение I /(Iд -I). Очевидно, что при I= Iд/2 это отношение равно 1, а его логарифм равен нулю. Строят график в координатах lg I /(Iд -I), Е представляющий собой прямую линию, отсекающую на оси потенциалов величину Е½. Тангенс угла наклона этой прямой h/0,058 определяется числом электронов, принимающих участие в электрохимической реакции. Найденное таким образом значение Е½ с учётом использованного полярографического фона позволяет на основании табличных данных идентифицировать деполяризатор. Потенциал полуволны можно рассчитать по уравнению:
|
|
|
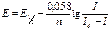 , (32)
, (32)
где Е – потенциал электрода, В; Е½ – потенциал полуволны, В; I – сила тока, мкА.
При затруднениях расшифровки полярограмм применяют метод «свидетеля»: после регистрации полярограммы анализируемого раствора к этому раствору в электролизер поочередно добавляют стандартные растворы предполагаемых соединений. Если предположение было верным, увеличивается высота полярографической волны (пика), при неверном предположении появится дополнительная волна при другом потенциале. Замена фонового электролита часто позволяет устранить мешающее влияние посторонних компонентов, наиболее эффективными оказываются комплексообразующие электролиты.
|
|
|
Количественный вольтамперометрический анализ. Количественной характеристикой анализируемого соединения в вольтамперометрии является величина предельного тока или высота волны h (пика), которая в соответствии с уравнением Ильковича является линейной функцией концентрации:
 , (33)
, (33)
где п – число электронов принимающих участие в реакции; D – коэффициент диффузии, см2/с; т – скорость вытекания ртути из капилляра, мг/с; τ – время капания, с; с – концентрация электроактивных ионов, ммоль/л.
при постоянстве условий эксперимента:
 (34)
(34)
Если скорость процесса ограничена скоростью диффузии вещества к электроду, то предельный ток равен диффузионному Iпр =Iдиф.
Для количественного определения какого-либо вещества вольтамперометрическим методом его переводят в раствор, создают определенную среду (рН), удаляют мешающие примеси (вещества, которые имеют близкие значения Е½ с деполяризатором), добавляют фон и ПАВ, удаляют растворенный кислород и проводят анализ.
Определить концентрацию деполяризатора можно одним из следующих методов.
Во всех случаях используют стандартные растворы, состав которых должен быть максимально приближен к составу раствора, условия вольтамперометрии стандартных и анализируемого растворов должен быть одинаковыми!
В методе стандартов анализируют раствор неизвестной концентрации и стандартный раствор в одних и тех же условиях анализа:
 , (35)
, (35)
где сх и сст – концентрация анализируемого и стандартного растворов; hх и hст – высота волны на вольтамперограмме этих растворов.
По методу градуировочного графика регистрируют вольтамперограмму анализируемого раствора и серии стандартных растворов, строят градуировочный график в координатах h=f(с), по которому для найденного значения hх определяют сх.
Метод добавок может быть использован только в интервале концентраций, для которых строго соблюдается линейная зависимость h=f(с). Полярографируют пробу анализируемого раствора объемом Vх, концентрация которого сх, на вольтамперограмме измеряют hх, затем в электролизер к анализируемому раствору добавляют определенный объем Vст стандартного раствора концентрации сст (необходимо следить, чтобы Vx>>Vст и сх< сст). Измеряют по вольтамперной волне высоту волны h, путем несложных преобразований уравнения Ильковича по этим данным можно рассчитать концентрацию анализируемого раствора:
 (36)
(36)
Чаще всего Vx= 9 мл, Vст= 1 мл, тогда формула (37) упрощается:
 (37)
(37)
Амперометрическое титрование. Вольтамперометрический метод анализа широко используют для индикации точки эквивалентности при титровании, а так как регистрируемым аналитическим сигналом при этом является ток, то такое титрование называют амперометрическим. Амперометрическое титрование проводят при потенциале, соответствующем предельному диффузионному току деполяризатора – одного из участников химической реакции, и регистрируют изменение тока в ходе титрования. По кривой зависимости I=f(V) находят точку эквивалентности. Амперометрическое титрование возможно при использовании химической реакции, отвечающей требованиям титриметрии, в ходе которой в объеме раствора изменяется содержание электроактивного компонента и, следовательно, в соответствии с уравнением Ильковича, предельный ток его электрохимического восстановления или окисления.
При амперометрическом титровании следует особое внимание уделять выбору фона, учитывая возможные побочные химические реакции, связанные с изменением равновесия химической реакции титрования и состояния ионов определяемого вещества и титранта в растворе.
Перед выполнением амперометрического титрования необходимо на амперометрической установке зарегистрировать вольтамперную кривую электроактивного вещества. По этой кривой выбирают потенциал для титрования, соответствующий участку предельного диффузионного тока.
Аналитические возможности метода амперометрического титрования широки. Этим методом можно определять практически все элементы периодической системы и большое число органических соединений, используя реакции осаждения, комплексообразования, окисления – восстановления и кислотно-основного взаимодействия. Основным достоинством метода является высокая избирательность, подбором потенциала достигают условий, при которых в электрохимической реакции участвует только одно вещество из многокомпонентной смеси – участник химической реакции. Нижний предел определяемых концентраций 10-6 моль/л, воспроизводимость результатов значительно лучше, чем в методе вольтамперометрии, поскольку регистрируют изменение тока в ходе титрования. По этой же причине отпадает необходимость удалять из раствора кислород и подавлять полярографические максимумы.
Метод прост и не требует сложной аппаратуры (титрование может быть проведено на любой полярографической установке).
Дата добавления: 2016-01-04; просмотров: 137; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
