Порядок выполнения работы
Для приготовления первичных и вторичных стандартов необходимо предварительно провести расчеты. Например, необходимо приготовить первичный стандарт объёмом 250 мл раствора с молярной концентрацией эквивалентов 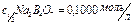 . По формуле рассчитываем необходимую массу навески:
. По формуле рассчитываем необходимую массу навески:

Мэ (Na2B4O7∙10H2O)=½(22,9∙2+10,8∙4+7∙15,9+10∙(1∙2+15,9)=½∙381,4=190,7 г/моль.
 .
.
Брать точную навеску на аналитических весах не имеет смысла, поэтому лучше взять на технических весах ~ 4-5 г тетрабората натрия (на часовом стекле), затем точно взвесить на аналитических весах и количественно перенести в мерную колбу вместимостью 250 мл. Растворяют тетраборат натрия (бура) в небольшом количестве горячей дистиллированной воды, раствор охлаждают, доводят до метки и тщательно перемешивают. Молярную концентрацию эквивалента и титр пересчитывают по точно взятой навеске.
В качестве вторичного стандарта (титранта) готовят раствор соляной кислоты приблизительной концентрации. Для этого отмеряют мерным цилиндром рассчитанный объем концентрированной кислоты и разбавляют до нужного объема дистиллированной водой, раствор тщательно перемешивают.
Например, необходимо приготовить 500 мл раствора соляной кислоты с молярной концентрацией эквивалента  . Сколько мл концентрированной соляной кислоты необходимо взять для этой цели?
. Сколько мл концентрированной соляной кислоты необходимо взять для этой цели?
Используя таблицы (см. справочник по аналит. химии), находят, что концентрированная соляная кислота имеет 38,32 %-ную концентрацию, а для приготовления 500 мл 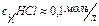 раствора необходимо взять:
раствора необходимо взять:
|
|
|

Мэ(HCl)= 1+35,5=36,5 г/моль.
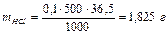
Рассчитаем, сколько необходимо взять 38,32 %-ного раствора:
 ;
;  .
.
Перейдя к объёму, получаем:  .
.
Отмеряют мерным цилиндром ~ 4 мл концентрированной соляной кислоты, переносят в мерный цилиндр вместимостью 500 мл и доводят объем раствора до метки и перемешивают.
Приготовленные растворы переносят в приготовленные стеклянные и пластиковые склянки для хранения растворов, которые предварительно тщательно моют и ополаскивают приготовленными растворами. На склянку приклеивают этикетку, в которой содержится информация о приготовленном растворе: концентрация раствора, дата приготовления, фамилия, имя, отчество и номер группы студента, который готовил раствор.
После приготовления растворов студенты тщательно моют химическую посуду, ополаскивают дистиллированной водой и сушат в сушильном шкафу; приводят в порядок рабочее место и сдают оставшиеся реактивы и посуду дежурному учебному мастеру.
Дата добавления: 2016-01-04; просмотров: 27; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
