Опыт 4.1 Гидролиз хлорзамещенных углеводородов
Реактивы, материалы, приборы: хлороформ; дихлорэтан; 10%-й раствор гидроксида натрия; 1%-й раствор нитрата серебра; азотная кислота (1:2); пробирки; водяная баня; капельницы.
В две пробирки наливают по 1 см3 10 %-го раствора гидроксида натрия и добавляют: в первую – 0,5 см3 хлороформа, во вторую – 0,5 см3 дихлорэтана. Смесь нагревают на водяной бане при 60 ºС в течение 10 мин, подкисляют разбавленной HNO3 (1:2), добавляют по 2-3 капли 1%-го раствора нитрата серебра. В условиях опыта гидролиз происходит не полностью, часть исходного вещества остается без изменения. Образуются соответственно этиленгликоль и формиат натрия:
С lCH2CH2Cl + 2NaOH ¾ ® Н OCH2CH2OH + 2NaCl
CHCl3 + 4 NaOH ¾ ® HCOONa + 3NaCl + 2H2O
Наблюдение:
Выводы:
Опыт 4.2 Различная реакционная способность хлорбензола
и хлористого бензила
Реактивы, материалы, приборы: хлорбензол; хлористый бензил, 10%-й раствор гидроксида натрия, 1%-й раствор нитрата серебра, азотная кислота (1:2), пробирки, водяная баня, капельницы.
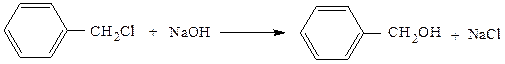
В две пробирки наливают по 1 см3 10%-го раствора гидроксида натрия, в одну добавляют 0,5 см3 хлорбензола, а в другую – 0,5 см3 хлористого бензила. Нагревают на водяной бане при кипении в течение 10 мин, подкисляют разбавленной HNO3 (1:2) и добавляют по 2-3 капли 1%-го раствора нитрата серебра.
Отмечают образование хлорида серебра в пробирке с хлористым бензилом и отсутствие осадка в случае хлорбензола.
|
|
|
AgNO 3 + NaCl ¾ ® AgCl ↓ + NaNO 3
Наблюдение:
Выводы:
Опыт 4.3 Образование и гидролиз алкоголятов
Реактивы, материалы, приборы: этанол, металлический натрий, фенолфталеин, пробирки, капельницы, пробка с газоотводной трубкой, мерные пробирки.
В сухую пробирку наливают 2 см3 этанола, вносят кусочек (не более размера горошины) очищенного от оксидной пленки металлического натрия. Пробирку закрывают пробкой с газоотводной трубкой, конец которой оттянут. Через 1-2 мин после начала реакции осторожно поджигают выделяющийся водород. После окончания реакции (в пробирке не должно быть натрия!) добавляют 1,5-2 см3 воды и 1-2 капли фенолфталеина. Наблюдают образование малиновой окраски раствора, что доказывает наличие его щелочной среды.
2R–OH + 2Na ¾ ® 2R–ONa + H2 ↑
R–ONa + H2O ¾ ® R–OH + NaOH
Наблюдение:
Выводы:
Опыт 4.4 Реакция многоатомных спиртов с
гидроксидом меди (II)
Реактивы, материалы, приборы: этанол, этиленгликоль, глицерин, маннит, 1%-й раствор сульфата меди, 10%-й раствор гидроксида натрия, пробирки, мерные пробирки.
Гидроксид меди (II) получают смешиванием 3 см3 1%-го раствора сульфата меди с 3 см3 10%-го раствора гидроксида натрия. Он образуется в виде студенистого светло-голубого осадка. Его разливают в четыре пробирки. В первую пробирку добавляют 1 см3 этанола. Растворения и изменения окраски гидроксида меди (II) не происходит. Во вторую и в третью пробирки добавляют по 1 см3 этиленгликоля и глицерина, а в четвертую – 0,5 г кристаллического маннита. Многоатомные спиртырастворяют свежеприготовленный осадок Cu(OH)2 c образованием темно-синих растворов комплексных соединений меди (II) хелатного типа:
|
|
|
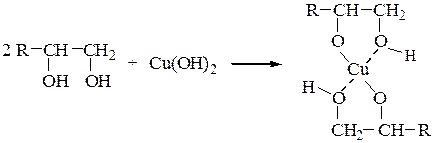
Наблюдение:
Выводы:
Опыт 4.5 Получение и свойства диэтилового эфира
Реактивы, материалы, приборы: этанол, серная кислота концентрированная, 1%-й раствор йодида калия, уксусная кислота, пробирки, спиртовки, капельницы, мерные пробирки.
а) Получение диэтилового эфира. Смешивают в пробирке 1 см3 этилового спирта с 1 см3 концентрированной серной кислоты. Разогревшуюся смесь осторожно нагревают до кипения и, прекратив обогрев, добавляют еще 5-6 капель этилового спирта. Образующийся при этом диэтиловый эфир легко обнаруживается по характерному запаху.
С H3CH2OH + HOSO3H ¾ ® С H3CH2OSO3H + H2O
С H3CH2OSO3H + HOCH2CH3 ¾ ® С H3CH2–O–CH2CH3 + H2O
б) Обнаружение пероксидов в диэтиловом эфире. Диэтиловый эфир при хранении и соприкосновении с воздухом (особенно на свету) окисляется с образованием взрывоопасных гидропероксидов:
|
|
|

Наличие пероксидов в эфире устанавливается по выделению йода из подкисленного раствора йодида калия:
ROOH + KI + 2H+ ¾ ® I2 + ROH + H2O + 2K+
К 1 см3 эфира добавляют 1 см3 1%-го раствора йодида калия, 2-3 капли уксусной кислоты и осторожно встряхивают. При наличии пероксидов через 1-2 мин эфирный слой окрашивается йодом в характерный цвет.
Наблюдение:
Выводы:
Дата добавления: 2020-04-08; просмотров: 615; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
