Опыт 3.1.1 Получение и свойства метана
Реактивы, материалы, приборы: ацетат натрия безводный, натронная известь, бромная вода, 2%-й раствор перманганата калия, пробирки, газоотводная трубка, штативы, пробирки, спиртовки.
В сухую пробирку, снабженную газоотводной трубкой, насыпают небольшое количество смеси безводного ацетата натрия и натронной извести. Пробирку закрепляют в лапке штатива почти горизонтально и нагревают вначале осторожно, а затем сильнее. Выделяющийся газ пропускают через отдельные пробирки с бромной водой и с раствором перманганата калия. Изменение окраски не наблюдается, так как метан не реагирует с этими веществами.
CH3COONa + NaO Н ¾ ® CH4 ↑ + Na2CO3
Наблюдение:
Выводы:
Опыт 3.1.2 Реакции алканов
Реактивы, материалы, приборы: петролейный эфир с т. кип. 50-70ºС, содержащий смесь пентана и гексана или вазелиновое масло (смесь высококипящих жидких алканов), 5%-й раствор карбоната натрия, 2%-й раствор перманганата калия, серная кислота концентрированная, 5%-й раствор брома в CCl4, 25%-й раствор аммиака, пробирки, стеклянная палочка, индикаторная бумага, пробирки, капельницы.
Отношение алканов к водному раствору перманганата калия. В две пробирки наливают по 1 см3 насыщенных углеводородов, 1 см3 5 %-го раствора соды, затем по каплям при встряхивании добавляют раствор KMnO4. Изменяется ли окраска перманганата калия?
Отношение алканов к концентрированной серной кислоте. В две сухие пробирки наливают по 1 см3 насыщенных углеводородов и 1 см3 концентрированной серной кислоты. Содержимое пробирок взбалтывают в течение 2-3 минут. Происходят ли изменения? Разогревается ли смесь?
|
|
|
Бромирование алканов. (РАБОТУ ПРОВОДИТЬ В ВЫТЯЖНОМ ШКАФУ) . В сухие пробирки наливают по 1 см3 насыщенных углеводородов и добавляют несколько капель 5 %-го раствора брома в CCl4. Содержимое пробирок встряхивают при комнатной температуре. Изменяется ли окраска брома?
Затем смесь нагревают на кипящей водяной бане. Окраска брома постепенно исчезает и выделяется бромоводород. Его обнаруживают по изменению окраски влажной индикаторной бумаги, поднесенной к пробирке, или по образованию тумана NH4Br при внесении в выделяющиеся пары стеклянной палочки, смоченной в 25 %-ном водном растворе аммиака.
Напишите уравнение реакции бромирования 3-метилпентана и разберите ее механизм.
Наблюдение:
Выводы:
Опыт 3.1.3 Получение и свойства этилена
Реактивы, материалы, приборы: этанол, серная кислота, концентрированная, натронная известь, раствор перманганата калия, бромная вода, пористая глина, хлоркальциевая трубка, изогнутая стеклянная трубка, спиртовка, пробирки, мерные пробирки.
|
|
|
В пробирку наливают 5 см3 смеси этанола и концентрированной серной кислоты, взятых в соотношении 1:2, для равномерного кипения бросают несколько кусочков пористой глины и через хлоркальциевую трубку, наполненную кусочками натронной извести (для связывания образующихся также CO2 и SO2), подсоединяют к стеклянной изогнутой трубке. Пробирку со смесью нагревают. Образующийся этилен пропускают в отдельные пробирки с раствором перманганата калия и бромной водой. Обесцвечивание растворов указывает на протекание следующих реакций:
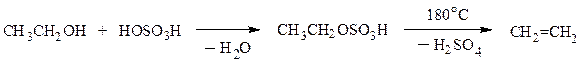
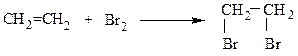

По окончании опыта отставляют горелку и тотчас же разбирают прибор во избежание засасывания раствора щелочи в смесь этилового спирта с серной кислотой.
Рассмотрите механизм электрофильного присоединения бромирования и окисления этилена при различных условиях:
Наблюдение:
Выводы:
Опыт 3.1.4 Свойства жидких ненасыщенных
углеводородов
Реактивы, материалы, приборы: бензин или керосин как источники непредельных углеводородов или скипидар, 5%-й раствор брома в CCl4, 2%-й раствор перманганата калия, серная кислота концентрированная, 10%-й раствор соды, индикаторная бумага, пробирки, капельницы.
|
|
|
Бромирование алкенов. В сухие пробирки наливают по 1 см3 алкенов и добавляют по каплям при встряхивании 5%-й раствор брома в CCl4. Если желтая окраска брома исчезает медленно, смесь осторожно подогревают. Цвет влажной индикаторной бумажки, поднесенной к пробирке, не изменяется.
Напишите уравнение реакции бромирования 2-метилпентена-2 и рассмотрите ее механизм (АЕ).
Окисление алкенов водным раствором перманганата калия (реакция Вагнера). В пробирки наливают по 1 см3 алкенов, добавляют 1 см3 10%-го раствора соды, затем по каплям при встряхивании – 2%-й раствор перманганата калия. Фиолетовая окраска исчезает, появляется бурый осадок
Напишите уравнение реакции окисления 2-метилпентена-2:
Реакции алкенов с концентрированной серной кислотой. В сухие пробирки наливают по 1 см3 алкенов, добавляют 1 см3 концентрированной серной кислоты и осторожно взбалтывают смесь в течение нескольких минут. Если смесь сильно разогревается, пробирку охлаждают водой. Слой алкена исчезает, смесь буреет.
Напишите уравнение реакции образования алкилсульфата и рассмотрите ее механизм (АЕ) на примере бутена-1:
Наблюдение:
Выводы:
Дата добавления: 2020-04-08; просмотров: 516; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
