ВОПРОСЫ ДЛЯ САМОПОДГОТОВКИ К ЗАНЯТИЮ
1. Классификация гетероциклических соединений.
2. Пятичленные гетероциклы с одним (пиррол, индол) и двумя (имидазол, пиразол) гетероатомами азота. Производные индола и имидазола, их структура и биологическая роль таутомерия имидазола. Пиразолон-5- основа ненаркотических анальгетиков.
3. Шестичленные гетероциклы с одним гетероатомом азота. Пиридин, проявление основности и нуклеофильности у атомов азота, реакции электрофильного и нуклеофильного замещения в цикле. Пиридиниевые ионы. Биологически важные производные пиридина, никотинамид, пиридоксаль, производные изоникотиновой кислоты (тубазид, фтивазид).
4. Шестичленные гетероциклы с двумя гетероатомами азота. Пиримидин, его гидрокси- и аминопроизводные: урацил, тимин, цитозин. Барбитуровая кислота.
5. Конденсированные гетероциклы. Пурин, его гидрокси- и аминопроизводные, гипоксантин, ксантин, мочевая кислота, таутомерия, ураты.
6. Понятие об алкалоидах. Простейшие представители: никотин. Пуриновые алкалоиды: теофиллин, теобромин, кофеин. Представление о строении морфина, хинина, кокаина, атропина.
ЛИТЕРАТУРА:
[1]. Тюкавкина Н.А., Биоорганическая химия. / Н.А.Тюкавкина, Ю.И. Бауков– М.: Медицина, 1991.– С. 275-308.
[2]. Гидранович Л.Г. Биоорганическая химия: Учеб. пособие. /Л.Г.Гидранович. – Витебск: ВГМУ, 2009.– С. 154-171.
[3]. Гидранович Л.Г. Лабораторные занятия по биоорганической химии.: Учеб. пособие / Л.Г.Гидранович. – Витебск: ВГМУ, 2012.– С. 77-83.
|
|
|
[4]. Гидранович Л.Г. Курс лекций по биоорганической химии.– Витебск.– 2003.– С. 132-150.
ЗАДАНИЯ ДЛЯ КОНТРОЛЯ САМОПОДГОТОВКИ К ЗАНЯТИЮ.
1. Изучить теоретический материал по вопросам для самоподготовки к занятиям.
2. Оформить протокол лабораторной работы.
3. Решить задачи 3,6,9-12,15, представленные на страницах 80-83 данного лабораторного практикума.
Примерный вариант заключительного контроля:
1. Сравните реакционную способность в реакциях SЕ пиррола и фурана. Напишите схему реакции нитрования более активного из них. Опишите механизм реакции по стадиям.
2. Напишите схемы реакций, обозначьте графически реакционные центры, укажите тип и механизм реакций:

СОДЕРЖАНИЕ ЛАБОРАТОРНОГО ПРАКТИКУМА.
Опыт 1. Окисление анальгина.
К 5 каплям анальгина добавьте 3 капли раствора НСl и 1 каплю КIO3 или FеCl3. Встряхните. Появляется окрашивание. Добавьте еще 1-2 капли КIО3. Фиксируйте изменения.
Схема реакции:
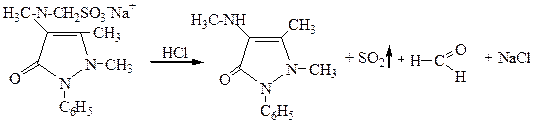

Вопросы:
1. Чем обусловлено появление бурого осадка в реакции окисления анальгина?
Опыт 2. Растворимость мочевой кислоты и ее натриевой соли в воде.
Поместите в пробирку небольшое количество (на кончике лопаточки) мочевой кислоты. Прибавьте по каплям воду, каждый раз встряхивая пробирку. Обратите внимание на плохую растворимость мочевой кислоты в воде. В холодной воде мочевая кислота почти нерастворима: 1 часть ее растворяется в 39000 частях воды. После добавления 8 капель воды растворения все еще не заметно. Стоит, однако добавить всего 1 каплю 2 н NaOH, как мутный раствор моментально просветляется вследствие образования относительно легко растворимой двузамешенной натриевой соли мочевой кислоты.
|
|
|
Полученный раствор сохраните для следующего опыта.
Схема реакции:

Вопросы:
1. Напишите таутомерные формы мочевой кислоты.
2. Сравните силу кислотных центров мочевой кислоты в разных таутомерных формах.
Опыт 3. Образование труднорастворимого урата аммония.
К прозрачному раствору средней двузамещенной натриевой соли мочевой кислоты, полученному в предыдущем опыте, добавьте 1 каплю насыщенного раствора хлорида аммония. Немедленно выпадает осадок мочекислого аммония.
Схема реакции:

Вопросы:
1. Каково физиологическое значение уратов аммония в организме человека?
Опыт 4. Общие реакции на алкалоиды.
Поместите в пробирку 1 каплю 1% раствора солянокислого хинина. Добавьте 5 капель воды. С помощью пипетки нанесите на предметное стекло 3 капли полученного раствора хинина, расположив их на некотором расстоянии друг от друга. К первой капле добавьте сбоку 1 каплю раствора йода в йодиде калия, ко второй- 1 каплю 0,5% раствора танина и к третьей- 1 каплю насыщенного раствора пикриновой кислоты. Во всех случаях в месте соприкосновения с реактивом образуются осадки.
|
|
|
К приведенным реактивам прибегают в первую очередь при судебно – медициском исследовании, когда имеется подозрение на отравление алкалоидами.
Схема реакции:
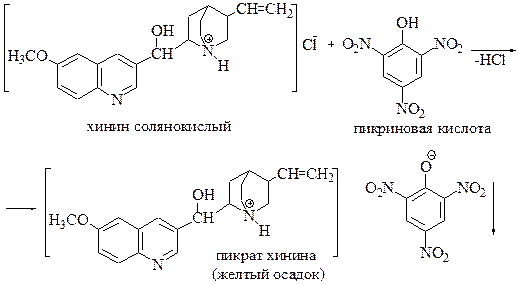
Вопросы:
1. Какой реакционный центр хинина участвует в реакциях солеобразования?
2. Для каких целей может быть использована данная реакция?
Дата добавления: 2019-09-13; просмотров: 598; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
