Соединения с комплексным катионом
А). Получение комплексного соединения меди с аммиаком.
Поместите в пробирку 5-6 капель сульфата меди СuSО4 и осторожно добавьте по каплям раствор аммиака NН4ОН до выпадения голубого осадка Cu(ОН)2. К осадку прибавьте еще несколько капель раствора аммиака до полного его растворения вследствие образования комплексных катионов  .
.
Б). Получение комплексного соединения серебра с аммиаком.
Поместите в пробирку 3-4 капли раствора хлорида натрия NаСl и добавьте по каплям раствор нитрата серебра АgNО3 до выпадения осадка АgСl. Затем прибавьте к осадку несколько капель раствора аммиака до его полного растворения вследствие образования комплексных катионов 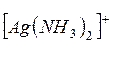 .
.
К опытам А) и Б) напишите уравнения реакций:
1) взаимодействия сульфата меди и раствора аммиака (2 уравнения),
2) взаимодействия хлорида натрия и нитрата серебра,
3) взаимодействия хлорида серебра и раствора аммиака,
4) электролитической диссоциации комплексных соединений и
комплексных ионов. Выразите константы нестойкости комплексных ионов.
Опыт № 2
Соединения с комплексным анионом
Поместите в пробирку 3-4 капли раствора нитрата висмута Вi(NО3)3 и прибавьте по каплям раствор йодида калия КI до выпадения осадка ВiI3. К осадку прибавьте несколько капель раствора йодида калия до его полного растворения. Составьте уравнения реакций (два уравнения), зная, что состав образующегося комплексного соединения КI×BiI3.
|
|
|
Опыт № 3
Прочность комплексных ионов
Возьмите две пробирки и налейте в одну 3-4 капли раствора хлорида железа FеСl3, в другую — столько же раствора  . Добавьте в каждую пробирку по 3-4 капли раствора роданида калия КSCN. Наблюдайте окрашивание раствора в красный цвет в первой пробирке, обусловленное образованием роданида железа Fе(SCN)3. Напишите уравнение реакции, протекающей в первой пробирке. Объясните отсутствие окрашивания во второй пробирке, сделав вывод о прочности комплексного иона.
. Добавьте в каждую пробирку по 3-4 капли раствора роданида калия КSCN. Наблюдайте окрашивание раствора в красный цвет в первой пробирке, обусловленное образованием роданида железа Fе(SCN)3. Напишите уравнение реакции, протекающей в первой пробирке. Объясните отсутствие окрашивания во второй пробирке, сделав вывод о прочности комплексного иона.
Контрольные вопросы
1. Какие соединения называются комплексными?
2. Как классифицируются комплексные соединения?
3. Что называется комплексообразователем? Лигандами?
4. Что называется координационным числом? Какие значения оно имеет? Чему равно К.Ч. в соединениях:
 ;
;  ?
?
5. Чему равна величина и знак заряда комплексных ионов:

6. Какой комплексный ион прочнее  если константа нестойкости первого иона 1×10-21, а второго 7,2×10-8?
если константа нестойкости первого иона 1×10-21, а второго 7,2×10-8?
Лабораторная работа № 4
ОПРЕДЕЛЕНИЕ ТЕПЛОТЫ ГИДРАТАЦИИ СОЛИ
Теоретическая часть
Химические процессы протекают обычно с выделением или поглощением энергии, формы проявления которой могут быть различны (теплота, электричество, свет и т.д.). Наиболее часто в химии приходится встречаться с процессами, сопровождающимися тепловыми явлениями. Изучением этих процессов занимается термохимия.
|
|
|
Чтобы отразить энергетические изменения, происходящие при химических реакциях, агрегатных и полиморфных превращениях веществ, процессах образования и разбавления растворов, пользуются термохимическими уравнениями, которые записывают как обычные уравнения, но с указанием величины и знака теплового эффекта реакции. Например, термохимическое уравнение реакции горения сероводорода имеет следующий вид:
 , DН = — 1038 кДж.
, DН = — 1038 кДж.
Выделяющаяся энергия в количестве 1038 кДж является тепловым эффектом реакции (ТЭР).
ТЭР называют количество теплоты, выделяемое или поглощаемое системой в результате химической реакции. Обычно измеряют ТЭР при постоянном давлении, т.е. изменение энтальпии (теплосодержания) DН. Тепловой эффект считается положительным, если теплота в реакции поглощается (эндотермическая реакция), т.к. это ведет к увеличению энтальпии (теплосодержания) системы (+DН). В экзотермических реакциях ТЭР отрицателен, т.к. происходит уменьшение энтальпии системы (—DН.).
Например, реакция разложения карбоната кальция
|
|
|
 , DН = + 157 кДж
, DН = + 157 кДж
сопровождается поглощением тепла, т.е. является эндотермической.
Реакция образования оксида серы(IV) из серы и кислорода
 , DН = — 297 кДж
, DН = — 297 кДж
экзотермическая, т.е. сопровождается выделением тепла.
Дата добавления: 2019-09-13; просмотров: 170; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
