Гены и наследственные болезни 4 страница
Автор ряда научно-популярных книг Рафаил Нудельман утверждает:
Каждый такой транспозон способен произвести белок, который «вырезает» его из данного места ДНК. Оказавшись благодаря этому свободным и подвижным, этот бывший кусок ДНК может заново встроиться в нее в любом другом месте, в том числе и внутри гена, что может существенно исказить работу последнего.
Вполне вероятно, что основательная «замусоренность» ДНК высших организмов как раз и является главной причиной многоэтапной передачи наследственной информации в клетках эукариот. В прокариотах матричная РНК образуется на молекулах ДНК без всяких сложностей и немедленно приступает к синтезу белка на рибосомах. А вот в ядерных клетках все совершенно иначе. Сначала они синтезируют неполноценную предшественницу матричной РНК, а потом подвергают ее решительному усекновению с помощью ферментативного аппарата. Ферменты режут молекулу РНК на короткие цепи, бо '
льшая часть которых распадается, после чего «огрызок», избавленный от ненужных пустот, выходит из ядра в цитоплазму и берется за дело. Этот процесс называется «созреванием РНК».
При внимательном изучении мусорная свалка внегенной ДНК обернулась настоящим золотым дном. Чуть больше года назад в джанке нашли удивительные микроскопические фрагменты – снипсы (от англ. SNP, single-nucleotide polymorphism – «однонуклеотидный полиморфизм»). Чтобы разобраться в этом, нужно сначала вспомнить, что молекула ДНК (и ген как ее часть) построена из азотистых оснований четырех типов – аденина (A), тимина (T), цитозина (C) и гуанина (G).
|
|
|
Дальше предоставим слово Рафаилу Нудельману:
Представим себе кусочек цепочки с таким, например, чередованием нуклеотидов: AAGGTTA. Допустим, что по каким-то причинам эта же цепочка у другого человека приняла вид ATGGTTA, где на втором месте взамен нуклеотида A встал нуклеотид T. Вот такая одиночная (точечная) замена и называется «снипсом». В данном конкретном случае говорят, что у этого отрезка ДНК есть две «аллели» (то есть две разновидности): A и T. Практически все выявленные снипсы имеют только две аллели (это значит, что почти у всех людей на данном отрезке A может быть заменено только на T, но не на G или C). Но таких «точек замены» может быть много, поэтому, двигаясь вдоль молекул ДНК каждого человека, мы обнаружим некую специфичность, свойственную ему последовательность таких замен. В сумме они образуют его «снипсовый профиль».
Поскольку в человеческом геноме содержится как минимум около трех миллиардов нуклеотидов, а снипсовые замены составляют примерно один процент, не составит большого труда отыскать по крайней мере около 30 миллионов точечных локусов, где имеется некоторый вполне ощутимый разнобой. Другими словами, индивидуальный снипсовый профиль – вещь вполне реальная, поскольку число возможных сочетаний однонуклеотидных замен астрономически велико. Это напоминает дактилоскопию, но только на уровне тонких генетических расхождений, поскольку совершенно невозможно себе представить двух разных людей с абсолютно идентичным снипсовым профилем.
|
|
|
Если бы все дело ограничивалось впечатляющими, но бесполезными цифрами, снипсам не уделили бы должного внимания. Однако совсем недавно выяснилось, что эти неуловимые различия ассоциированы с генетической предрасположенностью людей к тем или иным болезням. Речь, разумеется, не о том, что снипсы могут выступать в роли неких болезнетворных генов. Они всего лишь маркеры, своего рода опознавательные метки некоторых патологических состояний, помогающие специалистам выявить болезнь, вызываемую совокупным действием нескольких генов.
На подозрении оказались сахарный диабет обоих типов[8], некоторые разновидности злокачественных новообразований, глаукома, различные аутоиммунные болезни, рассеянный склероз и т. д. Поскольку во всех этих случаях удалось выявить статистически значимую связь «снипсового профиля» человека с его предрасположенностью к той или иной болезни, на повестку дня встал вопрос о тестировании граждан на предмет вероятности подцепить какую-нибудь хворь.
|
|
|
Иными словами, речь идет о своего рода генной диагностике, что позволит в перспективе подбирать лечение индивидуально. Например, абсолютной реальностью станет прицельная фармакотерапия, когда лекарственные препараты будут назначать в зависимости от чувствительности к ним больного. Но ведь можно поступить куда более радикально: научиться ремонтировать дефектные гены или, по крайней мере, вычеркивать из генома те из них, которые отвечают за тяжелые наследственные недуги. Однако сначала нужно как следует разобраться с взаимовлиянием генотипа и среды обитания, вычислить удельный вес наследственно обусловленных качеств.
Классическая формула «ДНК – РНК – белок» сегодня выглядит довольно наивной. Реальная картина оказалась гораздо сложнее. Помните микро-РНК, которые вмешиваются в работу генов? Сначала их обнаружили у растений и некоторых примитивных животных вроде круглого червя C. elegans[9] – крохи около миллиметра длиной. Микро-РНК (они и в самом деле очень невелики и состоят всего из 21–25 оснований) связываются с путешествующей в цитоплазме матричной РНК и блокируют ее работу. На матричной РНК, как мы помним, записана инструкция по производству белка, но если к ней прицепилась микро-РНК, белковый синтез тормозится. Налицо прямое воздействие на генетический аппарат клетки (ибо гены в первую очередь заняты регуляцией синтеза белка), о котором совсем недавно цитологии даже не подозревали!
|
|
|
Чуть более 10 лет назад микро-РНК обнаружили и у человека. На сегодняшний день в человеческом геноме найдено около 700 микро-РНК, и по оценкам ученых, скоро это число дойдет до 1000. Между тем у нас всего лишь около 20 тысяч генов, кодирующих белки. Если же допустить, что каждая микро-РНК может влиять на работу нескольких генов (установлено, что они могут связываться сразу с несколькими типами матричной РНК), то под контроль этих крошечных молекул попадает треть человеческого генома. Одним словом, перед нами система регуляции невообразимой сложности, поскольку микро-РНК влияют не только на матричную РНК, но и друг на друга.
Уже нащупываются терапевтические подходы, использующие микро-РНК. Например, блокируя miR122, можно регулировать синтез холестерина и лечить гепатит. Опыты на животных показали: уровень холестерина в крови снижается на 40 %. Онкологи тоже заинтересовались малыми РНК, поскольку выяснилось, что при некоторых лейкозах они синтезируются в повышенных количествах. Если же их заблокировать, то можно затормозить опухолевый рост. А при других формах рака наблюдается падение уровня микро-РНК, причем именно таких, которые подавляют активность онкогенов. Кроме того, введение некоторых микро-РНК повышает чувствительность опухолевой ткани к радиации и химиотерапевтическим препаратам. А совсем недавно было показано, что малые РНК определенного типа способны блокировать работу генов вируса иммунодефицита человека (ВИЧ). Вполне вероятно, что лет через восемь-десять появятся первые лекарственные препараты на основе микроРНК для лечения СПИДа и рака.
Гены, бактерии, вирусы

При слове «бактерия» у людей, далеких от биологии, возникают самые неприятные ассоциации. На памяти человечества – жуткие инфекционные напасти вроде опустошительной эпидемии «черной смерти», выкосившей в XIV столетии более 30 % населения Европы. Но это только средние цифры: в Норвегии умерли четыре пятых всего населения, а некоторые европейские страны совершенно обезлюдели. По мнению специалистов, это была вторая пандемия[10] чумы. Первая случилась в Византии, в годы правления императора Юстиниана (VI век новой эры), и потому называется юстиниановой. Третья пандемия пришлась уже на вполне исторические времена. Она началась в Гонконге в 1894 году и растянулась почти на три десятилетия, захватив большие портовые города. Именно тогда был открыт возбудитель инфекции – палочка под названием Yersinia pestis.
Микробиология делала большие успехи, но и в новые времена вспышки инфекционных болезней всегда были непременными спутниками социальных потрясений. Достаточно вспомнить хотя бы азиатскую холеру, разразившуюся в Европе в середине XIX века, или тифы – брюшной и сыпной – на фронтах Первой мировой и Гражданской войны. И даже сегодня, когда большинство грозных инфекций вроде бы давным давно канули в небытие, мы продолжаем сталкиваться с сальмонеллами, вызывающими тяжелые пищевые отравления, или с вездесущими стафилококками, прозванными чумой XX века.
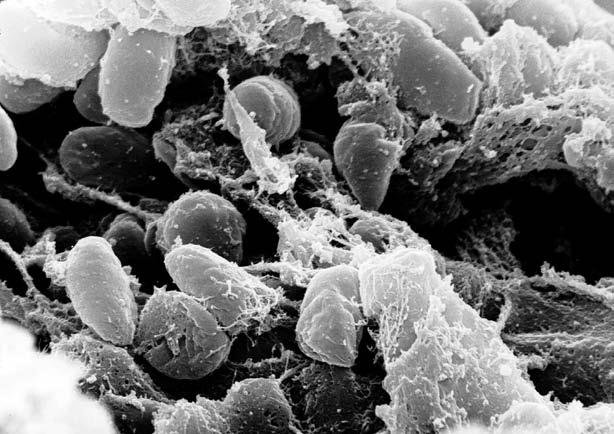
Чумная палочка под микроскопом
Однако не стоит демонизировать микробов. Уже к началу ХХ века биологи знали, что бактерии распространены повсеместно, а совокупность их маленьких тел образует тот незримый фундамент, на котором покоится весь органический мир[11]. Если этот микробный фундамент необратимо разрушить, то через короткое время рухнет и вся величественная пирамида жизни на планете Земля. Разумеется, патогенные (болезнетворные) бактерии способны доставить человеку массу неприятностей, но все же большая часть микробов приносит нам скорее пользу, чем вред.
Огромное количество различных микроорганизмов населяет почву. По некоторым оценкам, в одном грамме плодородного чернозема их содержится несколько миллиардов. На одном гектаре пахотной земли проживает около трех тонн микробов! А суммарная масса всех микробов нашей планеты примерно в 25 раз превышает массу всех животных.
Функции этих крох многообразны. Например, так называемые клубеньковые бактерии, или ризобии, селятся на корнях бобовых растений и специализируются на фиксации атмосферного азота, который растению жизненно необходим. Такое взаимовыгодное сотрудничество называется симбиозом . Растение снабжает клубеньковые бактерии питательными углеводами, а взамен получает азот, ценные витамины и некоторые вещества роста. Естественно, бобовые – не единственные растения, сумевшие «приручить» полезных азотфиксаторов, поскольку ботаникам известны по крайней мере шесть семейств высших цветковых растений, которые охотно прибегают к услугам одноклеточных накопителей азота. Правда, природа этих симбионтов пока окончательно не установлена.
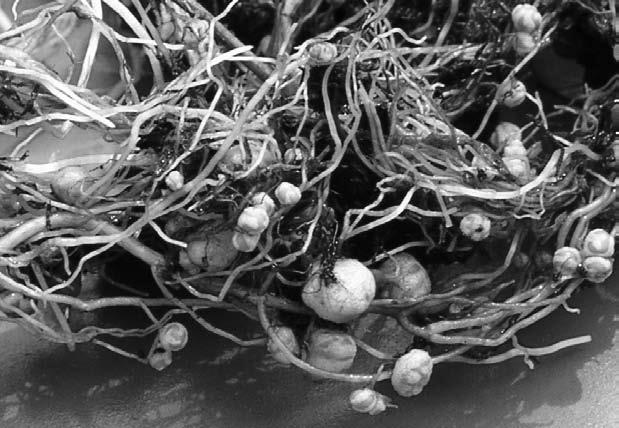
Клубеньковые бактерии (ризобии) под микроскопом
Организмы животных – от членистоногих до человека – тоже основательно «нафаршированы» разнообразной микрофлорой. Пугаться этого не стоит, ибо в абсолютном большинстве случаев это не вторжение извне безжалостного врага, а взаимовыгодный симбиоз, обеспечивающий виду эволюционное преимущество.
Например, термиты способны запросто переваривать не только древесину, но и всякие другие малосъедобные вещи. Причем исключительно благодаря постоянным обитателям их задней кишки – жгутиконосцам, спирохетам и бактериям. Состав кишечной микрофлоры термита уникален и не встречается у насекомых других видов. Если «постояльцев» кишечника термита убить (такие опыты неоднократно проделывались), и посадить искалеченное насекомое на привычную диету из древесных опилок и фильтровальной бумаги, то оно довольно быстро погибнет.
Очевидно, что секрет пищеварения этих удивительных насекомых теснейшим образом связан с естественными обитателями их кишечника. Когда ученые догадались высадить одноклеточных симбионтов термита на питательную среду, то без труда сумели получить особый фермент, эффективно разлагающий целлюлозу.
А электронно-микроскопическое исследование кишечника термитов позволило обнаружить целый зоопарк, работающий в поте лица над перевариванием пищи. Главной фигурой кишечного симбиоза оказался жгутиконосец, облепленный со всех сторон колышущимися спирохетами и палочковидными бактериями, а внутри его тела удалось разглядеть еще какие-то мелкие бактерии. Дружные усилия этой компании позволяют термиту с легкостью переваривать самые невообразимые вещи.
В человеческом организме бактерий тоже хоть отбавляй. Подсчитано, что в одном кубическом сантиметре желудочного содержимого обитает примерно 25 тысяч бактерий, а в одном грамме содержимого толстого кишечника (попросту говоря, в каловых массах) их на несколько порядков больше – до 30–40 миллиардов. По мнению специалистов, одноклеточные организмы, населяющие полости и ткани человека, представлены более чем 250 видами различных микробов.
Разумеется, все это гигантское бактериальное сообщество – отнюдь не бесполезные нахлебники, а наши верные друзья, добросовестно и неутомимо синтезирующие аминокислоты, витамины и ферменты, жизненно необходимые для нашего повседневного существования. Они выполняют и важную барьерную функцию, противодействуя вторжению патогенных микроорганизмов – дизентерийных, брюшнотифозных, гнилостных и прочих. Более того, сбалансированная и разнообразная кишечная микрофлора – бесспорный показатель здоровья.
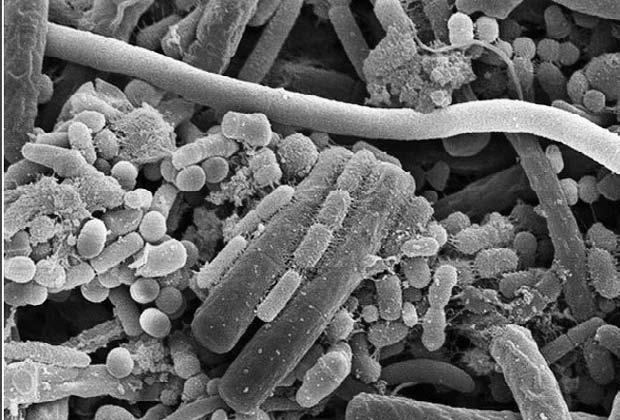
Микрофлора кишечника человека под микроскопом
К сожалению, мы часто относимся к нашим симбионтам без должного уважения. Едва ли нужно напоминать, что неумеренный прием антибиотиков по поводу и без повода, выкашивающий целые популяции полезных микроорганизмов, сплошь и рядом приводит к развитию тяжелого дисбактериоза, справиться с последствиями которого оказывается весьма и весьма непросто.
Бактерии, как мы помним, относятся к числу доядерных организмов – прокариот, ибо оформленного ядра у них нет. Их ДНК, которую принято называть нуклеоидом , или бактериальной хромосомой (хотя с хромосомами эукариотических клеток она не имеет ничего общего), представляет собой собранную в клубок двойную спираль, замкнутую в кольцо. Этот эквивалент клеточного ядра свободно плавает в цитоплазме, не имеет собственной мембраны и не содержит белков, хотя обычно зафиксирован на мембране бактериальной клетки. При этом гены внутри нуклеоида расположены в линейном порядке, как и в клетке эукариот, а сам нуклеоид в функциональном отношении полностью соответствует геному ядерной клетки. Кроме того, в клетках прокариот встречаются небольшие кольцеобразные фрагменты ДНК, никак не связанные с нуклеоидом, – так называемые плазмиды .
В бактериальных клетках нет органелл, типичных для эукариотических клеток, – ни хлоропластов, ни митохондрий, ни центриолей. А рибосомы (структуры, отвечающие за белковый синтез) свободно плавают в цитоплазме, поскольку аналог эндоплазматической сети в клетках прокариот отсутствует. Размножаются они тоже иначе – амитотически, путем простого бинарного (поперечного) деления. Сначала происходит удвоение нуклеоида, причем оно всегда начинается в точке прикрепления к цитоплазматической мембране, где локализован ферментативный аппарат, за нее отвечающий. Редупликация (удвоение) ДНК запускает механизм синтеза клеточной стенки, которая растет от периферии к центру. Образуется перетяжка, и бактерия делится пополам. Деление может осуществляться не только в одной, но и в нескольких плоскостях, и тогда возникают клеточные цепочки или скопления различной формы. Вариантом бинарного деления является почкование, когда на теле материнской клетки образуется увеличивающийся вырост. Достигнув величины материнской клетки, почка отшнуровывается. В среднем бактерии делятся каждые 20 минут.
Итак, бактерия гораздо примитивнее эукариотической клетки, но рядом с вирусом она – воплощение сложности, уникальная фабрика, нацеленная на бесперебойный выпуск сотен различных белков и ферментов. А вирус даже клеточного строения не имеет. Все, что у него есть, – это молекула нуклеиновой кислоты, упакованная в белковую оболочку. Но такая конструктивная простота имеет и отрицательную сторону: чтобы продолжить свой род, вирус должен просочиться в живую клетку и завладеть всеми ее ресурсами. Без посторонней помощи он размножаться не умеет. Вне клетки-хозяина вирус мертв и не обнаруживает никаких признаков жизнедеятельности. Вирусологи называют своих подопечных строгими (облигатными) паразитами, поскольку весь их жиз ненный цикл неотделим от клетки, в которую они стремятся проникнуть.
Вирусы гораздо мельче бактерий и вообще любых одноклеточных микроорганизмов – от грибов до простейших. Поэтому их величину измеряют не в микронах, то есть миллионных долях метра, а в нанометрах (нм) – миллиардных долях метра. Другими словами, нанометр в тысячу раз меньше микрона. Например, поперечник амебы составляет примерно 50 микрон, а размеры вируса полиомиелита находятся в пределах 27–29 нанометров, то есть «по росту» он меньше амебы почти в две тысячи раз. Понятно, что отношение объемов их тел выражается еще большей цифрой со многими нулями. Самые большие вирусы достигают величин вполне «бактериальных» – например, вирус оспы человека и животных вырастает до 300 нм.
Разнообразием форм вирусные частицы (вирионы ) не отличаются: чаще всего они похожи на миниатюрные шарики с выростами на поверхности или без них, а вирусы растений часто напоминают вытянутый цилиндр. Скажем, длина цилиндра вируса табачной мозаики достигает 350 нм, но разглядеть его в оптический микроскоп все равно невозможно, поскольку толщина этого цилиндра не превышает 15 нм. Нить с практически нулевой поперечной размерностью увидеть, естественно, нельзя.
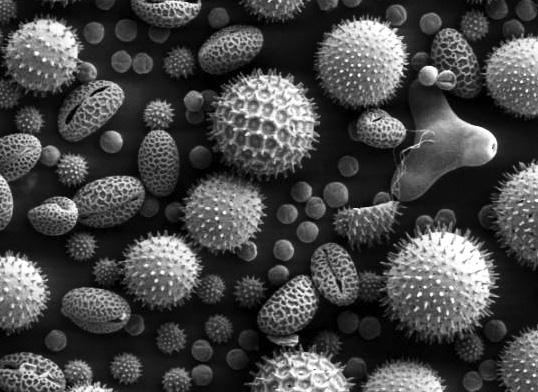
Вирусы под микроскопом
Однако ничтожные размеры большинства вирусов – далеко не самое удивительное. Гораздо интереснее тот факт, что они – единственные на Земле живые организмы, не имеющие клеточного строения. Вирус устроен настолько просто, что больше напоминает какой-то механизм, а не живое существо. В сердцевине вирусной частицы лежит нуклеиновая кислота, окруженная снаружи белковыми молекулами, которые образуют своего рода защитный чехол – капсид . Белки (или белок) оболочки вируса, как и любые другие белки, сотканы из аминокислот, уложенных в длинные цепочки. Капсид – не монолитная конструкция: он построен из отдельных субъединиц (капсомеров ), которые состоят, в свою очередь, из одной или нескольких идентичных или разных полипептидных цепей. Генетический материал в центре вириона может быть представлен любой из нуклеиновых кислот – как ДНК, так и РНК, и по этому параметру вирусы подразделяются на ДНК-содержащие и РНК-содержащие.
Вирусы различаются между собой не только по размерам, форме и строению генома (вирусная ДНК или РНК есть не что иное, как геном), но и по уровню сложности своей структуры. Если наиболее мелкие и простые вирусы состоят из обособленной молекулы РНК и белка, то у крупных вирионов можно обнаружить многослойную «упаковку», в состав которой входят не только белковые молекулы, но углеводы и липиды.
Например, конструкция бактериофагов[12], по форме напоминающих головастика или гимнастическую булаву, включает в себя шаровидную головку, где помещается нуклеиновая кислота, и полый чехол в виде длинного хвоста, собранный из молекул белка. С помощью этого выроста бактериофаг прикрепляется к оболочке бактериальной клетки, прокалывает клеточную мембрану и впрыскивает, как через шприц, свою нуклеиновую кислоту в цитоплазму бактерии.
А вирус иммунодефицита человека (ВИЧ), возбудитель СПИДа, представляет собой шарик диаметром 100 нм, поверхность которого утыкана многочисленными отростками, похожими на шляпки обойных гвоздей или головки шурупов. Это вирусный белок – гликопротеид, белково-углеводный комплекс (биологи обозначают его как gp 120), от которого зависит не только адсорбция (поглощение) вируса клеточной мембраной (а следовательно, начало инфекционного процесса), но и необычайная изменчивость вируса. Гликопротеидные «гвозди» пронизывают оболочку вируса и образуют под ней сложное переплетение, своего рода вироскелет, который сохраняет форму вириона и удерживает в определенном положении вирусную «начинку» – геном вируса.
Дата добавления: 2019-02-13; просмотров: 265; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
