Температурные параметры пожарной опасности
Температурные пределы распространения пламени (ТПР)
Температурными пределами распространения характеризуют пожарную опасность жидких горючих веществ. Нижний температурный предел распространения (НТПР) – это температура жидкости, при которой концентрация насыщенных паров над ее поверхностью равна НКПР. Аналогично при верхнем температурном пределе распространения пламени (ВТПР) концентрация насыщенных паров жидкости равна ВКПР. Из этого следует, что если для горючего вещества известны КПР, то по зависимости давления насыщенного пара от температуры могут быть найдены температурные пределы.
Допустим, известен НКПР пламени паров горючей жидкости. Необходимо найти НТПР, то есть температуру, при которой концентрация насыщенных паров над поверхностью этой жидкости будет равна НКПР. По концентрации паров φн (значение НКПР) можно найти парциальное давление насыщенных паров
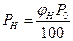 , ( 29)
, ( 29)
где P0 – атмосферное давление (общее давление паровоздушной смеси).
По давлению насыщенного пара нетрудно установить соответствующую температуру жидкости, которая и будет значением НТПР. Зависимость давления насыщенного пара от температуры для большинства жидкостей известна и приведена в справочной литературе в виде таблиц, графиков или задана уравнением Антуана lgP = f(T) (табл. 25 приложения).
Пример 9 . Определить значение НТПР метилового спирта по нижнему концентрационному пределу распространения пламени. Принять, что атмосферное давление равно нормальному (Р0 = 101,3 кПа).
|
|
|
Решение: 1. По справочнику или расчетом находят, что НКПР метилового спирта равен 6 % об. Затем определяют, какому давлению насыщенного пара соответствует значение нижнего концентрационного предела:
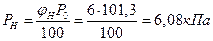 .
.
2. Для нахождения значения НТПР (Тн) по известной величине Рн можно, воспользоваться уравнением Антуана, выражающим зависимость давления насыщенного пара от температуры жидкости.
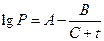 , ( 30)
, ( 30)
где Р выражено в кПа, а t в оС.
Константы уравнения Антуана приведены в табл. 25 приложения.
Решая уравнение относительно t, получают
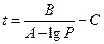 . ( 31)
. ( 31)
Для метилового спирта А = 7,3527, В = 1660,454, С = 245,818. Подставляя численные значения в уравнение (31), получают:
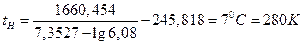
В табл. 33 приложения приведены показатели пожарной опасности некоторых жидкостей, из которой видно, что для метанола справочное значение НТПР составляет 280 К.
Температура самовоспламенения
Температура самовоспламенения Тсв, приведенная в справочниках, получена экспериментально по стандартной методике для горючей смеси стехиометрического состава. Установлено, что в пределах гомологического ряда величина Тсв является функцией длины углеродной цепи в молекуле. Чем длиннее цепь, тем ниже температура самовоспламенения. Метод расчета Тсв основан на эмпирической зависимости Тсв от средней длины углеродной цепи. Метод пригоден для расчета Т св алифатических углеводородов, алифатических спиртов и ароматических углеводородов. Задача состоит в том, чтобы по структурной формуле химического соединения найти для него среднюю длину углеродных цепей.
|
|
|
Углеродная цепь – это цепочка атомов углерода от одного конца молекулы до другого.
Длина цепи – это число атомов углерода в такой цепи.
Например, в нормальном гептане
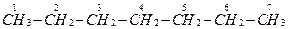
одна углеродная цепь и ее длина равна 7.
В изобутане

три цепи с одинаковой длиной (1-2-3, 1-2-4 и 3-2-4), длина каждой цепи равна 3. Средняя длина углеродных цепей в этом соединении тоже равна 3.
Определяют среднюю длину цепи, далее по табл. 29-31 приложения находят Тсв.
Например, для н-гептана Тсв = 496 К, а для изобутана Тсв = 743 К (табл. 29 приложения для предельных углеводородов).
В молекуле химического соединения со сложной структурой бывает трудно сразу найти все углеродные цепи. Поэтому для определения числа цепей используют формулу:
|
|
|
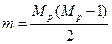 , ( 32)
, ( 32)
где Mp – число концевых функциональных групп, таких как: метил (-CH3), гидроксил (-ОH) и фенил ( 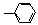 ).
).
Например, в н-гептане две группы CH3, то есть Mp=2, из формулы (32) следует, что число цепей равно 1. В изобутане Mp=3, подставляя это значение в формулу (32), получают m=3.
Пример 10. Вычислить температуру самовоспламенения 3-этил-4-изо-пропилгексана
Решение: 1. Записывают структурную формулу соединения, нумеруют все атомы углерода:
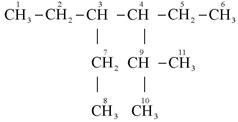
2. В молекуле соединения пять концевых метильных групп CH3, т. е. Mp = 5. Определяют число цепей:
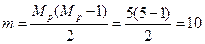
3. Находят эти цепи и устанавливают их длину. Для удобства составляют следующую таблицу
| Углеродная цепь mi | 1-6 | 1-8 | 1-10 | 1-11 | 6-8 | 6-10 | 6-11 | 8-10 | 8-11 | 10-11 |
| Длина цепи li | 6 | 5 | 6 | 6 | 6 | 5 | 5 | 6 | 6 | 3 |
4. Определяют среднее арифметическое значение длины углеродных цепей
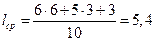
5. По табл. 29 приложения находят температуру самовоспламенения 3-этил-4-изопропилгексана по значению средней длины цепи в молекуле соединения: Тсв = 522 К = 249 0С.
Особенности расчета Т св алифатических спиртов
|
|
|
При определении длины углеродных цепей в молекуле алифатического спирта необходимо учитывать следующее правило. Гидроксильная группа в углеродной цепи увеличивает ее длину на единицу.
Пример 11. Вычислить температуру самовоспламенения 2,2-диметил-3-этилгексанола-1.
Решение:
1. Записывают структурную формулу соединения и пронумеровывают все атомы углерода, группу -ОН обозначают буквой Г (гидроксил)
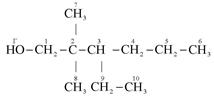
2. В молекуле пять концевых групп: четыре метильных (-CH3) и одна гидроксильная (-OH), т. е. Мр = 5. Тогда число цепей
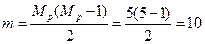
3. Составляют таблицу, в которую внесят цепи и их длину.
| Углеродная цепь mi | Г-6 | Г-7 | Г-8 | Г-10 | 7-6 | 7-8 | 7-10 | 6-8 | 6-10 | 8-10 |
| Длина цепи li | 7 | 4 | 4 | 6 | 6 | 3 | 5 | 6 | 6 | 5 |
Длина первых четырех цепей, содержащих гидроксильную группу -OH на единицу больше, чем число атомов углерода в цепи.
4. Рассчитывают среднюю длину углеродных цепей
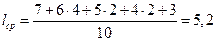 .
.
5. По табл. 30 приложения находят соответствующую температуру самовоспламенения Т0=582К = 309oС.
Особенности расчета Т св ароматических соединений
При определении числа цепей и их длины в молекуле ароматического соединения следует иметь в виду следующие правила:
1. Фенил (бензольное кольцо), находящийся внутри углеродной цепи, считается и как концевой.
2. При определении углеродной цепи атомы углерода в бензольном кольце в расчет не принимаются.
3. Фенил, находящийся в углеродной цепи, укорачивает ее на единицу.
Пример 12. Вычислить температуру самовоспламенения 1-изопропил-4-изобутилбензола.
Решение: 1. Записывают структурную формулу соединения и вводят обозначения:
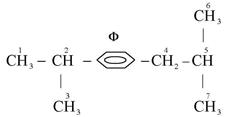
2. В молекуле соединения четыре концевые метильные группы -CH3 и одна концевая группа – фенил, т. е. Mp = 5:
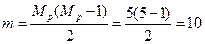 .
.
3. В этом соединении, согласно первому правилу, концевым необходимо считать и фенил. В этом случае углеродные цепи будут заканчиваться не только на метильных группах -CH3, но и на бензольном кольце. Составляют таблицу, в которую внесят углеродные цепи и их длину.
| Углеродная цепь mi | 1-6 | 1-7 | 3-6 | 3-7 | 1-Ф | 3-Ф | 6-Ф | 7-Ф | 1-3 | 6-7 |
| Длина цепи li | 4 | 4 | 4 | 4 | 1 | 1 | 2 | 2 | 3 | 3 |
Следует обратить внимание, что при определении длины цепи атомы углерода, имеющиеся в бензольном кольце, в расчет не принимаются (правило 2). У восьми углеродных цепей, которые имеют в своем составе фенил, как в середине, так и в конце цепи, длина цепи на единицу меньше, чем число атомов углерода (правило 3).
4. Рассчитывают среднюю длину углеродных цепей
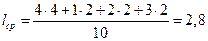 .
.
5. По табл. 31 приложения находят Тсв ароматического соединения с соответствующей длиной цепи Тсв = 698 К = 425 oС.
Пример 13. Вычислить температуру самовоспламенения 2,2-дифенилпропана.
Решение:
1. Записывают структурную формулу соединения и вводят обозначения

2. Определяют число цепей. В соединении четыре концевых группы (две метильные и две фенила), поэтому Mp = 4:
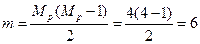 .
.
В этом соединении шесть цепей.
3. Находят эти цепи и определяют их длину
| Углеродная цепь mi | Ф1-Ф2 | Ф1-1 | Ф1-3 | Ф2-1 | Ф2-3 | 1-3 |
| Длина цепи li | -1 | 1 | 1 | 1 | 1 | 3 |
Цепи, содержащие фенил, укорачиваются на единицу. Так как в цепи Ф1–Ф2 содержится два фенила, то ее длина уменьшится на два.
4. Средняя длина цепи будет равна
 .
.
5. По табл. 31 приложения находят, что Тсв = 712 К = 439 oС.
Дата добавления: 2019-01-14; просмотров: 990; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
