Зацепка абсолютно черного тела
Джон Гриббин
В поисках кота Шредингера. Квантовая физика и реальность

«В поисках кота Шредингера. Квантовая физика и реальность / Д. Гриббин ; [пер. с англ. 3. А. Мамедъярова, Е. А. Фоменко]. Рипол классик, 2016. – 352 с.: ил. – (В поисках кота Шредингера).»: Рипол; Москва; 2016
ISBN 978-5-386-09614-4
Аннотация
Книга знаменитого британского автора Джона Гриббина «В поисках кота Шредингера», принесшая ему известность, считается одной из лучших популяризаций современной физики.
Без квантовой теории невозможно существование современной науки, без нее не было бы атомного оружия, телевидения, компьютеров, молекулярной биологии, современной генетики и многих других неотъемлемых компонентов современной жизни. Джон Гриббин рассказывает историю всей квантовой механики, повествует об атоме, радиации, путешествиях во времени и рождении Вселенной. Книга ставит вопрос: «Что есть реальность?» – и приходит к самым неожиданным выводам. Показывается вся удивительность, странность и парадоксальность следствий, которые вытекают из применения квантовой теории.
Предназначено для широкого круга читателей, интересующихся современной наукой.
Джон Гриббин
В поисках кота Шредингера. Квантовая физика и реальность
Мне все это не нравится, и я сожалею, что вообще был в этом замешан.
Эрвин Шрёдингер 1887-1961
Ничто не реально.
|
|
|
Джон Леннон 1940-1980
JOHN GRIBBIN
IN SEARCH OF SCHRÖDINGER’S CAT

Quantum Physics and Reality
Перевод с английского З. А. Мамедьярова, Е. А. Фоменко
© 1984 by John and Mary Gribbin
Благодарности
Мое знакомство с квантовой теорией состоялось более двадцати лет назад, еще в школе, когда я обнаружил, что теория оболочечного строения атома магическим образом объясняла всю периодическую систему элементов и практически всю химию, с которой я мучился на множестве скучных уроков. Я сразу же начал копать дальше, прибег к помощи библиотечных книг, как утверждалось, «слишком сложных» для моей скромной научной подготовки, и сразу же заметил прекрасную простоту объяснения атомного спектра с позиции квантовой теории и впервые открыл для себя, что лучшее в науке одновременно прекрасно и просто, а этот факт слишком многие учителя – случайно или нарочно – скрывают от своих учеников. Я чувствовал себя прямо как герой романа «Поиск» Ч. П. Сноу (хотя и прочитал его гораздо позже), который открыл то же самое:
Я заметил, как перепутанные случайные факты вдруг встали на свои места… «Но это истина, – сказал я себе. – Это прекрасно. И это истина». (Издание А, 1963, с. 27.)
Отчасти благодаря этому озарению в университете я решил изучать физику. В положенный срок мои амбиции осуществились, и я стал студентом университета Сассекса в Брайтоне. Но там простоту и красоту глубинных идей затмило многообразие деталей и математических методов решения конкретных проблем с помощью уравнений квантовой механики. Применение этих идей к миру современной физики давало, пожалуй, примерно такое же представление о глубинной красоте и истине, какое дает пилотирование Boeing 747 о дельтапланеризме. Хотя сила изначального озарения по-прежнему оказывала наиболее существенное влияние на мою карьеру, долгое время я не обращал внимания на квантовый мир и открывал для себя другие прелести науки.
|
|
|
Угольки того раннего интереса разгорелись вновь благодаря сочетанию нескольких факторов. В конце 1970-х и начале 1980-х годов начали появляться книги и статьи, которые с переменным успехом пытались объяснить странный квантовый мир далекой от науки аудитории. Некоторые из так называемых «популярных текстов» были так чудовищно далеки от правды, что я не мог даже вообразить, что найдется читатель, который поймет истинность и красоту науки, изучив их, а потому захотел рассказать все как есть. В то же время появились сведения о длительных сериях научных экспериментов, которые доказали реальность ряда самых странных аспектов квантовой теории, и эти сведения заставили меня снова отправиться в библиотеки и освежить свое представление об этих удивительных вещах. И наконец, однажды на Рождество представители ВВС пригласили меня принять участие в радиопрограмме в качестве своеобразного научного оппонента Малкольма Маггериджа, который только что объявил о своем обращении в католичество и был главным гостем в то праздничное время. После того как этот великий человек высказал свою точку зрения, подчеркнув загадочность христианства, он повернулся ко мне и сказал: «Но здесь есть тот, кто знает все ответы – или утверждает, что знает их все». Время было ограниченно, и я постарался дать достойный отпор, указав, что наука не утверждает, будто располагает всеми ответами, и как раз религия, а не наука, полностью полагается на безграничную веру и убеждение, что истина известна. «Я ни во что не верю», – сказал я и начал было объяснять свою позицию, но в этот момент программа подошла к концу. Все рождественские каникулы друзья и знакомые напоминали мне об этих словах, а я часами твердил, что отсутствие у меня безграничной веры во что-либо не мешает мне жить нормальной жизнью, используя вполне разумную рабочую гипотезу о том, что солнце вряд ли исчезнет за одну ночь.
|
|
|
|
|
|
Все это помогло мне разложить по полочкам собственные мысли о сущности науки в процессе длительных дискуссий о базовой реальности – или нереальности – квантового мира, и этого оказалось достаточно, чтобы я убедился, что могу написать книгу, которую вы теперь держите в руках. Работая над ней, я проверил многие из более тонких аргументов в ходе своих регулярных появлений в научной радиопрограмме Вещательной корпорации Британских вооруженных сил, ведущим которой был Томми Вэнс. Пытливые вопросы Тома быстро вскрывали несовершенства моей презентации, и с их помощью я смог организовать свои идеи лучшим образом. Основным источником справочных материалов, которые я использовал при написании книги, стала библиотека университета Сассекса, где содержится, пожалуй, одна из лучших коллекций книг по квантовой теории в мире, а более редкие материалы мне подобрала Мэнди Кэплин из журнала New Scientist, которая настойчиво слала мне сообщения по телетайпу, в то время как Кристина Саттон скорректировала мое неверное представление о физике частиц и теории поля. Моя жена не только оказала мне неоценимую помощь при обзоре литературы и организации материала, но и смягчила множество острых углов. Я также благодарен профессору Рудольфу Пирлсу за то, что он в деталях объяснил мне кое-какие тонкости эксперимента с часами в коробке и парадокса Эйнштейна – Подольского – Розена.
Всем хорошим, что есть в этой книге, она обязана: «сложным» текстам по химии, названий которых я уже не помню и которые я обнаружил в Библиотеке графства Кент в возрасте шестнадцати лет; горе-«популяризаторам» квантовых идей, убедившим меня в том, что я смогу описать их лучше; Малкольму Маггериджу и ВВС; библиотеке университета Сассекса; Томми Вэнсу и BFBS; Мэнди Кэплин и Кристине Саттон и особенно Мин. Любые жалобы, касающиеся тех недостатков, что все же остались в этой книге, должны быть, конечно, адресованы мне.
Джон Гриббин
Июль 1983 года
Введение
Если сложить все книги и статьи о теории относительности, написанные для простых людей, то стопка, вероятно, дотянется до Луны. «Все знают», что теория относительности Эйнштейна – это самое великое достижение науки XX столетия, и все ошибаются. Однако если сложить все книги и статьи о квантовой теории, написанные для простых людей, то они легко поместятся на моем столе. Это не значит, что о квантовой теории не слышали за стенами академий. Квантовая механика даже стала популярна в определенных слоях: при помощи нее пытались объяснить телепатию и сгибание ложек, в ней черпали вдохновение для множества научно-фантастических историй. В популярной мифологии квантовая механика связывается – если связывается вообще – с оккультизмом и экстрасенсорным восприятием, то есть странной, эзотерической ветвью науки, которую никто не понимает и которой никто не может найти практического применения.
Эта книга написана в противовес такому восприятию того, что по сути является самой фундаментальной и важной областью научного знания. Своим происхождением эта книга обязана нескольким обстоятельствам, которые возникли летом 1982 года. Во-первых, я только что дочитал книгу о теории относительности под названием «Искривления пространства» и решил, что пора взяться за демистификацию другой великой ветви науки двадцатого века. Во-вторых, в то время меня все больше раздражали неверные идеи, которые бытовали под именем квантовой теории в среде людей, далеких от науки. Великолепная книга «Дао физики» Фритьофа Капры способствовала появлению множества подражателей, которые не понимали ни физики, ни дао, но чувствовали, что можно сделать деньги, связав западную науку с восточной философией. И наконец, в августе 1982 года из Парижа пришли новости о том, что группа ученых успешно провела важнейший эксперимент, который подтвердил – для тех, кто все еще сомневался, – точность квантово-механического представления о мироздании.
Не ищите здесь «восточного мистицизма», сгибания ложек или экстрасенсорики. Ищите правдивую историю квантовой механики, истина в которой более удивительна, чем любой вымысел. Такова наука: она не нуждается в нарядах с плеча другой философии, ведь она и сама полна красот, таинств и сюрпризов. Эта книга пытается ответить на конкретный вопрос: «Что такое реальность?» И ответ (или ответы) может удивить вас. Возможно, вы в него не поверите. Но вы поймете, как смотрит на мир современная наука.
Пролог
Ничто не реально
Кот, который фигурирует в заглавии, – это мифическое существо, но Шрёдингер существовал на самом деле. Эрвин Шрёдингер был австрийским ученым, в середине 1920-х годов сыгравшим огромную роль в создании уравнений определенной ветви науки, которая теперь называется квантовой механикой. Однако сказать, что квантовая механика – это лишь ветвь науки, едва ли верно, ведь она лежит в основе всей современной науки. Ее уравнения описывают поведение очень маленьких объектов – размера атомов и меньше – и представляют собой единственное описание мира мельчайших частиц. Без этих уравнений физики не смогли бы разработать проекты рабочих атомных электростанций (или бомб), создать лазеры или объяснить, каким образом не снижается температура Солнца. Без квантовой механики химия по-прежнему пребывала бы в Темных веках и вовсе не появилась бы молекулярная биология: не было бы ни знаний о ДНК, ни генной инженерии – ничего.
Квантовая теория – это величайшее достижение науки, гораздо более значительное и гораздо более применимое в прямом, практическом смысле, чем теория относительности. И все же она делает кое-какие странные предсказания. Мир квантовой механики действительно так необычен, что даже Альберт Эйнштейн счел его непонятным и отказался признавать все следствия теории, выведенные Шрёдингером и его коллегами. Как и многие другие ученые, Эйнштейн решил, что удобнее поверить в то, что уравнения квантовой механики были лишь своеобразным математическим трюком, который по случайности предоставил разумное объяснение поведению атомных и субатомных частиц, но в них содержится более глубокая истина, которая лучше соотносится с нашим обыденным чувством реальности. Ведь квантовая механика утверждает, что реального нет и мы не можем ничего сказать о поведении вещей, когда не наблюдаем их. Мифический кот Шрёдингера был призван прояснить различия между квантовым и обычным миром.
В мире квантовой механики перестают работать законы физики, знакомые нам из обычного мира. Вместо этого событиями управляют вероятности. Радиоактивный атом, например, может распасться и, скажем, выпустить электрон, а может и нет. Можно провести эксперимент, представив, что есть ровно пятидесятипроцентная вероятность того, что один из атомов сгустка радиоактивного вещества в определенный момент распадется и детектор зарегистрирует этот распад, если он произойдет. Шрёдингер, столь же расстроенный выводами квантовой теории, как и Эйнштейн, попытался продемонстрировать их абсурдность, представив, что такой эксперимент проходит в закрытой комнате или коробке, где находятся живой кот и флакон с ядом, причем если распад происходит, сосуд с ядом разбивается и кот погибает. В обычном мире вероятность смерти кота составляет пятьдесят процентов и, не заглядывая в коробку, мы можем смело заявить лишь одно: кот внутри либо жив, либо мертв. Но тут-то и проявляет себя странность квантового мира. В соответствии с теорией ни одна из двух возможностей, которые существуют для радиоактивного вещества, а следовательно, и кота, не представляется реальной, если не происходит наблюдения за происходящим. Атомный распад не случился и не не случился, кот не погиб и не не погиб, пока мы не заглянем в коробку, чтобы узнать, что произошло. Теоретики, которые принимают чистую версию квантовой механики, утверждают, что кот существует в некотором неопределенном состоянии, будучи при этом ни живым и ни мертвым, пока наблюдатель не заглянет в коробку и не увидит, как сложилась ситуация. Ничто не реально, если не установлено наблюдение.
Эта идея была ненавистна Эйнштейну, как и многим другим. «Бог не играет в кости», – сказал он, ссылаясь на теорию о том, что мир определяется совокупностью результатов по сути случайного «выбора» возможностей на квантовом уровне. Что же до нереальности состояния кота Шрёдингера, Эйнштейн не принял ее во внимание, предположив, что должен существовать некий глубинный «механизм», который определяет истинно фундаментальную реальность вещей. Он много лет пытался разработать опыты, которые помогли бы показать эту глубинную реальность в работе, но скончался раньше, чем вообще стало возможным провести подобный эксперимент. Возможно, это к лучшему, что он не дожил до того момента, когда стал ясен результат цепочки рассуждений, запущенной им.
Летом 1982 года группа ученых из университета Париж-Юг под руководством Алена Аспе завершила серию экспериментов, разработанных для выявления глубинной реальности, определяющей нереальный квантовый мир. Этой глубинной реальности – фундаментальному механизму – присвоили имя «скрытых параметров». Суть эксперимента заключалась в наблюдении за поведением двух фотонов, или частиц света, летящих в противоположных направлениях от источника. Полностью эксперимент описан в десятой главе, но в целом его можно считать проверкой реальности. Два фотона из одного источника могут фиксироваться двумя детекторами, которые измеряют свойство, называемое поляризацией. В соответствии с квантовой теорией этого свойства не существует, пока оно не измерено. В соответствии с идеей о «скрытых параметрах» каждый фотон обладает «реальной» поляризацией с момента своего возникновения. Так как два фотона вылетают одновременно, величины их поляризации зависят друг от друга, но природа зависимости, которая измеряется на деле, различается в соответствии с двумя представлениями о реальности.
Результаты этого важнейшего эксперимента однозначны. Зависимость, предсказанная теорией скрытых параметров, не была обнаружена, а зависимость, предсказанная квантовой механикой, – была. Более того, как и предсказывала квантовая теория, измерения, проведенные на одном фотоне, оказывали мгновенный эффект на природу другого фотона. Некоторое взаимодействие неразрывно связывало фотоны, хотя они и разлетались в разные стороны со скоростью света, а теория относительности утверждает, что ни один сигнал не может передаваться быстрее, чем свет. Эксперименты доказали, что в мире нет глубинной реальности. «Реальность» в обыденном смысле не подходит для размышления о поведении фундаментальных частиц, которые составляют Вселенную, причем эти частицы в то же время, похоже, неразрывно связаны друг с другом в некоторое неделимое целое, где каждая знает, что происходит с другими.
Поиск кота Шрёдингера – это поиск квантовой реальности. Из этого короткого обзора может показаться, что поиск этот не увенчался успехом, так как в квантовом мире реальности в привычном смысле слова не существует. Но история на этом не заканчивается, и поиск кота Шрёдингера может привести нас к новому пониманию реальности, которая превосходит – и в то же время включает в себя – общепринятое толкование квантовой механики. Однако искать придется долго, и начать нужно с ученого, который, возможно, испугался бы сильнее Эйнштейна, будь у него шанс узнать данные нами сейчас ответы на мучившие его вопросы. Изучая три столетия назад природу света, Исаак Ньютон и не подозревал, наверное, что он уже ступил на путь, ведущий к коту Шрёдингера.
Часть первая
Квант
Кто не шокирован квантовой теорией, тот ее не понял.
Нильс Бор 1885-1962
Глава первая
Свет
Исаак Ньютон изобрел физику, и на ней покоится вся остальная наука. Хотя Ньютон, конечно, отталкивался от работ других, именно его публикация трех законов движения и теории гравитации свыше трех столетий назад вывела науку на путь, который в конце концов привел к покорению космоса, лазерам, атомной энергии, генной инженерии, пониманию химии и всего остального. На протяжении двух столетий ньютоновская физика (то, что сейчас называют «классической физикой») правила миром науки. Новые революционные идеи продвинули физику в двадцатом веке гораздо дальше Ньютона, однако без тех двух столетий научного роста эти идеи могли бы никогда не появиться. Эта книга не является историей науки: она рассказывает о новой физике – квантовой, а не о тех классических идеях. Однако даже в работе Ньютона трехсотлетней давности уже есть признаки того, что изменения неизбежны: они содержатся не в его трудах о движении планет и их орбитах, а в его исследованиях природы света.
Идеи Ньютона о свете во многом связаны с его идеями о поведении твердых объектов и орбитах планет. Он осознал, что наше повседневное восприятие поведения объектов может быть ошибочным и что объект, или частица, которая свободна от каких-либо внешних воздействий, должна вести себя совершенно иначе, нежели такая же частица, находящаяся на поверхности земли. Так, наш повседневный опыт указывает, что вещи склонны оставаться на одном месте, пока их не толкнешь, а если перестать их толкать, они перестанут двигаться. Тогда почему же тела вроде планет или Луны не останавливаются, двигаясь по орбитам? Что-то подталкивает их? Вовсе нет. Планеты находятся в естественном состоянии, свободные от внешнего воздействия, а взаимодействие происходит с телами на поверхности земли. Если я попробую заставить ручку скользить по столу, моему подталкиванию будет противодействовать сила трения ручки о стол, и именно она заставит ручку остановиться, когда я перестану толкать ее. В этом состоит первый закон Ньютона – каждое тело остается в состоянии покоя или движется с постоянной скоростью, пока на него не окажет воздействия внешняя сила. Второй закон показывает, насколько велико воздействие силы – подталкивания – на тело. Такая сила изменяет скорость тела, а изменение скорости называется ускорением. Если разделить силу, воздействующую на тело, на его массу, то в результате получится ускорение, придаваемое телу этой силой. Обычно этот второй закон описывают немного по-другому: сила равна массе, умноженной на ускорение. А третий закон Ньютона показывает, как тело реагирует на внешнее воздействие: на каждое действие существует равное по силе и противоположное по направлению противодействие. Если ударить ракеткой по теннисному мячу, то сила воздействия ракетки на теннисный мяч будет в точности равна силе, действующей обратно на ракетку. На ручку, которая лежит на столе, действует сила гравитации, притягивающая ее вниз, но в то же время стол оказывает на нее равное воздействие в противоположном направлении. Сила взрыва, которая выталкивает газы из камеры сгорания ракеты, создает равную и противоположную по направлению силу противодействия, действующую на саму ракету и толкающую ее в противоположном направлении.
Вместе с законом гравитации Ньютона эти законы объяснили вращение планет вокруг Солнца и Луны вокруг Земли. Когда было должным образом учтено трение, они также объяснили поведение тел на поверхности Земли и заложили основы механики. Но они имели и глубокое философское значение. Согласно законам Ньютона поведение частицы может быть в точности предсказано на основании ее взаимодействия с другими частицами и силами, воздействующими на нее. Если бы была возможность узнать положение и скорость каждой частицы во Вселенной, то стало бы возможным с огромной точностью предсказывать будущее каждой частицы, а следовательно, и будущее Вселенной. Означало ли бы это, что Вселенная работает подобно механизму, сконструированному и запущенному Творцом по какому-то абсолютно предсказуемому пути? Классическая механика Ньютона дала серьезную поддержку такому детерминистскому взгляду на природу Вселенной, сформировав картину, где мало места осталось для случайности или свободной воли человека. Неужели мы все просто марионетки, которые движутся по жизни по заранее установленным направлениям, не имея никакого настоящего выбора? Большинство ученых не возражало отдать этот вопрос на откуп философам. Но с полной силой он вернулся в сердце новой физики двадцатого столетия.
Волны или частицы?
Добившись такого успеха в физике частиц, Ньютон, что неудивительно, попытался с помощью частиц объяснить и поведение света. Что ни говори, лучи света с позиции наблюдателя распространяются по прямой, а свет отражается от зеркала очень схожим образом с тем, как мяч отскакивает от твердой стены. Ньютон сконструировал первый зеркальный телескоп, определил белый цвет как наложение всех цветов радуги и сделал многое другое в сфере оптики, но его теории всегда покоились на предположении, что свет представляет собой поток крошечных частиц, которые он называл корпускулами. Лучи света преломляются, проходя границу раздела двух сред, например воздуха и воды или стекла (именно поэтому соломинка в стакане джин-тоника кажется надломленной), и это преломление в точности объясняется корпускулярной теорией, которая предполагает, что корпускулы движутся быстрее в оптически более «плотной» среде. Однако даже во времена Ньютона существовало альтернативное объяснение всего этого.
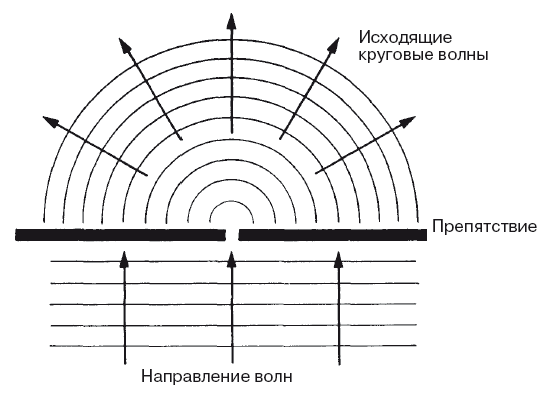
Рис. 1.1. Параллельно идущие волны воды проходят сквозь маленькое отверстие в препятствии и расходятся кругами от него, не оставляя «тени».
Голландский физик Христиан Гюйгенс родился в 1629 году, на тринадцать лет раньше Ньютона, и был его современником. Он развил идею о том, что свет является не потоком частиц, а волной и распространяется подобно волнам на поверхности моря или озера, однако по невидимой среде, называемой «светоносным эфиром». Как и рябь, создаваемая камнем, брошенным в пруд, световые волны в эфире, по представлениям Гюйгенса, должны распространяться во все стороны от источника. Волновая теория, как и корпускулярная, объясняла отражение и преломление. Однако она утверждала, что волны света должны не ускоряться, а, напротив, замедляться в оптически более плотной среде. Поскольку в XVII веке не существовало способа измерить скорость света, это различие не могло разрешить конфликт между двумя теориями. Однако в одном ключевом аспекте эти два представления давали различие в наблюдениях. Когда свет проходит мимо острого края, он оставляет после себя тень, также имеющую острый край. Именно так должны вести себя потоки частиц, движущихся по прямым линиям. Волна склонна огибать препятствия, или дифрагировать, немного заходя внутрь тени (представьте себе рябь на пруду, огибающую скалу). Триста лет назад это стало наглядным доказательством в пользу корпускулярной теории, а волновая теория хоть и не была забыта, но оказалась отвергнутой. Однако к началу девятнадцатого века статусы двух теорий практически поменялись местами.
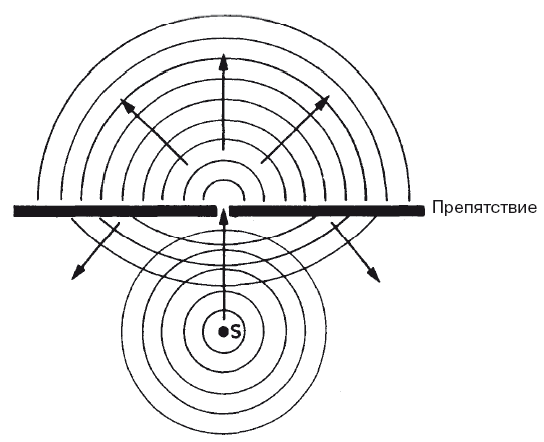
Рис. 1.2. Круговые возмущения, подобные тем, что создает камень, брошенный в пруд, распространяются подобно круговым волнам с центром в точке, где они проходят через узкое отверстие (и, разумеется, волны, наталкивающиеся на препятствие, отражаются обратно).
В XVIII веке очень немногие воспринимали волновую теорию света всерьез. Одним из тех, кто не только принимал ее всерьез, но и писал работы в ее поддержку, был швейцарец Леонард Эйлер – ведущий математик своего времени, внесший значительный вклад в развитие геометрии, математического анализа и тригонометрии. Современная математика и физика записываются на языке арифметики при помощи уравнений. Методы, на которых в значительной степени основывается это арифметическое описание, были развиты Эйлером, и в процессе работы над ними он ввел несколько удобных способов записи, дошедших и до наших дней, – число «пи» для отношения длины окружности к ее диаметру, символ ί для квадратного корня из минус единицы (мы встретимся с ним, как и с числом «пи», чуть позже), а также символы, используемые математиками для обозначения операции интегрирования. Забавно, но статья об Эйлере в Британской энциклопедии не упоминает о его взглядах на волновую теорию света, которых, по словам современников, не придерживался «ни один великий физик»[1]. Единственным значительным современником Эйлера, который разделял эти взгляды, был Бенджамин Франклин. Однако физикам удавалось легко игнорировать их, пока в начале девятнадцатого столетия англичанином Томасом Юнгом, а чуть позже французом Огюстеном Френелем не были проведены новые важные эксперименты.
Торжество волновой теории
Юнг использовал знание того, как волны движутся по поверхности пруда, чтобы разработать эксперимент, позволяющий проверить, ведет ли свет себя таким же образом. Мы все знаем, как выглядит волна воды, однако важно представить себе именно рябь, а не большую волну, чтобы аналогия была верной. Отличительной особенностью волны является то, что она слегка поднимает уровень воды, а затем, уходя, опускает. Высота гребня волны над уровнем невозмущенной водной поверхности является ее амплитудой, и для идеальной волны она равна высоте, на которую уровень воды снижается, когда волна отходит. Волны, идущие друг за другом, подобно тем, что отходят от камня, брошенного в пруд, имеют одинаковые промежутки, называемые длиной волны, которая измеряется как расстояние от одного гребня до другого. От места, в котором камень попал вводу, волны начинают распространяться кругами, тогда как волны на море или рябь от ветра на озере могут двигаться последовательными прямыми линиями, параллельными волнами, одна задругой.

Рис. 1.3. Способность волн огибать углы также означает, что они могут быстро заполнять тень позади препятствия, если только препятствие по размерам значительно не превышает длину волны.
Иными словами, число гребней, проходящих через некоторую фиксированную точку (вроде скалы) в секунду, показывает нам частоту волны. Частота – это число длин волн, проходящих каждую секунду, соответственно, скорость волны, то есть скорость движения каждого гребня, – это произведение длины волны и ее частоты.
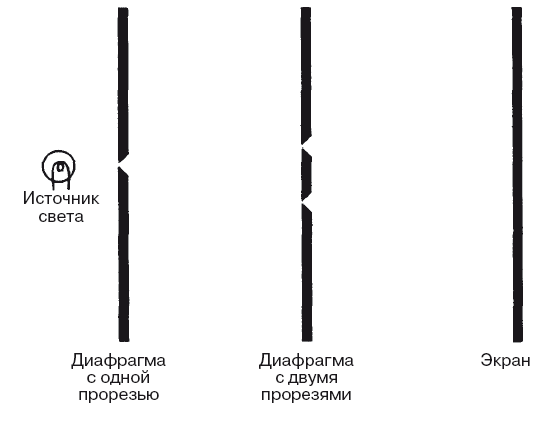
Рис. 1.4. Способность света дифрагировать на углах и маленьких отверстиях может быть проверена при помощи одиночной прорези для образования круговой волны и двух прорезей для возникновения интерференции.
Краеугольный эксперимент начинается с параллельно идущих волн, сходных с полосами волн, набегающих на пляж до того, как они обрушиваются. Вы можете представить себе эти волны, вообразив, что они исходят от очень большого объекта, упавшего в воду очень далеко от берега. «Рябь», распространяющаяся расширяющимися кругами, кажется параллельными, или плоскими, волнами, если находиться достаточно далеко от источника волн, поскольку трудно определить кривизну очень большого круга с центром в месте источника возмущений. Легко проверить, что происходит с такими волнами в емкости с водой, когда на их пути помещено препятствие. Если препятствие маленькое, то волны огибают его и оказываются позади из-за дифракции, оставляя очень маленькую «тень». Однако если преграда велика в сравнении с длиной волн, то они лишь слегка огибают ее, оставляя зону невозмущенной воды. Если свет – это волна, то появление теней с резкими углами все же возможно, при условии, что длина волны света гораздо меньше, чем размер объекта, отбрасывающего тень.
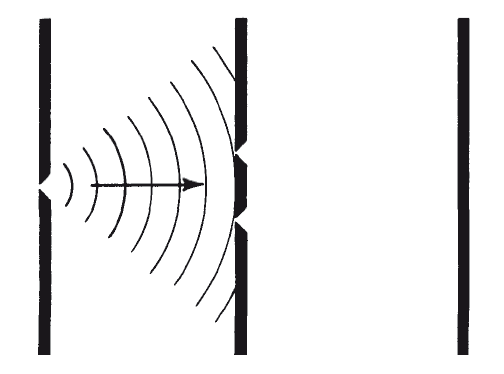
Рис. 1.5. Подобно водной ряби, проходящей через отверстие, волны света, распространяющиеся кругами от первой прорези, движутся «друг за другом».
Теперь посмотрим на это с другой стороны. Представим обычную последовательность волн, распространяющихся в емкости с водой и наталкивающихся не на препятствие, окруженное водой, а на сплошную стену на их пути, имеющую в центре промежуток. Если промежуток гораздо больше, чем длина волны, то дальше пройдет лишь та часть волны, которая умещается в него, при этом незначительно расширяясь, однако оставляя большую часть воды по ту сторону преграды невозмущенной – подобно волнам, приходящим к проему в стене бухты. Однако если промежуток в стене очень мал, то отверстие ведет себя как новый источник круговых волн, будто в этом месте в воду бросают гальку. На дальней стороне стены эта круговая волна (или, точнее, полукруговая) распространяется по всей поверхности воды, не оставляя невозмущенной зоны.

Рис. 1.6. Круговые волны, исходящие от каждого из отверстий в экране с двумя прорезями, интерферируют, создавая картину из светлых и темных полос на белом экране обзора. Это ясно доказывает, что в рамках эксперимента свет ведет себя как волна.
Пока все сходится. Теперь мы наконец подбираемся к опыту Юнга. Представим ту же конструкцию с емкостью с водой и параллельными волнами, движущимися к препятствию, но теперь в нем сделано уже две маленькие прорези. Каждая из прорезей ведет себя как новый источник полукруговых волн в области позади препятствия, и поскольку эти две вторичные волны являются производными одной плоской волны с другой стороны препятствия, они движутся согласованно, или в фазе. Теперь мы имеем две серии волн, распространяющихся по воде, и это создает более сложную картину на поверхности. В месте, где обе волны поднимают уровень воды, возникает более выраженный гребень. Там, где одна волна пытается создать гребень, а другая впадину, они нивелируют друг друга и уровень остается неизменным. Эти явления называются конструктивной и деструктивной интерференцией, и их легко наблюдать в грубом приближении, одновременно бросив два камня в воду. Если свет – это волна, то сходный эксперимент должен выявить такую же интерференцию и между световыми волнами. Именно это и открыл Юнг.
Он пустил свет на экран, в котором были проделаны две узкие прорези. Позади этого препятствия свет от двух прорезей расходился и интерферировал. Если аналогия с волнами воды была верна, то по ту сторону препятствия должна была появиться интерференционная картина из чередующихся зон света и темноты, вызванная конструктивной и деструктивной интерференцией волн от каждой прорези. Юнг наблюдал именно это – сменяющие друг друга полосы света и тени на экране, – когда поместил позади прорезей белый экран.
Однако эксперимент Юнга не перевернул научный мир, особенно в Британии. Научное сообщество там практически приравнивало любое несогласие с идеями Ньютона к ереси и отсутствию патриотизма. Ньютон умер только в 1727 году, а в 1705-м, менее чем за сто лет до оглашения Юнгом своих результатов, он стал первым ученым, которого посвятили в рыцари. В Англии не могли так скоро сбросить со счетов легенду, поэтому, возможно, в те годы Наполеоновских войн наилучшим стало то, что именно француз, Огюстен Френель, подхватил эту «непатриотичную» идею и в итоге развил волновое объяснение природы света. Работа Френеля появилась через несколько лет после опыта Юнга и, будучи более полной, дала волновое объяснение практически всех аспектов поведения света. Среди прочего Френель объяснил явление, известное всем нам сегодня, – красивые цветные разводы, которые возникают при попадании света на тонкую масляную пленку. Это происходит опять же из-за интерференции волн. Часть света отражается от поверхности пленки, тогда как другая проникает внутрь и отражается от нижнего слоя. Таким образом получаются два отраженных пучка, которые интерферируют друг с другом. Поскольку каждый цвет соответствует различной длине волны, а белый свет состоит из смеси всех цветов радуги, отражение белого света от масляной пленки создает множество цветов из-за того, что некоторые волны (цвета) интерферируют деструктивно, а некоторые конструктивно – в зависимости от того, где располагается глаз наблюдателя относительно пленки.
К моменту, когда французский физик Леон Фуко, известный благодаря маятнику, носящему его имя, в середине XIX века установил, что, вопреки предсказаниям корпускулярной теории Ньютона, скорость света в воде меньше, чем в воздухе, к этому уже был готов любой заслуживающий внимания ученый. К этому времени «все знали», что свет, чем бы он ни был, представлял собой некоторую форму волнового движения в эфире. Однако все же было не лишним продемонстрировать, что такое «волна» в пучке света. В 1860-х и 1870-х теория света, казалось, наконец была завершена, когда великий шотландский физик Джеймс Клерк Максвелл установил существование волн, связанных с изменением электрического и магнитного полей. Электромагнитное излучение, по предположению Максвелла, имело череду сильных и слабых электрических и магнитных полей, подобно гребням и впадинам на поверхности волн воды. В 1887 году Генрих Герц сумел произвести передачу и прием электромагнитного излучения в форме радиоволн, которые подобны волнам света, однако имеют гораздо большую длину. В конце концов волновая теория света была завершена, но лишь с тем чтобы вновь быть перевернутой великой революцией в научном понимании со времен Ньютона и Галилея. К концу XIX столетия лишь дурак или гений мог считать свет корпускулярным. Таким человеком стал Альберт Эйнштейн, однако, перед тем как мы поймем, почему он сделал этот смелый шаг, нам нужно обратиться глубже к идеям физики XIX столетия.
Глава вторая
Атомы
Многие популярные работы по истории науки рассказывают, что идея атомов восходит к древним грекам, ко времени рождения науки, и восхваляют древних ученых за их раннее понимание истинной природы материи. Однако такой взгляд немного преувеличен. Демокрит из Абдеры, умерший около 370 года до н. э., действительно предполагал, что сложная природа мироздания может быть объяснена, если все предметы состоят из различных неизменяемых и находящихся в постоянном движении атомов, каждый тип которых имеет собственную форму и размер. «Существуют лишь атомы и пустота, все остальное – во мнении»[2], – писал он, а позже Эпикур Самосский и римлянин Лукреций Кар заимствовали эту идею. Но этой опережающей свое время теории тогда не суждено было стать основой для объяснения мироздания, и мнение Аристотеля о том, что все во Вселенной состоит из четырех «элементов» – огня, земли, воздуха и воды, – оказалось гораздо более популярным и стойким. Тогда как идея об атомах была в основном позабыта ко времени появления Христа, четыре элемента Аристотеля продержались две тысячи лет.
Хотя в XVII веке англичанин Роберт Бойль использовал понятие атомов в своей работе по химии, а Ньютон подразумевал их в работах по физике и оптике, по-настоящему атомы стали частью научной мысли лишь в конце XVIII века, когда французский химик Антуан Лавуазье провел изучение причин горения. Лавуазье открыл множество настоящих элементов, чистых химических веществ, которые не могут быть разделены на другие химические вещества, и понял, что горение представляет собой процесс, в котором кислород из воздуха соединяется с другими элементами. В первые годы XIX столетия Джон Дальтон закрепил за атомами место в химии. Он утверждал, что вещество состоит из атомов, которые сами по себе делимы. При этом все атомы одного элемента идентичны, однако различные элементы состоят из различных атомов (по форме или размеру), при этом атомы не могут быть созданы или разрушены, но лишь реорганизованы посредством химических реакций. А химическая структура, включающая в себя два элемента и более, состоит из молекул, которые, в свою очередь, состоят из небольшого фиксированного числа атомов от каждого из элементов структуры. Таким образом два столетия назад концепция атомного строения материи получила жизнь в той форме, как она преподносится в учебниках сегодня.
Атомы в XIX столетии
И все же в XIX веке эта идея получала одобрение со стороны химиков весьма медленно. Жозеф Гей-Люссак провел эксперимент, показав, что если соединить два газообразных вещества, то необходимый объем одного газа всегда будет пропорционален объему другого. Если получившаяся смесь также представляет собой газ, то ее объем тоже находится в прямой зависимости от объемов двух других. Это согласуется с идеей о том, что каждая молекула смеси состоит из одного или двух атомов одного газа и нескольких атомов другого. В 1811 году это наблюдение использовал итальянец Амедео Авогадро, который выдвинул знаменитую гипотезу, утверждающую, что вне зависимости от химической природы газа при любой постоянной температуре и давлении равные объемы газа содержат одинаковое число молекул. Чуть позже гипотеза Авогадро была подтверждена экспериментально. Было доказано, что каждый литр газа при температуре 0 градусов Цельсия и давлении в одну атмосферу содержит около 27 000 миллиардов миллиардов (27 × 1021) молекул. Но лишь в 1850-х годах соотечественник Авогадро Станислао Канниццаро развил эту идею настолько, что химики стали воспринимать ее всерьез. Впрочем, еще в 1890-х годах было очень много химиков, отвергавших идеи Дальтона и Авогадро. Однако тогда их обогнало развитие физики – шотландец Джеймс Клерк Максвелл и австриец Людвиг Больцман, используя концепцию атомов, детально объяснили поведение газов.
В 1860-х и 1870-х годах эти первооткрыватели развили идею о том, что газ состоит из огромного числа атомов и молекул (число из гипотезы Авогадро дает вам представление о том, насколько их много), которые можно представить в виде крошечных твердых хаотически движущихся сфер, сталкивающихся друг с другом и со стенками сосуда, содержащего газ. Это напрямую соотносилось с представлением о том, что теплота является формой движения – когда газ нагревается, его молекулы начинают двигаться быстрее, что повышает давление на стенки сосуда, и, если они не закреплены, газ будет расширяться.
Ключевой особенностью этих новых идей было то, что поведение газа может быть объяснено посредством законов механики – то есть законов Ньютона – только статистически, с помощью усреднения очень большого числа атомов или молекул. Любая из молекул газа может в любой момент двигаться в произвольном направлении, однако суммарный эффект от столкновения всех молекул со стенками сосуда создает постоянное давление. Это привело к развитию математического описания газовых процессов, получившего название статистической механики. Тем не менее прямое доказательство существования атомов все еще отсутствовало.
Некоторые ведущие физики того времени упорно противостояли атомной гипотезе, и даже сам Больцман в 1890-х годах чувствовал себя (возможно, ошибочно) одиночкой, плывущим против течения научной мысли. В 1898 году он опубликовал подробные вычисления в надежде, что, «когда теория газов снова оживет, открывать понадобится не слишком много»[3]. В 1906 году, находясь в депрессии из-за болезни и в подавленном состоянии в результате ^прекращавшегося противостояния многих ведущих ученых его кинетической теории газов, Больцман покончил жизнь самоубийством, не подозревая, что за несколько месяцев до этого малоизвестный теоретик по имени Альберт Эйнштейн опубликовал работу, развеявшую все сомнения насчет существования атомов.
Атомы Эйнштейна
Эта работа была лишь одной из трех, которые Эйнштейн опубликовал в одном номере журнала «Анналы физики» за 1905 год, и любая из них могла обеспечить ему место в анналах науки. Одна из работ рассказывала о специальной теории относительности и в целом выходит за рамки этой книги. Другая описывала взаимодействие света с электронами и позже стала считаться первой научной работой на тему того, что теперь зовется квантовой механикой, – именно за нее в 1921 году Эйнштейн получил Нобелевскую премию. Третья работа обманчиво просто решала задачу, которая терзала физиков с 1827 года, – она доказывала существование атомов (насколько теоретическая статья вообще могла сделать это).
Позже Эйнштейн сказал, что его главной целью в то время было «обнаружить факты, которые насколько возможно гарантируют существование атомов конечного размера». Эта цель, быть может, показывает важность этой работы в начале прошлого столетия. Когда эти статьи были опубликованы, Эйнштейн работал в Бернском патентном бюро – его нестандартный подход к физике не сделал его явным кандидатом на академическую должность после завершения обучения, так что ему пришлось с головой погрузиться в работу над патентами. Логический ум позволял ученому успешно отсеивать новые изобретения от чепухи, а проворность на работе оставляла достаточно много свободного времени, в которое он мог размышлять о физике даже во время рабочего дня. Некоторые из его мыслей касались открытий британского ботаника Томаса Брауна, сделанных восьмьюдесятью годами ранее. Браун заметил, что если исследовать пыльцу, плавающую в капле воды, под микроскопом, то можно увидеть, что она хаотически дергается в разные стороны, совершая так называемое теперь броуновское движение. Эйнштейн показал, что это движение, хотя и является хаотическим, подчиняется определенному статистическому закону, а также что модель поведения пылинок в точности соответствует тому, как если бы пылинку постоянно «толкали» невидимые микроскопические частицы, двигающиеся в соответствии со статистической механикой Больцмана и Максвелла, которая описывает движение атомов в газе или жидкости. Сегодня это выглядит настолько очевидно, что трудно оценить, какой прорыв произвела эта работа. Вы, как и я, привыкшие к представлению об атомах, можете наконец увидеть, что если пылинка подталкивается невидимыми столкновениями, то, вероятно, это атомы толкают ее. Однако до того как Эйнштейн сделал этот вывод, уважаемые ученые все еще питали сомнения в существовании атомов. После того как работа вышла, сомнений не осталось. Все стало легко после объяснения, простого, как падение яблока на землю. Но почему, если это было так очевидно, никто не воспринимал идею в течение прошлых восьмидесяти лет?
По иронии судьбы эта научная статья была опубликована на немецком (в журнале «Анналы физики»), хоть она и противоречила суждениям ведущих немецких физиков, включая Эрнста Маха и Вильгельма Оствальда, которые, казалось, убедили Больцмана в том, что он был одиночкой в пустыне. В действительности к началу XX столетия было множество свидетельств реальности существования атомов, даже если учесть, что, строго говоря, эти свидетельства могли считаться лишь частными. Британские и французские физики поверили в атомную теорию гораздо сильнее, чем многие их немецкие оппоненты. Именно англичанин Дж. Дж. Томсон в 1897 году открыл электрон, который, как мы сегодня знаем, является одним из компонентов атома.
Электроны
В конце XIX века было много противоречий касательно природы излучения, исходящего от вакуумной трубки, по которой идет электрический ток. Эти катодные лучи, как их назвали, могли быть либо формой излучения, испускаемого колебаниями эфира, однако отличались от света и недавно открытых радиоволн, либо потоком крошечных частиц. Большинство немецких ученых поддержали идею эфирных волн. Большинство британских и французских ученых считали, что катодные лучи представляют собой частицы. Ситуация усложнилась, когда в 1895 году Вильгельм Рентген случайно открыл рентгеновские лучи (в 1901 году за это открытие Рентген получил первую в истории Нобелевскую премию по физике). Однако это не относилось напрямую к проблеме. Важным было то, что это быстрое открытие произошло до того, как был развит теоретический аппарат атомной физики, в который бы вписывались рентгеновские лучи. Мы встретимся с ними чуть позже в более подходящем контексте.
В 1870-х годах Томсон занимал должность первого в истории профессора физики Кавендишской лаборатории – основанного Максвеллом научного центра в Кембридже. Он разработал эксперимент, который основывался на уравновешивании электрических и магнитных свойств движущейся и заряженной частицы[4]. Траектория такой частицы может отклоняться как магнитным, так и электрическим полем, и прибор Томсона был сконструирован таким образом, что эти два эффекта нивелировали друг друга, так что оставался лишь пучок катодных лучей, двигавшихся напрямую от отрицательно заряженной металлической пластины (катода) к экрану детектора. Этот трюк работает только для электрически заряженных частиц, поэтому Томсон установил, что катодные лучи на самом деле являются отрицательно заряженными частицами (теперь называемыми электронами). Он смог использовать уравновешивание электрических и магнитных сил, чтобы рассчитать отношение электрического заряда электрона к его массе (е/m). Какой бы металл ни использовался в качестве материала для катода, Томсон всегда получал один и тот же результат и сделал вывод, что электроны являются частью атомов и что, хотя различные элементы состоят из различных атомов, все атомы содержат одинаковые электроны.
Это было не случайное удачное открытие, как открытие рентгеновских лучей, а итог аккуратного планирования и мастерских экспериментов. Кавендишскую лабораторию создал Максвелл, но именно под руководством Томсона она стала лидером в экспериментальной физике и, возможно, лидирующей физической лабораторией в мире, и принесла множество открытий, которые в XX веке привели к новому пониманию физики. Кроме самого Томсона, Нобелевскую премию получили еще семь человек, работавших с ним в лаборатории до 1914 года. Кавендишская лаборатория и в наши дни остается мировым центром физики.
Ионы
Катодные лучи, которые двигались по вакуумной трубке от отрицательно заряженной пластины, оказались отрицательно заряженными частицами, электронами. Атомы, однако, электрически нейтральны, а потому логично, что существуют и позитивно заряженные противоположности электронов – атомы, у которых отняли часть отрицательного заряда. В 1898 году Вильгельм Вин из университета Вюрцбурга впервые изучил эти положительные лучи, выяснив, что частицы, из которых они состоят, значительно тяжелее электронов, как будто бы это были атомы, которым просто не хватало электрона. Завершив эксперименты с катодными лучами, Томсон решил исследовать эти положительные лучи в серии сложных экспериментов, которые продолжались и в течение 1920-х годов. Сегодня эти лучи называются ионизированными атомами, или просто «ионами», а во времена Томсона их называли каналовыми лучами, потому что он изучал их, используя модифицированную трубку для катодных лучей, в которой вакуумный насос оставлял небольшое количество газа. Электроны, двигавшиеся сквозь этот газ, вступали во взаимодействие с его атомами и выбивали из них другие электроны, оставляя положительно заряженные ионы, на которые можно было оказывать воздействие при помощи электрического и магнитного полей таким же образом, как Томсон оказывал воздействие на сами электроны. К 1913 году группа Томсона произвела измерения отклонения положительно заряженных ионов водорода, кислорода и других газов. Одним из газов, которые Томсон использовал в этих опытах, был неон. Неон, через который проходит электрический заряд в вакуумной трубке, ярко вспыхивает, и аппарат Томсона стал предшественником современной неоновой трубки. Но его открытие было гораздо важнее, чем изобретение нового способа рекламы.
В отличие от электронов, которые имеют одно и то же отношение заряда к массе е/т, существует три различных типа ионов неона, которые имеют такой же заряд, как и электрон, однако не отрицательный (—е), а положительный (+е), но разные массы. Это стало первым свидетельством того, что химические элементы часто включают в себя атомы с разной массой (разной атомной массой), но одинаковыми химическими свойствами. Теперь такие варианты элементов называют «изотопами», но объяснение их существования смогли обнаружить лишь гораздо позже. Однако Томсон уже тогда располагал достаточным объемом информации, чтобы сделать первый шаг к описанию внутренней структуры атома, который был не неделимой основной частицей, как полагали некоторые древнегреческие философы, а совокупностью положительных и отрицательных зарядов, из которой можно вырывать электроны.
Томсон представил атом как своего рода арбуз – относительно крупную сферу, по которой был распределен весь положительный заряд и куда были, подобно семечкам, внедрены маленькие электроны, каждый из которых нес в себе частицу отрицательного заряда. Как выяснилось, он ошибался, но он предоставил ученым мишень для стрельбы – и постоянные тренировки привели их к более точному пониманию структуры атома. Чтобы узнать, как именно это произошло, нам нужно отступить на шаг назад в историю науки, а затем сделать два шага вперед.
Рентгеновские лучи
Ключевым открытием для понимания структуры атома стало совершенное в 1896 году открытие радиоактивности. Как и обнаружение рентгеновских лучей, состоявшееся несколькими месяцами ранее, оно произошло по счастливому стечению обстоятельств, хотя в обоих случаях это счастливое стечение обстоятельств не могло не произойти в какой-нибудь физической лаборатории того времени. Как и многие физики в 1890-х годах, Вильгельм Рентген экспериментировал с катодными лучами. Когда эти лучи – электроны – сталкиваются с материальным объектом, в результате их столкновения происходит вторичное излучение. Это излучение невидимо, можно заметить только его воздействие на фотографическую пластинку или пленку либо на аппарат, называемый флуоресцентным экраном, который искрится, принимая на себя излучение. Случилось так, что во время проведения опытов с катодными лучами на столе в лаборатории Рентгена лежал такой экран, и ученый сразу заметил, что экран вспыхивал при работе отводящей трубки в опыте с катодными лучами. Это привело его к открытию вторичного излучения, которое он обозначил как «икс», ведь икс обычно используется в математических уравнениях в качестве неизвестной. Вскоре выяснилось, что рентгеновские лучи ведут себя, как волны (теперь мы знаем, что они представляют собой особую форму электромагнитного излучения и очень похожи на световые волны, но при этом длина этих волн значительно короче), и это открытие, сделанное в немецкой лаборатории, помогло подтвердить мнение большинства немецких ученых о том, что катодные лучи, должно быть, тоже являются волнами.
Об открытии рентгеновских лучей было объявлено в декабре 1895 года, и это вызвало переполох в научном сообществе. Другие ученые стали пытаться найти иные способы создания рентгеновских лучей или подобных форм излучения, и первым преуспел Анри Беккерель, который работал в Париже. Самым удивительным свойством рентгеновского излучения стало то, что оно могло беспрепятственно проходить через многие непрозрачные вещества, например сквозь черную бумагу, создавая снимок на фотографической пластине, не подвергавшейся воздействию света. Беккереля интересовало фосфоресцирование, то есть способность вещества, которое раньше поглощало свет, излучать его. Флуоресцентный экран наподобие того, который использовался при открытии рентгеновского излучения, испускает свет только тогда, когда его «раздражает» попадающее на него излучение, в то время как фосфоресцирующее вещество обладает способностью накапливать попадающее на него излучение и высвобождать его в форме постепенно меркнущего света в течение нескольких часов после того, как его поместили в темноту. Было естественно поискать связь между фосфоресценцией и рентгеновским излучением, но открытие Беккереля стало столь же неожиданным, как и само открытие рентгеновских лучей.
Радиоактивность
В феврале 1896 года он обернул фотографическую пластину двойным слоем черной бумаги, пропитал бумагу бисульфатом урана и калия и оставил все это на несколько часов под солнцем. Когда он достал пластину, на ней видна была граница пропитанной химикатами области. Беккерель решил, что солнце привело к возникновению рентгеновского излучения в слое химикатов – соли урана – по тому же принципу, по которому возникает фосфоресцирование. Через два дня он таким же образом подготовил еще одну пластину для повторения опыта, но в тот день и на следующий небо было затянуто облаками, а потому подготовленная пластина осталась в его кабинете. Первого марта Беккерель вытащил пластину и снова обнаружил на ней границу соли урана. Что бы ни воздействовало на обе пластины, это не имело отношения к солнечному свету или эффекту фосфоресцирования, а, как выяснилось, было ранее неизвестной формой излучения, которое производил сам уран – спонтанно, без какого-либо внешнего воздействия. Сейчас эта способность к спонтанному излучению называется радиоактивностью.
Вдохновленные открытием Беккереля, другие ученые принялись за изучение радиоактивности, и вскоре экспертами в новой ветви науки стали Мария и Пьер Кюри, работавшие в Сорбонне. За изучение радиоактивности и открытие новых радиоактивных элементов они в 1903 году получили Нобелевскую премию по физике, а в 1911 году Мария получила вторую Нобелевскую премию – уже по химии – за дальнейшую работу с радиоактивными материалами (в 1930-х годах дочь Марии и Пьера Кюри Ирен тоже получила Нобелевскую премию за изучение радиоактивности). В начале 1900-х годов экспериментальные открытия в сфере радиоактивности значительно опережали теорию: целая серия практических результатов лишь позже оказалась подкреплена теоретическими знаниями. В этот период один человек особенно выделялся своими исследованиями радиоактивности, и это был Эрнест Резерфорд.
Резерфорд происходил из Новой Зеландии и в 1890-х годах работал вместе с Томсоном в Кавендишской лаборатории. В 1898 году он стал профессором физики в университете Макгилла в Монреале, и там в 1902 году вместе с Фредериком Содди доказал, что радиоактивность предполагает трансформацию радиоактивного элемента в другой элемент. Именно Резерфорд выяснил, что в процессе радиоактивного «распада» (как он теперь называется) производится два типа излучения, которые он назвал альфа– и бета-излучениями. Когда позже был открыт третий тип излучения, его, естественно, назвали гамма-излучением. Альфа– и бета-излучения, как выяснилось, представляли собой поток быстро двигавшихся частиц. Вскоре было доказано, что бета-лучи представляют собой электроны и являются радиоактивным эквивалентом катодных лучей, а затем доказали, что гамма-лучи – это еще одна форма электромагнитного излучения, подобная рентгеновским лучам, но с еще более короткой длиной волны. Альфа-частицы, однако, оказались чем-то совершенно иным – масса этих частиц примерно в четыре раза превышала массу атома водорода, а электрический заряд был в два раза больше заряда электрона, при этом будучи положительным, а не отрицательным.
Внутри атома
Никто еще не знал, что представляют собой альфа-частицы или как они на огромной скорости испускаются атомом, который в процессе этого превращается в атом другого элемента, но исследователи вроде Резерфорда нашли им применение. Такие высокоэнергетические частицы, будучи продуктом атомных реакций, могли использоваться в качестве моделей для изучения структуры атомов и, в очередной раз подтверждая цикличность научных исследований, помочь выяснить, откуда появляются сами альфа-частицы. В 1907 году Резерфорд уехал из Монреаля и стал профессором физики в университете Манчестера в Англии, а в 1908 году получил Нобелевскую премию по химии за свои исследования радиоактивности, и это позабавило ученого. Хотя изучение элементов рассматривалось Нобелевским комитетом как работа в области химии, сам Резерфорд считал себя физиком и не уделял химии, которая казалась ему наукой второго сорта, особенного внимания. (Новое понимание структуры атомов и молекул, предоставленное квантовой физикой, конечно, лишь подтвердило старую физическую шутку о том, что химия – это лишь ветвь физики.) В 1909 году Ханс Гейгер и Эрнест Марсден, работавшие на кафедре Резерфорда в Манчестере, провели серию опытов, в которых пучок альфа-частиц был направлен на тонкую металлическую фольгу и сквозь нее. В опытах использовались альфа-частицы, излучаемые естественно радиоактивными атомами, ведь в те времена еще не было генераторов искусственных частиц. Судьба частиц, направленных на металлическую фольгу, определялась сцинтилляционными детекторами, флуоресцентными экранами, которые вспыхивали при столкновении с такой частицей. Некоторые частицы прошли прямо сквозь фольгу, другие отклонились и прошли под углом к изначальному пучку, а третьи, к удивлению экспериментаторов, отразились от фольги и остались на той же стороне, с которой ее поразил пучок. Как это могло произойти?
Резерфорд дал этому объяснение. Каждая альфа-частица обладает массой, в 7000 раз превышающей массу электрона (фактически альфа-частица идентична атому гелия без двух электронов), и может двигаться на скорости, близкой к скорости света. Если такая частица сталкивается с электроном, она отбрасывает электрон в сторону и продолжает движение без каких-либо изменений. Отклонения должны объясняться положительным зарядом атомов металлической фольги (одинаковые заряды, как и одинаковые магнитные поля, отталкиваются друг от друга), но если арбузная модель Томсона была верной, частицы не могли отражаться. Если атом заполняла сфера положительного заряда, то альфа-частицы должны были проходить сквозь нее, ведь опыт показал, что большая часть частиц проходила прямо сквозь фольгу. Если арбуз пропустил сквозь себя одну частицу, он должен был пропустить и все остальные. Но если весь положительный заряд концентрировался в крошечном объеме, гораздо меньшем, чем объем целого атома, то время от времени альфа-частицы, со всего разбега налетающие на этот маленький сгусток материи и заряда, должны были отскакивать назад, в то время как большая часть альфа-частиц проходила бы сквозь пустое пространство между этими сгустками материи. Только таким образом положительный заряд атома мог иногда отталкивать положительно заряженные альфа-частицы, порой слегка сбивая их с пути, а порой практически не оказывая на них влияния.
Итак, в 1911 году Резерфорд предложил новую модель атома, которая стала основой нашего современного понимания атомной структуры. Он заявил, что в атоме должен быть маленький центр, который он назвал ядром. Ядро содержит в себе весь положительный заряд атома, который равен и противоположен отрицательному заряду облака электронов, окружающего ядро, и таким образом вместе ядро и электроны формируют электрически нейтральный атом. Последующие эксперименты показали, что размер ядра составляет всего около одной стотысячной размера всего атома: диаметр ядра обычно равняется 10-13 см, а диаметр облака электронов – 10-8 см. Чтобы вообразить себе это, представьте булавочную головку диаметром около миллиметра в центре собора Святого Петра, окруженную облаком микроскопических частичек пыли, выходящих далеко – скажем, на 100 метров – за пределы купола собора. Булавочная головка – это ядро атома, а частички пыли – это электроны. В атоме огромное количество свободного пространства, и все, казалось бы, твердые объекты материального мира состоят из таких пустых пространств, связанных вместе электрическими зарядами. Как вы помните, Резерфорд получил Нобелевскую премию, когда предложил новую модель атома (модель, основанную на опытах, которые он самостоятельно разработал). Но карьера его была еще далека от завершения, ведь в 1919 году он объявил о первой искусственной трансмутации элемента и в тот же год сменил Дж. Дж. Томсона на посту директора Кавендишской лаборатории. Его сначала посвятили в рыцари (в 1914 году), а затем, в 1931-м, сделали бароном Резерфордом Нельсоном. Несмотря на все это, включая Нобелевскую премию, самым значительным его вкладом в науку стала модель атома. Этой модели суждено было перевернуть всю физику, поставив очевидный вопрос: если противоположные заряды притягивают друг друга столь же сильно, как одинаковые заряды друг друга отталкивают, почему отрицательно заряженные электроны не падают на положительно заряженное ядро? Ответ нашелся в анализе взаимодействия атомов со светом, и это ознаменовало появление первого варианта квантовой теории.
Глава третья
Свет и атомы
Вопрос, поставленный моделью атома Резерфорда, покоился на известном факте, что движущийся электрический заряд, обладающий ускорением, испускает энергию в форме электромагнитного излучения: света, радиоволн или других подобных явлений. Если электрон просто находится рядом с ядром атома, то он должен упасть на ядро – то есть атом не будет стабильным. При разрушении такой атом должен испустить энергию. Чтобы справиться с этой склонностью атома к разрушению, естественным было предположить, что электроны вращаются вокруг ядра подобно тому, как планеты вращаются вокруг Солнца в Солнечной системе. Однако орбитальное движение предполагает наличие постоянного ускорения. Модуль скорости вращающейся частицы может оставаться неизменным, но направление ее движения меняется, и важным является то, что скорость (будучи вектором. – Примеч. пер.) определяется и модулем, и направлением. Если скорость вращающихся электронов изменилась, то они должны испустить энергию, а поскольку они потеряли ее часть, то в результате они должны упасть на ядро. Даже введя в модель орбитальное движение, теоретики не могли избавить атом Резерфорда от разрушения.
Пытаясь улучшить эту модель, теоретики отталкивались от представления об электронах, вращающихся вокруг ядра, и стремились найти способ удержать их на орбитах без потери энергии и падения на ядро. Это было естественной начальной точкой, которая хорошо согласовывалась с представлением о Солнечной системе. Однако это было неверно. Как мы увидим, это настолько же ошибочно, как представлять электроны находящимися в пространстве на некотором расстоянии вокруг ядра и не вращающимися вокруг него. Проблема та же самая – как предотвратить падение электронов? – однако это, как по волшебству, рождает совершенно другую картину, нежели та, в которой планеты вращаются вокруг Солнца. И это очень хорошо. Чтобы объяснить, почему электроны не падают, теоретики применили трюк, который не зависит от того, используем мы орбитальную аналогию или нет. Является ли она чрезмерной и неверной, также не имеет значения. Большинство людей до сих пор считают – из школы или популярной науки, – что атом подобен Солнечной системе и в центре него находится ядро, вокруг которого по круговым орбитам вращаются электроны. Теперь настало время избавиться от этого представления и постараться без предубеждений воспринять странный мир атома – мир квантовой механики. Давайте просто представим ядро и электроны, находящиеся рядом в пространстве, и зададимся вопросом, почему притяжение между положительным и отрицательным зарядами не приводит к тому, что атом разрушается, испуская при этом энергию.
К моменту, когда во втором десятилетии XX века теоретики начали ломать голову над этой загадкой, уже были сделаны важные открытия, которые должны были дать им улучшенную модель атома. Они основывались на изучении того, как материя (атомы) взаимодействует с излучением (светом).
В начале XX века лучший научный взгляд на природу предполагал дуализм. Материальные объекты могли быть описаны с помощью частиц или атомов, однако электромагнитное излучение, в том числе свет, должно было рассматриваться с позиции волн, поэтому изучение взаимодействия света и материи в 1900-х годах, казалось, должно было стать лучшим шансом для объединения физики. Однако именно при попытке объяснить, как излучение взаимодействует с материей, классическая физика, настолько успешная во всех остальных областях, потерпела неудачу.
Проще всего увидеть (в буквальном смысле), как материя взаимодействует с излучением, посмотрев на горячий предмет. Горячий предмет испускает электромагнитную энергию, и чем он горячее, тем больше энергии испускается, при этом длина волны становится короче (а частота – выше). Поэтому нагретая докрасна кочерга холоднее, чем нагретая добела, а кочерга, которая недостаточно нагрета, чтобы излучать видимый свет, может все равно казаться теплой, поскольку она испускает низкочастотное инфракрасное излучение. Даже в конце XIX столетия было очевидно, что это электромагнитное излучение должно быть связано с движением крошечных электрических зарядов. Сам электрон был только открыт, но легко видеть, как заряженная часть атома, которую мы теперь отождествляем с электроном, колеблясь из стороны в сторону, может создавать поток электромагнитных волн, почти как дергающийся в воде палец может распространять вокруг себя рябь.
Проблема заключалась в том, что сочетание лучших классических теорий – статистической механики и электромагнетизма – предсказывало, что излучение должно быть совершенно другим, нежели то, которое наблюдается от горячих предметов.
Зацепка абсолютно черного тела
Чтобы сделать эти предположения, теоретики, как обычно, использовали идеализированный воображаемый пример – в этом случае «идеальный» поглотитель или испускатель излучения. Такой предмет обычно называется «абсолютно черным телом», поскольку он поглощает все излучение, которое падает на него. Название это, однако, не слишком подходит такому предмету, так как абсолютно черное тело, как выяснилось, эффективнее всего превращает тепловую энергию в электромагнитное излучение: «абсолютно черное тело» легко может быть накалено докрасна или добела – в некотором роде даже поверхность Солнца ведет себя как абсолютно черное тело. В отличие от многих идеализированных концепций, разработанных теоретиками, абсолютно черное тело легко создать в лаборатории. Для этого достаточно взять полую сферу или трубку с запаянными концами и проделать в ней небольшое отверстие. Любое излучение, такое как свет, которое проникнет внутрь через это отверстие, окажется запертым внутри и будет отражаться от стенок сосуда до своего поглощения. Вероятность того, что оно выйдет наружу через то же самое отверстие, очень мала, поэтому отверстие в сущности является абсолютно черным телом. Это дает излучению другое имя: излучение абсолютно черного тела.
Нам, однако же, более интересно, что происходит с абсолютно черным телом при его нагревании. Как и кочерга, оно сначала становится теплым, а потом раскаляется докрасна или добела в зависимости от температуры. Спектр испускаемого излучения – распределение излучения по длинам волн – можно изучить в лаборатории, наблюдая за тем, что выходит из маленького отверстия на боку горячего сосуда, и наблюдения показывают, что он зависит только от температуры абсолютно черного тела. На очень малых длинах волн (высоких частотах) излучения очень мало, как и на очень больших длинах волн, тогда как большая часть энергии испускается на средних частотах. Пик спектра сдвигается в сторону более коротких длин волн, по мере того как тело нагревается (от инфракрасного к красному, синему и ультрафиолетовому участку спектра), однако всегда существует обрыв на очень коротких длинах волн. Именно здесь измерения излучения абсолютно черного тела в конце XIX столетия вступили в противоречие с теорией.
Звучит странно, но лучшие предсказания классической теории сходились на том, что полость, полная излучения, на самых коротких длинах волн должна всегда обладать бесконечным количеством энергии – и вместо пика в спектре абсолютно черного тела и падения энергии до нуля при нулевой длине волны измерения должны зашкалить на коротковолновом участке. Эти вычисления были основаны на кажущемся естественным предположении, что электромагнитные волны излучения в полости могут рассматриваться таким же образом, как колебания струны, например струны скрипки, и что могут существовать волны любого размера – любой длины волны и частоты. Поскольку необходимо учесть очень много различных длин волн (много «колебательных мод»), законы статистической механики должны быть перенесены из мира частиц в мир волн, с тем чтобы предсказать поведение излучения в полости, и это напрямую ведет к выводу, что энергия, испускаемая на каждой частоте, прямо пропорциональна ей. Частота является всего лишь обратной величиной от длины волны, и очень короткие длины волн означают очень высокие частоты. Поэтому полное излучение абсолютно черного тела должно давать огромное количество высокочастотной энергии – то есть в зоне ультрафиолета и далее. Чем больше частота, тем больше энергия. Это предсказание называется ультрафиолетовой катастрофой и показывает, что в предположениях, на которых оно основано, присутствует какая-то ошибка.
Однако не все потеряно. На низкочастотном участке спектра абсолютно черного тела наблюдения очень хорошо согласуются с предсказаниями, основанными на классической теории и известными как закон Рэлея – Джинса. По крайней мере, классическая теория верна наполовину. Загадка в том, почему энергия колебаний на высоких частотах не является очень большой и в действительности падает до нуля, по мере того как увеличивается частота излучения.
Эта загадка привлекла внимание многих физиков последнего десятилетия XIX века. Одним из них был немецкий физик старой школы Макс Планк. Будучи трудолюбивым и основательным, Планк был по духу консерватором, а не революционером. Он питал особенный интерес к термодинамике, и самой главной его надеждой в то время было разрешить ультрафиолетовую катастрофу, применив законы термодинамики. В конце 1890-х годов было известно два приблизительных уравнения, которые вместе давали грубое выражение спектра абсолютно черного тела. Ранняя версия закона Рэлея – Джинса работала при больших длинах волн, а Вильгельм Вин предложил формулу, которая примерно соответствовала наблюдениям при малых длинах волн, а также «предсказал» длину волны, соответствующую пику кривой при любой температуре. Планк начал с исследования того, как маленькие электрические осцилляторы должны поглощать и излучать электромагнитные волны, – этот подход отличался от того, который Рэлей использовал в 1900 году, а Джинс немного позже, – но именно он привел к получению стандартной кривой, заканчивающейся ультрафиолетовой катастрофой. С 1895 по 1900 год Планк изучал эту проблему и опубликовал несколько ключевых работ, которые определили связь между термодинамикой и электродинамикой, – и все же он не мог разрешить загадку спектра абсолютно черного тела. В 1900 году он совершил прорыв, но не благодаря спокойному и взвешенному логическому подходу, а в результате удачного стечения обстоятельств: в отчаянии он смешал удачу и вдохновение с одним из использовавшихся им математических инструментов, который он, к счастью, понимал неправильно.
Конечно, никто сегодня не может точно знать, что творилось в голове Планка, когда он сделал революционный шаг, ведущий к квантовой механике, но его работа была тщательно изучена историком Мартином Кляйном из ħельского университета, который специализируется на истории физики периода рождения квантовой теории. Кляйн, вероятно, точнее всего воссоздал роли, которые сыграли Планк и Эйнштейн в этом рождении, и это ставит открытие в убедительный исторический контекст. Первый шаг, сделанный в конце лета 1900 года, не был связан с удачей и был обязан всем вдохновению талантливого физика-математика. Планк понял, что два неполных описания спектра абсолютно черного тела могут быть связаны одной простой математической формулой, которая описывала форму всей кривой, – в действительности он использовал небольшой математический фокус, чтобы свести воедино две формулы: закон смещения Вина и закон Рэлея – Джинса. Это был большой успех. Уравнение Планка прекрасно согласовывалось с наблюдениями излучения абсолютно твердого тела. Однако в отличие от двух полузаконов, на которых оно базировалось, в нем не было физической основы. И Вин, и Рэлей, и даже Планк в предшествующие четыре года пытались построить на основе разумных физических предположений теорию, которая вела бы к кривой абсолютно черного тела. Теперь же Планк вытащил правильную кривую из шляпы, и никто не знал, какие физические допущения «присутствовали» в этой кривой. Выяснилось, что они были совершенно «неразумны».
Непрошеная революция
Формула Планка была представлена публике в октябре 1900 года на собрании Берлинского физического общества. Следующие два месяца Планк пытался найти физическую основу для закона, пробуя различные комбинации физических допущений, чтобы найти те, которые бы согласовывались с математическими уравнениями. Позже он заметил, что это был самый интенсивный период работы за всю его жизнь. Многие попытки провалились, пока наконец у Планка не осталась лишь одна – менее всего желанная для него – альтернатива.
Я упоминал, что Планк был физиком старой школы, и это правда. В своих ранних работах он неохотно принимал молекулярную гипотезу и питал особенное отвращение к статистической интерпретации свойства, известного как энтропия – эту интерпретацию в термодинамику ввел Больцман. Энтропия является ключевым понятием физики, в фундаментальном смысле соотносящимся с течением времени. Хотя простые законы механики – законы Ньютона – являются полностью обратимыми во времени, мы знаем, что реальный мир другой. Представьте себе камень, брошенный на землю. Когда он падает, энергия его движения превращается в тепло. Но если мы положим такой же камень на землю и нагреем его до той же величины, он не подпрыгнет в воздух. Почему? В случае с падающим камнем упорядоченная форма движения (все атомы и молекулы падают в одном направлении) превращается в беспорядочную форму движения (все атомы и молекулы энергично и хаотично толкают друг друга). Кажется, что законы природы требуют, чтобы беспорядок всегда увеличивался, а беспорядок определяется энтропией. Этот закон является вторым законом термодинамики и утверждает, что естественные процессы всегда протекают так, что беспорядок увеличивается, то есть энтропия всегда возрастает. Если поместить беспорядочную тепловую энергию в камень, то в этом случае он не может использовать эту энергию, чтобы создать упорядоченное движение всех молекул в камне, с тем чтобы они все вместе прыгнули вверх.
Или все же может? Больцман дал различные варианты. Он сказал, что такой удивительный случай может произойти, но это крайне маловероятно. Таким же образом в результате случайного движения молекул воздуха может произойти так, что весь воздух в комнате внезапно соберется в ее углах (должно быть больше одного угла, поскольку молекулы движутся в трех пространственных измерениях). Однако опять же такая возможность настолько маловероятна, что на практике ее можно игнорировать. Планк долго и упорно выступал против этой статистической интерпретации второго закона термодинамики, делая это как публично, так и в переписке с Больцманом. Для него второй закон был окончателен: энтропия должна постоянно возрастать, и вероятности не вписываются в эту картину. Поэтому несложно представить, как, должно быть, чувствовал себя Планк ближе к концу 1900 года, когда, исчерпав все остальные варианты, он неохотно попробовал внедрить в свои расчеты спектра абсолютно черного тела статистическую версию термодинамики Больцмана и обнаружил, что она сработала. Однако ситуация оказалась еще комичнее: плохо знакомый с уравнениями Больцмана, Планк применил их непоследовательно. Он получил верный ответ неверным способом, и истинное значение работы Планка стало очевидно только тогда, когда в дело вступил Эйнштейн.
Стоит особо отметить, что большим шагом вперед в науке стало уже то, что Планк установил, что статистическая интерпретация возрастания энтропии Больцмана является лучшим описанием реальности. Из работы Планка стало ясно, что нет никаких сомнений в том, что возрастание энтропии хотя и очень вероятно, но не гарантировано. Это имеет интересные следствия для космологии, изучающей Вселенную в целом, в которой мы сталкиваемся с большими промежутками во времени и пространстве. Чем больше область, которую мы рассматриваем, тем больше там возможностей для того, что произойдут маловероятные события. В принципе даже возможно (хотя и весьма маловероятно), что целая Вселенная, которая является упорядоченным местом, в общем и целом представляет собой некий вид термодинамической статистической флуктуации – очень большого и редкого всплеска, создавшего зону низкой энтропии, которая сейчас разрушается. Однако «ошибка» Планка приоткрыла кое-что еще более фундаментальное о природе Вселенной.
Статистический подход Больцмана к термодинамике предполагал математическое разделение энергии на куски, рассматривавшиеся как реальные величины, к которым можно было применить уравнения теории вероятности. Перед этим этапом вычислений энергия разделялась на порции, которые на более поздней стадии необходимо было сложить воедино (интегрировать), чтобы получить полную энергию – в этом случае энергию, соответствующую излучению абсолютно черного тела. Впрочем, на полпути Планк понял, что у него уже есть математическая формула для того, что он хотел получить. Перед тем как Планк приступил к стадии интегрирования кусков энергии обратно в единое целое, уравнение абсолютно черного тела уже было получено. И он взял его. Это был весьма радикальный шаг, который ничем не оправдан с точки зрения классической физики.
Любой хороший классический физик, начавший с уравнения Больцмана для вывода формулы излучения абсолютно черного тела, завершил бы интегрирование. Затем, как позже показал Эйнштейн, соединение кусков энергии снова привело бы к ультрафиолетовой катастрофе – в самом деле, Эйнштейн выяснил, что любой классический подход к задаче неизбежно приводит к этой катастрофе. И лишь потому, что Планк уже знал ответ, который он искал, он смог прервать полное, кажущееся правильным классическое решение уравнений. В результате этого он остался наедине с кусочками энергии, которые предстояло объяснить. Он интерпретировал это явное разделение электромагнитной энергии на куски как то, что электрические осцилляторы внутри атома могут лишь поглощать и испускать энергию фрагментами определенного размера, называемыми квантами. Вместо того чтобы делить имеющееся количество энергии бесконечным образом, ее можно разделить по резонаторам на конечное число кусков, и энергия каждого такого куска излучения (Е) должна соотноситься с частотой излучения, которую обозначают греческой буквой ню (ν), согласно новой формуле:
E=hv ,
где h – это новая постоянная, теперь называемая постоянной Планка.
Что такое h?
Легко заметить, как это решает ультрафиолетовую катастрофу. На очень высоких частотах энергия, необходимая для того чтобы испустить один квант излучения, весьма велика, и лишь несколько осцилляторов будут обладать такой энергией (в соответствии с уравнениями статистической механики), поэтому будут испущены лишь несколько квантов с высокой энергией. На очень низких частотах (длинных волнах) испускается очень много квантов с низкой энергией, но каждый из них имеет так мало энергии, что даже в сумме ее очень мало. Лишь на средних частотах существует много осцилляторов, которые обладают достаточной энергией для испускания излучения кусками средних размеров, которые вместе создают пик на кривой абсолютно черного тела.
Однако открытие Планка, оглашенное в декабре 1900 года, дало больше вопросов, нежели ответов, и не смогло перевернуть мир физики. Ранние статьи Планка о квантовой теории не вполне ясны, что, возможно, отражает то смятение, с которым он был вынужден внедрить эту идею в его любимую термодинамику. На протяжении долгого времени многие – почти все – физики, которые знали о его работе, считали ее просто математической уловкой, способом избавиться от ультрафиолетовой катастрофы, который едва ли имел физическое значение. Сам Планк также пребывал в замешательстве. В письме Роберту Уильяму Вуду в 1931 году он вспоминал о своей работе 1900 года: «Я могу охарактеризовать весь процесс как акт отчаяния… Теоретическая интерпретация должна была быть найдена любой ценой, какой бы она ни была»[5]. И все же он знал, что наткнулся на что-то важное и, согласно Гейзенбергу, позже сын Планка рассказывал, как его отец описывал свою работу в то время, когда он подолгу гулял по Грюневальду на окраине Берлина, объясняя, что это открытие может сравниться с открытием Ньютона[6].
В начале 1900-х годов физики были заняты тем, что осваивали новые открытия в области атомного излучения, и новый «математический трюк» Планка, призванный объяснить спектр излучения абсолютно черного тела, не казался особенно важным в сравнении с ними. В самом деле, Нобелевскую премию за свою работу Планк получил лишь в 1918 году – а это очень большой промежуток времени по сравнению с тем, как быстро были оценены работы Кюри или Резерфорда. (Отчасти это было связано с тем, что требуется больше времени для признания кардинально новых теоретических прорывов. Новая теория не так осязаема, как новая частица или рентгеновские лучи, и она должна выдержать проверку временем или получить экспериментальное подтверждение, прежде чем получит всеобщее признание.) Также было нечто странное в новой постоянной Планка – h. Это очень маленькая постоянная: 6,6 × 10-34Дж·с. Но это не должно удивлять, ведь если бы она была гораздо больше, то ее присутствие стало бы очевидно для физиков гораздо раньше, до того, как они стали решать проблему излучения абсолютно черного тела. Странность постоянной в другом – в величине, которой она измеряется: энергия (Джоули), умноженная на время (секунды). Такая величина называется «действием» и не особенно часто появляется в классической механике. Не существует «закона сохранения действия», аналогичного законам сохранения массы или энергии, однако действие имеет одно интересное свойство, которое среди прочего есть и у энтропии. Постоянное действие является абсолютно постоянным и имеет одинаковую величину для всех наблюдателей в пространстве и времени. Оно имеет четыре измерения, и значение этого стало очевидным, лишь когда Эйнштейн вывел свою теорию относительности.
Поскольку Эйнштейн является следующим человеком, который появится на квантово-механической сцене, стоит немного отклониться в сторону, чтобы пояснить несколько основных принципов. Специальная теория относительности рассматривает три пространственных измерения и время как четырехмерное целое – пространственно-временной континуум. Наблюдатели, движущиеся в пространстве на разных скоростях, видят вещи по-разному: например, они получат различные значения длины палочки, которую они измеряют по мере прохождения мимо нее. Однако можно представить, что палочка существует в четырех измерениях и, по мере того как она движется «сквозь» время, она оставляет за собой четырехмерный след – гиперпрямоугольник, длина которого – это длина палочки, а ширина – количество прошедшего времени. «Площадь» этого прямоугольника измеряется как длина, умноженная на время, и эта площадь является одинаковой для всех наблюдателей, которые измеряют ее, хотя при этом они получают различные значения длины и времени. Таким же образом действие (энергиях время) является четырехмерным эквивалентом энергии, и действие оказывается одинаковым для всех наблюдателей, даже когда они получают различные значения компонентов действия – энергии и времени. В специальной теории относительности существует закон сохранения действия, и он настолько же важен, как и закон сохранения энергии. Постоянная Планка выглядела особенной лишь потому, что была открыта до теории относительности.
И это, возможно, указывает на холистическую природу физики. Из трех великих вкладов Эйнштейна в науку, опубликованных в 1905 году, один – специальная теория относительности – кажется совершенно отличным от двух других: работ о броуновском движении и фотоэлектрическом эффекте. И тем не менее все они связаны воедино форматом теоретической физики, и, несмотря на известность, которую получила теория относительности, самым главным вкладом Эйнштейна стала его работа о квантовой теории, которая оттолкнулась от работы Планка с помощью фотоэлектрического эффекта.
Революционный аспект работы Планка 1900 года заключался в том, что она показывала границы классической физики. По сути не так важно, что это за границы. Одного лишь факта, что существуют явления, которые не могут быть объяснены лишь с помощью классических идей, основанных на работе Ньютона, было достаточно, чтобы начать новую эру в физике. Впрочем, первоначальный вид работы Планка был гораздо более ограничен, чем зачастую кажется сегодня. Существует школа приключенческих романов, в которой
герой чудесным образом выходит из сложнейших ситуаций в конце каждого эпизода и все заканчивается фразой: «Один прыжок – и Джек освободился». Многие популярные тексты о рождении квантовой механики будто бы рассказывают о научном аналоге прыгуна Джека. «В конце XIX века классическая физика наткнулась на стену. И Планк одним прыжком изобрел квант, освободив физику». Далеко от действительности. Планк лишь предложил квантование электрических осцилляторов внутри атома. Он лишь подразумевал, что они способны испускать энергию только порциями, поскольку что-то мешает им поглощать и излучать «промежуточные» значения энергии.
Банкомат во многом работает сходным образом. Когда я снимаю деньги, банкомат выдает необходимую сумму, но лишь если она кратна 10 фунтам. Он не может выдавать промежуточные значения (и не может дать меньше, чем 10 фунтов), но это не означает, что таких значений, например 12,47 фунта, не существует. Сам Планк не сказал, что квантуется излучение, и он, вероятно, всегда настороженно относился к более глубоким следствиям квантовой теории. Позже, по мере развития квантовой теории, Планк внес свой вклад в эту науку, однако провел большую часть времени, пытаясь согласовать новые идеи с классической физикой. Не то чтобы он изменил свое мнение, просто он никогда не был доволен тем, как далеко от классической физики оказалось его уравнение для абсолютно черного тела – он вывел его, используя две классические теории: термодинамику и электродинамику. Вместо того чтобы изменить точку зрения, Планк пытался найти промежуточный вариант между квантовыми идеями и классической физикой, что было для него глубоким сдвигом в сторону от классических идей, на которых он был взращен. Однако его корни в классической физике были настолько крепки, что нечего удивляться тому, что настоящий прогресс был сделан новым поколением физиков, которые были меньше связаны со старыми идеями и привержены им. Они были воодушевлены новыми открытиями в атомном излучении и искали новые ответы как на старые, так и на новые вопросы.
Эйнштейн, свет и кванты
В марте 1900 года Эйнштейну был 21 год. Как известно, летом 1902 года он устроился на работу в Швейцарское патентное бюро и в те первые годы XX века в основном уделял свое внимание проблемам термодинамики и статистической механики. Его первые научные публикации были так же традиционны по стилю и затрагивали такие же классические проблемы, как и труды предыдущего поколения физиков, включая Планка. Но в первой же опубликованной работе, которая ссылалась на идеи Планка о спектре излучения абсолютно черного тела (она была опубликована в 1904 году), Эйнштейн нацелился на новые горизонты и начал развивать свой собственный стиль решения физических загадок. Мартин Кляйн свидетельствует, что Эйнштейн первым всерьез воспринял физические следствия работы Планка и расценил, что они являются не просто математической уловкой[7]. А через год его уверенность в том, что уравнения имеют под собой физическое основание, привела к совершенно новому озарению – возрождению корпускулярной теории света.
Помимо работы Планка, существовала и другая отправная точка для публикации 1904 года – исследования фотоэлектрического эффекта, осуществленные в конце XIX века Филиппом Ленардом и Дж. Дж. Томсоном, которые работали независимо друг от друга. Ленард родился в 1862 году в той части Венгрии, которая сейчас принадлежит Чехии, и в 1905 году получил Нобелевскую премию по физике за свое исследование катодных лучей. В 1899 году в ходе экспериментов он продемонстрировал, что катодные лучи (электроны) могут производиться светом, который светит на металлическую поверхность в вакууме. Каким-то образом энергия света заставляет электроны выпрыгивать из металла.
В опытах Ленарда использовались одноцветные пучки света (монохроматический свет), а это означает, что все световые волны обладают одинаковой частотой. Изучив, как интенсивность света влияла на процесс вырывания электронов из металла, Ленард пришел к удивительному результату. При использовании более яркого света (он просто передвигал тот же источник света ближе к металлической поверхности, что оказывало тот же самый эффект) на каждый квадратный сантиметр металлической поверхности попадало больше энергии. Если электрон получает больше энергии, он должен быстрее вырываться из металла и вылетать с большей скоростью. Однако Ленард обнаружил, что если длина световой волны оставалась неизменной, все вырванные электроны вылетали с одинаковой скоростью. Когда источник света придвигали ближе к металлической поверхности, количество вырываемых электронов увеличивалось, но каждый из этих электронов вылетал с той же скоростью, что и электроны, вырванные более слабым пучком света того же цвета. С другой стороны, электроны действительно двигались быстрее, когда использовался пучок света большей частоты – скажем, ультрафиолет вместо синего или красного цвета.
Все это объясняется очень просто, если вы готовы забыть о прочно укоренившихся идеях классической физики и посчитать уравнения Планка физически значимыми. Важность этой оговорки становится очевидна, когда узнаешь, что за пять лет, прошедших с начальной работы Ленарда над фотоэлектрическим эффектом и введения Планком концепции кванта, никто не предпринял этот, казалось бы, простой шаг. В сущности, Эйнштейн лишь применил уравнение Е = hv к электромагнитному излучению, а не к маленьким осцилляторам внутри атома. Он сказал, что свет не является непрерывной волной, как целое столетие считали ученые, а распространяется отдельными пакетами – квантами. Весь свет определенной частоты v, то есть определенного цвета, распространяется пакетами, обладающими одинаковой энергией Е. Каждый раз, когда один из этих квантов света ударяет электрон, он передает ему одинаковое количество энергии, а следовательно, одинаковую скорость. Большая мощность света означает лишь то, что квантов света (теперь мы называем их фотонами), обладающих одинаковой энергией, становится больше, но изменение цвета света изменяет его частоту, а значит, и количество энергии, переносимое каждым фотоном.
Именно за эту работу Эйнштейн в итоге получил Нобелевскую премию, которую вручили ему в 1921 году. И снова пришлось подождать, пока теоретический прорыв обретет полное признание. Идею о фотонах приняли не сразу, и, хотя опыты Ленарда в целом совпадали с теорией, потребовалось больше десяти лет, чтобы экспериментально доказать точное предположение о взаимозависимости скорости электронов и длины световых волн. Это удалось американскому экспериментатору Роберту Милликену, который в процессе опыта провел очень точное измерение значения h, постоянной Планка. В 1923 году Милликен тоже получил Нобелевскую премию по физике за свою работу и точные измерения заряда электрона.
Год у Эйнштейна выдался не из легких. Одна его работа в итоге привела к получению Нобелевской премии, другая раз и навсегда доказала реальность атомов, а в третьей родилась теория, прославившая его, – теория относительности. Практически случайно в том же 1905 году он закончил еще одну небольшую работу о размере молекул, которую подал в качестве докторской диссертации в университет Цюриха. Докторскую степень он получил в январе 1906 года. Хотя в те времена она не распахивала двери к активным исследованиям, как сегодня, все же примечательно, что три великие работы 1905 года были опубликованы человеком, который в момент их создания мог называть себя только «мистером» Альбертом Эйнштейном.
В последующие годы Эйнштейн продолжил интегрировать идеи Планка о кванте в другие области физики. Он обнаружил, что они объясняли давние загадки теории удельной теплоемкости (удельная теплоемкость вещества – это количество теплоты, которое необходимо сообщить телу, чтобы поднять его температуру на данную величину; она зависит от того, каким образом атомы колеблются внутри вещества, и эти колебания, как выяснилось, необходимо проквантовать). Эта физическая идея не столь привлекательна, и на нее часто не обращают внимания при изучении работ Эйнштейна, но квантовая теория вещества была принята быстрее, чем разработанная Эйнштейном квантовая теория излучения. Так многие физики старой школы начали убеждаться, что квантовые идеи стоит воспринимать всерьез. Эйнштейн долгие годы, вплоть до 1911-го, работал над улучшением своей концепции квантового излучения и доказал, что квантовая структура света является неизбежным следствием уравнения Планка, а также продемонстрировал невосприимчивому научному миру, что лучше понять природу света можно, связав волновую и корпускулярную теории, которые соперничали друг с другом с XVII века. К 1911 году его внимание переключилось на другие вещи. Он убедил самого себя в реальности квантов, а значение имело лишь его собственное мнение. Теперь его интересовала гравитация, и за пять лет – до 1916 года – он разработал общую теорию относительности, величайшую из его работ. Реальность квантовой природы света была окончательно подтверждена только в 1923 году, и это, в свою очередь, привело к новому спору о частицах и волнах, который помог трансформировать квантовую теорию и подтолкнуть появление ее современной версии, квантовой механики. Подробнее об этих идеях будет рассказано далее. Первый расцвет квантовой теории пришелся на десятилетие, в ходе которого Эйнштейн отдалился от этой области науки и сконцентрировался на других проблемах. Этот расцвет был связан с переплетением идей Эйнштейна с моделью атома Резерфорда и во многом произошел благодаря трудам датского ученого Нильса Бора, который работал вместе с Резерфордом в Манчестере. Когда Бор предложил свою модель атома, уже никто не смог усомниться в значении квантовой теории для описания физического мира мельчайших частиц.
Глава четвертая
Атом бора
К 1912 году кусочки атомной мозаики начали складываться воедино. Эйнштейн дал широкое обоснование идее кванта и ввел представление о фотонах, хотя оно пока не получило всеобщего признания. Продолжая аналогию с банкоматом, можно сказать, что Эйнштейн полагал, будто энергия распространяется лишь кусками определенного размера – банкомат дает только суммы, кратные десяти фунтам, потому что это самая мелкая купюра, с которой он работает, а не из того, что так захотел программист, настроивший его. Резерфорд предложил новую картину атома, с маленьким ядром в центре и облаком электронов вокруг, хотя эта идея тоже не получила всеобщей поддержки. Впрочем, атом Резерфорда не мог быть стабилен согласно классическим законам электродинамики. Решение крылось в том, чтобы использовать квантовые законы для описания поведения электронов внутри атомов. И опять прорыв совершил молодой исследователь со свежим взглядом на проблемы – квантовая теория развивалась именно так.
Датский физик Нильс Бор окончил аспирантуру летом 1911 года и в сентябре отправился в Кембридж, чтобы работать вместе с Дж. Дж. Томсоном в Кавендишской лаборатории. Он был очень молодым исследователем, сильно стеснялся и не владел в совершенстве английским языком. Ему было непросто найти себе место в Кембридже, однако во время поездки в Манчестер Бор познакомился с Резерфордом и тот по-дружески отнесся к нему, заинтересовавшись его исследованиями. В итоге в марте 1912 года Бор переехал в Манчестер и приступил к работе в команде Резерфорда, сконцентрировавшись на загадке структуры атома[8]. Через шесть месяцев он вернулся в Копенгаген, но лишь на короткое время, до 1916 года оставшись вместе с группой Резерфорда в Манчестере.
Прыгающие электроны
Бор обладал редким гением, который и был необходим, чтобы толкнуть атомную физику вперед на десять – пятнадцать лет. Он не стремился объяснить все детали в полной теории, а пытался свести воедино различные идеи, чтобы создать воображаемую «модель», которая хотя бы в первом приближении согласовывалась бы с экспериментальными данными наблюдений реальных атомов. Когда у него появлялось грубое представление о том, что происходит, с помощью него он сшивал вместе кусочки и таким образом продвигался к цельной картине. Он отталкивался от представления, что атом являет собой миниатюрную Солнечную систему, в которой электроны движутся по орбитам согласно законам классической механики и электромагнетизма, и утверждал, что электроны не могут сойти с этих орбит, излучая при этом, поскольку они могут испускать только целые куски энергии – кванты, – а не непрерывное излучение, как того требует классическая теория. «Устойчивые» орбиты электронов соотносились с некоторыми фиксированными величинами энергии, каждая из которых была кратна основному кванту, при этом промежуточные орбиты отсутствовали, поскольку они требовали бы дробного значения энергии. Если продолжить аналогию с Солнечной системой, то это все равно что сказать, что земная орбита вокруг Солнца устойчива и орбита Марса тоже, но между ними невозможно существование ни одной другой устойчивой орбиты.
То, что сделал Бор, не имело права на жизнь. Идея об орбите всецело опирается на классическую физику. Идея о состояниях электрона, соответствующих определенному количеству энергии, – или, как их позже назвали, энергетических уровнях – происходит из квантовой теории. Модель, построенная на соединении классической и квантовой теорий, не дала верного понимания, почему атомы дергаются, однако предоставила Бору достаточно сведений, чтобы пойти дальше. Его модель оказалась в итоге неверна почти во всем, однако она обеспечила переход к истинной квантовой теории атома, и это неоценимо. К сожалению, из-за своей простоты, легкого смешения квантовых идей с классическими и привлекательной картины атома в виде миниатюрной Солнечной системы эта модель продолжает существовать на первых страницах не только популярных книг, но и учебников и университетских работ. Если вы изучали атомы в школе, я уверен, что вы изучали модель атома Бора, как бы ее ни называли на уроках. Не буду призывать вас забыть все, что вам говорили, однако приготовьтесь к тому, что во многом все обстоит иначе. И вы должны постараться забыть об электронах в виде маленьких «планет», вращающихся вокруг ядра, – эта первая мысль Бора оказалась совсем не верна. Электрон представляет собой лишь нечто, находящееся рядом с ядром и обладающее определенным количеством энергии и рядом других свойств. Как мы убедимся, он движется таинственным образом.
Крупный ранний успех работы Бора в 1913 году состоял в том, что она прекрасно объяснила спектр излучения водорода – простейшего атома. Корни спектроскопии как науки уходят в ранние годы XIX столетия, когда Уильям Волластон открыл темные линии в спектре излучения Солнца, однако именно после работы Бора она стала инструментом для исследования структуры атома. Подобно Бору, смешавшему во имя прогресса классические и квантовые теории, нам придется сделать шаг назад от идей Эйнштейна о световых квантах, чтобы понять, как работает спектроскопия. В этом контексте нет смысла считать свет чем-то иным, нежели электромагнитной волной[9].
Как установил Ньютон, белый цвет состоит из всех цветов радуги, или спектра. Каждый цвет соответствует различной длине световой волны, и, используя стеклянную призму, можно разложить белый цвет на цветовые компоненты, то есть получить спектр, в котором волны разных частот располагаются на экране или фотопластинке друг под другом. Синие и фиолетовые цвета, имеющие короткие длины волн, находятся на одном конце оптического спектра, а длинноволновые красные – на другом. Однако спектр распространяется и дальше – в обе стороны за пределами видимого диапазона. При таком разложении солнечного света получающийся спектр имеет очень резкие темные линии в определенных местах, соответствующих определенным частотам. Не зная, почему возникают эти линии, исследователи Йозеф Фраунгофер, Роберт Бунзен (его именем названа горелка Бунзена) и Густав Кирхгоф в XIX веке экспериментально установили, что различные химические элементы дают собственный набор спектральных линий. Когда элемент (например, натрий) подогревается на горелке Бунзена, он приобретает характерное свечение (в случае натрия – желтого цвета), которое является следствием сильного излучения в виде яркой линии или линий на одном участке спектра. Когда белый цвет проходит через жидкость или газ, содержащие тот же элемент, то даже если этот элемент находится в химическом веществе в соединении с другими, спектр света приобретает темные полосы поглощения, подобные тем, что наблюдаются в солнечном излучении. Эти полосы соответствуют частотам, характерным для этого элемента (характеристическим частотам. – Примеч. пер.).
Таким образом были объяснены темные линии в солнечном спектре. Должно быть, они происходят от более холодных облаков вещества в атмосфере Солнца, которые на характеристических частотах поглощают проходящее через них излучение света от более горячей поверхности Солнца. Такой подход дал химикам удобный способ определять элементы, присутствующие в химическом веществе. Например, если бросить в огонь обычную соль, пламя приобретет характерный для натрия желтоватый оттенок (так же светятся дорожные фонари). В лаборатории можно увидеть характеристический спектр, если поместить тестируемое вещество на проволоку (обмакнуть ее) и держать ее в пламени горелки Бунзена. Каждый химический элемент дает собственный набор спектральных линий, и их структура всегда остается одинаковой, даже если изменяется температура пламени, хотя может меняться интенсивность. Резкость каждой спектральной линии означает, что каждый атом элемента излучает или поглощает на одной и той же частоте без исключений. Проводя сопоставления с подобными тестами на пламени, спектроскописты выяснили природу большинства линий в солнечном спектре и объяснили их наличием известных на Земле химических элементов. Известно, что английский астроном Норман Локьер (основатель научного журнала Nature) нашел в спектре Солнца линии, которые не могли быть объяснены спектром какого-либо известного элемента, и предположил, что они обязаны своим появлением неизвестному тогда элементу, который он назвал гелием. В свое время гелий был обнаружен и на Земле, и было установлено, что его спектр в точности соответствует тому, чего требовали линии в спектре Солнца.
С помощью спектроскопии астрономы могут изучать химический состав отдаленных звезд и галактик. В свою очередь, физики-атомщики этим методом могут исследовать внутреннюю структуру атома.
Спектр излучения водорода является особенно простым, что, как мы знаем сегодня, следует из простейшей структуры этого элемента – каждый атом содержит лишь один положительно заряженный протон в качестве ядра и связанный с ним отрицательно заряженный электрон. Линии в спектре водорода называются серией Бальмера в честь швейцарского школьного учителя Иоганна Бальмера, предложившего в 1885 году (в том же году родился Нильс Бор) формулу, описывающую спектр водорода. Формула Бальмера описывает взаимосвязь частот спектра, на которых появляются линии водорода. Отталкиваясь от частоты первой линии водорода в красной части спектра, формула Бальмера дает частоту следующей линии в зеленой части. Отталкиваясь от зеленой линии, та же самая формула, примененная к этой частоте, дает частоту следующей линии в фиолетовой части спектра – и так далее[10]. Когда Бальмер вывел свою формулу, ему было известно только о существовании четырех линий водорода в видимом спектре, но к тому моменту были открыты и другие линии, которые прекрасно вписывались в его простую численную схему, как и линии в ультрафиолетовой и инфракрасной части спектра, обнаруженные позже. Формула Бальмера явно сказала что-то важное о структуре атома водорода. Но что?
К моменту появления Бора формула Бальмера была известна всем физикам и входила в любой университетский курс. Но она была лишь частью огромного количества сложных сведений о спектрах, а Бор не был спектроскопистом. Взявшись за загадку структуры атома водорода, он не сразу понял, что серия Бальмера была очевидным ключом к ее разгадке, но однажды коллега показал ему, насколько простой была формула Бальмера (вне зависимости от сложности спектров других атомов), и он тотчас понял ее ценность. В то время, в начале 1913 года, Бор уже уверился, что ответ на загадку отчасти заключался в том, чтобы ввести постоянную Планка ft в уравнения, описывающие атом. В структуру атома Резерфорда были вписаны только два фундаментальных числа: заряд электрона е и массы задействованных частиц. Неважно, как играть с величинами: смешав массу и заряд, невозможно получить величину с размерностью длины, поэтому модель Резерфорда не имеет «естественной» единицы размера. Однако если добавить к этому действие – например ft, – можно создать число, включающее в себя значение длины, которое в очень грубой форме даст нам представление о размере атома. Выражение h2/me2 имеет размерность длины и равно приблизительно 20 × 10~8 см, что в целом согласуется со свойствами атомов, выявленными в опытах по рассеянию и других экспериментах. Бору было очевидно, что ft должна присутствовать в атомной теории, и серия Бальмера показала ему как.
Как атом может давать очень резкую спектральную линию? Либо излучая, либо поглощая энергию на очень точной частоте v. Энергия связана с частотой постоянной Планка (Е = hν ), и если электрон в атоме излучает квант энергии hν , то энергия электрона должна измениться в точности на соответствующее количество Е. Бор утверждал, что электроны на «орбите» ядра атома оставались на месте, потому что не могли постоянно излучать энергию, но в этой модели они могли излучать (или поглощать) целый квант энергии – один фотон – и перепрыгивать с одного энергетического уровня (одной орбиты в соответствии со старой моделью) на другой. Эта, казалось бы, простая мысль стала очередным значительным шагом в сторону от классических идей. Это все равно что Марс вдруг исчез бы со своей орбиты и мгновенно появился бы вновь на орбите Земли, при этом излучив в космос сгусток энергии (в этом случае речь шла бы о гравитационном излучении). Теперь вы видите, как плохо планетарная модель атома описывает происходящее и насколько лучше представлять себе электроны внутри атома в разных состояниях, соответствующих разным энергетическим уровням.
Прыжок от одного состояния к другому может происходить в любом направлении, как вверх, так и вниз по энергетической лестнице. Если атом поглощает свет, то квант hv используется для того, чтобы передвинуть его на более высокий энергетический уровень (на следующую ступеньку лестницы). Если электрон затем падает на свое изначальное место, излучается ровно такая же энергия hv. Таинственная константа 36,456 × 10-5 в формуле Бальмера может быть свободно записана с помощью постоянной Планка, а это означало, что Бор мог рассчитать возможные энергетические уровни, «открытые» для одиночного электрона в атоме водорода. Кроме того, измеренная частота спектральных линий теперь могла толковаться как определение энергетической разницы между различными уровнями[11].
Водород получает объяснение
Обсудив свою работу с Резерфордом, в серии статей в 1913 году Бор опубликовал собственную теорию атома. Теория хорошо работала для водорода, и казалось, что она может быть развита дальше, чтобы объяснить также спектры более сложных атомов. В сентябре Бор посетил восемьдесят третью ежегодную встречу Британской ассоциации развития науки и представил свою работу аудитории, которая в основном состояла из самых именитых физиков того времени. В общем и целом его доклад восприняли хорошо, а сэр Джеймс Джинс назвал его изобретательным, убедительным и заставляющим задуматься. Дж. Дж. Томсон оказался в числе тех, кого доклад не убедил, однако именно благодаря этой встрече ученые, которые сочли аргументы недостаточными, хотя бы услышали о Боре и его работе над атомами.
Спустя тринадцать лет с отчаянного решения Планка ввести квант в теорию света Бор ввел квант в теорию атома. Однако потребовалось еще тринадцать лет, чтобы появилась настоящая квантовая теория. В то время прогресс шел болезненно медленно – нужно было делать шаг назад, чтобы потом продвигаться на два шага вперед, а иногда и два шага назад взамен на один шаг в правильном направлении. Атом Бора представлял собой настоящую мешанину. Он сочетал квантовые идеи с классическими, используя любую кажущуюся необходимой смесь, чтобы сметать куски и сделать модель работоспособной. Он «разрешал» существование гораздо большего количества спектральных линий, чем наблюдалось в излучении различных атомов, и приходилось вводить произвольные правила, чтобы некоторые переходы между различными энергетическими состояниями в атоме стали «запрещенными». Новые свойства атома – квантовые числа – назначались от случая к случаю, чтобы соответствовать наблюдениям, хотя не существовало должного теоретического обоснования того, зачем нужны были эти квантовые числа или почему некоторые из переходов оказывались запрещены. В процессе этого европейский мир потрясло начало Первой мировой войны, разразившейся на следующий год после того, как Бор представил свою первую модель атома.
Как и любая другая сфера жизни, наука после 1914 года уже не могла быть прежней. Из-за войны ученые больше не могли свободно переезжать из одной страны в другую. Начиная с Первой мировой войны некоторым ученым из ряда стран стало трудно общаться с коллегами по всему миру. Война также оказала прямое воздействие на научные исследования в крупных исследовательских центрах, где в начале XX века физики добились существенного прогресса. В условиях войны многие молодые ученые покинули лаборатории и ушли на фронт, оставив более зрелых профессоров вроде Резерфорда продолжать исследования в одиночку. Многие из этих юношей, представителей поколения, которое должно было подхватить идеи Бора и начало подхватывать их в 1913-м, погибли в боях. Война повлияла и на работу нейтральных ученых, хотя в некотором роде они получили преимущество из-за проблем остальных. Сам Бор стал лектором физики в Манчестере, в Геттингене голландец Петер Дебай хорошо изучил структуру кристаллов, используя рентгеновские лучи. В то время Дания и Голландия стали настоящими научными оазисами, и в 1916 году Бор вернулся в Данию, где стал профессором теоретической физики в Копенгагене, а в 1920 году основал исследовательский институт, названный в его честь. Вести от немецкого исследователя Арнольда Зоммерфельда (одного из физиков, которые улучшили модель атома Бора, внесшего в нее такой вклад, что иногда эту модель называют «атомом Бора – Зоммерфельда») могли приходить в нейтральную Данию, а затем от Бора – к Резерфорду, находившемуся в Англии. Прогресс продолжался, но все уже было иначе.
После войны немецких и австрийских ученых многие годы не приглашали на международные конференции, Россия оказалась охвачена пламенем революции, а наука вместе с молодыми исследователями потеряла и свой международный характер. Совершенно новому поколению предстояло подхватить квантовую теорию, которая остановилась в своем развитии на полпути после представления запутанного атома Бора (который, стоит признать, был значительно улучшен благодаря усилиям многих ученых и стал эффективной, хоть и беспорядочной моделью), и привести ее к расцвету. Имена исследователей этого поколения знакомы любому современному физику: Вернер Гейзенберг, Поль Дирак, Вольфганг Паули, Паскуаль Йордан и другие. Представители первого квантового поколения, они все родились и выросли уже после великого открытия Планка (Паули в 1900 году, Гейзенберг в 1901-м, Дирак и Йордан – в 1902-м) и пришли в науку в 1920-х годах. Им не нужно было преодолевать прочно засевшие в сознании идеи классической физики, и они, в отличие от великих ученых вроде Бора, уже не чувствовали необходимости идти на полумеры и сохранять связь с классическими идеями, представляя свои концепции атома. Все это было абсолютно закономерно: вероятно, не было совпадением и то, что с момента открытия Планком уравнения излучения абсолютно черного тела до расцвета квантовой физики прошло всего двадцать шесть лет – ровно столько, сколько нужно было новому поколению физиков, чтобы превратиться в настоящих исследователей. Более старшие ученые, которые все еще принимали активное участие в работе, оставили этому поколению в наследство две идеи, помимо самой постоянной Планка. Первой был атом Бора, который явно показал, что квантовые идеи должны быть вплетены в любую удовлетворительную теорию объяснения атомных процессов. Вторая стала заслугой одного великого ученого того времени, который, казалось, наперекор всему никогда не хватался за идеи классической физики. В 1916 году, в разгар войны работая в Германии, Эйнштейн ввел в атомную теорию понятие вероятности. Это была уловка – еще одно дополнение к атому Бора, благодаря которому его поведение стало похожим на наблюдаемое поведение настоящих атомов. Но эта уловка продлила жизнь атома Бора и сделала его крепкой основой истинной квантовой теории – хотя по иронии судьбы впоследствии Эйнштейн сам же отказался от нее, как известно, заявив: «Бог не играет в кости».
Дата добавления: 2018-10-26; просмотров: 259; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
