ВЗАИМОДЕЙСТВИЕ МЕТАЛЛОВ С АЗОТНОЙ КИСЛОТОЙ
HNO3 как сильная одноосновная кислота взаимодействует:
а) с основными и амфотерными оксидами:
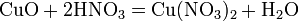
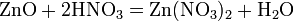
Азотная кислота в любой концентрации проявляет свойства кислоты-окислителя, при этом азот восстанавливается до степени окисления от +4 до −3. Глубина восстановления зависит в первую очередь от природы восстановителя и от концентрации азотной кислоты. Как кислота-окислитель, HNO3 взаимодействует:
а) с металлами, стоящими в ряду напряжений правее водорода:
Концентрированная HNO3
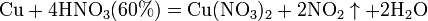
Разбавленная HNO3
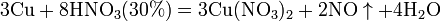
б) с металлами, стоящими в ряду напряжений левее водорода:
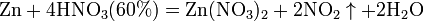
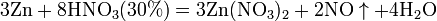
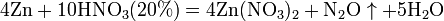
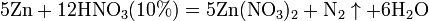
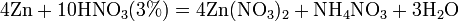
С золотом и платиной азотная кислота, даже концентрированная не взаимодействует. Железо, алюминий, хром холодной концентрированной азотной кислотой пассивируются. С разбавленной азотной кислотой железо взаимодействует, причем в зависимости от концентрации кислоты образуются не только различные продукты восстановления азота, но и различные продукты окисления железа:
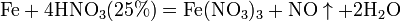
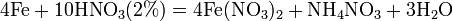
Смесь 3 объемов концентрированной соляной и 1 объема азотной кислоты называют «царской водкой». Это название отражает тот факт,что указанная смесь растворяет «царя металлов»- золото:
Au+4HCl+HNO3=H[AuCl4]+NO+2H2O
3Pt+4HNO3+18HCl=3H2[PtCl6]+4NO+8H2O
3HgS + 8HNO3(конц.) + 6HCl(конц.) = 3HgCl2+ 3H2SO4 + 8NO↑ + 4H2O
Соли азотной кислоты — нитраты — при нагревании необратимо разлагаются, продукты разложения определяются катионом:
а) нитраты металлов, стоящих в ряду напряжений левее магния:
|
|
|
2NaNO3 = 2NaNO2 + O2
б) нитраты металлов, расположенных в ряду напряжений между магнием и медью:
4Al(NO3)3 = 2Al2O3 + 12NO2 + 3O2
в) нитраты металлов, расположенных в ряду напряжений правее ртути:
2AgNO3 = 2Ag + 2NO2 + O2
г) нитрат аммония:
NH4NO3 = N2O + 2H2O
Общая характеристика и химические свойства фосфора его получение в промышленности.
Оксиды фосфора: получение, строение молекул и свойства.
Фосфорноватистая и фосфористая кислоты: получение, строение молекул, кислотно-основные и окислительно-восстановительные свойства. Фосфиты и гипофосфиты.
Кислоты фосфора (+5) и качественные реакции на них. Получение фосфорной кислоты в промышленности.
В природных условиях фосфор представлен минералами фосфоритом Сa3(PO4)2 и апатитом 3Ca3(PO4)2*CaX2 (X=F,Cl,OH).Тело человека в среднем содержит около полутора килограммов фосфора. Описано 11 модификаций фосфора, причем каждая модификация полиморфна. Наибольший интерес представляют белый, красный и черный фосфор. Белый фосфор-мягкое, реакционноспособное очень токсичное вещество, хранят под слоем воды, так как на воздухе он самовоспламеняется.Белый фосфор представлен молекулами P4,имеющими форму тетраэдра и распадающимися при температурах выше 800 на молекулы состава P2.Эти молекулы менее прочны чем молекулы N2.При длительном нагревании свыше 250 белый фосфор переходит в красный фосфор, который вполне устойчив на воздухе, не ядовит и воспламеняется только при нагревании свыше 400.Черный фосфор, являющийся наиболее устойчивой модификацией, получается из белого фосфора при высоком давлении. Черный фосфор жирен на ощупь, похож на графит, полупроводник не ядовит.
|
|
|
Из всех аллотропных модификаций фосфора за стандартное состояние принят белый фосфор, хотя он не является термодинамически наиболее стабильной модификацией.
Белый фосфор получают путем прокаливания фосфорной руды с коксом и кварцевым песком в электропечи: Ca3(PO4)2+5C+3Sio2=(t)=2P+3CaSiO3+5CO.
Химические свойства.
Валентные возможности атома фосфора по методу ВС 3 и 5,степени окисления в соединениях изменяются от -3 до +5,у атома фосфора в отличие от атома азота имеется возможность донорно-акцепторного механизма за счет свободных d-орбиталей.
Окисление фосфора ведет к Двум оксидам P4O6 и P4O10,первый образуется при недостатке кислорода(избытке фосфора),а второй-при избытке кислорода
P4+3O2(нед.)=P4O6
P4+5O2(изб.)=P4O10
В молекулах этих оксидов сохраняется тетраэдрическое строение молекулы белого фосфора. В оксиде P4O6 каждое ребро тетраэдра P4 «встраивается» атом кислорода, а в оксиде P4O10-еще и к каждому атому фосфора, находящемуся в вершинах тетраэдра, присоединяется по атому кислорода.
|
|
|
Фосфор реагирует сравнительно легко с серой, галогенами и другими неметаллами:
P4+6Г2(недост)=4PГ3
P4+10Г2(изб)=4PГ5
P4+10S=P4S10 (и другие соединения)
При спекании порошков металлов с фосфором образуются Фосфиды металлов
P4+6Zn=t=2Zn3P2
12K+P4=4K3P
Фосфор безразличен к водным растворам минеральных кислот. Медленно реагирует с кислотами-окислителями:
3P4+20HNO3(конц)+8H2O=12H3PO4+20NO
P4+20HNO3(конц)=4HPO3+20NO2+8H2O
P4+10H2SO4(конц)=4HPO4+10SO2+4H2O
В теплом растворе щелочи P4 диспропорционирует
P4+3NAOH+3H2O=PH3+3NaH2PO2
Фосфорноватистая кислота может быть получена
P4+3Ba(OH)2+6H2O=PH3+3Ba(H2PO2)2
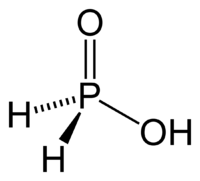 Ba(H2PO2)2+H2SO4=BaSO4+2H3PO2
Ba(H2PO2)2+H2SO4=BaSO4+2H3PO2
H3PO2-одноосновная, достаточно сильная
Соли фосфорноватистой кислоты называются гипофосфитами являются хорошими восстановителями,легко окисляются до соединений фосфора 3 и 5,находят применение для химической металлизации диэлектриков:
H3PO2+4AgNO3+2H2O=H3PO4+4Ag+4HNO3
2CuSO4+NaH2PO2+2H2O=2Cu+NaH2PO4+2H2SO4.
Ангидрида кислота H3PO2 не имеет.
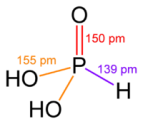
Фосфористая кислота, H2(PHO3), двухосновная в водных растворах, а формально трёхосновная кислота средней силы.
|
|
|
P4O6+6H2O(холод)=4H3PO3
 7P4O6+30H2O(гор)=2PH3+2P4+18H3PO4
7P4O6+30H2O(гор)=2PH3+2P4+18H3PO4
H3PO3+Cl2+H2O=2HCl+H3PO4
Na2HPO3+2AgNO3+H2O=Na2HPO4+2Ag+2HNO3
Фосфиты являются неплохими восстановителями, в ОВР окисляются до соединений фосфора 5
H3PO3+Cl2+H2O=2HCl+H3PO4
Na2HPO3+2AgNO3+H2O=Na2HPO4+2Ag+2HNO3
P4O10+2H2O=4HPO3(мета)
2HPO3+H2O=H4P2O7(пиро)
H4P2O7+H2O=2H3PO4(орто)
Растворы мета- и пирофосфорной кислот достаточно трудно отличить,до сих пор для определения этих кислот используется буквально старинный рецепт мета-сворачивает яичный белок,пиро-нет.
Н3РО4 + 3AgNO3 = Ag3PO4 + 3HNO3
Качественной реакцией на ион РО43− является образование ярко-жёлтого осадка молибденофосфата аммония:
H3PO4 + 12(NH4)2MoO4 + 21HNO3 = (NH4)3PMo12O40·6H2O + 21NH4NO3 + 6Н2О
Получение в промышленности
4Р + 5О2 = Р4О10
Р4О10 + 6Н2О = 4Н3РО4
Дата добавления: 2018-08-06; просмотров: 1092; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
