Работа 4.3. ОПРЕДЕЛЕНИЕ ИНДЕКСОВ КОВАЧА ВЕЩЕСТВ И ИХ ТЕМПЕРАТУРНЫХ КОЭФФИЦИЕНТОВ НА АПЬЕЗОНЕ
Цель работы - получить исправленные времена выхода (VR) для веществ, предложенных преподавателем, для температур от 75 до 150°С и определить индексы Ковача и температурные коэффициенты этих индексов (ΔI / Δt).
Оборудование: Газовый хроматограф, микрошприц, газовый шприц, секундомер.
Реактивы: эквимолярная смесь нормальных углеводородов: гексана, гептана, октана и нонана , контрольная смесь.
Порядок выполнения работы:
1. Получить у лаборанта эквимолярную смесь н- углеводородов: гексана, гептана, октана и нонана, исследуемое вещество, микрошприц на 10 мкл, медицинский шприц и секундомер.
2. Включить хроматограф согласно описанию "Порядок работы на хроматографе". Установить лимб "Температура колонок" на одной из температур;75; 100; 125 или 150°С.
3. После выхода хроматографа на режим, измерения расхода газа-носителя пенометром и температуры колонок (точно) сделать впуск 0,3 мл воздуха газовым шприцем и определить время его выхода по максимуму обратного (в левую сторону) пика на хроматограмме.
4. Сделать два впуска 1-2 мкл эквимолярной смеси н-углеводородов, определить времена выхода всех 4 пиков. Записать результаты в табл. 4.8.
5. Сделать два впуска исследуемого вещества и записать в табл. 4.8 времена удерживания.
6. Рассчитать величины Wиспр. по (4.15), VR по (4.6) и lgVR.
7. Проделать подобные опыты при 75, 100, 125 и 150°С.
8. Построить график зависимости lg Vr от числа атомов углерода (nC•100) для каждой температуры.
|
|
|
9. Найти по графику индекс Ковача исследуемого вещества для каждой температуры и температурные коэффициенты ΔI/Δt для каждого интервала температур в 25°С. Записать в таблицу 4.9.
10. Рассчитать индексы Ковача Ix неизвестного вещества для каждой температуры по формуле (4.8). Полученные результаты записать в таблицу 4.9. Сравнить рассчитанные Ix со справочными данными и определить неизвестное вещество
Таблица 4.8
| t кол. | Воздух t0,С | Углеводород | tуд | tуд сред | tR | Wиспр см3 мин | vr |
InVR | I= nc x 100 | ||
| °С | К | 1 впуск | 2 впуск | ||||||||
|
75
|
|
| С6 |
|
|
|
|
|
|
|
|
|
| С7 |
|
|
|
|
|
|
|
| ||
|
| С8 |
|
|
|
|
|
|
|
| ||
|
| С9 |
|
|
|
|
|
|
|
| ||
|
| X |
|
|
|
|
|
|
|
| ||
|
100
|
|
| С6 |
|
|
|
|
|
|
|
|
|
| С7 |
|
|
|
|
|
|
|
| ||
|
| С8 |
|
|
|
|
|
|
|
| ||
|
| С9 |
|
|
|
|
|
|
|
| ||
|
| X |
|
|
|
|
|
|
|
| ||
|
125
|
|
| С6 |
|
|
|
|
|
|
|
|
|
| С7 |
|
|
|
|
|
|
|
| ||
|
| С8 |
|
|
|
|
|
|
|
| ||
|
| С9 |
|
|
|
|
|
|
|
| ||
|
| X |
|
|
|
|
|
|
|
| ||
|
150
|
|
| С6 |
|
|
|
|
|
|
|
|
|
| С7 |
|
|
|
|
|
|
|
| ||
|
| С8 |
|
|
|
|
|
|
|
| ||
|
| С9 |
|
|
|
|
|
|
|
| ||
|
| X |
|
|
|
|
|
|
|
| ||
Работу 4.3 можно выполнять при выполнении работ 4.1 и 4.2.
Таблица 4.9
| Вещество | 75 – 100 ˚C | 100 – 125 ˚C | 125 – 150 ˚C |
| Ix (графически) | |||
| Ix(рассчитанное) | |||
| ΔI / Δt |
КОНТРОЛЬНЫЕ ВОПРОСЫ К РАБОТЕ 4.3
Перед выполнением работы:
1. Какова цель работы?
2. Нарисуйте схему газового хроматографа. Расскажите, из каких узлов состоит хроматограф. Порядок включения узлов.
3. Какие параметры хроматографического опыта нужно измерить перед впуском смеси в хроматограф?
|
|
|
4. Как задать и измерить температуру колонок?
5. Какие параметры надо измерять в процессе получения хроматограммы вещества или смеси веществ?
6. Зачем делают впуски воздуха в колонку?
7. Как рассчитать VR из параметров опыта?
К защите работы:
1. Что является качественной характеристикой данного вещества в хроматографическом анализе?
2. Какие зависимости параметров удерживания наблюдаются в гомологических рядах углеводородов?
3. Дайте определение индекса Ковача.
4. От каких параметров зависит индекс Ковача вещества?
5. Как использовать индексы Ковача, известные из литературы, для качественного анализа смесей?
- ХИМИЧЕСКАЯ КИНЕТИКА
Химическая кинетика – раздел физической химии, в котором изучаются скорости протекания химических процессов, их зависимости от различных факторов: концентрации реагирующих веществ, температуры, давления, присутствия катализатора и т.д.
Различаются простые (элементарные) химические реакции, протекающие в одну стадию, и сложные реакции, протекающие через несколько стадий (т.е. являющиеся совокупностью простых реакций). Механизмом (кинетической схемой) химической реакции называется совокупность простых реакций, через которые она протекает.
|
|
|
В ходе химической реакции концентрации её участников изменяются. Исходные вещества (реагенты) расходуются, и концентрация их уменьшается, продукты образуются, их концентрация растет. Если реакция является сложной, то образуются промежуточные вещества, концентрация которых сначала возрастает, а затем уменьшается до нуля. Кинетической кривой называется зависимость концентрации какого-либо участника реакции от времени. Как и любая функция, кинетическая кривая может быть задана в виде графика, таблицы или уравнения (аналитически).
Важнейшими понятиями являются «скорость химической реакции» и «скорость химической реакции по данному веществу». Пусть в гомогенной системе объёмом V проходит химическая реакция, и за время dτ количество i-го участника реакции системе изменилось на величину dni. В том случае, если стехиометрическое уравнение реакции неизвестно, её скорость определяется по веществу i, как изменение количества этого вещества ni (в молях) в единицу времени τ в единице реакционного пространства R, взятую со знаком «+», если вещество образуется в ходе химической реакции, и со знаком «–», если оно расходуется
 5.1
5.1
Реакционным пространством R для гомогенных реакций, протекающих в объеме данной фазы, является объем (R=V), для гетерогенных реакций, протекающих на поверхности раздела фаз – площадь поверхности (R=S).
Скорость wi называется скоростью химической реакции по веществу i.
Рассмотрим скорость реакции в закрытой гомогенной системе. Если объём реакционной системы постоянен, его можно внести под знак дифференциала, и скорость химической реакции по веществу i будет равна производной его концентрации по времени:
 , 5.2
, 5.2
Различают среднюю и инстинную скорость химической реакции. Средняя скорость реакции 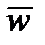 равна:
равна:
 , 5.3
, 5.3
где ni1, ni2 – количество молей реагирующего вещества в моменты времени τ1 и τ2, соответственно, V – объем системы. Если объем системы не меняется в ходе реакции, то
 , 5.3*
, 5.3*
В различных интервалах времени средняя скорость химической реакции имеет разные значения; истинная (мгновенная) скорость реакции определяется как производная от концентрации по времени:

Графическое изображение зависимости концентрации реагентов от времени есть кинетическая кривая (рисунок 5.1).
|
Рис. 5.1 Кинетические кривые для исходных веществ (А) и продуктов реакции (В).
|
Рис. 5.2 Графическое определение w. |
Истинную скорость реакции можно определить графически, проведя касательную к кинетической кривой (рис. 5.2); истинная скорость реакции в данный момент времени равна по абсолютной величине тангенсу угла наклона касательной.
Если стехиометрическое уравнение реакции известно, скорость можно определить по любому из её участников. Пусть, например, уравнение реакции имеет вид:

Тогда:  ;
;  ;………
;………
 ;
;  ; ……….
; ……….
Скорости  не равны друг другу. Из стехиометрического уравнения следует, что если в ходе реакции израсходовалось νА1 моль вещества А1, то одновременно израсходовалось и νА2 моль вещества А2, и образовалось νВ1 и νВ2 моль веществ В1 и В2, т.е.
не равны друг другу. Из стехиометрического уравнения следует, что если в ходе реакции израсходовалось νА1 моль вещества А1, то одновременно израсходовалось и νА2 моль вещества А2, и образовалось νВ1 и νВ2 моль веществ В1 и В2, т.е.
 5.4
5.4
Тогда, с учетом (5.4):
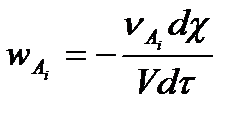 ,
, 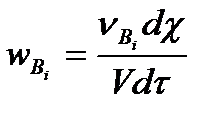 5.5
5.5
и имеет место равенство:
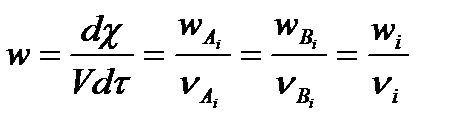 5.6
5.6
Скорость w называется скоростью химической реакции. Она одинакова для всех веществ, участвующих в данной реакции и не зависит от выбора реагента. Скорость реакции равна скорости образования какого либо реагента, деленной на его стехиометрический коэффициент с учетом принятых знаков. Для реакции H2 + I2 = 2HI из одного моля Н2 и одного моля I2 получается два моля HI, поэтому скорость образования HI будет вдвое больше скоростей расходования Н2 и I2, а значит скорость реакции будет равна:
 .
.
Размерность скорости реакции  … для гомогенных реакций и
… для гомогенных реакций и  для гетерогенных реакций.
для гетерогенных реакций.
Кинетическим уравнением химической реакции называется уравнение, описывающее зависимость скорости реакции от концентрации компонентов реакционной смеси:
 5.7
5.7
Математический вид этой зависимости может быть более или менее сложным. Например, для сложной реакции в газовой фазе H2 + Br2 = 2HBr
 ,
,
где k, k1 – постоянные. Для другой сложной реакции COCL2→ CO + CL2 кинетическое уравнение имеет более простой вид:  .
.
Опыт показывает, что часто кинетическое уравнение можно представить в виде произведения концентраций реагирующих исходных веществ, возведенных в некоторые степени n1, n2, …
 5.8
5.8
Величина k называется константой скорости реакции (или удельной скоростью реакции) и равна скорости реакции при единичных концентрациях всех реагирующих веществ. n1, n2 - порядки реакции по веществам-реагентам (иногда их называют частными порядками). Порядок реакции по данному веществу - это показатель степени, в которой концентрация этого вещества входит в уравнение скорости реакции. Сумма n1+n2+… определяет порядок реакции в целом (п) (общий порядок). Для сложных реакций порядки реакции могут быть целыми, дробными, положительными и отрицательными.
Для элементарных реакций справедлив закон действующих масс, согласно которому скорость реакции пропорциональна произведению концентраций реагирующих веществ, взятых в степенях, равным стехиометрическим коэффициентам:
 5.9
5.9
Величина  называется молекулярностью реакции.
называется молекулярностью реакции.
Молекулярность элементарной реакции – число частиц, которые, согласно экспериментально установленному механизму реакции, участвуют в элементарном акте химического взаимодействия.
Мономолекулярные – реакции, в которых происходит химическое превращение одной молекулы (изомеризация, диссоциация и т. д.): I2 ––> I• + I•
Бимолекулярные – реакции, элементарный акт которых осуществляется при столкновении двух частиц (одинаковых или различных): СН3Вr + КОН ––> СН3ОН + КВr
Тримолекулярные – реакции, элементарный акт которых осуществляется при столкновении трех частиц:
О2 + NО + NО ––> 2NО2
Реакции с молекулярностью более трёх неизвестны.
Для элементарных реакций, проводимых при близких концентрациях исходных веществ, величины молекулярности и порядка реакции совпадают. Тем не менее, никакой чётко определенной взаимосвязи между понятиями молекулярности и порядка реакции не существует, поскольку порядок реакции характеризует кинетическое уравнение реакции, а молекулярность – механизм реакции.
Для сложных реакций понятие молекулярности неприменимо. Реакции с большими стехиометрическими коэффициентами являются сложными, так как протекают через ряд промежуточных стадий, поэтому частные порядки и стехиометрические коэффициенты, как правило, не совпадают.
В отличие от молекулярности порядок реакции - формальная характеристика. Тем не менее, зная порядки реакции в целом и порядки по реагентам, можно рассчитать константу скорости реакции, а также судить о соответствии предполагаемого механизма реакции (совокупности промежуточных элементарных стадий сложной реакции) опытным данным.
Кинетические уравнения реакций различных порядков
Реакции нулевого порядка
Для реакций нулевого порядка кинетическое уравнение имеет следующий вид:
 5.9
5.9
Скорость реакции нулевого порядка постоянна во времени и не зависит от концентраций реагирующих веществ; это характерно для многих гетерогенных (идущих на поверхности раздела фаз) реакций в том случае, когда скорость диффузии реагентов к поверхности меньше скорости их химического превращения.
Реакции первого порядка
Рассмотрим зависимость от времени концентрации исходного вещества А для случая реакции первого порядка А ––> В. Реакции первого порядка характеризуются кинетическим уравнением вида:
 5.10
5.10
Пусть в объеме V в начальный момент времени находилось а молей исходного вещества (С0), за время τ происходит превращение х молей этого вещества, следовательно, к моменту τ его остается (а-х) молей (Сτ=С), тогда
 и
и 
Поскольку  , то после разделения переменных и интегрирования получаем:
, то после разделения переменных и интегрирования получаем:
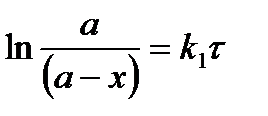 и
и 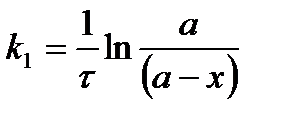 5.11
5.11
либо  5.11*
5.11*
|
Рис 5.3 Зависимость логарифма концентрации от времени для реакций первого порядка
| Т.о., логарифм концентрации для реакции первого порядка линейно зависит от времени (рис. 5.3) и константа скорости численно равна тангенсу угла наклона прямой к оси времени.
|
Размерность константы: к1=τ-1=[с-1; мин-1,…]
Еще одной кинетической характеристикой реакции является период полупревращения τ1/2 – время, за которое концентрация исходного вещества уменьшается вдвое по сравнению с исходной. Учитывая, что С = ½Со:
 5.12
5.12
Как видно из полученного выражения, период полупревращения реакции первого порядка не зависит от начальной концентрации исходного вещества.
Реакции второго порядка
Для реакций второго порядка кинетическое уравнение имеет следующий вид:  5.13
5.13
либо  5.14
5.14
Рассмотрим простейший случай, когда кинетическое уравнение имеет вид (5.13) или, что то же самое, в уравнении вида (5.14) концентрации исходных веществ одинаковы. Пусть в объеме V в начальный момент времени находилось а молей исходного вещества (С0), за время τ происходит превращение х молей этого вещества, следовательно, к моменту τ его остается (а-х) молей (Сτ=С), тогда
 5.15
5.15
После разделения переменных и интегрирования получаем:
 или
или  5.16
5.16
| Т.о., для реакций второго порядка, имеющих кинетическое уравнение вида (5.13), характерна линейная зависимость обратной концентрации от времени (рис. 5.4) и константа скорости равна тангенсу угла наклона прямой к оси времени:
|
|
Период полупревращения равен:  5.16
5.16
Если начальные концентрации реагирующих веществ Cо,А=и Cо,В различны, то константу скорости реакции находят интегрированием уравнения (5.17), в котором а и в – числа молей веществ в начальный момент, а (а-х) и (в-х) - в момент времени τ от начала реакции:
 5.17
5.17
В этом случае для константы скорости получаем выражение:
 5.18
5.18
Размерность константы: к2=τ-1С-1 =[л·моль-1·с-1; л·моль-1· мин-1,…]
Реакции n-го порядка
Для реакций n-го порядка кинетическое уравнение имеет следующий вид:
nA → D + … и  5.19
5.19
Решение кинетического уравнения:
 5.20
5.20
Информация для реакций различных порядков приведена в таблице 5.1.
Дата добавления: 2018-04-15; просмотров: 424; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!







 Рис. 5.4 Зависимость обратной концентрации от времени для реакций
Рис. 5.4 Зависимость обратной концентрации от времени для реакций