Методика експерименту та обробка даних
Катод перед початком експерименту зачищають наждачним папером, знежирюють в содовому розчині та промивають водою. Потім висушують і зважують на аналітичних терезах.
Величину струму розраховують виходячи з прийнятої густини струму та розмірів катода за формулою:
 , (2.5)
, (2.5)
де j – густина струму, приймається j=5 А/дм2;
S – площа катода, дм2.
Перевіривши правильність зібраної схеми лабораторної установки, електроди занурюють в електроліт і пропускають через систему електричний струм. На протязі всього експерименту (приблизно 1год) струм підтримують постійним і визначають напругу в електролізері.
По закінченню електролізу катод обережно промивають водою, залишки води видаляють за допомогою фільтрувального паперу. Катод висушують і зважують на аналітичних терезах.
Потім розраховують вихід за струмом (формула 2.4).
Витрату електроенергії на одиницю видаленого металу (Wпит) визначають за формулою:
Wпит = U·105/(m·Вт), кВт·год/т, (2.6)
де U – напруга на клемах електролізера, В.
Експерименти проводять із стічними водами, які містять: в першому випадку 250 г/л CuSO4·5H2O та 64г/л H2SO4; в другому випадку 100г/л CuSO4·5H2O та 64г/л H2SO4.
Результати експериментів заносять до таблиці 2.1.
Таблиця 2.1 - Результати експериментів при катодному осадженню міді
| Хімічний склад електроліту | Концентра-ція компо-нентів Co, г/л
| Площа катода S, дм2 | Густина струму j, А/дм2 | Величина сили струму J, А | Напруга U, В | Вага катода | Вихід за струмомВт, % | Витрата електро-енергії Wпит, кВт·год/m | |||
| початкова, г | кінцева, г | ||||||||||
| CuSO4·5H2O H2SO4 | 250 64 | ||||||||||
| CuSO4·5H2O H2SO4 | 250 64 | ||||||||||
Зміст звіту
В звіті зазначаються: назва та мета лабораторної роботи; наводиться схема лабораторної установки; описується методика експерименту та наводяться результати розрахунків у вигляді табл. 2.1.
В кінці роботи пишеться висновок.
Контрольні запитання
1. Сформулювати закони Фарадея. Фізичний зміст сталої Фарадея.
2. Хімічний та електрохімічний потенціали металів.
3. Які основні хімічні процеси проходять на катоді та аноді в електролізері.
4. Як визначається вихід за струмом.
Лабораторна робота №3
Визначення оптимальної дози коагуляНту при очищенні промислових стічних вод
Мета роботи
Вивчити методику пробної коагуляції та визначити оптимальні дози коагулянту без підлужування та за підлужуванням води.
Загальні положення
Для очищення промислових стічних вод, які містять забруднення у вигляді тонкодисперсних домішок та колоїдів, застосовують метод коагуляції. В якості коагулянтів використовують: сульфат алюмінію Al2(SO4)3, оксохлорид алюмінію Aln(OH)mCl, хлорид заліза FeCl3, сульфат двохвалентного заліза FeSO4, сульфат трьохвалентного заліза Fe2(SO4)3. Особливістю цих солей є здатність утворювати в результаті гідролізу малорозчинні сполуки:
|
|
|
 ;
;
 ;
;
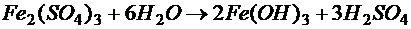 ;
;
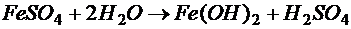 .
.
Гідроокис двовалентного заліза має значну розчинність, тому його переводять в тривалентну форму, використовуючи окислювачі, наприклад кисень повітря, хлор, озон та інші:
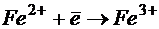 ;
;
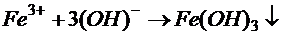
В процесі гідролізу утворюються сірчана або соляна кислоти, які треба нейтралізувати вапном або іншими лугами. Нейтралізація кислот може проходити за рахунок лужного резерву стічної води:
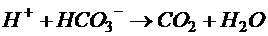 .
.
На ефективність дії коагулянтів впливає багато чинників (факторів), таких як: склад та якість забрудненої стічної води, температура, рН води, умови введення та перемішування реагуючих речовин, доза та склад коагулянту.
Для максимального видалення забруднень процес коагуляції необхідно здійснювати в діапазоні оптимальних величин рН. При відсутності цих даних можна приймати, що найбільший ефект очищення стічних вод при використанні в якості коагулянту сульфату алюмінію досягається в інтервалі значень рН середовища від 6.5 до 8; при використанні хлориду заліза – в інтервалі значень від 7 до 8,5; при використанні сульфату двовалентного заліза від 9 до 9,5.
|
|
|
Оптимальну дозу коагулянту визначають експериментально, пробним коагулюванням для кожного конкретного складу стічних вод при суворо визначених умовах проведення експерименту.
Реактиви, посуд та прилади
1. рН-метр.
2. Циліндри по 500 мл – 5 штук.
3. Бюретка, колби по 250 мл для титрування, хімічні стакани.
4. 0,1н разчин НСl.
5. Метилоранж – індикатор.
6. Гідроокис кальцію, 0,1%-й розчин: 1г попередньо прокаленого окису кальцію СаО при 900оС на протязі 5 годин розтирають в ступці і змивають киплячою дистильованою водою в мірну колбу ємністю 1000мл. Після того як рідина охолола розчин доводять до 1л дистильованою водою.
7. Сульфат алюмінію, 1%-й розчин: навіс 19,5г Al2(SO4)3·18H2O, що відповідає 10г безводного сульфату алюмінію Al2(SO4)3, насипають в мірну колбу, розчиняють при нагріванні в 300-500 мл дистильованої води, охолоджують і доводять до 1л дистильованою водою.
8. Сульфат заліза, 1%-й розчин: навіс 18,6г FeSO4·7H2O, що відповідає 10г безводному сульфату заліза FeSO4, насипають в мірну колбу ємністю 1000мл, розчиняють в 300-500 мл дистильованої воді; якщо розчин мутний, то добавляють до нього (краплинами) соляну кислоту (концентровану) до отримання прозорого розчину, потім розчин доводять до 1л дистильованою водою.
|
|
|
9. Хлорид заліза, 1%-й розчин: навіс 16,7г FeCl3·6H2O, що відповідає 10г безводного хлориду заліза FeCl3, насипають в мірну колбу ємністю 1000мл і розчиняють дистильованою водою так, як сульфат заліза.
Дата добавления: 2018-04-05; просмотров: 170; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
