Задачи для самостоятельной работы
Задачи 1 - 8. Противоионы диффузного слоя в золе, полученном по приведенной реакции в водном растворе (табл.), перемещаются к катоду (отрицательный электрод). Как заряжены частицы дисперсной фазы золя? Какое вещество было взято в избытке для получения данного золя? Составьте схему мицеллы золя.
Таблица к задачам 1 - 8
| № задачи | Реакция получения золя |
Pb(NO3)2 + Na2SO4 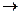 CuCl2 + NaOH
CuCl2 + NaOH 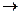 Pb(CHСOO)2 + KI
Pb(CHСOO)2 + KI 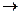 HCl + Na2SiO3
HCl + Na2SiO3 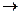 BaCl2 + Na2SO4
BaCl2 + Na2SO4 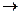 CuCl2 + H2S
CuCl2 + H2S 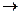 SbCl3 + Na2S
SbCl3 + Na2S 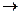 AgNO3 + KCl
AgNO3 + KCl 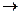
|
Задачи 9–15. Для получения золя смешали водные растворы веществ А и Б (табл.). Какое вещество надо взять в избытке, чтобы получить золь с положительно заряженными частицами? Составьте схему мицеллы.
Таблица к задачам 9 - 15
| № задачи | Вещество А | Вещество Б |
| AgNO3 | KI | |
| FeCl2 | Na2S | |
| KI | Pb(NO3)2 | |
| Na2S | Cd(NO3)2 | |
| Na2SO4 | BaCl2 | |
| K2SiO3 | HNO3 | |
| AgNO3 | KBr |
Задача 16. Какой объем раствора AgNO3 с СЭК = 0,018 моль экв/л надо прибавить к 0,025 л раствора НCl с СЭК = 0,16 моль экв/л, чтобы получить золь с отрицательно заряженными частицами? Составьте схему мицеллы.
Задача 17. Какой объем раствора FeCl3 с СЭК = 0,003 моль экв/л надо прибавить к 0,03 л раствора AgNO3 с СЭК = 0,002 моль экв/л, чтобы частицы полученного золя в электрическом поле двигались к аноду (положительный электрод)? Составьте схему мицеллы.
Задача 18. Какой объем раствора АlСl3 с концентрацией 0,001 моль/л надо прибавить к 0,02 л раствора Н2S с СЭК = 0,003 моль экв/л, чтобы образовался золь с отрицательно заряженными частицами? Составьте схему мицеллы.
|
|
|
Задача 19. Какой объем раствора KI с СЭК = 0,0025 моль экв/л надо прибавить к 0,035 л раствора Pb(NO3)2 с СЭК = 0,003 моль экв/л, чтобы получить золь с отрицательно заряженными частицами? Составьте схему мицеллы золя.
Задача 20. Какой объем раствора NaOH с СЭК = 0,002 моль экв/л надо добавить к 0,003 л раствора Fe2(SO4)3 с СЭК = 0,0003 моль экв/л, чтобы получить золь с положительно заряженными частицами? Составьте схему мицеллы золя.
Задачи 21 - 30. Для получения гидрофобного золя используется реакция между веществами А и Б, взятыми в виде растворов с концентрациями СА и СБ в объемах VА и VБ. Определите заряд частиц дисперсной фазы и составьте схему мицеллы (табл.).
Таблица к задачам 21 – 30
| № задачи | Вещество А | C ЭК, А (моль экв/л) | VA, л | Вещество Б | СЭК, Б (моль экв/л) | VБ, л |
| NaOH | 0,002 | 0,020 | Fe2(SO4)3 | 0,0003 | 0,030 | |
| KI | 0,001 | 0,010 | Pb(NO3)2 | 0,0025 | 0,015 | |
| AgNO3 | 0,005 | 0,028 | KCl | 0,0100 | 0,020 | |
| Na2S | 0,003 | 0,015 | CuSO4 | 0,0020 | 0,035 | |
| KBr | 0,007 | 0,010 | AgNO3 | 0,0003 | 0,040 | |
| Pb(NO3)2 | 0,001 | 0,020 | K2S | 0,0025 | 0,020 | |
| CuCl2 | 0,001 | 0,045 | Na2S | 0,0010 | 0,030 | |
| SbCl3 | 0,005 | 0,020 | Na2S | 0,0004 | 0,030 | |
| Na2SiO3 | 0,004 | 0,015 | HCl | 0,0020 | 0,015 | |
| FeCl3 | 0,003 | 0,030 | NaOH | 0,0050 | 0,030 |
Задача 31. Вычислите порог коагуляции золя раствором сульфата натрия, если добавление 0,003 л Na2SO4 с СЭК = 0,1 моль экв/л вызывает коагуляцию 0,015 л золя.
|
|
|
Задача 32. Какой объем раствора FeСl3 с СЭК = 0,0002 моль экв/л потребуется для коагуляции 0,025 л золя сульфида мышьяка, если порог коагуляции золя этим электролитом
 = 0,067 ммоль экв /л?
= 0,067 ммоль экв /л?
Задача 33. Вычислите порог коагуляции золя раствором K2SO4, если добавление 0,002 л раствора K2SO4 с СЭК = 0,15 моль экв/л вызывает коагуляцию 0,02 л золя.
Задача 34. Какой объем раствора Сr(NО3)3 с СЭК = 0,0003 моль экв/л требуется для коагуляции 0,02 л золя сульфида мышьяка, если порог коагуляции этим электролитом  = 0,060 ммоль экв/л?
= 0,060 ммоль экв/л?
Задача 35. Вычислите порог коагуляции золя раствором сульфата аммония, если добавление 0,01л (NН4)2SO4 с СЭК = 0,3 моль экв/л вызывает коагуляцию 0,015 л золя.
Задача 36. В две колбы налито по 0,1 л золя Fe(OH)3. Коагуляция золя в первой колбе наступила при добавлении 0,01 л раствора NН4Сl с СЭК = 1 моль экв/л, во второй – при добавлении 0,064 л раствора Nа2SО4 с СЭК = 0,01 моль экв/л. Вычислите порог коагуляции золя каждым электролитом, определите, катион или анион является коагулянтом для данного золя, и установите знак заряда частиц золя.
Задача 37. Частицы золя иодида серебра заряжены отрицательно. Порог коагуляции этого золя нитратом лития равен 165 ммоль экв/л. Вычислите пороги коагуляции этого золя нитратами бария и алюминия.
|
|
|
Задача 38. В две колбы налито по 0,1 л золя Fe(OH)3. Коагуляция золя в первой наступила при добавлении 0,063 л раствора Nа2SО4 с СЭК = 0,01 моль экв/л, а во второй – при добавлении 0,037 л раствора Nа3РО4 с СЭК = 0,001 моль экв/л. Вычислите порог коагуляции золя каждым электролитом и определите знак заряда частиц золя.
Задача 39. Порог коагуляции золя оксида мышьяка хлоридом алюминия равен 0,093 ммоль экв/л. Вычислите молярную концентрацию эквивалентов СЭК раствора АlСl3, 0,0008 л которого хватило для коагуляции 0,125 л золя.
Задача 40. В две колбы налито по 0,1 л золя гидроксида алюминия. Коагуляция золя в первой колбе наступает при добавлении 0,02 л раствора NН4Сl с СЭК = 0,05 моль экв/л, во второй – при добавлении 0,037 л раствора Nа3РО4 с СЭК = 0,001 моль экв/л. Вычислите порог коагуляции каждым электролитом и определите знак заряда частиц золя.
Задача 41. Порог коагуляции золя оксида мышьяка нитратом трехвалентного железа равен 0,067 ммоль экв/л. Какой должна быть концентрация раствора Fе(NО3)3 СЭК, чтобы 0,0006 л его вызвали коагуляцию 0,12 л золя?
Задача 42. Для коагуляции 0,05 л золя сульфида мышьяка Аs2S3 в первом случае взяли 0,005 л раствора NН4Сl с СЭК = 2 моль экв/л, во втором - 0,005 л раствора Na2SO4 с СЭК = 0,03 моль экв/л. Рассчитайте, у какого из данных электролитов меньший порог коагуляции для золя Аs2S3 , определите, катион или анион соли вызывает коагуляцию золя и определите знак заряда частиц золя.
|
|
|
Задача 43. Для коагуляции 0,05 л золя сульфида мышьяка Аs2S3 в первом случае взяли 0,0025 л раствора NаСl с СЭК. = 4 моль экв/л, во втором - 0,004 л раствора K3[Fe(CN)6] с СЭК = 0,0005 моль экв/л. Рассчитайте, у какого из данных электролитов меньший порог коагуляции и определите знак заряда частиц золя.
Задача 44. Для коагуляции 0,05 л золя сульфида мышьяка Аs2S3 в первом случае взяли 0,07 л раствора К2SO4 с СЭК. = 0,02 моль экв/л, во втором - 0,002 л раствора К3РО4 с СЭК = 0,001 моль экв/л. Рассчитайте, у какого из данных электролитов меньший порог коагуляции для золя Аs2S3 и определите знак заряда частиц золя.
Задача 45. Порог коагуляции золя хлорида серебра нитратом алюминия равен 0,41 ммоль экв/л. Какой объем раствора Аl(NO3)3 с СЭК = 0,001 моль экв/л нужно взять, чтобы вызвать коагуляцию 0,01 л этого золя?
Варианты задач для самостоятельной работы
| № варианта | № задачи | ||
Продолжение таблицы
Дата добавления: 2015-12-21; просмотров: 93; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
