Кинетика коагуляции

 Для начала коагуляции необходимо, чтобы частицы преодолели энергетический барьер
Для начала коагуляции необходимо, чтобы частицы преодолели энергетический барьер  и попали в первый энергетический минимум (I min) (рис. 53). Для этого требуется уменьшить силы электростатического отталкивания, т.е. снизить
и попали в первый энергетический минимум (I min) (рис. 53). Для этого требуется уменьшить силы электростатического отталкивания, т.е. снизить  потенциал, например, за счет введения электролита. Если скорость коагуляции зависит от концентрации электролита (
потенциал, например, за счет введения электролита. Если скорость коагуляции зависит от концентрации электролита ( ,
,  ,
,  ), то идет медленная коагуляция. Потенциальный барьер исчезает при пороговой концентрации электролита
), то идет медленная коагуляция. Потенциальный барьер исчезает при пороговой концентрации электролита  . После этого скорость коагуляции не зависит от концентрации электролита, т.е. идет быстрая коагуляция.
. После этого скорость коагуляции не зависит от концентрации электролита, т.е. идет быстрая коагуляция.
Процесс коагуляции включает две последовательные стадии:
1) диффузия (сближение частиц);
2) агрегирование (укрупнение частиц).
При быстрой коагуляции каждое столкновение частиц приводит к их слипанию, поэтому скорость быстрой коагуляции определяется только диффузионной стадией. При медленной коагуляции к слипанию частиц приводят не все соударения. Скорость медленной коагуляции зависит как от диффузии частиц, так и от их взаимодействия.
Теория быстрой коагуляции М. Смолуховского (польский ученый)
Основные положения:
1. Частицы дисперсной фазы монодисперсны и имеют сферическую форму.
2. Частицы имеют коллоидные размеры и перемещаются за счет броуновского движения.
3. Силы взаимодействия между частицами не учитываются.
4. Все столкновения частиц являются эффективными, т.е. каждое столкновение приводит к слипанию.
|
|
|
5. Учитывается взаимодействие только двух частиц, одновременное взаимодействие трех и более частиц считается маловероятным, т.е. кинетика коагуляции подобна кинетике химической реакции второго порядка.
Уравнение для скорости реакции 2-го порядка запишется:
 ,
,
где 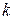 – константа скорости коагуляции;
– константа скорости коагуляции;
 – время.
– время.
Разделим переменные и проинтегрируем в интервале от  до
до  и от 0 до
и от 0 до  :
:
 ,
,
где  ,
,  – концентрация частиц до начала коагуляции (
– концентрация частиц до начала коагуляции ( ) и в момент времени
) и в момент времени  .
.
В результате интегрирования получаем
 . (57)
. (57)
Преобразуем уравнение. Умножим левую и правую часть на  и решим уравнение относительно
и решим уравнение относительно  :
:
 . (58)
. (58)
Приведем уравнение к виду:
 . (59)
. (59)
Из уравнения (59) легко получить формулу для расчета численной концентрации частиц в момент времени  :
:
 . (60)
. (60)
и формулу для расчета константы скорости:
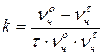 . (61)
. (61)
Уравнения (57)–(61) называют уравнениями кинетики быстрой коагуляции Смолуховского.
Часто для характеристики быстрой коагуляции используют время половинной коагуляции  – время, за которое начальная численная концентрация снизится в два раза. Из уравнения (58) получим:
– время, за которое начальная численная концентрация снизится в два раза. Из уравнения (58) получим:
 ;
;
 ;
;
 . (62)
. (62)
С учетом (62) уравнение Смолуховского (59) примет вид:
 . (63)
. (63)
Дата добавления: 2015-12-18; просмотров: 24; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
