Порядок выполнения работы
Подготовка исследуемого образца к анализу. Навеску исследуемого образца 0,3±0,6 г, взвешенную на аналитических весах, помещают в коническую колбу вместимостью 250 мл, мерным цилиндром добавляют 50-100 мл дистиллированной воды и по каплям – концентрированной серной кислоты, тщательно перемешивают до полного растворения навески и добавляют еще 100-50 мл дистиллированной воды.
Определение железа в растворе. К полученному раствору мерным цилиндром приливают 7-10 мл смеси кислот, добавляют 1-2 капли дифениламина, перемешивают и титруют раствором дихромата калия до перехода зеленой окраски раствора в сине-фиолетовую.
6FeCl2+K2Cr2O7+14HCl→6FeCl3+2CrCl3+2KCl+7H2O 
1│Cr2O72-+14H++6e→2Cr3++7H2O
6│Fe2+-e→Fe3+
Cr2O72-+14H++6Fe2+→2Cr3++6Fe3++7H2O
Объём дихромата калия, пошедший на титрование анализируемой пробы, записывают в тетрадь и рассчитывают общее содержание железа (%) в исследуемом образце:
 ,
,
где: 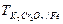 – титр раствора дихромата калия по железу, г/мл; V (K2Cr2O7) – объём дихромата калия пошедший на титрование пробы, мл; т – масса анализируемого образца, г.
– титр раствора дихромата калия по железу, г/мл; V (K2Cr2O7) – объём дихромата калия пошедший на титрование пробы, мл; т – масса анализируемого образца, г.


Получают у преподавателя контрольное значение содержания железа ωFeконтр,% в анализируемом образце и рассчитывают относительную ошибку определения:

Полученная относительная ошибка определения не должна превышать 5 %.
По окончании выполнения лабораторной работы студенты приводят в порядок рабочее место, тщательно моют химическую посуду, ополаскивают дистиллированной водой и сушат в сушильном шкафу. Оставшиеся реактивы и высушенную посуду сдают дежурному учебному мастеру.
|
|
|
Дата добавления: 2016-01-04; просмотров: 26; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
