Крахмал декстриндер мальтоза глюкоза
Макромолекуланың ыдырауы біртіндеп іске асады, әуелі ірі молекулалы қосылыс декстрин, содан кейін дисахарид мальтоза жөне гидролиздің соңғы өнімі глюкоза түзіледі.
Крахмалдың маңызы және қолданылуы. Крахмал
негізгі азығымыздың бірі. Бірақ оны организм бірден
cіңіре алмайды. Тағамның қүрамындағы крахмал майлар
сиякты әуелі гидролизге ұшырайды. Гидролиздену процесі тамақты шайнағанда сілекеймен бөлінетін ферменттердің әсерінен ауызда басталады. Гидролиздену одан әрі асқазан мен ішекте жалғасады. Түзілген глюкоза ішектенқанға сіңіп, одан бүкіл организмге тарайды.Глюкозаның
артық мөлшері гликогенге-"жануар крахмалына" айналып, бауырда қор болып жиналады. Оның кұрамы крахмал сиякты (С6Н10О5)n бірақ құрылысы крахмалдан тармакты және молекулалық массасы да үлкен
Болады.
Организмнің гликоген жинауы шектеулі. Адам салмағының 1 килограмына 50-60г гликоген жиналған соң,одан артық мөлшері майға айналып, адам толысып кетуі мүмкін. Гликоген кажеттілікке байланысты глюкозаға
айналып, биохимиялық процестерге қатысады.
Крахмал гидролизінің аралық өнімдері декстрин мен
мальтозаны организм онай сіңіреді. Декстриндер -крахмалға қарағанда күрделілігі төмен полисахарид. Тамақ дайындаған кезде крахмалдекстринге айналады.
|
|
|
Өнеркәсіпте крахмалды гидролиздеп, сірнемен глюкозаға айналдырады. Егер гидролизді сонына дейін жүргізбесе, декстрин мен глюкозаның қоспасы сірне алынады.
Cipнеден кондитер тағамдарын, кәмпиттер, мармелад, джем, тосап жасайды.
Декстрин желім ретінде де пайдаланылады. Крахмал мата өнеркәcібінде колданылады. Ыстык үтіктің әсерінен крахмал декстринге айналып, жұқа кабықша түзеді. Ол матаға әр береді және тез кірлеуден сақтайды.
Крахмалдан химия өнеркәсібінде глюкоза, этил спиртін, ацетон және лимон қышқылын алады. Крахмал қағаз және картон өндірісінде қолданылады.
ЦЕЛЛЮЛОЗА
Целлюлоза да крахмал сияқты табиғи полимер – полисахарид. Оның молекулалық формуласыда крахмалдікі сияқты (C6H10O5)n.
Целлюлозаны клетчатка деп те айтады. Целлюлоза - табиғатта едәуір көп таралған биополимер. Мақта талшығында 98%-ға дейін, ағаш сүрегінде 50% -ға жуық, жасыл жапырақтарда, шөпте (10-25%) болады. Зығыр мен зығыр талшықтары, негізінен, целлюлозадан тұрады. Целлюлозаны көбіне ағаштан алады. Тазартылған мақта целлюлозаның үлгісі болып табылады.
|
|
|
Целлюлозаның құрылысы. Целлюлозаның макромолекуласы циклді В-глюкозаның қалдықтарынан тұрады, түзу қүрылымды. Целлюлозаныңмакромолекулалары бір бағытта орналасқандықтан талшық түзеді (зығыр, мақта, кендір, т.б.).
Целлюлозаның қарапайым буыны крахмалдікі сияқты (-C6H10O5-), Бірақ B-глюкозаның қалдығынан құралған.
Целлюлозаны тек қана күйіс қайыратын жануарлар қорыта алады.Адамдар мен кейбір басқа жануарлар ферменттері целлюлозаны қорыта алмайды.
Целлюлозаның полимерлену дәрежесі –n-нің мәні крахмалдан көп, молекулалық массасы да крахмардан үлкен (шамамен мақтада-1,7 млн. Зығырда-6 млн-ға дейін) болады.
Целлюлозаның құрылымы түзу сызықты болады:
- C6H10O5 – C6H10O5 – C6H10O5 –C6H10O5 –
Целлюлозаның қасиеттері. Целлюлоза ақ немесе сұр түсті талшықты қатты механикалық берік зат. Целлюлоза суда, спиртте, эфирде, ацетонда жөне т.б. органикалық еріткіштерде ерімейді.
1. Целлюлозаның жақсы жанатынын күнделікті өмірден білесіңдер
|
|
|
2. Целлюлоза крахмалға қарағанда қиын гидролизденеді. Минерал қышқылының қатысында ұзақ уақыт қыздырғанда, бірнеше аралық өнімдер түзіледі:
(C6H10O5)n -> (C6H10O5)x -> n/2C12H22O11 -> nC6H12O6
целлюлоза амилоид целлобиоза глюкоза
(дисахарид)
3.Целлюлозаның гидроксил топтары арқьшы әртүрлі эфирлерін алуға болады. Целлюлозаның қарапайым буыны құрамындағы глюкозаның әр қалдығында үш гидроксил тобынан болады:
Реакцияны жүргузу жағдайына байланысты целлюлозаның әртүрлі нитраттары (нитроцеллюлоза, динитроцеллюлоза,
 |
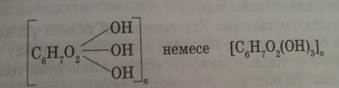 |
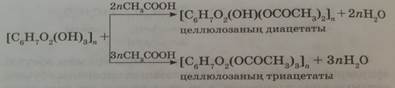 |
тринитроцеллюлоза) алынады
Целлюлозаның нитраттары өте жанғыш және қопарылғыш заттар.Целлюлозаны толық емес нитрлеп, нитросырлар және лак алады. Толық нитрлеп қопарылғыш зат (түтінсіз оқ-дәрі) өндіреді.
4. Целлюлозаға сірке қышқылымен күкірт қышқылы қатысында әсер етіп, целлюлозаның диацетатын немесе триацетатын (диацетилцеллюлоза, триацетилцеллюлоза) алуға болады:
Целлюлозаныңацетатын жасанды жібек талшығы өндірісінде қолданады.
|
|
|
Ацетатты талшық. Құрамында екі немесе үш ацетат тобы бар целлюлоза ацетонда ериді. Талшық алу үшін полимер ерітіндісін ацетонда ерітіп, кішкентай тесіктер арқылы (фильер деп аталатын) өткізіп, жылы ауамен үрлеп кептіреді. Жылудың әсерінен еріткіші ұшып кетіп, ацетилцеллюлоза жіңішке жылтыр жіпке айналады. Бұл жіп ацетатты жібек талшығы деп аталады.
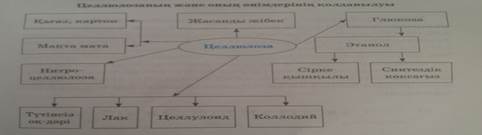 |
Целлюлозаныңқолданылуы. Мақта мен зығырдан талшықтap, мақта мата өнімдерін, арқандар жөне т.б. алады. Ағаштан қағаз, картон алынады. Целлюлозаны химиялық өңдеп, глюкоза, этанол, көксағыз, сірке қышқылын, қопарылғыш заттар, жасанды жібек, т.б. заттар өндіріледі.
3.20 Генетикалық байланыстар
Көмірсутектерді галогентуындыларына айналдыра отырып, олардан спирттер,спирттерден альдегидтер, альдегидтерден-карбон қышқылдарын алуға болады:
1) RCH3->RCH2CL->RCH2OH->R-COH-
>RCOOH->RCOONa
2)жай эфир<-спирт->күрделі эфир->карбон қышқылы
3)CaC2-C2H2-C6H6-C6H5Cl-C6H5O
4)Al3C4-Ch4-Ch3Cl-C2H6
5)CO2-C6H12O6-C2H5OH-C2H4-C2H5Cl-C4H10
4.1 Аминдер
Аминдер-сутек атомы көмірсутек радикалына алмасқан аммиактың туындылары
NH2-амин тобы.Аминдер алифатты және ароматты:
C2H5-NH2(алифатты) C6H5-NH2(ароматты)
Халықаралық атау:ди,три,...
Алу жолдары:0
1.Ni,Pt,Pd
R-NO2+3H2->R-NH2+2H2O
Анилин алу: C6H5NO2+3H2->C6H5NH2+2H2O
Н.Н.Зинин нитробензолды күкіртсутекпен тотықсыздандырып анилин алған:
C6H5NO2+3H2S->C6H5NH2+3S+2H2O
Физикалық қасиеттері:
Қарапайым алифатты аминдер газ тәрізді заттар,суда жақсы ериді.Иістері аммиактың иісіне ұқсас.Ортаңғы аминдер сұйық заттар,иістері балықтың иісіне ұқсайды.Құрамында көміртек атомы көп аминдер-иіссіз,қатты заттар.
Химиялық қасиеттері:
Аминдердің негіздік қасиеті-аммиактан жоғары
1)Аминдердің протон қосып алуы.
C2H5-NH2+HOH->[C2H5-NH3]+OH
Сілтілік орта береді, лакмусты көк түске,фенофталеинді таңқурай түске бояйды.
2)Негіздік қасиет көрсетендіктен,аминдер қышқылдармен әрекеттесіп тұз түзеді: C2H5-NH2+HCL->[C2H5NH3]CL
3)Аминдер ауада жанады:CO2,H2O,N2 түзіледі
Анилин(фениламин)
C6H5NH2- өзіне тән иісі бар,түссіз майлы сұйықтық.Анилин дәрі-дәрмектер,қопарылғыш заттар,антитотықтырғыштар алуда қолд.
C6H5NH2+HCl->C6H5NH3Cl
Жеке өкілдері:Метиламин-өткір иісті,түссіз газ.Жақсы ериді.Аммиак иісіне ұқсайды.Дәрі-дәрмек,бояғыш зат,белсенді қосылыстар алынады.
Гексаметилендиамин H2N(CH2)6NH2-түссіз кристалды зат.Полиамидтер және синтездік талшық-нейлон алады.
4.4Нәруыздар (Белоктар)
Үлкенмолекулалытабиғибиополимерлер-нәруыздармен нуклеин қышқылдары.
Нәруыздар - а-аминқышқылдарыныңқалдығынанқұралғанқұрылысыкүрделіжоғарымолекулалыбиополимерлер.
Нәруыздардыпротеиндердеп те атайды (гр. Протос – алғашқы, маңыздыдегенмағынаныбілдіреді.)
Тіріорганизмніңбүкіләрекетінәруыздызаттарменбайланысты.
Нәруызсызтіршілікболмайды.
Нәруыздаразықтыңқұрамынакіреді.
Адам тәулігінешамамен80-100 грнәруызқабылдауыкерек.
Азықпентүскеннәруызәуеліасқазанда, сосынішектегіферменттердіңәсеріненгидролизденіп, а-аминқышқылдарыныңдейіныдырайды.
Нәруыздарнегізіненкөміртек(50-55%) оттек(20-24%) азот(15-19%) сутектен(6-7%) тұрады.
Нәруыздардыңқұрамынабұларданбасқакүкірт, фосфор, теміркіреді.
Нәруыздардыңқасиеттерінолардыңқұрамы мен құрылымыанықтайды.
Салыстырмалымолекулалықмассаларыбірнешемыңнанмиллионғадейінжетеді.
Жұмыртқанәруыздыңмолекулалықмассасы36000, бұлшықетнәруыздыңмолекулалықмассасы150000, адамгемоглобинді67000, көптегеннәруыздардікі300000шамасында.
| Қызметтерінеқарайжіктелуі | Қызметі | Мысалдары |
| Серпімділік Тасымалдаушы Қорғағыштық, жамылғыш Энергетикалыққуаткөзі Катализдік Жиырғыштық Реттегіштік | Жасушаныңқұрылыс материалы Әртүрлізаттардытасымалдайды Бөтензаттардызиянсыздандырады Организмдіэнергияменқамтамасызетеді Организмдегі химия- лықреакцияларды тездетеді Организм мен жасушаларғатәнбарлыққозғалыстардыатқарады Алмасупроцестерінреттейді | Коллаген, қабықша, мембраналықнәруыздар Гемоглабин (02, СО2 тасымалдау) Қансарысуыныңгаммоглобулині 1 грнәруызыдырағанда 17,6 кДж энергиябөлінеді Барлықферменттердің табиғатынэруыздық. Мысалы, рибонуклеза Миозин (бұлшықетнәруызы) Гормондар, инсулин |
Нәруыздаргидролизденгенде а-аминқышқылдарыныңқоспасытүзіледі.
Әрбірорганизмніңөзінетәннәруыздарыбар.
Барлықнәруыздар20-дан астам а-аминқышқылынанқұралады.
А-аминқышқылдарыныңжалпыформуласы: R-CHNH2-COOH
Нәруыздартүзілетіна-аминқышқылдарының радикалы құрамындаашықтізбек те, тұйықтізбектіәртүрлісақиналар мен функцияналдықтоптар да кездеседі.
Нәруызмолекуласындағы а-аминқышқылдарыныңқалдықтарыныңсаны әртүрліболады, кейдебірнешемыңғадейінжетеді.
Әрнәруыздаа-аминқышқылдарытек осы нәруызғағанатәнретіменорналасады.
Нәруыздардыңқұрылысыөтекүрделі.
Нәруызмолекуласықұрылымын:біріншіреттік, екіншіреттік, үшіншіреттікжәнетөртіншіреттікдепбөліпқарастырады.
Полипептидтіктізбектегіаминқышқылдарықалдықтарыныңқатаңтәртіппенбіріненкейінбірініңорналасуынбіріншіреттікқұрылыманықтайды.
Нәруыздықұрайтынжүздеген, мыңдаған, миллиондаған а-аминқышқылдарыныңқалдықтарыөзарапептидтік (амидтік) байланыс(-СО-NH-) арқылыжалғасып, полипептид түзеді.
Полипептид тізбегіндегіаминқышқылыныңбірқалдығыныңбасқасыменауысуынемесеолардыңорындарыныңалмасуы осы нәруыздыңқызметінбұзады.
Адам гемоглобиніндегі 564 аминқышқылдарыныңқалдықтарынанқұралғанполипептид тізбегіндегібірқышқылдыңқалдығыекіншісінеауысса, адамауырсырқатқаұшырайды.
Аминқышқылдарықалдықтарыныңинсулинніңкейбірбөлігіндеорналасуынмынадайтізбектүріндекөрсетугеболады: глицин-изолейцин-валин-глутамин
Бірполипептидтіңқұрамына21 аминқышқылыныңқалдығы, ал екіншісіне30 амнқышқылыныңқалдығыкіреді.
Табиғаттанәруыздардыңкейбіреуітек созылыңқыполипептидтіктізбектеболады.
Нәруыздардыңкөбініңкеңістіктеоралматәріздіоратылуыекіншіреттікқұрылымдепаталады.
Бұлқұрылымнегізіненоралмаоралымдарындаорналасқанкарбонилтобының оттек атомы мен аминтобыныңсутекатомдары -СО…НN- арасындағысутектікбайланыстарарқылыіскеасады.
Шиыршықтыңбірорамында3 және 5 аминқышқылдарыныңқалдықтарыболады.
Оралымдардыңарақашықтықтары~0,54 нмшамасында.
Нәруыздыңоралматектесмолекуласыбиологиялықпроцестердіңәсеріненмолекула арасындағысутектікбайланыс дисульфид көпіршесікүрделіэфирліккөпіршежәнебүйіртізбектегі анион мен катиондарарасындағыиондықбайланыстарарқылыөзарабайланысады да күрделіүшіншіреттікқұрылымтүзіледі.
Бұлкездеоралмақұндақталыпшумаққаайналады.
Үшіншіреттікқұрылымнәруыздыңөзінетәнқасиеттері мен белсенділігінежауапбереді.
Нәруызмолекуласы тек қанабірполипептидтіктізбектентұрсаоныңқұрылымдарыбіріншіекіншіжәнеүшіншіреттікболады.
Нәруызмолекуласыбірнешеполипептидтіктізбектенқұралса, ондатөртіншіреттікқұрылымтүзіледі.
Төртіншіреттікқұрылым- кейбірнәруыздардабірнешеполипептидтіктізбектердіңбір-біріменкүрделікешендергебірігуі.
Гемоглобин құрамына 141 аминқышқылыныңқалдығыкіретінтөртполипептидтіктізбектенжәнеқұрамындатемір атомы бар нәруыздыемесбөлшекгемнентұратынкешентүзіледі.
Гемоглобин тек осы құрылымдағанаоттектітасымалдайалады.
Нәруыздарқұрамынабайланыстыпротеиндержәнепротеидтерболыпбөлінеді.
Қарапайымпротеиндер тек қанааминқышқылдарықалдықтарынантұрады, күрделіпротеидтерқұрамынанәруыздыемесбасқақосылыстардыңқалдықтарыкіреді.
Нәруыздардың денатурациясы
Нәруыздардың екінші және үшінші реттік құрылымдарына жауапты байланыстар (сутектік, дисульфид көпіршесі) әлсіз болғандықтан, оңай үзіліп нәруыздардың кеңістік құрылымдарының қайтымсыз бұзылуы нәруыздың денатурациясы деп аталады.
Денатурацияға ұшыраған нәруыз өзінің биологиялық функциясын атқара алмайды.
Қыздыру, радиация, ортаның өзгеруі. Кейбір химиялық әсерлерден, шайқап сілкуден нәруыз денатурацияланады.
Жұмыртқан пісіргенде альбумин нәруызының, сүт ашығанда казеиннің ұюынан олардың кеңістік құрылымдары бұзылады.
Шашты химиялық бұйралау, теріні илеу де нәруыздардың денатурациясына жатады.
Қасиеттері
Қыздырғанда денатурацияланатын немесе айырылып кететін болғандықтан, нәруыздардың нақты балқу температуралары болмайды.
Нәруыздардың ерігіштіктері әртүрлі.
Тауық жұмыртқасының нәруызы суда ериді, кейбіреулері суда ерімейді.
Нәруыздар ерігенде, басқа да жоғары молекулалы қосылыстар сияқты коллоидті ерітінділер түзеді.
Нәруыздарға спиртті немесе формалинді қосқанда, нәруыздар қайтымсыз ұйиды, сондықтан бұл заттарды биологиялық препараттарды сақтауға пайдаланады.
Басқа нәруыздар тұздардың сұйытылған ерітінділерінде ериді.
Әлсіз тұз ерітінділерінде еритіндер- альбуминдер, спиртте еритіндер- проламиндер, сұйытылған қышқыл және сілті ерітінділерінде еритіндер- глутелиндер.
Нәруыздар – екідайлы электролиттер.
Ортаның белгілі бір рН мәнінде олардың молекулаларындағы оң және теріс зарядтар бірдей (изоэлектрлік нүкте деп аталады) болады.
Бұл нүктеде нәруыздар электрбейтарап болып, суда еруі азаяды.
Нәруыздардың осы қасиеті технологияда нәруызды өнімдер алуға қолданылады.
Сілті немесе қышқыл ерітінділерін қосып қыздырғанда, нәуыздар гидролизденіп, аминқышқылдарын түзеді.
Биурет реакциясы. Мыс (ІІ) гидроксидінің сілтідегі ерітіндісімен нәруыздарға әсер еткенде, ашық күлгін түс пайда болады.
Бұл реакция нәруыздардың құрамындағы пептидтік байланыстарды анықтайды.
Ксантропртеин реакциясымен құрамында бензол ядрос бар нәруыздар концентрлі азот қышқылымен сары түс береді.
Құрамында күкірті бар нәруыздарға қорғасын ацетатын және сілті қосып қыздырғанда, қорғасын сульфидінің қара тұнбасы түзіледі.
Организмдегі өзгерісі
Көмірсулар мен майлардан айырмашылығы- аминқышқылдары организмде қор болып жиналмайды.
Аминқышқылдарының бір бөлігі нәруыз емес азотты қосылыстардың, нуклеин қышқылдарының синтезіне жұмсалады.
Кейбіреулері тотығып, ең ақырғы өнімдерге (СО2, Н2О) дейін ыдырап, энергия бөледі.
Нәруыз синтезінің проблемасы
Нәруызды синтездеу проблемасының теориялық және практикалық маңызы бар.
Нәруыз молекулалары үздіксіз қозғалыста болады.
Жоғары деңгейлі организмдерде нәруыз биосинтезі таңғаларлықтай тез жүреді: 350 аминқышқылынан тұратын полипептид бар болғаны 10 секундта түзіледі.
Нәруыз синтезінің құпия сырын ашу көптеген вирус ауруларын жеңуге мүмкіндік береді, жаңа химиялық талшықтар мен пластмассалар жасауға, тамақ және химия өнеркәсібінде жаңа өндіріс процестерін ойлап табуға көмектеседі.
Алғаш рт қарапайым нәруызды заттар гипофиздің гормондары вазопрессие мен окситоцин алынды.
Нәруыз синтездеудегі зор табыстарға инсулин мен интерферон алу жатады.
Полипептидтік теория ашылғаннан бері нәруыздық қасиеттері бар полипептидтер синтезделіп, жемдік қоспа, дәрі-дәрмек ретіндеқолданылып жүр.
Қазіргі замандағы маңызды міндеттердің бірі- синтездік тағам жасау проблемасы.
Несмиянов бастаған ғалымдар тобы жұмыс істеп, біраз жетістіктерге жетті.
Сапасы жөнінен табиғи түрінен кем соқпайтын қара уылдырық синтездеп алынады.
4.5.Нуклеин қышқылы
1.Нуклейн қышқылдары бөлінеді: РНҚ жəне ДНҚ
2.Нуклкейн қышқылдарының толық емес гилролизі нəтижесінде түзіледі: нуклеотид
3.Нуклеотидтерді гидролиздесе түзіледі: нуклеозидтер (пентоза мен азотты негіз)
жəне ортофосфор қышқылы
4.Нуклеин қышқылдарының құрамына кіреді: фосфор қышқылы,азотты негіздер,
Моносахаридтер
5.ДНҚ мен РНҚ құрамының айырмашылығы: нуклеин қышқылын толық
гидролиздеу арқылы анықталады
6.Мононуклеотидтер белгілі тəртіппен орналасады: нуклеин қышқылдарының
бірінші құрылымы
7.Макромалекулалардың кеңістікте қос шиыршық болып орналасуын
көрсетеді: нуклеин қышқылының екінші құрылымы
8.Нуклеин қышқылының екіншіқұрылымы: сутектік байланыс түзеді;қос оралма
түщеді; оралманы фосфор қышқылының полиэфирі түзеді, пиримидин жəне
пурин туындылары оралма ішінде болады;
9.Пиримидин жəне пурин туындыларының арасында түзіледі: комплементарлы жұп:
тимин-аденин; цитозин-гуанин;
10.ДНҚ мен РНҚ-ның кеңістікте шумақталып орналасуы: нуклеин қышқылының
үшінші құрылымы
11.Нəруыз биосинтезіне қатысады жəне тірі организмде тұқымқуалаушылықты сақтап,
оның бір ұрпақтан екінші ұрпаққа берілуін қамтамасыз етеді: нуклеин қышқылы
12. ДНҚ жасуша ядросының: хромосомасында(99%), рибосомада,хлоропластарда
Болады
13.РНҚ жасуша ядросының: ядрошықтарда,рибосомаларда,
Дата добавления: 2021-03-18; просмотров: 256; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
