Майларды гидрлеу (гидрогендеу)
Алкандар
Органикалыққосылыстардыңжіктелуінебайланыстыкімнің құрылыс теориясына сүйенеміз: Бутлеров
Көмірсутектер көміртек атомдарының бйланысу ретіне қарай қалай бөлінеді: Ациклді (молекулада көміртек атомдарының тұйық тізбегі болмайтын), карбоциклді (атомдардың тұйық тізбегі болатын)
Карбоциклді көмірсутектер қалай бөлінеді: алициклді, ароматты
Молекула құрамына кіретін атом түріне қарай органикалық қосылыстарды ұандай топтарға жіктейді: көмірсутектер, оттекті, азотты органыикалық қосылыстар
Қаныққан көмірсутектер: алкандар, циклоалкандар
Алкан дегеніміз: молекула құрамындағы көміртек атомдары өзара тек дара σ-байланыстар арқылы байланысқан жалпы формуласы СпН2п+2 болатын алифатты қаныққан көмірсутектер
Алкандар неліктен қаныққан көмірсутектерге жатады: себебі, алкандардың молекуласындағы әр көміртек атомының барлық 4 валенттігі толығымен, яғни, шегіне дейін сутек және көміртек атомдарымен қаныққан.
Алкандарды басқаша атаулары: парафиндер,метан қатарының көмірстектері
Гомолог дегеніміз: Жалпы формулалары бірдей,химиялық қасиетері ұқсас, ал құрамдары бір немесе бірнеше СН2 тобына өзгеріп отыратын заттар
|
|
|
Алкандардың гомологтық айырымы: СН2
Радикал түзілуі: Алкан көмірсутектерінен бір сутек атомы үзілгенде түзіледі
Радикалға жалғанатын жұрнақ: -ил
Алкандарға тән изомерлену: құрылымдық( көміртек қаңқасына байланысты)
Алкандардың изомерленуі басталады: Бутаннан
Изобутанда көміртек атомдары қалай орналасады: тармақталып
Тармақталған көміртек тізбегі қалай аталады: нормальды
Изомерлер саны: бутан-2, пентан-3, гексан-5, декан-75
Алкандардың бастапқы қанша көмірсутегі тривиальды атпен: метан,этан,пропан,бутан
Пентаннан бастап қалай аталады: грек сандарына –ан жұрнағы жалғанып аталады
Тармақталған алкандарды қалай нөмірлейміз:радикал жақын орналасқан жағынан бастап нөмірлейміз
Тармақталған көмірсутекті қалай атаймыз: радикал байланысқан көміртектің нөмірін, содан кейін сызықша арқылы радикалдың атын атап, сосын негізгі тізбекке сай көмірсутек аталады(егер 4 көмірсутек тізбектеліп тұрса, онда бутан),егер бір көміртекте бірдей екі радикал болса, нөмірді екі рет қайталайды.Бірдей радикалдардың сандары грек сандарымен көрсетіледі: ди-, три-, тетра-; 2,2-диметил...; 2,2,3 триметил... т.с.с
|
|
|
2.1 Алкандардың құрылысы
•Қаныққан көмірсутектердің ең қарапайым өкілі: метан
•Метан молекуласының кеңістік пішіні: тетраэдр тəрізді
•Гибредтену түрі: sp3
•Көмірсутектердің метил жəне метилен топтары сигма байланыс осьі бойынша кеңістікте əртүрлі жағдайда болады,бұл құбылыс: Конформация деп ал пайда болған геометриялық пішін:конформерлер
Алкандардың табиғатта кездесуі мен алынуы
•метан:табиғатта көп тараған көмірсутек.Метан өсімдіктермен жануарлар организмдерінің анаэробты микробтар əсерінен ауа қатыспай ыдырауы нəтижесінде түзіледі. Батпақты суларда,таскөмір шахталарында кездеседі.Табиғи газдың құрамында 80-97%.Мұнай өндіргенде бөлінетін газдың құрамында да метан көп.Сұйық алкандар мұнайдың,қатты алкандар мұнай,таскөмір мен озокериттің құрамында болады.
•Шахталарда қопарылыстың көбі метанның кесірінен болатындықтан,бұл газ 《шахтерлердің қас жауы деп аталады.
|
|
|
2.2-2.3 Алкандардың алынуы
1)Мұнайды фракциялап айдап, крекингілеу арқылы.
Крекингке мысал ретінде : C16H34=C8H18+C8H16
2)Вюрц реакциясы бойынша алкандардың галогентуындыларына металл натриймен əсер етіп алады: 2CH3Cl+2Na=C2H6+2NaCl(температура қатысында), CH3I+2Na+C2H5I=CH3-C2H5+2NaI
3) Метанды зертханада алюминий карбидін гидролиздеп алуға болады: Al4C3+12H2O=4Al(OH)3+3CH4
•Алкандарды көмірді гидрлеп алуға болады.500градуста өршіткі (темір оксидтері) қатысында:
nC+(n+1)H2=CnH2n+2
немесе метанды синтездеу реакциясы Ni өршіткісі қатысында жүреді:
C+2H2=CH4
2.4 Алканның қасиеті
Гомолоктік қатарда байқалатын диалектикалық заң: сан өзгерісінің сапа өзгерісіне ауысу заңы
Алкандардың бастапқы төрт мүшесі: газдар
Пентаннан бастап пентадеканға дейін: Сұйық заттар
Көп көміртек атомдары бар жоғары молекулалы алкандар: Қатты заттар
Қалыпты жағдайда қысымды жоғарылатқанда: Пропан мен бутан сұйыққа айналады
Жақсы еріткіштер болып табылады: Сұйық алкандар
Метан мен этанның иісі: Жоқ
|
|
|
Кейбір ортаңғы мүшелерінің иісі: Өзіне тән
Алкандар: Жанғыш заттар
Алкандар түсетін реакциялар: Айырылу,орынбасу,изомерлену,тотығу
Алкандардың ерекшелігі: Көміртек атомдарының валенттіліктері толығымен сутек атомдарымен қаныққан, едәуір берік коваленттік сигма байланыстың болуы
Алкандар түспейтін реакция: Қосылу
Алкандардың басқаша атауы: Парафиндер
Парафин сөзінің латын тілінен аударылғандағы мағынасы: Бейғам,енжар,әрекетсіз немесе белсенді емес
Қаныққан көмірсутектерге тән реакция: Орынбасу
Алкандарда галогендену реакциясы жүзеге асады: Жарықтың немесе жоғары температураның әсерінен
Алкандағы сутектердің орнын галогендерге ауыстырғанда: Галогенсутектер түзіледі
Жарықтың әсерінен жүретін реакциялар: Фотохимиялық
Алкандардың галогендермен орынбасу реакциясы: Хлормен жеңіл,броммен қиындау, йодпен қиын, фтормен қопарылыс түзе жүреді.
Метанның галогендену реакциясының механизмі: Бос радикалды механизм
Алкандардың нитрлену реакциясы : М.И.Коновалов ашқан, Коновалов реакциясы деп аталады
Метанды жоғары температурада 1000°С шамасында ауа қатыстырмай қыздырғанда: Жай заттарға ыдырайды
Метанды 1500°С шамасында қыздырғанда: Ацетилен мен сутек түзіледі
Сутек бөліне жүретін реакция: Дегидрлену
Метанның гомолоктері 500°С жоғары температурада көміртек атомдарының сандары азырақ көмірсутектерге ыдырауы : Крекинг
Алкандардың ароматты көмірсутектерге айналуы: Реформинг
Изомерлену процесі жүреді: AlCl3 өршіткісі қатысында
Шахталарда қопарылыс туғызады: Метан
Оттек жетіспеген жағдайдағы жану: Толық жүрмейді. Күйе және улы иіс газы-СО түзіледі
Автокөліктерден бөлінетін газдардың құрамында СО болады : 5%дейін
Алкардарға әсер етпейтін күшті тотықтырғыштар: KMnO4,K2Cr2O7
Метанның конверсиялануы : Оттекпен, су буымен, көміртек (IV) оксиді мен тотығуы
Метанның конверсиялануы нәтижесінде түзіледі: Синтез газ
Синтез газдан алынады : Метанол метаналь көмірсутектер
Метан: Түссіз иіссіз ауадан екі есе жеңіл жанғыш газ.Суда нашар ериді.
Метанды пайдаланады: ЗКүйе,көксағыз бен резеңке өндірісінде, типографиялық бояу ретінде. Экологиялық таза отыр ретінде, аммиак және азотты тыңайтқыштар ретінде
Пропан мен бутан:Баллондарға құйып, отын ретінде тұрмыста пайдаланады
Изооктан(2,2,4-триметилпентан):Жоғары сапалы іштен жанатын қозғалтқыштардың жанармайларырың негізгі құрамы.
Бензин сапасы сипатталады: Изооктан санымен
Антидетонаторлар: Тармақталмаған көмірсутектердің деионациялануын төмендеткіш қасиеттері бар заттар
Негізінен еріткіш ретінде қолданылатын алкандардың мүшелері: Ортаңғы мүшелері
Мотор отыны ретінде қолданылады: Сұйық алкандар
Жоғары алкандар: спирттер, карбор қышқылдары,синтетикалық майлар, сабын, жағармай, қанықпаеан қосылыстар т.б. алуда қолданылады.
Циклоалкандар
Циклоалкандар: Құрамяндағы көміртек атомдары өзара дара байланыс арқылы байланысқан, жалпы формуласы СnН2n болатын карбоциклді қаныққан көмірсутектер
Циклоалкандардың алғашқы өкілі басталады: Циклопропаннан
Циклоалкандардың гибридтенуі: sp3
Циклоалкандардың басқаша атауы: Циклопарафиндер немесе мұнай құамында болатындықтан нафтендер
Циклоалкандардың сәйкес алкандардан ерекшелігі : Молекуласында сутектің екі атомы кем болады
Циклоалкандардың изомерленуі: Цикл құрамындағы көміртек атомдарының санына, көмірсутек молекулаларындағы орынбасушылардың түрі мен олардың орындарына байланысты және алкендермен класаралықизомер
Бес және алты мүшелі циклопарафиндердің кездесуі: Мұнайдың кейбір түрлерінің құрамында болады
Циклоалкандарды мұнай құрамында болатындықтан не атайды: Нафтендер
Құрамындағы галоген атомдары екі шеткі көміртек атомдарында орналасқан алкандардың дигалогентуындыларынан алады: Мырышпен немесе натриймен әсер етіп
Циклоалкандардың алғашқы екі мүшесінің физ.күйі : Газдар
Циклоалкандардың үшінші мүшесінен бастап физ.күйі : Сұйық заттар
Жоғары циклоалкандар: Қатты заттар
Циклоалкандар суда ериді ма: Жоқ
Циклоалкандардың тұрақтылығы мен химиялық қасиеті байланысты: Циклдегі көмірсутек атомдарының санына байланысты
Циклді алкандардың ішіндегі химиялық ең тұрақтылары: Құрамында бес және алты көміртек атомы бар циклоалкандар
Құрамында үш және төрт көміртек атомдары бар циклоалкандардың гибридтенуі: 109°28'-тан сәл ауытқиды
Циклоалкандардың алкандарға ұқсас қасиеттері: Химиялық белсенділіктері төмен, жану және орынбасу реакцияларына түседі
Циклоалкандардың алкандардан айырмашылығы: Қосылу реакциясына түседі
Циклоалкандарда қосылу реакциясы қалай жүреді: Байланыс үзілген жерге басқа элемент атомдары қосылады
Бес және оданда көп мүшелі циклді қосылыстарға тән: Орынбасу реакциясы
Айырылу реакциясына жатады: Дегидрлену
Циклопропан : Газ тәрізді зат. Медицинада қолданылады.
Циклогексан: Сұйық зат, еріткіш ретінде қолданылады. Циклогексанол, циклогексанон, адиптин қышқылы және капролактам алынады.
Циклогексан мен метилциклогексан: Бензол мен толуол сияқты химиялық синтезге қажетті ароматты көмірсутектерге айналады
Алкен
Алкендер: құрамында қос байланысы бар жалпы формуласы CnH2n
Қарапайым өкілі басталады: этиленнен
Алкеннің басқаша атауы: олефиндер н/е этилен қатарының көмірсутектері
Гибирдтенуі: sp²
Байланыс ұзындығы: 0,134 нм
Байланыс энергиясы: 612 кдж/моль
С5H10: пентен ( амилен )
Тривиальды атауда: -илен жұрнағы
Халықаралық атауда: -ен жұрнағы
Алкендердің радикал: СH2=CH- (этенил,винил)
Изомерлерленуі: 1)Көміртек қаңқасы 2)Еселі байл орнына 3) Циклоалканмен кл ар изомер 4)Кеңістік(геометриялық н/е –цис,-транс)
Бір жақта: -цис
Әр жақта: - транс
-Транс изомер –цис изомерге қарағанда: тұрақты
2.7. Алкендердің алынуы, қасиеті
Алкендердің газ тәрізді мүшелері алынады: мұнайға серік газдан н/е мұнайды өңдегенде ж/е көмірді кокстегенде
Алынуы:
Алкандарды дегидрлеу: C2H6—C2H4+H2 (өрш. Cr2O3)
Алкандарды крегингілеу: C8H18—C4H10+C4H8
Спирттерді дегидраттау: C2H5OH—C2H4+H2O (өрш. Су сорғыш заттар H 2 SO 4 конц. H3PO4, Al2O3)
Физикалық қасиет: алғашқы 3 мүшесі газ (этен,пропен,бутен), С5H10 бастап сұйық, С18H36 бастап қатты
Алкендер: судан жеңіл, суда нашар, орг. еріткіштерде жақсы ериді
Сапалық анықтау: бромдану(қызыл қоңыр түсі жойылып, түссізденеді), тотығу кезіндегі KMnO4 (күлгін түсі жойылады)
Химиялық қасиет: қосылу 1) Сутектің қосылуы(өрш, Pt.Pd.Ni): C3H6+H2—C3H8
2) Галогендену: C2H4+Br2—C2H4Br2 3) Галогенсутек қосу: C2H4+HCl—C2H5Cl
Гидраттану: С2H4+H2O—C2H5OH 5) Полимерлену: nCH2=CH2--- (-CH2-CH2-)n
Алкендердің фтормен әрекеттесуі шабытты жүреді, Йодпен баяу жүреді
Жеке өкілдері: Этилен- түссіз,иіссіз,суда нашар ериді,ауадан жеңілдеу, жанғыш газ,оттекпен ж/е ауамен қопарылғыш қоспа түзеді, жеміс-жидектерді пісуін тездететін ерекше қасиеті бар. Этиленнен алынады: полиэтилен, синтездік көксағыз, этил спирті, этиламин, этилбензол, стирол, сірке альдегиді, сірке қышқылы. Полиэтилен-диэлектрик болғандықтан электр сымдарын кабельдерді оқшаулағыш материал ретінде электротехникада қолданылады, шынының орнына пайдаланады. Этил спитрі- көксағыз,резеңке алынады. Пропилен- суда нашар, спирт пен эфирде жақсы еритін түссіз газ, Пропиленен алынады: полипропилен, глицерин, изопропил спирті, ацетон,фенол,синтездік көксағыз
Полимерлену: жоғары молекулалы қосылыс түзіледі, өршіткі қатысында жоғары tͦ мен қысымда іске асады
Крекинг- ұзын тізбекті көмірсутектердің қысқа көмірсутектерге айырылуы
В.В.Марковников ережесі: галогенсутектің сутек атомы сутек көп көміртек атомына, ал галоген сутек аз көміртек атомына қосылады: H2C=CH-CH3(пропенн)+H-Br----H3C-CHBr-CH3(2-бромпропан)
2.9. Көксағыз бөлінеді табиғи синтездік
Өсімдіктердің сүтті шырындарында кездеседі-табиғи көксағыз
Табиғи көксағызды алады-Бразилияда гевея ағашынан
Өсімдіктің қабығын кертіп алады-көксағыз
Көксағыздың коллоидті ерітіндісін жинап алады-өсімдік тіліктен ағатын сүтті шырынынан(латексті)
Коллоидті ерітіндіні электролитпен қыздыру арқылы коагуляциялап(ірілендіріп) алады -көксағызды
Қанықпаған көмірсутектің полимері (С5Н8)n- табиғи көксағыз
Орташа салыстырмалы молекуланың массасы-15000-30000
Эксперименттік жолмен көксағыз негізінен -2-метилбутадиен-1,3-тің (изопреннің)полимері (С5Н8)n
Алкадиендерді полимерлеп алады -синтездік көксағызды
Молекулалар бір-бірімен С4 және С1 көміртек атомдары арқылы өзара сызықты қосылады -полимерлену барысында
Табиғи көксағыз изопреннің цис-полимері -құрамындағы метилен топтары - СН2– қос байланыстың бір жағын ала орналасады
Стереореттелген цис-дивинил көксағызды үйкеліске төзімділігі мен серпімділігі жағынан табиғи көксағыздан-жоғары
Стереоретсізбутадиен көксағызының үйкеліске төзімділігі мен серпімділігі жағынан табиғи көксағыздан-төмен
Изопреннің құрылым мономері -ретті қайталанып отырады
Полимердің осындай құрылымының арқасында оған -майысқақтық қасиет тән болады
Көксағыз макромолекулаларының құрылысы-сызықтық
Оратылып бірнеше рет иіліп түйіншектеліп жатады -көксағыздың макромолекулалардың құрылысы
Көксағызды созған сайын олар жазылып көксағыз- ұзарады
Көксағызды созуды тоқтатқанда-оратылып түйіншектелген бастапқы қалпына қайта келеді
Көксағызды қатты созса -молекулалары жазылып қана қоймай үзіліп кетуі де мүмкін
Көксағыз –қатты зат
Табиғи көксағыздың макромолекулалары тізбекті құрылымды -оратылып түйіншектеліп жатады
Көксағыздың аса маңызды қасиеті –майысқақтығы
Сыртқы күштің әсері тоқтағаннан кейін-бастапқы қалпына қайта келеді
Көксағыз-суды газды өткізбейді және электроқшаулағыш
Көксағыз-суда ерімейді
Көксағыз-этил спиртінде аздап ериді
Бензин мен хлороформ сияқты еріткіштерге -әуелі ісініп сосын ериді
Температура жоғарылаған сайын -көксағыз жұмсарып жабысқақ болады
Температура төмендеген сайын- қатайып морт сынғыш болады ұзақ сақтағанда ол қатайып кетеді
Қолайсыз қасиеттерін жою үшін көксағызды вулканизациялап(вулкандап) күкірт қосу арқылы алады-резеңкені
Көксағызға күкірт пен толықтырғыштар қосып қыздырады -130-140С*
Күкірт атомдары көксағыздың қос байланыстарының кейбіреулері бойынша қосылып сызықтық молекулаларын бір-біріне жөрмеп байланысып-полимер кеңістіктік құрылымға ие болады
Резеңкенің иілгіш созылғыш қасиеттері көксағыздікінен де -жоғары
Көксағыздан берігірек және температураның ауытқуына төзімдірек болатын зат -резеңке
Көксағыз -бензинде біртіндеп ериді
Резеңке-бензинде ерімейді тек ісінеді
Көксағызды вулканизациялағанда оның массасының -2-3% -ындай күкірт қосады
Егер күкірт резеңкеге қажетті мөлшерден көбірек қосылса онда созылмайтын қатты зат –эбонит алынады
Резеңкеден алынады –шиналар шлангтер конвейер ленталары тұрмыста қолданылатын көптеген заттар
Алкиндер
Құрамында үш еселі байланыс бар көмірсутектер –алкиндер
Жалпы формуласы-СnH2n-2
Бірінші мүшесі ацетиленнен басталатындықтан -ацетилен көмірсутектері д.а.
Алкиндерде гибридтенуі –sp
Байланыс бұрышы- 180
Байланыс ұзындығы -120нм
Байланыс энергиясы -830кДж/моль
Молекуланың кеңістік пішіні-сызықтық
Халықаралық номенклатура бойынша –ин жалғауы жалғасады
Алкиндерге тән изомерлер -көміртек қаңқасына еселі байланыс орнына классаралық
Алкиннің классаралық изомері-алкадиендер
Өнеркәсіпте ацетиленді алады –табиғи газдан
Метанды айырғанда(1500С*) -ацетилен аралық өнім ретінде түзіледі
2СН4 -> C 2 H 2 +3 H 2
Этанды (1200С*)қыздырғанда -ацетилен мен сутек түзіледі
С2Н6 -> С2Н2+2Н2
Зертханада күнделікті тұрмыста ацетиленді -кальций карбидінен сумен әрекеттесіп алады
Кальций карбидін- электрпеште сөндірілмеген әк пен коксті жоғары температурада (2000С*) қыздыру арқылы алады
СаО+3С->CaC2+CO2
CaC2+2H2O->Ca(OH)2+C2H2
2.11 Алкиндердің қасиеті
Ацетилен:түссіз,иіссіз газ,суда нашар ериді Алкиндердің бастапқы үш мүшесі:газ С5Н8 сұйық С16дан қатты Алкин:судан жеңіл,суда нашар,орг ерткіштерде жақсы ериді Гидрлену:Ni,Pt,Pd өршіткілер арқылы жүреді Галогендену:С2Н2+Br2àBrHC=CHBrBrHC=CHBr+Br2-àBr2HC-CHBr2 Галогенсутектерді қосып алу:HC=CH+HCLàH2C=CHCL Гидратация су қосып алу:сынап(II)сульфат,1881ж М.Г Кучеров Полимерлену рекциясы:3С2Н2àC6H6 Алкиндердің қасиетін зерттеуге үлес қосқан:Е.Н Әзербев Ацетиленнен:сірке альдегиді,сірке қышқылы,этил спирті,синтездік көксағыз,пластмассалар алынады
2.12 Арендер(ароматты көмірсутек) Арендер:молекулалрының құрамында бензол сақинасы(бензол ядросы) бар Жалпы формуласы:CnH2n-6 Ең қарапайым мүшесі:С6Н6 Бензолдың құрылымдық формуласы ең алғаш неміс ғалымы:А.Кекуле ұсынды Гибридтену:sp2Ұзындығы:0,140нмБайланыс бұрышы:120 Бензол:С6Н5-Н Метилбензол:С6Н5-СН3,ксилол Этилбензол:С6Н5-С2Н5 Пропилбензол:С6Н5-С3Н7 Диметилбензол:ксилол Изопропилбензол:кумол Винилбензол:стирол Бензолдың туындылары:орто-,мета-,пара- С6Н5:Фенил радикалы С6Н5-СН2:бензил радикалы
2.13. Арендерді алу әдістері:
Таскөміршайыры мен мұнайды фракциялап айдап алады.
Алкандарды өршіткі қатысында дегидрлеп (риформинг) бензол мен оның туындылары алынады:
С6 Н14= C6Н6+ 4H2 (өрш, температура қатсысында).
Арендерді циклогексан мен оның гомологтарын дегидрлеп алуға болады. Зелинский құрамындағы циклогександы Pt,Pd өршіткілері қатысында 300С дегидрлеп бензол алынады:C6H12=C6H6+3H2
C6H11-CH3=C6H5-CH+3H2
3C2H2=C6H6
2.14 Арендердің қасиеттері
Бензол:улы, оның буы аннемия,лейкемия ауруларына ұшырайды,бояғыш заттар,дәрі дәрмектер,қопарылғыш заттар,синтездік талшықтар алу үшін қолданылады Арендердің:бастапқы мүшелері өзіне тән иісі бар,суда ерімейді,судан жеңіл сұйық зат Химиялық қасиеті:арендер оынбасу ,қосылу,тотығу реакциясына түседі Галогендену Орынбасу реак:темір(III)бромидінің қатысында жүреді Нитрленуі:концентрлі күкірт пен азот қыш қоспасы қатысында қыздырғанда бензолдан нитробензол түзіледі 2,4,6тринитротолуолды:тротил,тол,ТНТ д.а қопарылғыш зат ретінде қолданылады Қосылу реакциясы:қиын түседі Гидрленуі:Ni,Pd,Pt өрш қатысында жүреді,бензол сутекті қосып циклогексанға айналады Галогенді қосып алу:ультракүлгін сәулеледің әсерінен бензол хлордың алты атомын қосып алып,нәтижесінде гексахлорциклогексан түзіледі Тотығу реак:қалыпты жағдайда калий перманганаты ерітіндісін түссіздендірмейді Толуол:С6Н5-СН3 судан жеңіл,суда ерімейтін,түссіз сұйықтық, бояғышзаттар,дәрі дәрмектер,қопарылғыш заттар,синтетикалық жуғыш заттар,капролактам алады Этилбензол:С6Н5-С2Н5-С2Н5түссіз сұйықтық стирол алуға қолданылады Изопропилбензол:С6Н5-СН(СН3)2 түссіз сұйық зат Фенол мен ацетон алуға пайдаланылады Стирол винилбензол:С6Н5-СН=СН2 суда ерімейтін, жағымды иісті сұйықтық Полистирол,бутадиенстирол көксағызын алуға пайдаланылады ,полистирол мшиналар мен құрал-жабдықтар жасағанда қолданылады
2.15-2.16 Көмірсутектер мен олардың туындыларының арасындағы генетикалық байланыстар.Табиғи және мұнайға серік газдар
Табиғатта газтектес, сұйық және қатты көмір сутектер таралған. Олар көбіне күрделі қоспалар түрінде таралған, оларға: табиғи газ, мұнайға серік газдар, мұнай,таскөмір.
Газдар кездесетін орнына қарай: табиғи және мұнайға серік газдар.
Жер қыртысындағы бос кеңістіктерді толтырып тұрады: табиғи газ.
Жер астындағы мұнай қабатының бетін бүркеп жатады: мұнайға серік газдар.
Табиғи газдың құрамында : 80-90% метан, қалған бөлігі метанның жақын гомологтары этан, пропан, бутаннан тұрады.
Табиғи газдың құрамында өте аз мөлшерде: пентан, күкіртсутек, көмірқышқылгазы, азот, т.б газдар болуы мүмкін.
Табиғи газды сұйылту арқылы : пропан мен бутан қоспасын бөліп алады.
Құрғақ газ- метан(СН4) мен этан (С2Н6) қоспасы, отын ретінде кең пайдаланылады.
Құрғақ газдан- күйе, формальдегид, метил спирті ж\е т.б еріткіштер алынды.
Күйе қолданылады- автомобиль дөңгелектерін жасағанда, бояу ретінде қолданылады.
Пропан-бутан қоспасын дегидрлеу жолымен белсенділігі жоғары қанықпаған көмірсутектер алып ,олардан: көксағыз, пластмассаларды синтездейді.
Көмірсутектерді тотықтырып: органикалық қышқылдар, спирттер ж\е басқа өнімдер алады.
1м3 табиғи газды жаққанда- 54400 кДж жылу бөлінеді.
Пропан- бутан қоспасын: сұйылтылған газ түрінде тұрмыстық отын ретінде немесе оттықты толтыруға пайдаланады.
Мұнайға серік газдар- мұнайда еріген күйінде немесе мұнайдың бетін бүркеп жатады.
Мұнайға серік газдардың негізгі құрам бөлігі.: метан.
Мұнайға серік газдарды 3 фракцияға бөледі: 1) құрғақ газ (СН4, С2Н6); 2) пропан-бутан қоспасы (С3Н8 , С4Н10); 3) газды бензин (С5Н12, С6Н14).
Мұнайға серік газдардың құрамындағы алкандардан- сутек, ацетилен, қанықпаған ж\е ароматты көмірсутектер мен олардың туындыларын алады.
Газды бензин- өте ұшқыш ж\е тез қайнайды.
Газды бензин төмен температураның өзінде жақсы буланатын болғандықтан- өте суық болатын жақтарда автомобиль бензиніне оталуын тездету үшін қосады.
2.17 Мұнай құрамы өңдеу әдістері және өнімдері
Мұнайдың негізін:парафиндер,циклопарафиндер,ароматты көмірсутектер
Шикі мұнай:жер астынан өндірілген мұнай-суы көп
Тауарлық мұнай:Тазартылған мұнай
Мұнай:Қара қоңыр түсті,өзіне тән иісі бар,май тәріздес,қоймалжың сұйық зат,сүда ерісейді,бірақ орг.еріткіште ериді,судан жеңіл,жанғыш зат
Мұнай өндіру әдісі:Шикі мұнайды тұндырып,сеператордан өткізіп,газынан және суынан айырады 1.Мұнарада мұнайды фракциялау-мұнайды айдау 2.ауыр көмірсутектерді бөлшектеу арқылы жеңіл көмірсутектер алу (Крекинг)және көмірсутектерді ароматтандыру(Риформинг)процесі
Мұнайды айдауға арналған қондырғы 2 бөліктен тұрады:түтікті пеш және ректификациялық мұнара
Мұнай фракциялары:Газойль,бензин,лигроин,керосин,мазут
Мұнайды тікелей айдаудан бөлінетін бензиннің шығым:15-20%
2300-2500-ұршық май
260-305-Машина майы
315-325-жеңіл цилиндр майы
350-370-ауыр цилиндр майы,ең соңында Гудрон қалдық түрінде бөлінеді
Крекингті ұсынған ғалым-Шухов
Термиялық крекинг арқылы бензин өндіреді:C16H34—C8H16+C8H16
C8H18—C4H10+C4H8
Катализдіккрекинг:4500-5200Сжәне өршіткі қатысында жүргізіледі-бұл әдіспен авиация бензині өндіріледі.
Риформинг:Мұнай және мұнай өнімін терең деструциялау әдісімен өңдеудің крекингтен басқа әдісі
Риформинг процесінің шикізаты –Бензин мен Лигроин
Риформинг процесін-ароматтандырудепатайды.
Мұнай өнімдерін құрамындағы қанықпаған көмірсутектерден және азотты негіздерден тазарту үшін аз молшерде: күкірт қышқылымен өңдейді.
Нафтен қышқылынан және күкірт қышқылының қалдығынан тазарту үшін: сілтімен өңдейді.
Қышқылмен өңдегенде қалған қалдық қышқыл: гудрон.
Сілтімен өңдеген қалдық: нафт деп аталады.
Мұнай өнімдерін тазарту әістері: адсорбциялау және абсорбциялау д.а.
Мұнай өнімдерінің тұрақтылығын арттырып сапасын жоғарылату үшін қосады: антитотықтырғыштар (ингибиторлар) қосады.
Тежегіштер ретінде: фенол, ароматты аминдер, амин фенолдар қолданылады.
Бензин фракциясы 40-120С0 айдалатын, құрамында С4-С12 көміртек атомдары бар көмірсутектер қоспасы.
Керосин фракциясы 180-300С0 құрамында С9-С16 - бұлар мұнайдың ашық түсті өнімдерін береді.
Бензин фракциясын қайта өңдеуден өткізіп: газолин С5-С11 немесе петролейн эфирін 40-70С0 бензин 70-120С лигроин С8-С14, 120-140С
Бензин: авиациялық, автомобильдік д.а.
Керосин: жарықтандырушы, тракторлық, реактивтік деп бөлінеді.
Керосиннің газойльмен қоспасын- дизель отыны деп атайды.
Мұнайды айдаудың соңғы өнімі- мазут д.а.
Мазут- қара түсті, тұтқыр, қоймалжың масса.
Мазутты қайта өңдеу арқылы әртүрлі жағармайлар: соляр майлары, түрлі машина майлары, парафин алынады.
Мазуттың сонғы қалдығы- гудрон алынады.
Бензин төменірек температурады қайнайтын көмірсутектер фракциясынан тұратын болса: жаздық бензин
Бензин жоғары температурада қайнайтын көмірсутектер фракциясынан тұратын болса: қыстық бензин д.а.
Бензиннің қозғалтқышты қопарылыс түзіп жануы: детонация д.а.
Бензинді шартты түрде: изооктан мен н-гептан қоспасы ретінде қарастырады.
Таскөмір: көміртек, сутек, азот, оттек ж\е күкірттен тұрады.
Отын агрегаттық күйіне байланысты: қатты, сұйық ж\е газтектес болып бөлінеді.
Отын тегіне қарай: табиғи ж\е жасанды болып бөлінеді.
Отынның құрамында көміртек пен сутек неғұрлым көп болса: жылу бөлу қабілеті соғұрлым жоғары болады.
Көмірдің химиялық өңдеудің әдістері: пиролиз, газдандыру, гидрогендеу, ж\е кокстеу.
Пиролиз : көмірді ауа қатыстырмай жабық реакторда қыздыру.
Газдандыру : 1000С қатты отынның органикалық массасын ауамен, су буымен н\е олардың қоспасымен щала тотықтыру арқылы жанғыш газдарға айналдыру.
Жанатын газдардан генератор пештерінде өндіретін болғадықттан, оларды генератор газдары д.а.
Гидрогендеу: өршіткі қатысында жоғары температурады ж\е қысымда отынды сутекпен өңдеу.
2.18 Таскөмір. Таскөмірді кокстеу
Таскөмірді ауа қатыстырмай кокс пештерінде 900-1050С өдеу әдісін : таскөмірді кокстеу д.а.
Тасеөмір шикізат ретінде 350-400С: пластикалық күге ауысады.
Кокс пеші 70 астам камерадан тізілген жоғары температураға төзімді реакторлар батареясы.
Кокс пешінен алғашқы түзілетін өнімдер: кокс ж\е ұшқыш заттар.
Кокс кеуекті қатты зат оны: домна пешінде, металлургия зауытында қолданады.
Кокстың жану жылуы: 31400 кДж
Таскөмір шайыры құрамында: нафталин, фенонтрен, корбозол, антроцен. Фенол, крезол, бензол, толуол, ксилол 50-60% жоғары температурада қайнайтын ауыр молекулалы өнімдер
Жерасты генератор газының құрамы: СО, N 2 , , СО2, Н2, СН4 жану жылуы 3000-4000кДж\м3
2.19 Қазақстандағы мұнай, газ және көмірдің негізгі кен орындары
Таскөмір:Қазақстанның энергетикалық ресурстарының негізгі түрі Республиканың отын балансындағы көмірдің арасалмағы:70% Таскөмірдің, кокстелетін көмірдің, қоңыр көмірдің Қазақстанда жалпы геологиялық қоры:160 млрд тонна Қазіргі кезде республикада жалпы алғанда:400-дей кен орнынан жылына 100 млн тоннаға жуық таскөмір мен қоңыр көмір өндіріледі Қазақстанның ең ірі көмір базасы:Қарағанды көмір алабы Қарағанды көмір алабы республикамыздың орталық бөлігінің: 3000км² ауданың алып жатыр Қарағанды көмір алабының жалпы геологиялық қоры:60 млрд тонна Қарағанды көмір алабының негізгі кен орындары: Абай, Сарань, Шерубайнұра, Шахтинск, Михайловка және т.б. Қарағанды көмір алабының көмір қатпарларының тереңдігі: 50-300 м-ге дейін Екінші орын алатын Қазақстан көмір алабы: Екібастұз Екібастұз көмір алып жатқан ауданы: 200 км² Екібастұз көмір алабының жалпы қоры: 17 млрд тонна Екібастұз көмір алабының артықшылығы: Көмір қабаттары жер бетіне жақын (100 н-ге дейін) жатқандықтан өндіру ашық өдіспен жүргізіледі де, өзіндік кұны арзанға түседі Екібастұз көмірі негізінен: отын ретінде электр және жылу станцияларында қолданылады Екібастұз көмір алабының негізгі кен орындары: «Алып»(«Богатырь»), «Солтүстік» және «Шығыс» кеніштері Қоры жөнінен болашағы зор таскөмір және қоңыр көмір кеніштірі қатарына: Қостанай облысындағы Құсмұрын, Майкөбе, Шығыс Қазақстандағы Кендірлік Мұнай мен газ: көмірге қарағанда жану жылуы жоғары отын әрі химиялық өнеркәсіп үшін бағалы шикізат Қазіргі кезде Қазақстанда:160-тай мұнай кен орны жұмыс істейді, 60-қа жуық кен орнында зерттеу жүргізілуде Негізінен республикамыздың:батыс өңірі мұнайлы өлке болып табылады Атырау мұнай кен орнын ең алғаш орыс ғалымы: Н.А.Северцев зерттеген Атырауда алғашқы мұнай ұңғымасынан мұнай:1899 жылы атқылады Табиғи газ өндірісі: Қазақстанның ең жас өнеркәсіп саласы Табиғи газ негізінен: Маңғыстау түбегінде, Ембі алабында, Атырау кеніштерінде,Жамбыл облысындағы Амангелді кен орнында өндіріледі Қазақстан аумағындағы барлық газ қоры: 9,5 трлн метр куб. Оның 68%-ы Батыс Қазақстан облысында орналасқан
Спирттер
Спирт сөзі латынның: шараптың рухы сөзінен шыққан XVIII ғасырдан бастап спирт деген сөзбен қатар: алкоголь (араб. әл-кугул) деген сөз қолданылды Шарап спирті немесе этил спиртінің формуласы: C2H5OH Жүзімнің, қанттың, крахмалдың ферменттік ашуы нәтижесінде түзілетін бұл затты тұрмыста жай ғана: спирт деп атайды Құрамында функционалдық гидроксил тобы бар органикалық қосылыстар: спирттер мен фенолдар Спирттер: молекуласындағыбір немесе бірнеше сутек атомдары гидроксил тобына алмасқан көмірсутектердің туындылары Спирттердің жалпы формуласы:R(OH)x Спирттер қүрамындағы гицроксил тобының санына байланысты: біратомды және көпатомды болып белінеді Біратомды спирттерде: бір гицроксил тобы болады Көпатомды спирттердің құрамындағы гидроксил тобының саны: x>2 Э тиленгликоль:екіатомды спирт Глицерин: үшатомды спирт Сорбит: алтыатомды спирт Гидроксил тобымен байланысқан көміртек атомының табиғатына байланысты спирттер:біріншілік, екіншілік және үшіншілік болып бөлінеді.
қалыпты температурада С10ға дейінгі спирттер сүйық заттар, 011ден бастап қатты заттар
Алғашқы үшеуі сумен кез келген мөлшерде араласады,молекулалық массасының артуына қарай сүйық спирттердің суда ерігіштігі төмендейді.
спирттердің өздеріне тән иісі болады
Спирттердің қайнау және балқу температурасы молекулалық массасының артуына байланысты өседі
Спирттердің қайнау температуралары сәйкес көмірсутектердің қайнау температурасынан жоғары боладыспирттерде молекулааралық сутектік байланыс түзіледі
Спирт молекуласында электртерістігі жоғары оттек атомы сутектің электрондарын өзіне тартып, оларда ішінара теріс және оң зарядтар пайда болады
Осы зарядтардың әсерінен оттек атомы мен спирттің басқа молекуласындағы гидроксилдің сутек атомының арасында сутектік байланыс түзіледі
Сутектік байланысты үзуге 5 ккал/моль энергия жұмсалады
Энергиясы аз болғанымен, оны үзу үшін температураны көтеру керек, сондықтан спирттердің қайнау температуралары жоғарылайды.
Гидроксил тобы қатысында ететін реакциялар О-Н немесе С-ОН байланыстарын үзу арқылы жүреді
Спирттер (алканолдар)полюсті қосылыстар, көміртек пен оттек және оттек пен сутек атомдарының арасында екі полюсті байланысы бар
Оттектің жүп электрондары спирттерге әлсіз электрондонорлық қасиет береді.
Спирттер индикаторға әсер етпейді.
Гидроксил тобындағы сутек атомы әлсіз қышқылдық қасиет көрсетеді,қозғалғыш келеді, орынбасу реакциясына түседі.
Сутектің қозғалғыш болу себебі, оттектің электртерістігі жоғары болғандықтан оттек электрон тығыздығын өзіне қарай тартады,оыдан О-Н байланысы полюстенеді
Спирттің гидроксил тобындағы сутек атомының орнын белсенді металдар баса алады.2R-ОН+2Nа->2R-ОNa+Н2O
Этанол натриймен әрекеттескенде натрий этилаты мен сутек түзіледі: 2C2H5OH+ 2Na=2C2H5Ona+H2
Спирттің металл туындыларын алкоголяттар деп атайды.
Алкоголяттар қатты заттар. гидролизге оңай үшырайды: C2H5ONa+HOH=C2H5OH+NaOH
Этерификация реакциясы карбон қышқылы мен спирт арасында жүреді
Спирттің гидроксил тобындағы сутек атомының орнын карбон қышқылындағы ацил тобы басады. Реакция қайтымды,күрделі эфир мен су түзіледі:
Спиирт молекуласындағы С-ОН байланысының үзілуі арқылы жүреді.
Спирттер галогенсутектермен әрекеттеседі
гидроксил тобының орнын галоген басу арқылы өтетін қайтымцы реакция: R-OH+HBr=R-Br+H2O
Реакцияны сутартқыш заттардың қатысында өткізеді (мысалы, концентрлі күкірт қышқылы), сонда реакция галогеналкил түзілу жағына қарай бағытталады.
Спирттерге сутартқыш заттар (концентрлі күкірт қышқылы, фосфор қышқылы және т.б.) қосыпқыздырса, су бөлініп шығады, реакцияның жүруі температураға жөне жағдайға байланысты болады.
Егер дегидратация реакциясын төменірек температурада жүргізсе, онда реакция молекула аралық өтеді де, жай эфир түзіледі:
Жоғарырақ температурада t°> 14ОС дегидратациялағанда, реакция молекула ішінде өтеді, нөтижесінде алкен түзіледі: CH3-CH2OH=CH2=CH2+H2O
Тотығу реакциялары. Мыс оксидімен тотығып, альдегид түзуі біріншілік спирттердің сапалықреакциясы: CH3-CH2OH+CuO=CH3COH+H2O+Cu
Реакция барысында қара түсті мыс (ІІ) екенді тотықсызданып, қызғылт түсті мыс түзіледі және альдегидтіңөткір иісі сезіледі.
Спирттер жанғанда энергия бөлінеді.
Этанол көгілдір жалынмен жанады: C2H5OH+3O2=2CO2+3H2O+Q
Спирттердк қолданғанда осы реакцияны пайдаланады.
“Спирттерді дегидрлегенде альдегидтер түзіледі.
М етил спирті -метанол
СНЗОН -түссіз сүйықтық, спиртке тән иісі бар.
Қайнау температурасы 64,7 °С.
Метанолды өнеркәсіпте өршіткі қатысында синтез-газдан алады: CO+2H2=CH3OH+Q
Синтез-газды өз кезегінде метанды су буымен әрекеттестіріп алады.
Бастапқы кезде метил спиртін ағашты қүрғақ айдау арқылы алған, “ағаш спирті” деген атау содан шыққан.
Метанол өндірісте формальдегид, полимерлер, бояғыш заттар, фармацевтік препараттар алу үшін, бояулар мен дақтарды ерітетін еріткіш ретінде және т.б. заттар алуда кең түрде қолданылады.
Метил спиртімен жүмыс істегенде, оның өте улы екенін үмытпау керек. Бірнеше грамынан адам соқыр болады, одан кебірек қабылдаса, уланыпөледі.
Этил спирті этанол
С2 Н5 ОН өзіне тән иісі бар түссіз сүйықтық
Қайнау температурасы 78,3° С. Сумен кез келген мөлшерде араласады.
Егер спирттің қүрамында 4-4,5% су болса, оны ректификат, ал сусыз спиртті абсолютті спирт дейді.
Сусыз (абсолютті) спиртті су тартқыш заттар (СаО, СиS04) қосып қайнатып алады.
Этил спиртін әртүрлі жолдармен алады. Соның бірі ашытқы қатысында глюкозаның (жүзім қанты) ашуы
Мүндай жолмен алынған спирт таза болады, тамақ өнеркәсібінде және медицинада пайдаланылады.
Этил спиртінің біраз мөлшерін ағаш қалдықтарынан -целлюлозаны гидролиздеу және түзілген глюкозаны ашыту арқылы алады.
Целлюлозаны гидролиздеп алынған спиртті гидролиз спирті деп атайды:(C6H10O5)n+nH2O=nC2H5OH
метанол- мұндай спирт көбіне техникада қолданылады, тамақ өнімдер үшін пайдалануға болмайды.
Синтездік жолмен этил спиртін этиленді гидратациялап алады. .
Этанол дәрі-дәрмек жасауда, зарарсыздандырғыш зат ретінде медицинада пайдаланылады.
Этил спирті химия өндірісінде сірке қышқылын, бояу, синтездік көксағыз,
диэтил эфирін және т.б. заттар алуда қолланылады.
Ең арзан еріткіштердің бірі
Этанолдан ішімдіктер дайындайды. Этил спиртінің улы және есірткі заты екенін ескерген жөн. Ол суда жақсы еритіндіктен қан қүрамына бірден енеді де, адам организміне қауіп төндіреді. Оны ішкенде, асқазан-ішек жолдарының шырышты қабығы зақымданады, бауырдың жүмысы, қан тамырларының, жүректің қызметі бүзылады. Этил спирті адам организміне есірткілік әсер етеді. Спирт миға әсер етіп, жүйке жасушаларын уландырады. Осыдан адамның ақыл-ойы, сөйлеу, ойлау қабілеттері, қимыл үйлесіМДілігі бүзылады
3.2Қаныққан біратомды спирттер
қаныққан біратомды спирттер:гидроксил тобына алмасқан алкандардың туындылары
қаныққан біратомды спирттердің жалпы формуласы:CnH2n+1OH
ИЮПАК халықаралық атаулар жүйесі бойынша спирттерді сәйкес көмірсутектердің атына қосылатын жұрнақ:ол
Функционалдық то:ОН
Спирттердің нөмірленуі: ОН тобы байланысқан ең ұзын тілек таңдап алынып,көміртек атомдарын гидроксил тобы жақын орналасқан жағынан бастап нөмірлерді,орнын көрсетіп радикалдық сосын көмірсутектің негізгі тізбегін атап,гидроксил байланысып тұрған көміртек атомының нөмірін көрсетеді
Спирттердің изомерлері:a)көміртек қаңқасының құрылысына Ә)көмірсутек тізбегіндегі гидроксил тобының орнына Б)жай эфирлермен класаралық изомерлену
Метил спиртінің(CH3OH) изомерлері:жоқ
Этил эфирінің класаралық изомері:диметил эфирі CH3-O-CH3
Пропил спиртінің изомер саны:3
Пропанолдың класаралық изомері:Метилэтил эфир
көмірсутек тізбегіндегі көміртек атомының саны өскен сайын:спирттердің изомерлерңнің саны арта береді
Бутил спиртінің изомерлерінің саны:6
.қаныққан біратомды спирттерді өнеркәсіпте көмірсутектердің моногалогентуындыларын гидролиздеп алады:сілті қатысында C 2 H 5 Cl + NaOH = C 2 H 5 OH + NaCl
Спирттердің алынуы :көмірсутектердің моногалогентуындыларының гидролизі,алкендерді гидратациялау,құрамында қанты бар заттардың ашуы
Спирттердікүкіртқышқылықатысындаэтилен көмірсутектеріне су қосыпалады:CH2=CH2+HOH=CH3-CH2OH
Су қосып ала жүретінреакция:гидратация
Глюкозаныңспирттік ашуы:C6H12O6=2C2H5OH+2CO2,шарап өндірісіндеқолданылады
3.3Спирттердің қасиеттері
Қалыпты температурада С10ға дейінгі спирттер сүйық заттар, 011ден бастап қатты заттар
Алғашқы үшеуі сумен кез келген мөлшерде араласады,молекулалық массасының артуына қарай сүйық спирттердің суда ерігіштігі төмендейді.
спирттердің өздеріне тән иісі болады
Спирттердің қайнау және балқу температурасы молекулалық массасының артуына байланысты өседі
Спирттердің қайнау температуралары сәйкес көмірсутектердің қайнау температурасынан жоғары боладыспирттерде молекулааралық сутектік байланыс түзіледі
Спирт молекуласында электртерістігі жоғары оттек атомы сутектің электрондарын өзіне тартып, оларда ішінара теріс және оң зарядтар пайда болады
Осы зарядтардың әсерінен оттек атомы мен спирттің басқа молекуласындағы гидроксилдің сутек атомының арасында сутектік байланыс түзіледі
Сутектік байланысты үзуге 5 ккал/моль энергия жұмсалады
Энергиясы аз болғанымен, оны үзу үшін температураны көтеру керек, сондықтан спирттердің қайнау температуралары жоғарылайды.
Гидроксил тобы қатысында ететін реакциялар О-Н немесе С-ОН байланыстарын үзу арқылы жүреді
Спирттер (алканолдар)полюсті қосылыстар, көміртек пен оттек және оттек пен сутек атомдарының арасында екі полюсті байланысы бар
Оттектің жүп электрондары спирттерге әлсіз электрондонорлық қасиет береді.
Спирттер индикаторға әсер етпейді.
Гидроксил тобындағы сутек атомы әлсіз қышқылдық қасиет көрсетеді,қозғалғыш келеді, орынбасу реакциясына түседі.
Сутектің қозғалғыш болу себебі, оттектің электртерістігі жоғары болғандықтан оттек электрон тығыздығын өзіне қарай тартады,оыдан О-Н байланысы полюстенеді
Спирттің гидроксил тобындағы сутек атомының орнын белсенді металдар баса алады.2R-ОН+2Nа->2R-ОNa+Н2O
Этанол натриймен әрекеттескенде натрий этилаты мен сутек түзіледі: 2C2H5OH+ 2Na=2C2H5Ona+H2
Спирттің металл туындыларын алкоголяттар деп атайды.
Алкоголяттар қатты заттар. гидролизге оңай үшырайды: C2H5ONa+HOH=C2H5OH+NaOH
Этерификация реакциясы карбон қышқылы мен спирт арасында жүреді
Спирттің гидроксил тобындағы сутек атомының орнын карбон қышқылындағы ацил тобы басады. Реакция қайтымды,күрделі эфир мен су түзіледі:
Спиирт молекуласындағы С-ОН байланысының үзілуі арқылы жүреді.
Спирттер галогенсутектермен әрекеттеседі
гидроксил тобының орнын галоген басу арқылы өтетін қайтымцы реакция: R-OH+HBr=R-Br+H2O
Реакцияны сутартқыш заттардың қатысында өткізеді (мысалы, концентрлі күкірт қышқылы), сонда реакция галогеналкил түзілу жағына қарай бағытталады.
Спирттерге сутартқыш заттар (концентрлі күкірт қышқылы, фосфор қышқылы және т.б.) қосыпқыздырса, су бөлініп шығады, реакцияның жүруі температураға жөне жағдайға байланысты болады.
Егер дегидратация реакциясын төменірек температурада жүргізсе, онда реакция молекула аралық өтеді де, жай эфир түзіледі:
Жоғарырақ температурада t°> 14ОС дегидратациялағанда, реакция молекула ішінде өтеді, нөтижесінде алкен түзіледі: CH3-CH2OH=CH2=CH2+H2O
Тотығу реакциялары. Мыс оксидімен тотығып, альдегид түзуі біріншілік спирттердің сапалықреакциясы: CH3-CH2OH+CuO=CH3COH+H2O+Cu
Реакция барысында қара түсті мыс (ІІ) екенді тотықсызданып, қызғылт түсті мыс түзіледі және альдегидтіңөткір иісі сезіледі.
Спирттер жанғанда энергия бөлінеді.
Этанол көгілдір жалынмен жанады: C2H5OH+3O2=2CO2+3H2O+Q
Спирттердк қолданғанда осы реакцияны пайдаланады.
“Спирттерді дегидрлегенде альдегидтер түзіледі.
М етил спирті -метанол
СНЗОН -түссіз сүйықтық, спиртке тән иісі бар.
Қайнау температурасы 64,7 °С.
Метанолды өнеркәсіпте өршіткі қатысында синтез-газдан алады: CO+2H2=CH3OH+Q
Синтез-газды өз кезегінде метанды су буымен әрекеттестіріп алады.
Бастапқы кезде метил спиртін ағашты қүрғақ айдау арқылы алған, “ағаш спирті” деген атау содан шыққан.
Метанол өндірісте формальдегид, полимерлер, бояғыш заттар, фармацевтік препараттар алу үшін, бояулар мен дақтарды ерітетін еріткіш ретінде және т.б. заттар алуда кең түрде қолданылады.
Метил спиртімен жүмыс істегенде, оның өте улы екенін үмытпау керек. Бірнеше грамынан адам соқыр болады, одан кебірек қабылдаса, уланыпөледі.
Этил спирті этанол
С2 Н5 ОН өзіне тән иісі бар түссіз сүйықтық
Қайнау температурасы 78,3° С. Сумен кез келген мөлшерде араласады.
Егер спирттің қүрамында 4-4,5% су болса, оны ректификат, ал сусыз спиртті абсолютті спирт дейді.
Сусыз (абсолютті) спиртті су тартқыш заттар (СаО, СиS04) қосып қайнатып алады.
Этил спиртін әртүрлі жолдармен алады. Соның бірі ашытқы қатысында глюкозаның (жүзім қанты) ашуы
Мүндай жолмен алынған спирт таза болады, тамақ өнеркәсібінде және медицинада пайдаланылады.
Этил спиртінің біраз мөлшерін ағаш қалдықтарынан -целлюлозаны гидролиздеу және түзілген глюкозаны ашыту арқылы алады.
Целлюлозаны гидролиздеп алынған спиртті гидролиз спирті деп атайды:(C6H10O5)n+nH2O=nC2H5OH
метанол- мұндай спирт көбіне техникада қолданылады, тамақ өнімдер үшін пайдалануға болмайды.
Синтездік жолмен этил спиртін этиленді гидратациялап алады. .
Этанол дәрі-дәрмек жасауда, зарарсыздандырғыш зат ретінде медицинада пайдаланылады.
Этил спирті химия өндірісінде сірке қышқылын, бояу, синтездік көксағыз,
диэтил эфирін және т.б. заттар алуда қолланылады.
Ең арзан еріткіштердің бірі
Этанолдан ішімдіктер дайындайды. Этил спиртінің улы және есірткі заты екенін ескерген жөн. Ол суда жақсы еритіндіктен қан қүрамына бірден енеді де, адам организміне қауіп төндіреді. Оны ішкенде, асқазан-ішек жолдарының шырышты қабығы зақымданады, бауырдың жүмысы, қан тамырларының, жүректің қызметі бүзылады. Этил спирті адам организміне есірткілік әсер етеді. Спирт миға әсер етіп, жүйке жасушаларын уландырады. Осыдан адамның ақыл-ойы, сөйлеу, ойлау қабілеттері, қимыл үйлесіМДілігі бүзылады
3.4 Көпатомды спирттер
Көпатомды спирттер –құрамында бірнеше гидроксил тобы бар көмірсутектердің туындылары.
R-(OH)nn>2
Этиленгликоль –С2Н4(ОН)2 Қарапайым өкілі/этандиол-1,2/
Глицерин-С3Н5(ОН)3 Үш атомды спирт/пропантриол-1,2,3/
Сорбит-С6Н8(ОН)6
Халықаралық атаулар жүйесі бойынша екі және үш атомды спирттерді атағанда ,көмірсутек атына диол немесе триол жұрнағы қосылады.
KMnO4
 C2H4+H2O+[O] C2H4(OH)2
C2H4+H2O+[O] C2H4(OH)2
Физик қасиет:Этиленгликоль мен глицерин-тәтті дәмі бар түссіз,қоймалжын сұйықтар.Суда жақсы ериді.
-ОН -ONO2
С3Н5-ОН+НОNO2=C3H5-OH+H2O
-ОН -OH
Мононитроглицерин
-ОН -ONO2
С3Н5-ОН+3НОNO2=C3H5-ONO2+3H2O
-ОН -ONO2
1,2,3 тринитроглицерин
Сапалық реактиві:Сu(OH)2
-ОН -OH
2С3Н5-ОН+Cu(ОH)2=(C3H5-OH)2Cu+2H2O
-ОН -OH
Ашық көк түсті ерітінді мыс (2) глицераты
ЭтиленгликольСН2ОН-СН2ОНЕкіатомды спирттердің ішіндегі маңыздысы.Қайнау темп. 197,6 С.Сумен кез келген мөлшерде араласады.Сусыз гликоль гигроскопиялық /сутартқыш/ зат.Этиленгликольді қату темп төмен болғандықтан автомобильдердің радиаторына құятын ,қыста қатпайтын сұйық зат-антифриз дайындау үшін пайдаланады.
Этиленгликольдің судағы 36%-дық ерітіндісі -20 С-та, 66%-дық ерітіндісі -60% С-та қатады. Лавсан синтездік талшығын алу үшін және қопарылғыш заттар дайындауда қолданады.
ГлицеринСН2ОН-СНОН-СН2ОНГигроскопиялық зат,ауадан суды сіңіреді.Атмосфералық қысымда 290 С-та қайнап,ыдырай бастайды,сондықтан оны белгілі бір қысымда айдайды.Өнеркәсіпте пропиленнен алады.Көп мөлшерде химия және тамақ өнеркісібінде қолд.Парфюмерияда,мата,былғары өнеркәсібінде ,сонымен қатар қопарлғыш заттар және медицинада дәрі-дәрмектер өндіруде қолданады.
Глицерин тринитратыСН2ОNO2-CHONO2-CH2ONO2 Өте қуатты қопарылғыш зат.Динамиттің құрамына кіреді. Нитроглицериннің 1% ерт. медицинада жүрек-қантамыр ауруларына қол.
С3Н5(RCOO)3+3HOH=C3H5(OH)3+3RCOO
Фенолдар
Фенолдар-гидроксил тобы бензол сақинасымен тікелей байланысқан органикалық қосылыстар. Халықаралық атаулар жүйесі бойынша гидроксибензол деп атайды.
Бензол сақинасы тікелей байланысса-фенол. Бензол сақинасы тікелей байланыспаса-ароматты спирттер
Бензол сақинасының фенил радикалы С6Н5-электронды өзіне тартады.
Өндірісте фенолды,негізінен ,таскөмір шайырынан бөліп алады.
Физикалық қасиет:Фенол-суда нашар еритін түссіз кристалды зат.Өзіне тән иісі бар,оңай балқиды, улы зат,теріні күйдіреді. Антисептик қасиеті бар.Бөлме темп. нашар ерігенмен,70 С-та суда жақсы ериді.Ауада тотығып, алдымен қызғылт түске,сосын қоңырқай түске боялады.
Химиялық қасиет:Фенолдың қышқылдық қасиеті спирттерден басым болғанымен,әлсіз қышқыл.Тіпті көмір қышқылы мен сірке қышқылынан да әлсіз, лакмустын түсін өзгерте алмайды.Спирттен өзгешелігі-фенол қышқылдармен әрекеттеспейді.
 1.Белсенді металдармен әрекеттесуі.
1.Белсенді металдармен әрекеттесуі.
2C6H5OH+2Na=2C6H5ONa+H2
натрий феноляты
2.Сілтілермен реакциясы.
C6H5-OH+NaOH=C6H5ONa +H2O
натрий феноляты
C6H5ONa+H2O+CO2=C6H5-OH+NaHCO3
Бензол сақинасының реакциялары.
3.Фенол бромды сумен оңай әрекеттеседі. Бромның қызыл қоңыр түсі жойылып,ақ түсті 2,4,6-трибромфенол тұнбаға түседі.Бұл-фенолдың сапалық реакциясы.
C6H5OH+3Br2=C6H2Br3OH+3HBr
2,4,6-трибромфенол
4.Фенол азот қышқылыменәрекеттескенде:
H2SO4
C6H5OH+HONO2C6H2(NO2)3OH+3H2O
2,4,6-тринитрофенол
пикрин қышқылы
Пикрин қышқылы– сары түсті қопарылғыш зат.
5.Фенол формальдегидпен оңай әрекеттеседі.
Нәтижесінде жоғары молекулалы қосылыс фенолформальдегид шайыры алынады.
6.Фенол+FeCl3күлгін түсті кешенді қосылыс түзеді.
Қолданылуы:Фенолды медицинада зарарсыздандыру үшін,тамақ өнеркәсібіндеантиоксидант ретінде пайдал.
Өндірісте көп мөлшерде пластмассалар,дәрі-дәрмектер,қопарылғыш заттар,бояулар,фенол-формальдегид шайырын алу үшін жұмсалады,одан өндірісте фенопласт алынады. Фенолды гидрлеп циклогексанол алады.Оны өндірісте синтездік талшық алуда пайдаланады.
C6H12-циклогексан синтезд.талшық
Фенолформальдегид +ағаш ұнтағы пресс ұнтақ
Фенолформальдегид+қысқа талшықты материал волокнит
енолформальдегид+мақта текстолит
Фенолформальдегид+шыны талшық шыны пластик
Капрон- синтезд. талшық алуға да пайдаланылады.
Фенол және оның туындылары-улы заттар.Фенол көз және тыныс алу органдарының шырышты қабығын тітіркендіреді,тері қабатының бұзылуына әкеледі.
3,6-3,7 Альдегидтер, олардың қасиеттері
АльдегидтерАльдегидтер мен кетондардың құрамындағы топ-карбонил Альдегидидтердің жалпы формуласы-RCOH Альдегидтердің изомерленуі-көмірсутек қаңқасының құрылысына байланысты және кетондармен класаралық изомер Изомерлену альдегидтерде басталады-төрт атомды көміртек өкілінен Альдегидтерді алады-көмірсутектерді және спирттерді тотықтырып,Кучеров реакциясы Метанды толық емес тотықтырса түзіледі-метаналь Пропанол-1-ді тотықтырып алады-пропаналь Альдегид атауы шықты-алкагольды дегидрлеу Кучеров реакциясы-ацетилен+су-альдегид(сынап сульфаты қатысында,300градуста) Құмырсқа альдегиді-өткір иісті газ Сірке альдегидінен бастап келесі мүшелерінің агрегаттық күйі-сұйық Молекулалық массалары жоғары альдегидтердің агрегаттық күйі-қатты Альдегидтердің спирттерден өзгешелігі-сутектік байланыс түзілмейді,сондықтан сәйкес спирттермен салыстырғанда қайнау температуралары төмен HCOH-метаналь,құмырсқа альдегиді,формальдегид CH3COH-этаналь,сірке альдегиді,ацетальдегид(өткір иісті сұйықтық,суда жақсы ериді) C2H5COH-пропаналь,пропион альдегиді C3H7COH-бутаналь,май альдегиді CH3COCH3-пропанон,ацетондиметилкетон Альдегидтер түсетін реакциялар-қосылу,тотығу,полимерлену,поликонденсациялану,орынбасу Альдегидтер мен кетондар осы металл өршіткілері қатысында сутекті қосып алып тотықсызданады-Ni,Pt,Pd Тотықсызданғанда альдегидтер-біріншілік спиртке,кетондар-екіншілік спиртке айналады:CH3COH+H2=C2H5OH Альдегидтерге сапалық реакция-Күміс-айна реакциясы(тотығу)-CH3COH+Ag2O=CH3COOH+2Ag(аммиак,температура қатысында) Альдегидтерге сапалық реакция-CH3COH+2Cu(OH)2=CH3COOH+2CuOH(сары тұнба)~~~Cu2O(қызыл)+H2O~~~+H2O Формальдегидтің 40%-дық ерітіндісі-формалин(дезинфекциялағыш зат) Құмырсқа альдегиді қолданылады-фенолформальдегид шайырын,карбамидті шайыр,органикалық бояулар,қопарылғыш заттар,лактар алуда,нәруыздарды ұйыту қасиетіне байланысты анатомиялық препараттарды консервациялауға,дезинфекциялауға,дәрі-дәрмек алуға,тері илеу өндірісінде,егін егу алдында дән тұқымдарын өңдеуде Сірке альдегиді қолданылады-сірке қышқылын,этил,бутил спирттерін,күрделі эфирлер,бутадиен алуда Ацетон-түссіз,оңай тұтанатын сұйықтық,сумен кез келген мөлшерде араласады Ацетонды алады-изопропил спиртін немесе изопропилбензолды тотықтырып Ацетон қолданылады-изопрен,ацетат талшығын алуда,нитроцеллюлоза мен ацетилцеллюлозаны ерітуде
3.8-3.9 КАРБОН ҚЫШҚЫЛДАРЫ
Құрамында 1 немесе бірнеше корбоксил тобы бар көмірсутек туындылары-КАРБОН қышқылы
Карбон қышқылыдарының жалпы формуласы-R-(COOH)
Карбон қышқылдары кабоксил тобы байланысқан радикалдың табиғатына қарай бөлінеді-Қаныққан,қанықпаған,ароматты
Құрамында карбоксил тобының санына байланысты карбон қышқылдары бөлінеді-Бірнегіді,көпнегізді
Қаныққан(шектелген) карбон қышқыл өкілдері-CH3COOH(сірке қыш),C2H5COOH(пропион кыш)
Қанықпаған (шектелмеген) карбон қыш өкілдері-CH2=CH-COOH пропен(акрил)қышқылы
Ароматты карбон қышқылы-C6H5COOH (бензой қышқылы)
Қалақай мен шыршада кездесетін карбон кышқылы-HCOOH метан кышқылы,құрмырсқа қыш
HCOOH метан қышқылының тұзы-формиат
1,25% сулы ерітіндісі медицинада «ревматизм» ге қарсы қолданылатын карбон қышқылы –HCOOH метан (құмырсқа) қышқылы
Бір негізді карбон қышқылдарының ішінде ең күштісі-HCOOH
Карбон қышқылында болатын байланыс-Димерленген сутектік (екі еселенген)
Карбон қышқылдарының қайнау Т0 сы –спирттерден жоғары
HOOC-COOH (этанти)қыш тривиалды атауы-Қымыздық қышқылы Тұзы-оксалат
Қаныққан карбон қышқылының физ.қасиеті –алғашқы 9 өкілі сұйық,10 шы өкілі қатты
Қаныпаған карбон қышқылның өкілдері –сұйық
Пентан қышқылының тривиалды атауы-валераин (тұзы- валерат )
Пентан қышқылын алады-валерин өсімдігінен
Бутан немесе пропион қышқылының тривиалдыатауы –май қышқылы(тұзы -бутериат)
Карбон қышқылдарының изомерленуі –көміртек қаңқсына( күрделі эфирмен классаралық )
Гексан қышқылы (капрон қышқылы)-С5Н11СООН
Гептан қышқылы(энант)-С6Н13СООН
Гексадекан қышқылы (пальмитин)-С15Н31СООН
Гептадекан қышқылы (маргарин)-С16Н33СООН
Октадекан қышқылы (стеарин)-С17Н35СООН
Октадецен қышқылы(олеин)-С17Н33СООН
Пропион қышқылының классаралық изомері –этилформиат НСООС2Н5
Бутан қышқылының изомер саны-5
Бірнегізді қаныққан карбон қышқылының формуласы-СnH2n+1COOH
3.10 Карбон қышқылдарының табиғатта кездесуі және алу
жолдары .
Құмырсқа қышқылы құмырсқада,қалақайда,шыршажапырағында кездеседі
Сіркеқышқылы зат алмасу процесінде маңызды рөл атқарады.
Адам организімінде тәулігіне400грамдай сіркеқышқылы түзіледі .
Майқышқылы- майдыңқұрамында болады .
Валериан қышқылы - валерианөсімдігініңтамырында , Лауринқышқылы (С11-Н23-СООН) лавр өсімдігінде , кокосмайында болады .
Ешкісүтінің құрамында алты 6 ,сегіз 8,он көміртек атомдары бар қышқылдарболады.
Алу жолдары : 1) Алкандарды , спирттерді,альдегидтерді өршіткі (марганец тұздары) қатысында ауадағы оттекпен тотықтырыпалады:
 CH3- CH2 - CH2 - CH O
CH3- CH2 - CH2 - CH O

 - H2O 2CH3 - COOH
- H2O 2CH3 - COOH
( O)
 CH3 - CH2OH CH3-COOH
CH3 - CH2OH CH3-COOH
- H2O
O
 CH3 - CHO CH3-COOH
CH3 - CHO CH3-COOH
2) Алкендердікөміртек (ll) оксидімен және су буымен өршіткі қатысында белгілі бір қысымда қыздырып әрекеттестіріп , карбон қышқылдарын алады :
өрш.
 R-CH=CH2+CO+H2O R-CH2-CH2-COOH
R-CH=CH2+CO+H2O R-CH2-CH2-COOH
3) Спирттерді көміртек (ll) оксидімен әрекеттестіргенде , карбон қышқылдары түзіледі :
өрш.
 R-OH+СО R-COOH
R-OH+СО R-COOH
3.11 Карбон қышқылдарының қасиеттері.
Физикалыққасиеттері: құмырсқа , сірке және пропионқышқылдары - Өткіриісті , сұйықзаттар , суда ериді.
Май қышқылының жағымсызиісі бар , суданашарериді .
Жоғары карбон қышқылдары С10 - нан бастап қатты заттар .
Гомологтыққатарда молекулалық массаларынңөсуіне қарай суда ерігіштігікемиді, қайнаутемператураларыөседі.
Карбон қышқылдарының арасында Екісуттектікбайланыс болады.
Химиялыққасиеттері - құрылысына байланысты .
- Карбосил тобының О-Н байланысы үзілуарқылы жүретін реакциялар,мысалы :диссоциациялану,тұз түзу реакц.
O
R - C
O - H
Карбоксил тобынан ОН тобы үзілу арқылы жүретін реакц. Мыс : күрделіэфир,ацилгалогенит түзу, тотықсыздану реакциялары .
Радикалдық альфа - галоген карбон қышқылының түзілуі .
1) Суда еритін карбон қышқылдары Диссоциацияланады , индикатордыңтүсінөзгертеді , электртоғынөткізеді.
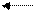
 RCOOH RCOO- + H+
RCOOH RCOO- + H+
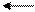
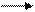 RCOOH + H2O RCOO- + H3O+
RCOOH + H2O RCOO- + H3O+
Бейорганикалық қышқылдармен салыстырғанда - Әлсізқышқылдары, Күштісі - Құмырсқа қышқылы .
Көмірсутек радикалының өсуіне қарай қышқылдың Диссоциациялану дәрежесі мен күші кемиді
2) Тұздар түзілуі . Карбон қышқылдары бейорганикалық қышқылдар сияқты металдармен, металоксидтерімен және меттал гидроксидтерімен әрекеттесіп тұз түзеді .
а)белсенді және орташа белсенді металдармен әрекеттескенде,тұз түзіліп, сутегі ығысады:
2RCOOH+Mg ® (RCOO)2Mg+H2
ә) метал оксидтерімен және гидроксидтерімен әрекеттескенде,тұз және су түзіледі:
2RCOOH+MgO ® (RCOO)2Mg+H2O
б) метал гидроксидтерімен әрекеттескенде,тұз бен су түзіледі:
RCOOH+NaOH ® RCOONa+H2O
в)әлсіз қышқылдарды тұздарынан ығыстырады:
2CH3COOH+Na2CO3 ® 2CH3COONa+H2O+CO2
Г)аммиакпен әрекеттескенде,аммоний тұзы түзіледі:
RCOOH+NH3 ® R-COONH4
Қышқыл молекуласында R-дің орнына әртүрлі радикал болады.
! Егер карбон қышқылының карбоксил тобындағы гидроксил ОН бөлініп кетсе,онда бір валентті
O
RCO-ацил тобы,ал сутек бөлінсе,R-COO-(ацилат) ацилокси тобы түзіледі. Бір валентті R-CO-(R--C-)тобын қышқыл қалдығы немесе ацил деп атайды. Ацилдер атауы қышқылдардың латынша атауынан түзілген.
3. 13Бірнегізді қанықпаған қышқылдар .
Қанықпаған карбон қышқылдары.
Қанықпаған көмірсутек радикалы Карбоксил тобымен байланысқан қосылыстар .
Құрамында бір қос байланысы бар қанықпаған карбон қыш. Жалп форм.-CnH2n-1COOH.
Мысалы: CH2=CH-COOH - пропен (акрил) қышқылы .
СH2= C -C OOH – 2 – метилпропен (метакрил қышқылы) .
CH 3
Қанықпаған жоғары қышқылдарға Олеин (C17-H33-COOH), Линол( C17-H31-COOH) , Линолен (C17-H29-COOH) жатады . Бұл қышқылдар – тармақталмаған нормальды тізбекті .
Химиялық қасиеттері .
Қанықпаған бірнегізді қышқылдар Күштірек, себебі қос байланыс әсер етеді .
Қанықпаған қышқылдардың химиялық қасиеттерін карбоксил тобы мен қос байланыс анықтайды. Сондықтан олар да карбоксил тобы бойынша карбон қыш. Тән реакцияға түсіп,тұздар,күрделі эфирлер және ангидридтер түзеді.
Еселі байланыс бойынша : қосылу, полимерлену және тотығу реакц. Түседі .
Галогенмен әрекеттесіп қаныққан қыш. Дигалоген туындыларн түзеді .
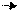 Бромды сумен әрекеттескенде бромның түсі жойылады : CH2=CH-COOH+Br2 CH2Br-CHBr-COOH
Бромды сумен әрекеттескенде бромның түсі жойылады : CH2=CH-COOH+Br2 CH2Br-CHBr-COOH
Пропен(акрил) қыш. 2,3-дибромпропан қыш.

 Қанықпағанқышқылдар қос байланыс бойынша полимерленеді :
Қанықпағанқышқылдар қос байланыс бойынша полимерленеді :
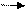 nCH2=CH-COOH - CH2 – CH -
nCH2=CH-COOH - CH2 – CH -
акрил қыш. COOH n
полиакрил қыш.
Акрил (пропен) қышқылы CH2 = CH – COOH . Өткір иісті сұйық зат.
Құрамындағы еселі байланыс және карбоксил тобы бойынша химиялық реакц. Түседі.
Акрил қыш. Эфирлерінің маңызы Полимер алу үшін қажет.
Метакрил (2- метилпропен) қыш. CH2 = C ( CH3 )- СООН.
Қанықпаған жоғары карбон қышқылдары күнбағыс,зығыр,зәйтүн,мақта т.б. өсімдік майларында құрамында Глицерин түрде кездеседі.
Қанықпаған қышқылдар – қан тамырларының иілімділігін (жұмсақтығын) арттырады.
Бромды суды түссіздендіруді қышқылдардың құрамында еселі байланыс бар екендігін дәлелдейді.
Олеин қышқылы синтездік көксағыз,тоқыма өнеркәсібінде,сабын алуға , косметикалық заттар өндіруге қолданады.
Оңай тотығатын және полимерленетін болғандықтан , қанықпаған қышқылдар бояу және сарымай (олифа) жасауға пайдаланады.
3,14Жай жəне күрделі эфирлер
1.Спирттер молекуласындагы гидроксил тобының сутек атомын радикалга алмастырганда эфирлер алынады.
2.Эфирлердің жалпы формуласы: R—О—R'
3.Жай эфирлер — молекуласындағы екі көмірсутек радикалы бip-бipiмен оттек атомы арқылы байланысатын
органикалық қосылыстар.
4.Əртүрлі радикалдары бар эфирлерді араласэфирлер деп атайды.
5.Жай эфирлерді сутартқыш заттар қатысында спирттерді молекулааралық дегидратациялап алады.
6. CH3-O-CH3(диметил эфирі)
CH3-O-C2H5(метилэтил эфирі)
7.Жай эфирлер жалпы формуласы CnH2n+2O бойынша спирттерге изомер болыпкеледі.C4H10O-ның изомерлері:
CH3-O-C3H7 (метилпропил эфирі)
C2H5-O-C2H5 (диэтил эфирі)
CH3-O-CH-CH3
|
CH3 (метилизопропил эфирі)
C4H90H (бутанол)
8.Жай эфирлердің маңызды өкілі-диэтил эфиріC2H5-O-C2H5 түссіз сұйықтық,өзіне тəн иісі бар,ұшқыш,тез оталғыш.Суда ерімейді,судан жеңіл.Ауамен жанасқанда жарылғыш зат түзеді.Оны сақтаған кезде жарылғыш пероксидтер түзіледі.Суда нашар ериді (6%,20 С).Еріткіш ретінде қолданылады.Медицинада этил эфирі наркоз ретінде жəне жүрек қызметін күшейту үшін пайдаланылады.Өндірісте жасанды талшық алуда жəне түтінсіз оқ-дəрі жасауда қолданылады.
Күрделі эфирлер
(карбон қышқылымен+спирт)
9.Табиғатта кең таралған маңызды биологиялық қосылыстар.Гүлдер мен жемістердің құрамында күрделі эфирлер болуына байланысты олардың хош иістері болады.Өсімдік жəне жануарлар майлары күрделі эфирлерге жатады.
10.R-COOR’
R’-O-COR
R МЕН R’-БІРДЕЙ НЕМЕСЕ ƏРТҮРЛІ КӨМІРСУТЕК РАДИКАЛДАРЫ.
11.Күрделі эфирлер кіші жəне үлкен молекулалы,қаныққан,қанықпаған,ароматты қышқылдар мен спирттерден түзілуі мүмкін.Күрделі эфирлерді спирттер мен бейорганикалық қышқылдарды əрекеттестіріп те алады.
12.Халықаралық номенклатура бойынша қышқылдың атына спирт радикалының атын қосымша етіп атайды:
H-C//O
\OCH3(құмырсқа қышқылының метил эфирі (метилформиат)
CH3-C//O
\OC2H5 (этилацетат)
13.Күрделі эфирлер-карбон қышқылдарымен классаралық изомерлер.Мысалы,C3H6O2 изомерлері:
H-C//O
\OC2H5 (этилформиат)
CH3-C//O
\OCH3(метилацетат)
C2H5-C//O
\OH(пропан қышқылы)
Алу əдістері.
l. Күрделі эфирлерді көбіне табиғи өнімдерден алады.
2. Карбон қышқылдары мен спирттерді минерал қыш.қылдар (мысалы, концентрлі күкірт қышқылы) қатысында әрекеттестіріп күрделі эфирлер алады. Этерификация реакциясында спирт пен карбон қышқылдары әрекеттесіп, нөтижесінде күрделі эфир мен су түзілетінін білесіңдер. Эфирлену реакциясықайтымды процесс.
Физикалық қасиеттері.
Қарапайым карбон қышқылдарының күрделі эфирлері түссізсұйықтықтар, суда ерімейді. Күрделі эфирлердің көбінің иістері жағымды. Молекула арасында сутектік байланыс жоқ болғандықтан, сәйкес қышқылдарға қарағанда күрделі эфирлердің қайнау температуралары төмен болады.
HCOOC2H5(этилформиат)
HCOOC4H9(бутилформиат)
HCOOC5H11(амилформиат)
HCOOCH2-CH2CH(CH3)2(изоамилформиат)
CH3COOC2H5(этилацетат)
CH3COOCH2-CH2-CH (CH3)2(изоамилацетат)
C3H7COOC2H5(этилбутират)
C3H7COO-CH2-CH2-CH(CH3)2(изоамилбутират)
Химиялық қасиеттері.
Гидролиздену реакциясы. Күрделі эфирлердің гидролизі этерификация реакциясынa кері реакция, қышқыл немесе сілті қатысында жүреді. Күрделі эфир сумен әрекеттесіп айырылып, реакция нөтижесінде қышқыл және спирт түзіледі:
CH3COOC2H5+H2O--->CH3COOH+C2H5OH.
Этилацетат (CH3COOC2H5) -өзіне тән иісі бар түссіз сүйық зат, судан жеңіл және суда нашар ериді.Тамақөнеркəсібінде,парфюмерияда жəне полимерлерге еріткіш ретінде қолданылады. Метилметакрилат (CH2=C-COOCH3
|
CH3)
метакрил қышқылының метил эфирі). Метилметакрилатты полимерлегенде, полиметилметакрилатқа айналады. Полиметилметакрилат-шыны тәрізді түссіз, мөлдір, берік, қатты зат органикалық шынынемесе плексиглас деп аталады. Техникада қолданылады.
МАЙЛАР .
Майлар- үшатомды спирт глицерин мен жоғары карбон қышқылдарының күрделі эфирлері.
Майлардың табиғатта кездесуі мен маңызы . Барлық өсімдіктер мен жануарлар организмдерінде майлар болады. Көмірсулар мен нәруыздар сияқты майлар тағамның негізгі құрам бөлігі.
Майлы тағамдарға сарымай,мал майы жəне өсімдік майы жатады.Адамға тəулігіне 50-70г май қажет.Сұйық майдың биологиялық белсенділігі басқа майлармен салыстырғанда жоғары болады.Мысалы сұйық майдың құрамында витамин Е жəне қан тамырларында холестериннің жиналуына кедергі келтіріп,атероскрелозды болдырмайтын зат-бетта-ситостерин кездеседі.Сары майда көздің көруі мен адамның бойы мен шашының өсуін қолдайтын зат бетта-каротин болады.Тазартылмаған (рафинадталмаған)майда организмге аса қажет фосфолипидтер болады.
Майлар гидролизденіп, өнімдері біртіндеп тотығады. Ең соңында олар көміртек (IV) оксиді мен суға айналады. Бүл процестер экзотермиялық --организмнің тіршілігіне қажетті энергия бөледі. Осылайша майбиологиялық отын, тірі организм үшін энергиякөзі болып табылады. Май қорытылғанда бөлінетін энергияның мөлшері көмірсулар
мен нәруыздардан бөлінетін энергиядан екі еседей артық.
Майлардың құрамы мен құрылысы. Майдың құрамын француз ғалымдар М.Шеврель мен М. Бертло анықтады. ХІХ ғасырдың басында Шеврель майға су қосып сілті қатысында қыздырғанда, глицерин және карбон қышқылдары (стеарин және олеин) түзілетінін тапты.
Ал Бертло кері реакция жүргізді (1854 ж.). Глицерин мен карбон қышқылдарының қоспасын қыздырып майларға ұқсас зат алды.
Май қүрамына енетін күрделі эфирлерді түзуге глицерин және карбон қышқылдары (бір түрлі немесе әртүрлі) қатысады. Сондықтан осы күрделі эфирлер глицеридтер деп аталады:
CH2-O-H HO-OC-R CH2-O-OC-R
| |
CH-O-H + HO-OC-R ----> CH-O-OC-R +3H2O
| |
CH2-O-H HO-OC-R CH3-O-OC-R
глицерин карбон триглиицерид ( май )
қышқылы
Майдың құрамына кіретін көп таралған қышқыл қалдықтарында (ациклдерде)көміртек атомдарының саны 12ден 18ге дейін болады.Глицеридтер қарапайым жəне аралас болып бөлінеді.Қарапайым глицеридтердің радикалдары бірдей қышқыл қалдықтарынан,ал аралас глицеридтер əртүрлі қышқыл қалдықтарынан тұрады.
Глицеридтерді түзуге негізінен қаныққан қышқылдардан пальмитин C15H31COOH,стеарин C17H35COOH,қанықпаған қышқылдардан олеин C17H33COOH,линол C17H31COOH,линолен C17H29COOH қышқылдары қатысады.Кейбір төмен қышқылқалдықтары кіреді. Мыс:сарымайда май қышқылының қалдығы (C4H9COOH)қалдығы болады.Сиырдың сарымайы құрамына май қышқылымен қатар пальмитин жəне олеин қышқылдарының қалдықтары да кіреді.
Алу жолдары
Майларды жануарлар мен өсімдіктерден бөліп алады. Майларды синтездеуді алғаш рет француз химигі М. Бертло 1854 ж.) жүзегеасырды. Бірақ тиімсіз болғандықтан, майлар синтездік жолмен алынбайды.
Физикалық қасиеттері
Майлар судан жеңіл, тығыздығы О,9-О,95 г/смз. Суда ерімейді, көптеген органикалық еріткіштерде (бензол, бензин, дихлорэтан) ериді.
Агрегаттық күйіне байланысты майлар сұйық және қатты болып бөлінеді. Өсімдікмайы, əдетте, сұйық, ал жануар майы қаттыболады. Бірақ кейде жануар майының ішінде сұйығы ( балық майы ), ал есімдік майларының қаттысы да ( кокос майы ) кездесіп қалады . Майдың сұйық немесе қатты болуы оның құрамына кіретін карбон қышқылының табиғатына байланысты.Құрамына қанықпаған карбон қышқылының қалдығы кірсе-сұйық,қаныққан карбон қышқылының қалдығы кірсе-қатты.
Химиялық қасиеттері
1. Майлардың гидролизі.
CH2-O-OC-R HO-H CH2-OH
| |
CH-O-OC-R + HO-H ---> CH-OH + 3RCOOH
| ←- |
CH2-O-OC-R HO-H CH2-OH
2.Сілті қатысында гидролизденгенде глицерин мен жоғары карбон қышқылының тұзы (сабын)түзіледі.Бұл майдың сабындану реакциясы деп аталады:
CH2-O-OC-C17H35
| CH-O-OC-C17H35 + 3NAOH------>
|
CH2-O-OC-C17H35
тристеарин (май)
CH2-OH
|
----->CH-OH + 3C17H35COONA
|
CH2-OH натрий стеараты (сабын)
глицерин
Майларды гидрлеу (гидрогендеу)
Қыздырылған май ( 50-160°C) және ұнтақталған никель өршіткісі қоспасына сутек жібергенде, май құрамындағы еселі байланыстар сутекпен қанығады. Реакция нәтижесінде сұйық май қатты майға айналады. Ол майды саломас немесе құрама май деп атайды:
CH2-O-OC-C17H33 CH2-O-OC-C17H35
| |
CH-O-OC-C17H35 + 3H2--->CH-O-OC-C17H35
| |
CH2-O-OC-C17H35 CH2-O-OC-C17H35
триолеат (сұйық май) тристеарат(қаттымай)
Mr (884) Mr (890)
Қатты майлар өнеркəсіпте маргарин мен сабын алуға жұмсалады.Марганин жасау үшін саломасқа аздап сарымай,сүт,витаминдер,дəм жəне түс беретін қоспалар қосады.
Құрамында майы бар дәмді тағамдардың бірі _майонез. ОЛ негізінен өсімдік майынан (65%) тұрады. Майонезді майға су (25% ), жұмыртқа ұнтағын (5-6%), құрғақ сүт (2-3% ), қант, сіркесуын жөне дәм беретін, т.б. заттар қосып дайындайды. Сонымен қатар майларды техникалық мақсаттарға да пайдаланады. Мысалы, олардан сабын жасайды.
3.16 Сабын ж ә не Синтетикалық жуғыш заттар .
Сабын – жоғары карбон қышқылдарының тұздары RCOOMe.
Сабынның құрамына , негізінен, Пальмитин C15-H31-COOH және Стеарин C17-H35COOH қышқылдарының тұздары (натри мен калий тұздары ) кіреді .
Сұйық сабынның құрамына Калий , Қатты сабынның құрамына Натрий катиондары кіреді.
Сабынның суда ерігіштігі құрамындағы металл катионына байланысты .
Калий тұздары суда натрий тұздарына қарағанда жақсы ериді, ал магний , кальций,барий тұздары суда ерімейді.
 Сабын алу . Сабындану реакциясын майды натрий гидроксидімен немесе натрий карбонатымен қосып қыздыру арқылы жүргізеді .Реакция нәтежиесінде глицерин мен жоғары карбон қышқылының натрий тұзы (сабын) түзіледі : май + NaOH глицерин + сабын .
Сабын алу . Сабындану реакциясын майды натрий гидроксидімен немесе натрий карбонатымен қосып қыздыру арқылы жүргізеді .Реакция нәтежиесінде глицерин мен жоғары карбон қышқылының натрий тұзы (сабын) түзіледі : май + NaOH глицерин + сабын .
Түзілген сабынды бөліп алу үшін реакция өнімдеріне натрий хлоридін қосады, сонда сабын қоспаның бетіне қалқып шығып , глицерин астында қалады. Сабынды жинап алады және пішін береді .
Сабын жасағанда , жоғары май қышқылы тұзынан (RCOOMe) басқа оған хош иісті заттар, бояулар, антисептиктер және т.б. заттар қосады.
Қазіргі кезде майды үнемдеу мақсатында сабын алу үшін Мұнай өнімдері құрамындағы Көмірсутектерден карбон қышқылы алады.
Сабынның суда еруі кезінде жоғары қышқылдармен сілті түзе гидролиздену процесі бірге жүреді:
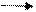 C17 H35 COONa + H2O C17 H35 COOH + NaOH
C17 H35 COONa + H2O C17 H35 COOH + NaOH
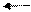
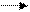 2C17 H35 COO- + Na+ + HOH 2C17 H35 COOH + Na+ + OH –
2C17 H35 COO- + Na+ + HOH 2C17 H35 COOH + Na+ + OH –
Сілті майлы заттарды ыдыратады , ал карбон қышқылы – беттік белсенді зат (ББЗ). Ол екі сұйықтықтың немесе сұйық пен газ шекарасында беттік керілуді төмендететін зат.
Карбон қышқылында гидрофобты көміртек қалдығы және гидрофилді сүйеді . Карбоксил тобы бар.
Сабын молекуласы екі бөліктен тұрады , көмірсутек тізбектегі майдың құрамында , ал СООNa+ тобы суда болады.
Сабынның жуғыш қасиетті – жуылатын беттердегі жабысқан кір бөлшектерін эмульсия,суспензия түріне ауыстыра алатын мүмкіндігіне байланысты.
Кермек суда сабын іріп кетеді де, кір ашылмайды. Себебі кермек суда карбон қышқылының кальций , магний тұздары тұнбаға түседі :
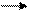 2C17 H35 COONa + CaCl2 (C17 H35 COO)2 Ca+ 2 NaCl
2C17 H35 COONa + CaCl2 (C17 H35 COO)2 Ca+ 2 NaCl
Жоғары карбон қышқылдарытұздарының қолданылуы жуғыш заттар ретінде шектелмейді . Кальций тұзын мұнай майларына қосып, солидол жағар майын алады .
Тығыз маталарды алюминий тұзымен өңдеп, су өткізбейтін брезенттер жасайды .
Қорғасын, марганец тұздарын майлы бояулар дайындағанда пайдаланады.
Синтетикалық (СЖЗ) жуғыш заттар негізінен , алкинсульфаттардың натрий тұзынан тұрады RO-SO2-Ona R –құрамында 8-18 көміртек атомы бар көмірсутек радикалы .
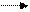 СЖЗ алуүшінәуелі спирт пен күкірт қышқылын әрекеттестіріп күкірт қышқылының күрделі эфирін алады: R – OH + OH – SO2 – OH R – O –SO2 – OH + H2O
СЖЗ алуүшінәуелі спирт пен күкірт қышқылын әрекеттестіріп күкірт қышқылының күрделі эфирін алады: R – OH + OH – SO2 – OH R – O –SO2 – OH + H2O
Күкірт қышқылы алкильсулфат
Түзілген алкилсульфаттан күрделі эфирдің натрий тұзын алады :
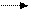 R – O – SO2 – OH + NaOH R – O – SO2 – ONa + H2O
R – O – SO2 – OH + NaOH R – O – SO2 – ONa + H2O
СЖЗ күкірт сутектің ұзын тізбегі (R) мен ерігіш функционалдық топтан тұратындықтан , Сабын сияқты жуғыш заттық қасиеті жоғары. Сабынан айырмашылығы – кальций мен магний тұздары ерігіш болғандықтан , жуғыштық қасиетін кермек суда жоймайды.
Дисахаридтер
Дисахарид-гидролизденгенде екі молекула моносахарид түзетін көмірсулар.
Дисахаридтер молекулалары өзара оттек атомы арқылы жалғасқан моносахаридтердің екі қалдығынан құралады. Дисахаридтерге сахароза, лактоза, мальтоза, т.б. жатады.
R'-O-R"
Сахароза(қызылша қанты) C12 H22 O11. Сахарозаның молекуласы әртүрлі моносахарид қалдығынан – глюкоза және фруктозадан түзеледі: C6H11O5-O-C6H11O5.
Ол қызылша қантының құрамында (20%-ға дейін) кіреді. Оны өнеркәсіпте қант қызылшасынан және қант қамысынан алады.Сахароза көптегенөсімдіктерде, қантқызылшасында, қантқамысында, сәбізде, қауында, қайың мен үйеңкініңшырындарындаболады.
Сахароза — ақтүстікристалдызат, суда жақсыериді, дәмітәтті, балқутемпературасы 184-185° С. Сахарозаныбалқытып, содансоңқатырса, аморфтымөлдір масса карамель түзіледі.
Сахарозаныңерітіндісі мыс (II) гидроксидіменәрекеттескенде, ашықкөктүстіерітіндініңтүзілуі, сахарозаныңкөпатомдыспирткежататынынкөрсетеді.
Сахарозаныкүміс (I) оксидініңаммиактағыерітіндісіменқыздырғанда, "күмісайна" түзілмейді. Бұл сахароза құрамында альдегид тобыжоқекеніндәлелдейді.
Сахарозанықышқылқатысындақыздырғандагидролизденіп, екі моносахарид — глюкоза мен фруктоза түзіледі:
C12H22O12 + H2O → C6H12O6 + C6H12O6
Дисахаридтердісатылапгидролиздепполисахаридтерденалуғаболады:
(C6H12O5)n + nH2O → n/2 C12H22O11
СахарозаныңизомерлеріӨңдеу
Лактоза — сүтқанты. Молекуласы глюкоза мен оныңизомерігалактозаныңқалдығынанқұралған. Гидролиздегенде глюкоза мен галактозағаайналады:
C12H22O11 + H2O → C6H12O6 + C6H12O6
Лактоза коректілігіөтежоғарыөнім. Тәттілігісахарозадантөмендеу.
Мальтоза. Табиғатта бос күйіндекездеспейді, бұлдисахаридтікрахмалданалады. Гидролиздегендеглюкозаныңекімолекуласынтүзеді:
С12H22O11 + H2O → 2C6H12O6
Сахароза кальций гидроксидіментұнбағатүспейтінерігішсахараттүзеді: С12Н22О11 • СаО • 2Н2О. Бұлзаттыкөміртек (IV) оксидіменөңдейді. Кальций карбонаты тұнбағатүсіп, қантерітіндісіалынады:
С12Н22О11 • СаО • 2Н2О + СО2 → С11Н22О11+ СаСО3 + 2Н2О
Полисахаридтер
· Полисахаридтер –табиғи жоғары молекулалық қосылыстар.
· Полисахаридтердің жалпы формуласы:(C6H10O5)көптеген моносахарид молекуласының қалдықтарынан тұрады.
· Макромолекуладағы моносахаридтер қалдықтары полисахаридтерде де оттек «көпіршесі» арқылы жалғасқан: ...R – O – R – O – R...
· Фотосинтез нәтижесінде түзілген моносахарид молекулалары поликонденсацияланып полисахарид түзіледі:
6CO2+6H2O -- à C6H12O6+6O2
Моносахарид Поликонденденсациялану реакция: nC6H12O6 --à (C6H10O5)n+nH2O
· Полисахаридтердің маңызды өкілдері – крахмал мен целлюлоза.
· КРАХМАЛ (C6H10O5) –табиғатта кең тараған полисахарид. Күріште 80%-ға дейін, бидай мен жүгеріде 70-75%, картоп түйіндерінде 20% крахмал болады.
Крахмалдың құрылысы. Крахмал – табиғи полимер. Ол екі полисахаридтен: амилоза(түзу тікбекті) мен амилопектиннен(тармақты) тұрады.
Полимерлену дәрежесі -'п-нің мәні крахмалдың әртүрлі молекуласында шамамен 200-ден 2000-ға дейін болады. Крахмалдың молекулалық массасы бірнеше жүз мыңнан (амилоза) миллионға дейін (амилопектин) жетеді.
Крахмалдың макромолекуласы циклді альфа-глюкозаның қалдықтарынан түрады. алтфа-глюкозаның поликонденсацияланып крахмал түзілу процесінің сызбанүсқасы:
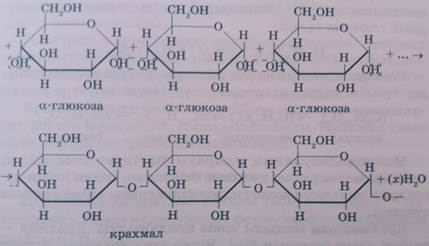 |
Крахмалды алу. Өндірісте крахмалды картоптан немесе жүгеріден алады. Картоптан крахмал алу үшін оны үнтақтап турап, сүзгіге салып, сумен шаяды. Сумен шайылған крахмалды ыдыстарда тұнғаннан кейін бөліп алып кептіреді.
Крахмалдың қасиеттері. Крахмал- салқын суда epiмейтін ақ түсті ұнтақ зат. Ыстық суда ісініп, коллоид ерітінді -клейстер түзеді. Крахмал- химиялық белсенділігі төмен зат.
1 . Крахмалдың маңызды химиялық қасиеттерінің бірі -йод ерітіндісімен әрекеттескенде көк түстің пайда болуы крахмалдың сапалықреакциясы. Оны картоптың немесе ақ нанның кесіндісіне, крахмал клейстріне йод ерітіндісін тамызып көруге болады. Бұл реакция тағам өнімдерінде крахмалдың бар-жоғын анықтау үшін қолданылады.
2. Крахмал ферменттердің әсерінен немесе минерал қышқылдың (H2S04) қатысында қыздырғанда гидролизденіп глюкоза түзеді:
(C6H10O5)n + nН²О -> nC6H12O6
Реакция жағдайына байланысты әртүрлі аралық өнімдер түзіліп, гидролиз сатылап жүруі мүмкін:
(С6Н1005)n -> ( C6H1005) -> xC12H22O11 -> nС6Н1206
Дата добавления: 2021-03-18; просмотров: 561; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
