Реакция образования сложных эфиров
Спирты в присутствии кислоты серной концентрированной образуют с органическими кислотами сложные эфиры. Низкомолекулярные эфиры имеют характерный запах, высокомолекулярные – определенную температуру плавления:

Спирт Этилацетат
Этиловый (характерный запах)
Методика: к 2 мл спирта этилового 95% прибавляют 0,5 мл кислоты уксусной, 1 мл кислоты серной концентрированной и нагревают до кипения – ощущается характерный запах этилацетата [3.9, 3.11].
Реакции окисления
Спирты окисляются до альдегидов при добавлении окислителей (калия дихромата, калия гексацианоферрата (III), реактива Фреде, иода).
Спирт этиловый окисляется йодом в щелочной среде при нагревании до трийодацетальдегида, который разрушается до йодоформа и соли кислоты муравьиной (первичные спирты):

|
|

Методика: 0,5 мл спирта этилового 95% смешивают с 5 мл раствора натрия гидроксида, прибавляют 2 мл 0,1 М раствора йода – постепенно выпадает желтый осадок йодоформа, который обнаруживают также по характерному запаху [3.9].
Реакции образования комплексных соединений (многоатомные спирты)
Многоатомные спирты (глицерин и др.) образуют с раствором меди сульфата в щелочной среде комплексные соединения синего цвета:
|
|
|
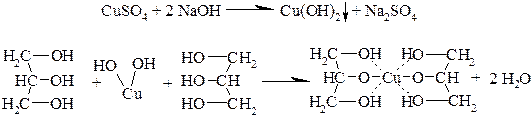
Глицерин осадок голубого интенсивно-синяя окраска раствора
Цвета
Методика: к 5 мл 5% раствора меди сульфата прибавляют 1 – 2 мл раствора натрия гидроксида до образования осадка меди (II) гидроксида. Затем прибавляют раствор глицерина до растворения осадка. Раствор окрашивается в интенсивный синий цвет [3.9].
4.2. ИДЕНТИФИКАЦИЯ ФЕНОЛЬНОГО ГИДРОКСИЛА
Фенолы – это ароматические вещества, содержащие в своей структуре одну или несколько гидроксильных групп, непосредственно связанные с бензольным кольцом.
Фенолы обладают более выраженными, по сравнению со спиртами, кислотными свойствами и взаимодействуют со щелочами, образуя легкогидролизуемые соли. При этом отрицательный заряд делокализован в орто- и пара-положениях бензольного кольца.
Лекарственные вещества, содержащие фенольный гидроксил:
А) Фенол д) Парацетамол


Б) Резорцин в) Синэстрол


Г) Кислота салициловая
|
|
|

4.2.1. Реакция с железа (III) хлоридом
Фенолы в нейтральной среде в водных или спиртовых растворах образуют соли с железа (III) хлоридом, окрашенные в сине-фиолетовый (одноатомные), синий (двухатомные: резорцин), зеленый (пирокатехин) или красный (флороглюцин). Это объясняется образованием катионов С6Н5ОFе2+, С6Н4О2Fе+ и др.


Методика: к 1 мл водного или спиртового раствора исследуемого вещества (фенол - 0,1:10, резорцин – 0,1:10, натрия салицилат – 0,01:10, пиридоксина гидрохлорид – 0,01:10) прибавляют от 1 до 5 капель раствора железа (III) хлорида. Наблюдается характерное окрашивание [3.9].
Дата добавления: 2020-11-23; просмотров: 90; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
