Управления простыми необратимыми реакциями . Влияние температуры на скорость и степень превращения в простых обратимых реакциях . Получение соляной кислоты
Управления простым необратимым гомогенным процессом
Характеристика модели:
1) Процесс простой – можно описать одним стехиометрическим уравнением
аА + bВ → cС + dD, где С – целевой продукт;
β = α, так как весь реагент превращается только в целевой продукт.
2) Процесс необратимый – αmax = 100%.
Величина конверсии реагента изменяется во времени α = f (τ), стремясь к максимальной величине 100%, так как текущая концентрация реагента «С» уменьшается во времени, стремясь к нулю. 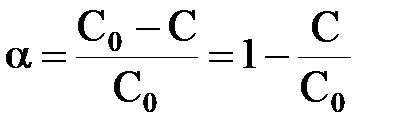
Чем меньше время достижения 100%-ной конверсии, тем эффективнее протекает реакция. То есть эффективность зависит от скорости химической реакции r .
3)Процесс гомогенный – скорость процесса равна скорости химической реакции.
На основе приведенной характеристики модели видно, что эффективность проведения простого необратимого гомогенного процесса определяется величиной скорости химической реакции, то есть единственным объектом управления является скорость химической реакции.
Инструментами управления простым необратимым гомогенным процессом являются те технологические параметры, которые влияют на скорость химической реакции, то есть температура, давление, концентрация реагента, природа и концентрация катализатора.
r = f (t, p, C, kat)
1) Влияние температуры
При повышении температуры скорость химической реакции увеличивается за счет увеличения константы скорости причем, чем больше энергия активации процесса, тем больше влияние температуры на скорость.
|
|
|
энергия активации эндотермического процесса всегда больше энергии активации обратного экзотермического процесса на величину теплового эффекта реакции. Следовательно, повышение температуры увеличивает в большей степени скорость эндотермической реакции.
В области низких температур при повышении температуры скорость процесса увеличивается за счет увеличения скорости прямой экзотермической реакции; обратная эндотермическая реакция при этих температурах еще практически не протекает.
Температура, при которой достигается максимальная скорость, называется оптимальной.
Получение Н Cl
H 2(г) + Cl 2(г)=2Н Cl (г)
Дельта Н=-183.7 кдж/моль

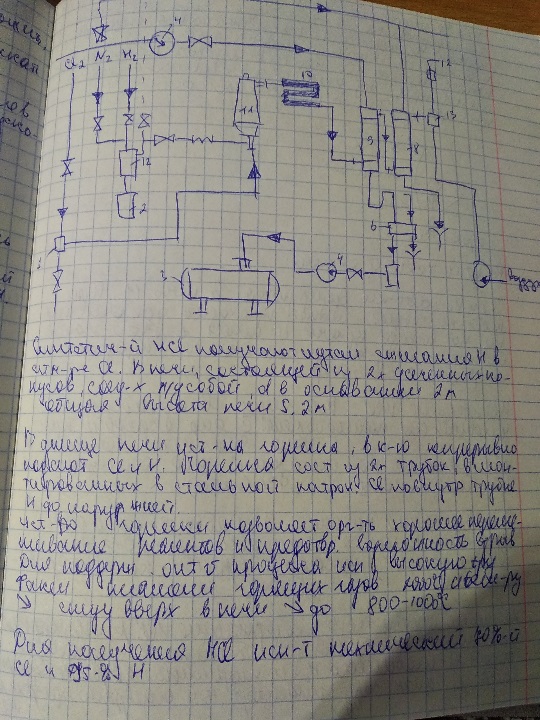

Понятие о равновесии. Влияние температуры , давления, концентрации на скорость и положение равновесия обратимых реакций
Обратимыми называются процессы, в которых одновременно протекают прямая и обратная реакции.
Рассмотрим реакцию aA + bB ↔ cC + dD.
В начальный момент времени скорость прямой реакции, которая пропорциональна произведению концентраций реагентов А и В
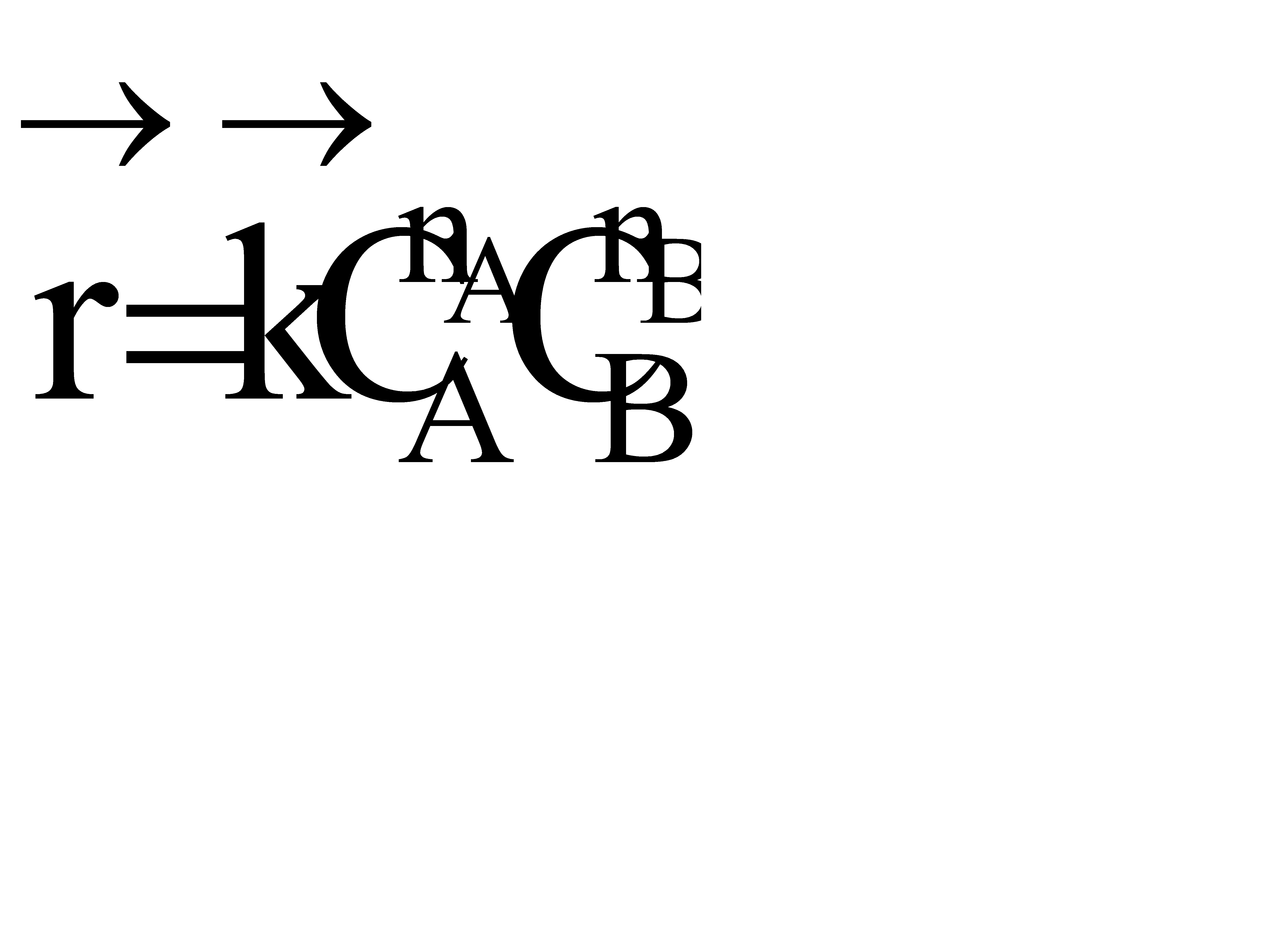 ,
,
больше скорости обратной реакции, пропорциональной произведению концентраций продуктов С и D
|
|
|
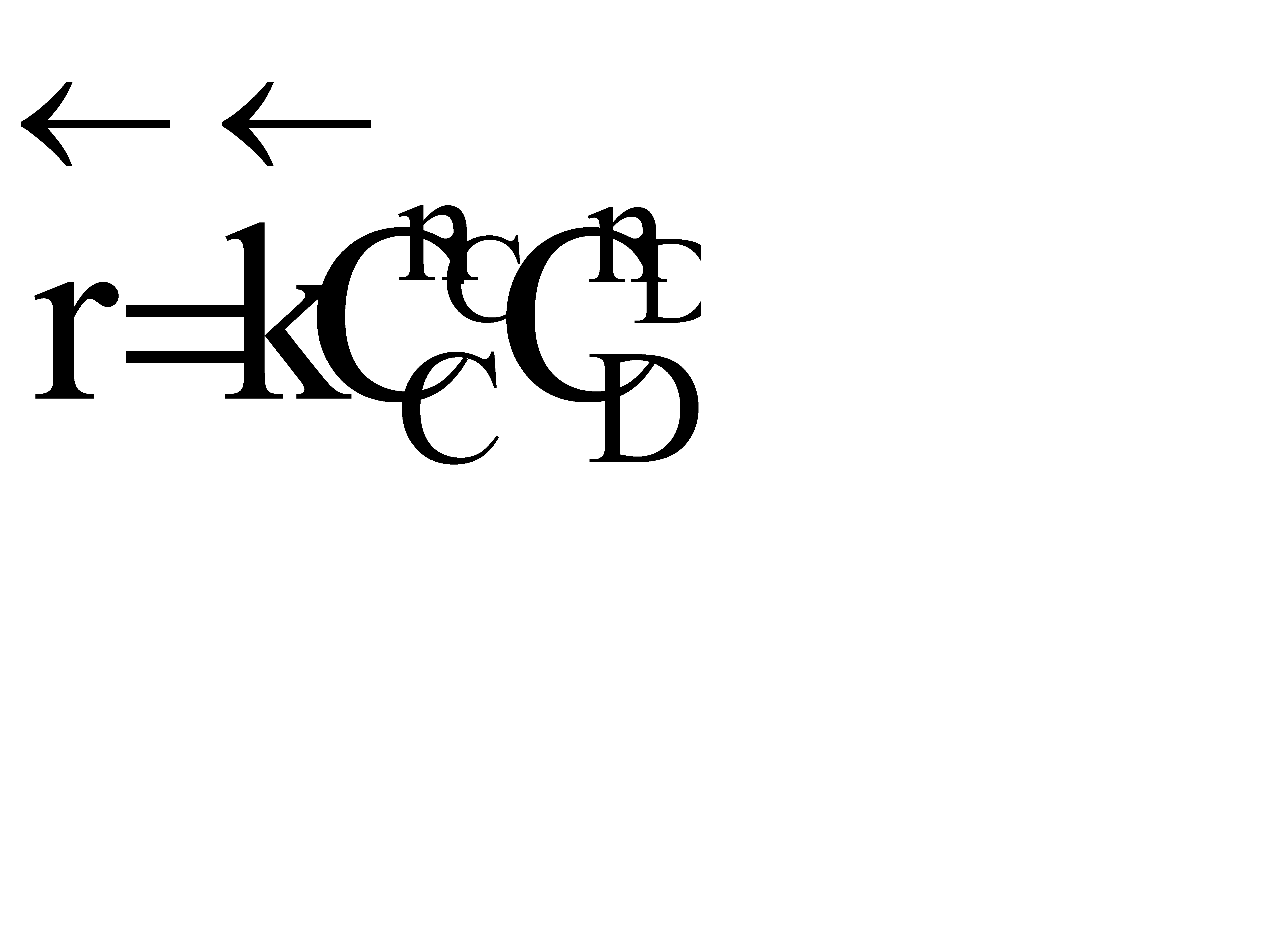 .
.
Но с течением времени, по мере увеличения концентрации веществ C и D скорость обратной реакции увеличивается, а скорость прямой реакции уменьшается. В некоторый момент времени они становятся равными
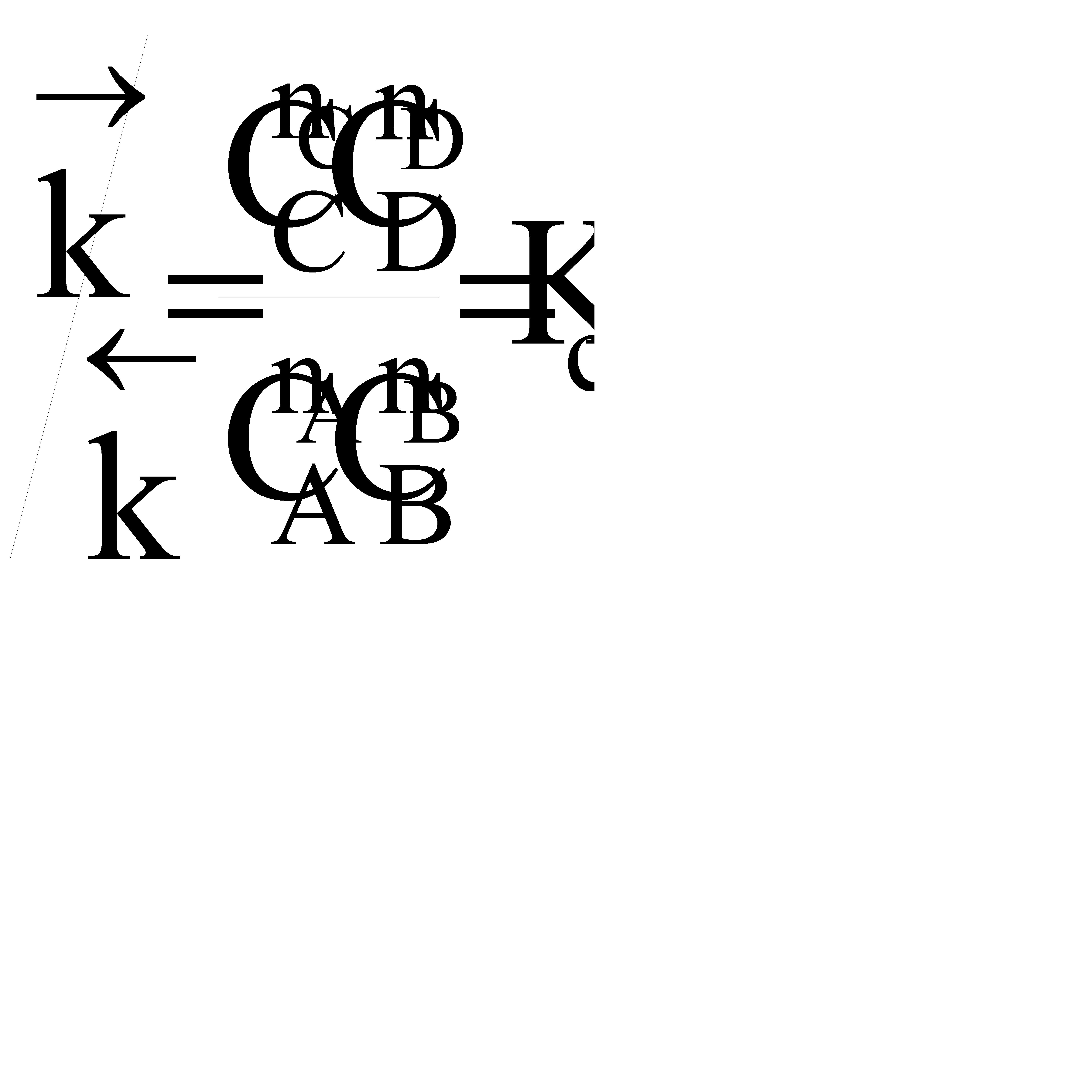
; наступает химическое равновесие. После достижения равновесия соотношение участников реакции остается постоянным во времени. Это соотношение называется константой равновесия.
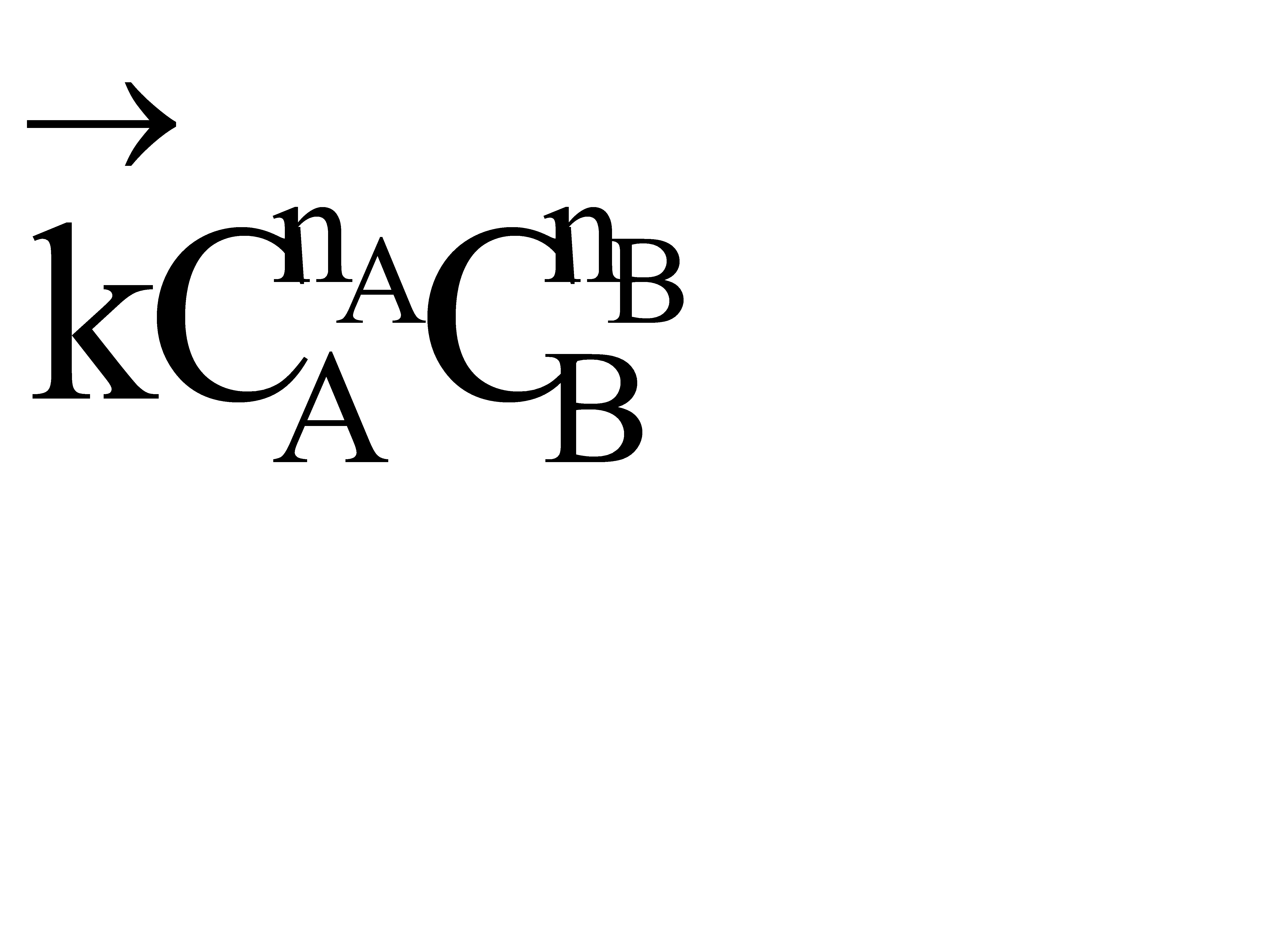 =
= 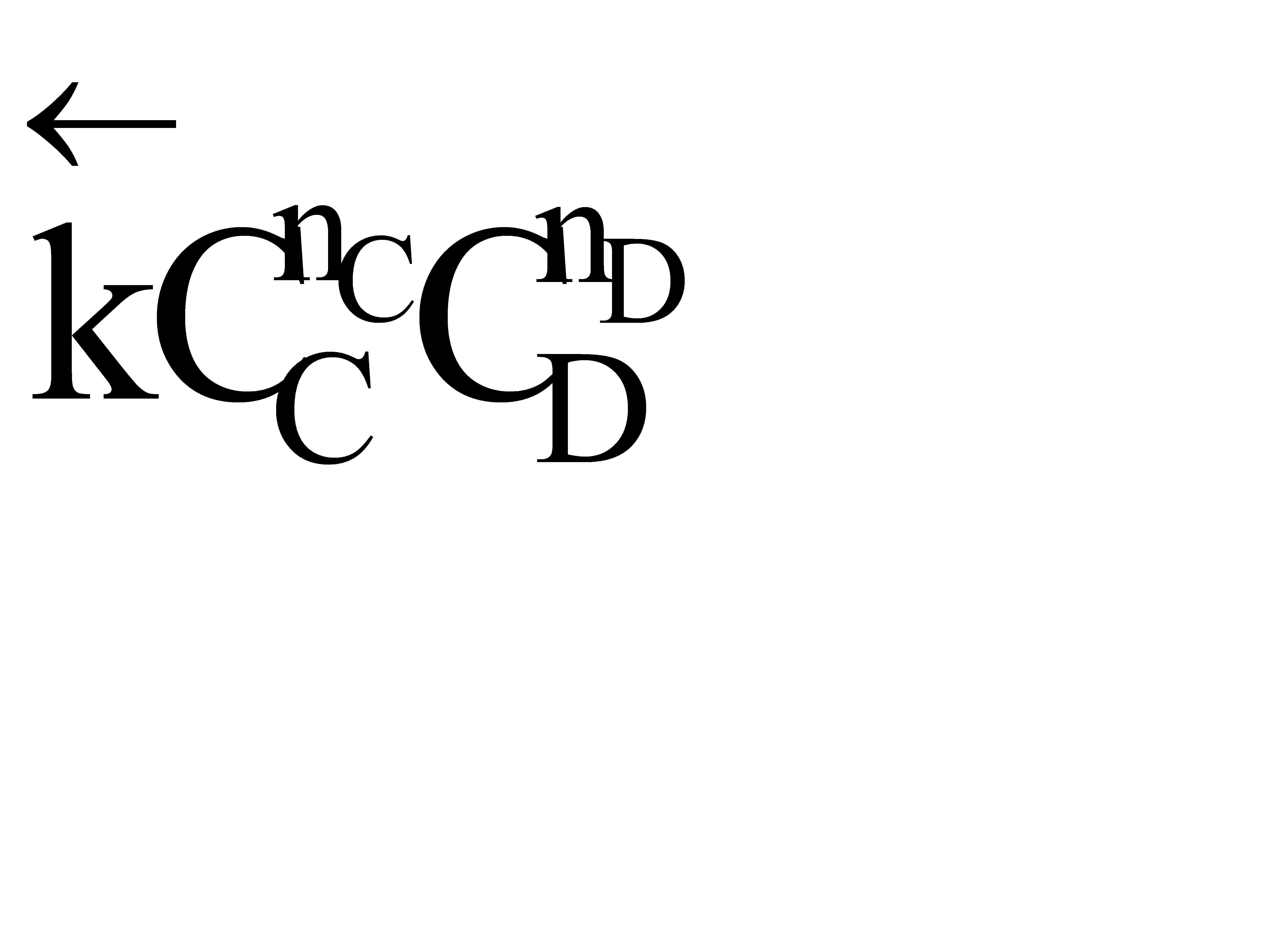
Для газофазных реакций константу равновесия можно выразить через парциальные давления участников реакции, которые пропорциональны их концентрации pi = Ci RT.
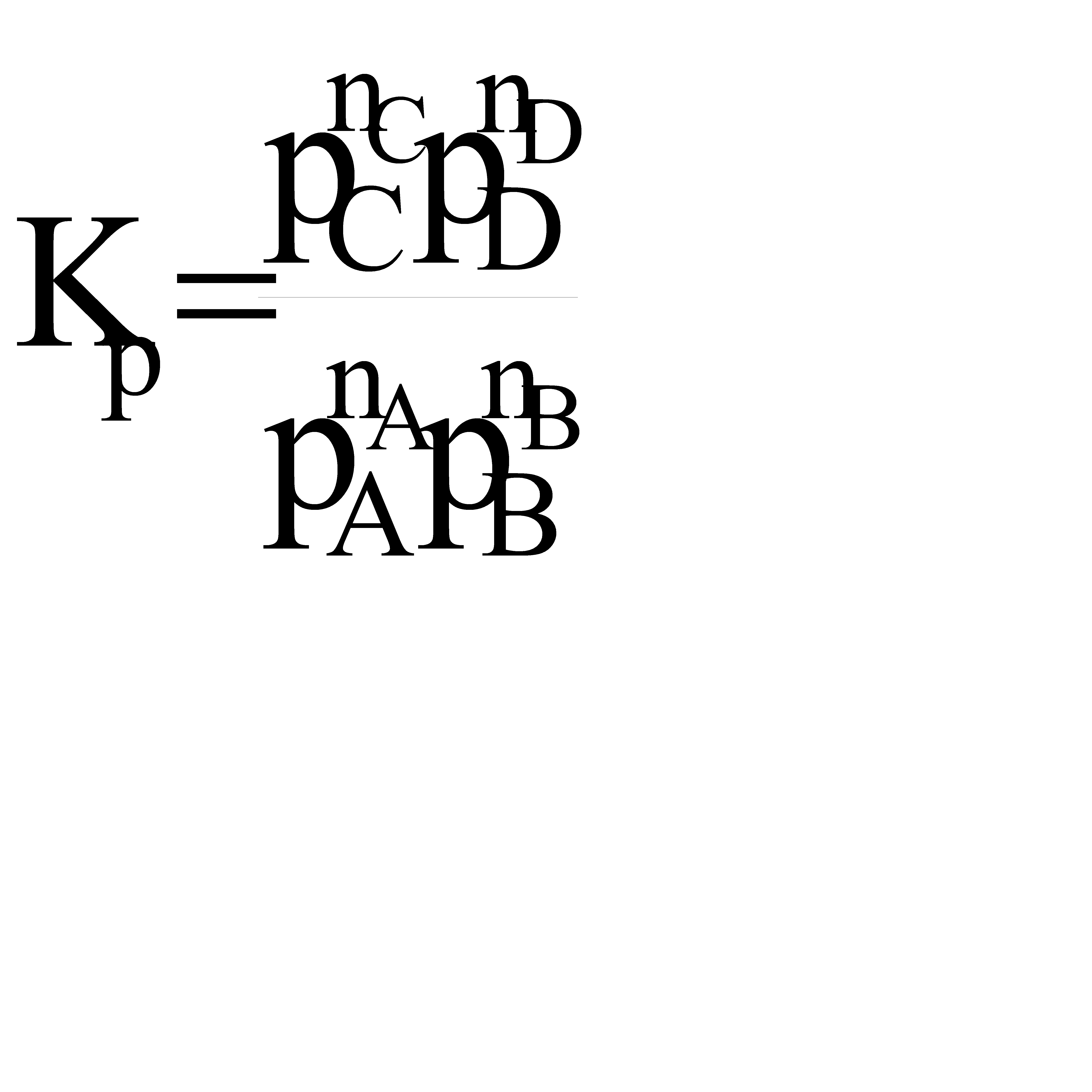
Между этими константами существует связь  , где
, где 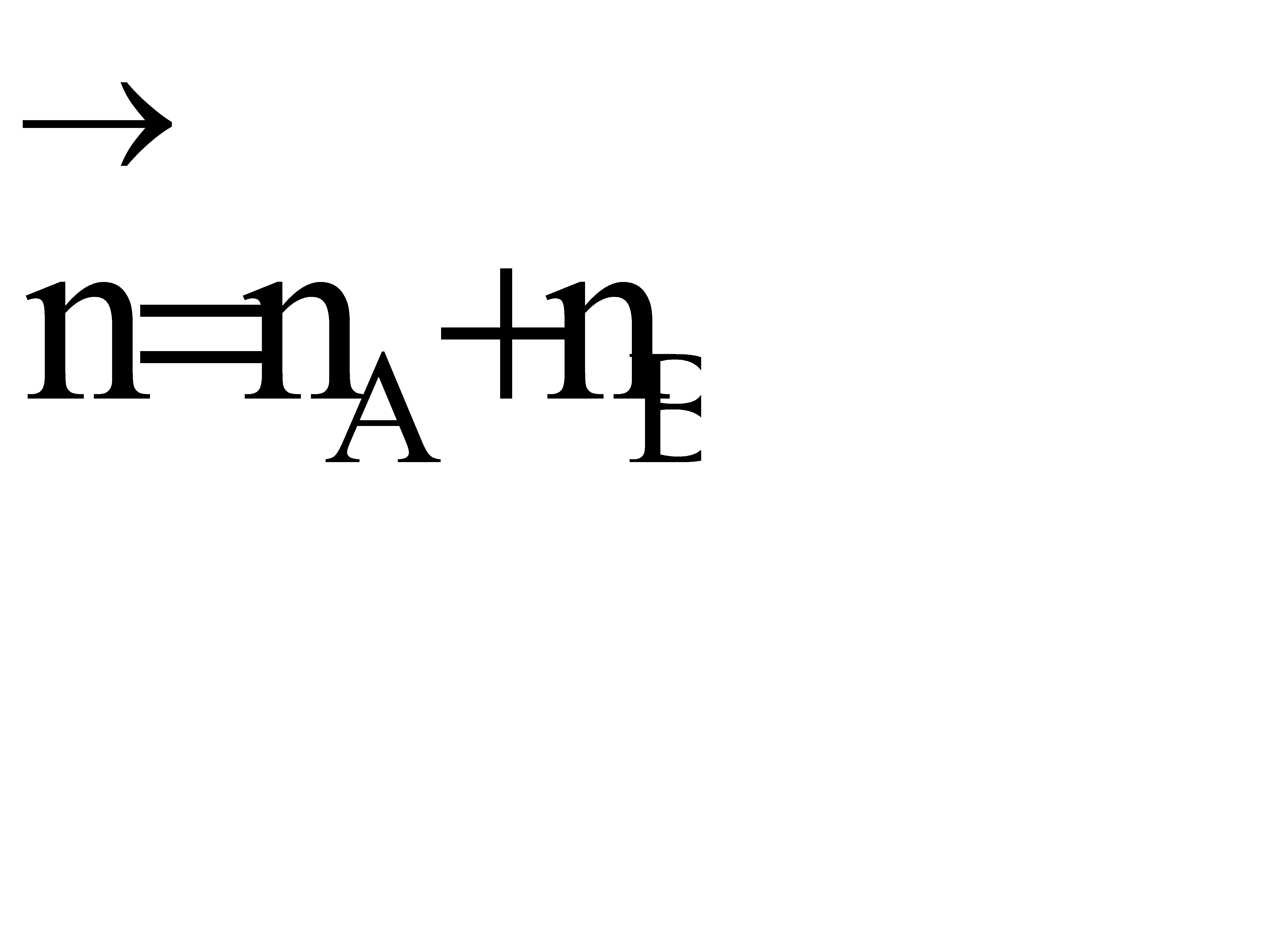 - суммарный порядок прямой реакции,
- суммарный порядок прямой реакции, 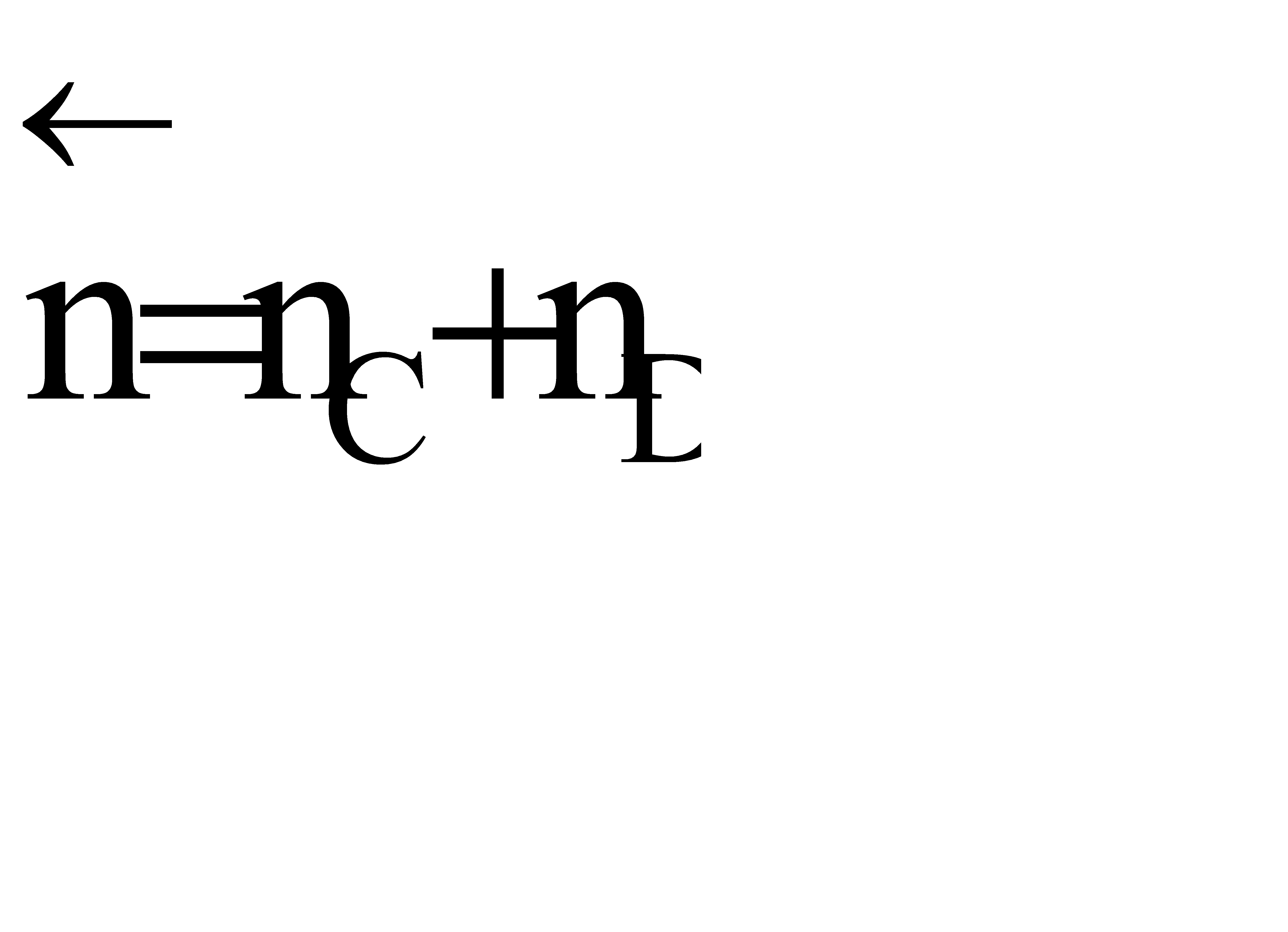 - суммарный порядок обратной реакции.
- суммарный порядок обратной реакции.
Константу равновесия газофазной реакции можно также выразить через мольные доли компонентов
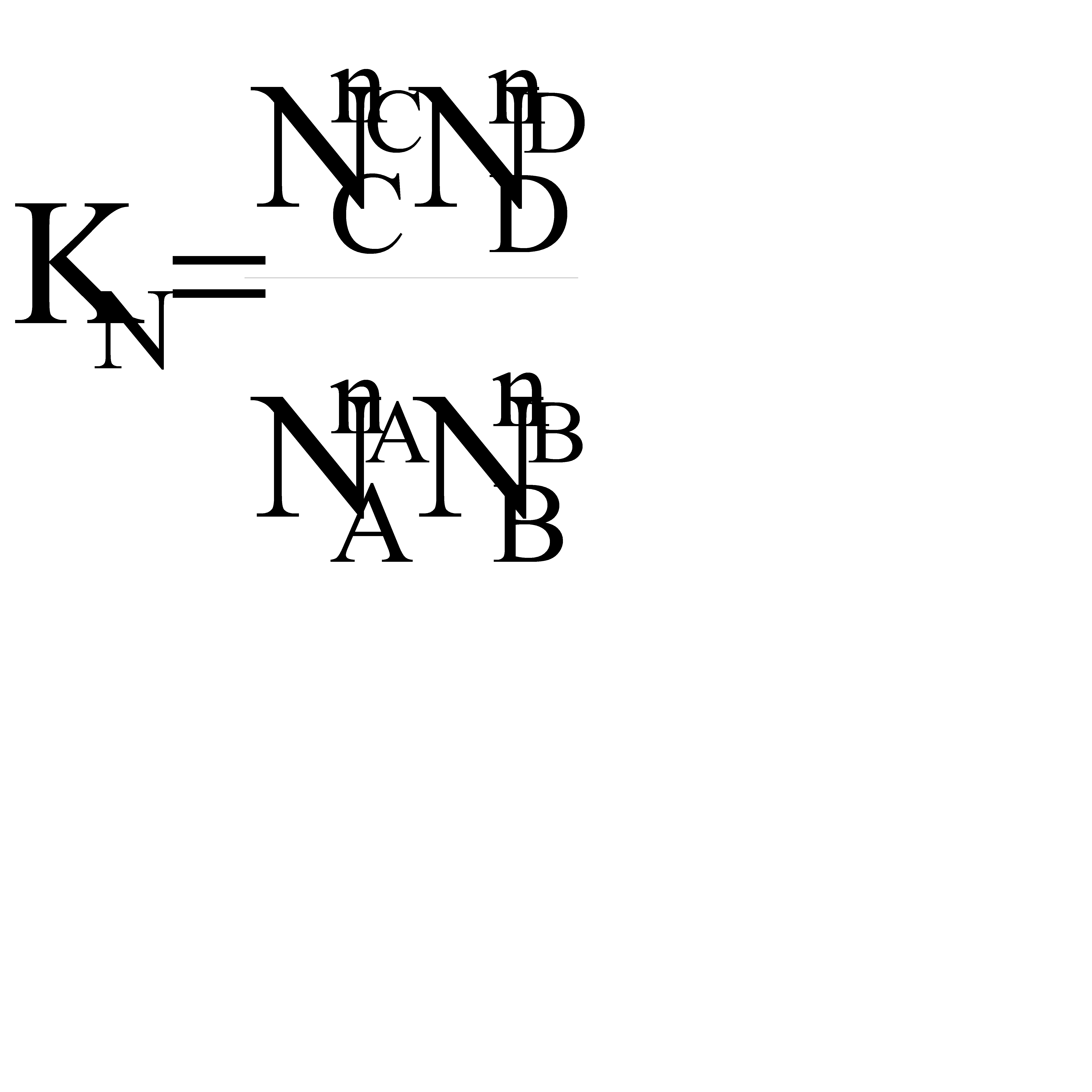 .
.
Парциальное давление каждого компонента пропорционально мольной доле его в смеси pi = p Ni, где р – общее давление системы, 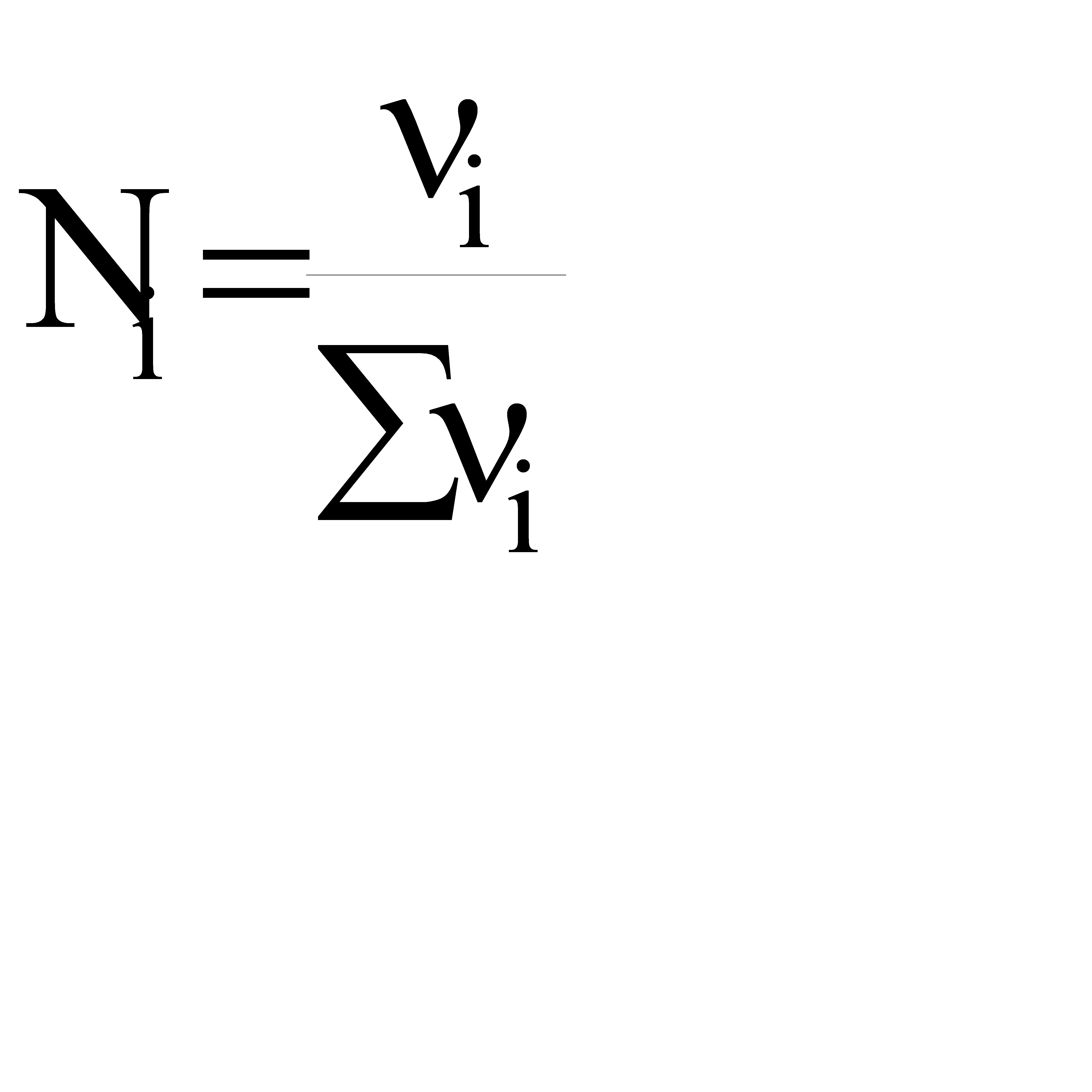 , νi – число молей данного компонента. Тогда
, νi – число молей данного компонента. Тогда 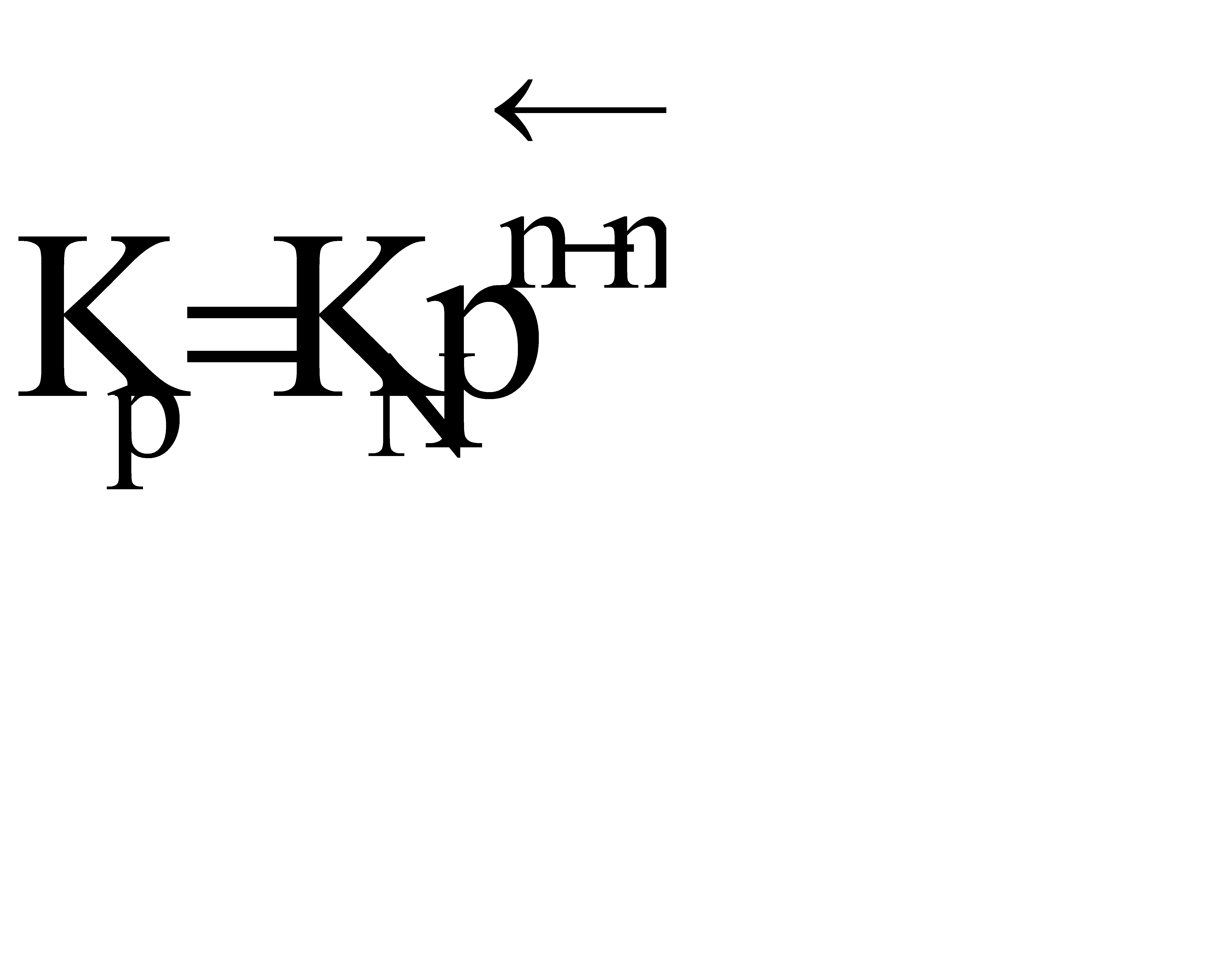 .
.
Константы Кс и Кр зависят только от температуры, а константа КN еще и от давления.
В случае реальных газовых смесей и растворов концентрации и парциальные давления в выражении констант меняют на активность «а» и фугитивность «f».
|
|
|
Итак, пределом протекания обратимых процессов является состояние равновесия, при котором скорости прямой и обратной реакции равны, а концентрации и парциальные давления продуктов и реагентов остаются постоянными во времени. При этом достигается некоторая максимальная в этих условиях степень превращения реагентов – равновесная конверсия α* и равновесный выход целевого продукта -β*. Их величина зависит от степени смещения равновесия в сторону образования целевого продукта. Следовательно, при управлении обратимым процессом важно не только обеспечить высокую скорость процесса, но и создать условия, при которых химическое равновесие смещено в сторону образования целевого продукта.
Характеристика модели:
1) Процесс простой – можно описать одним стехиометрическим уравнением аА + bВ ↔ cС + dD, где С – целевой продукт;
β = α, так как весь реагент превращается только в целевой продукт.
2) Процесс обратимый – αmax = α*≠ 100%.
| C* |
| С |
| τ |
| α |
| τ |
| α* |
| С0 |
1) Процесс гомогенный – скорость процесса равна скорости химической реакции. Однако следует помнить, что в обратимых процессах скорость равна разности скорости прямой и обратной реакции 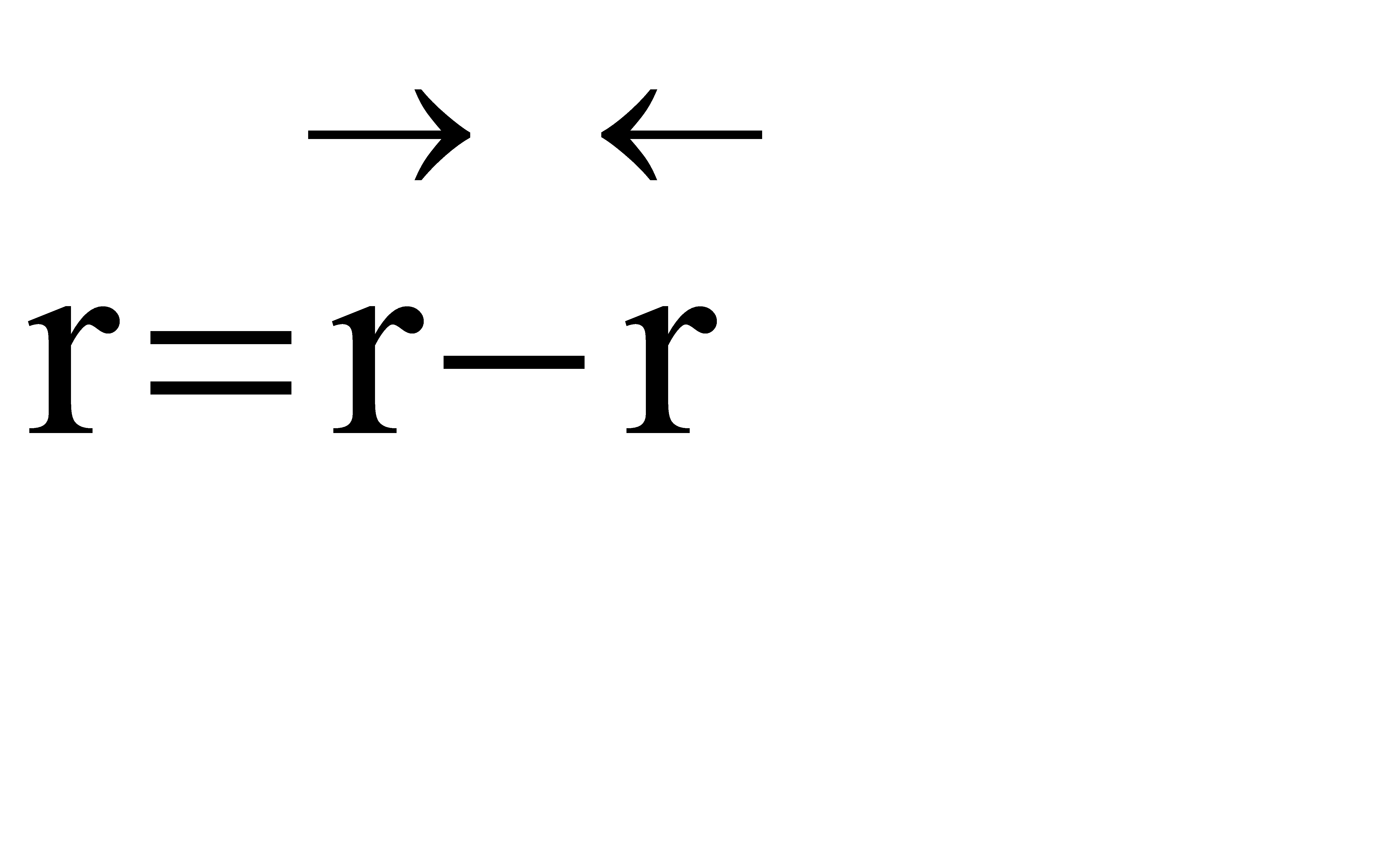 . Она уменьшается во времени и при
. Она уменьшается во времени и при 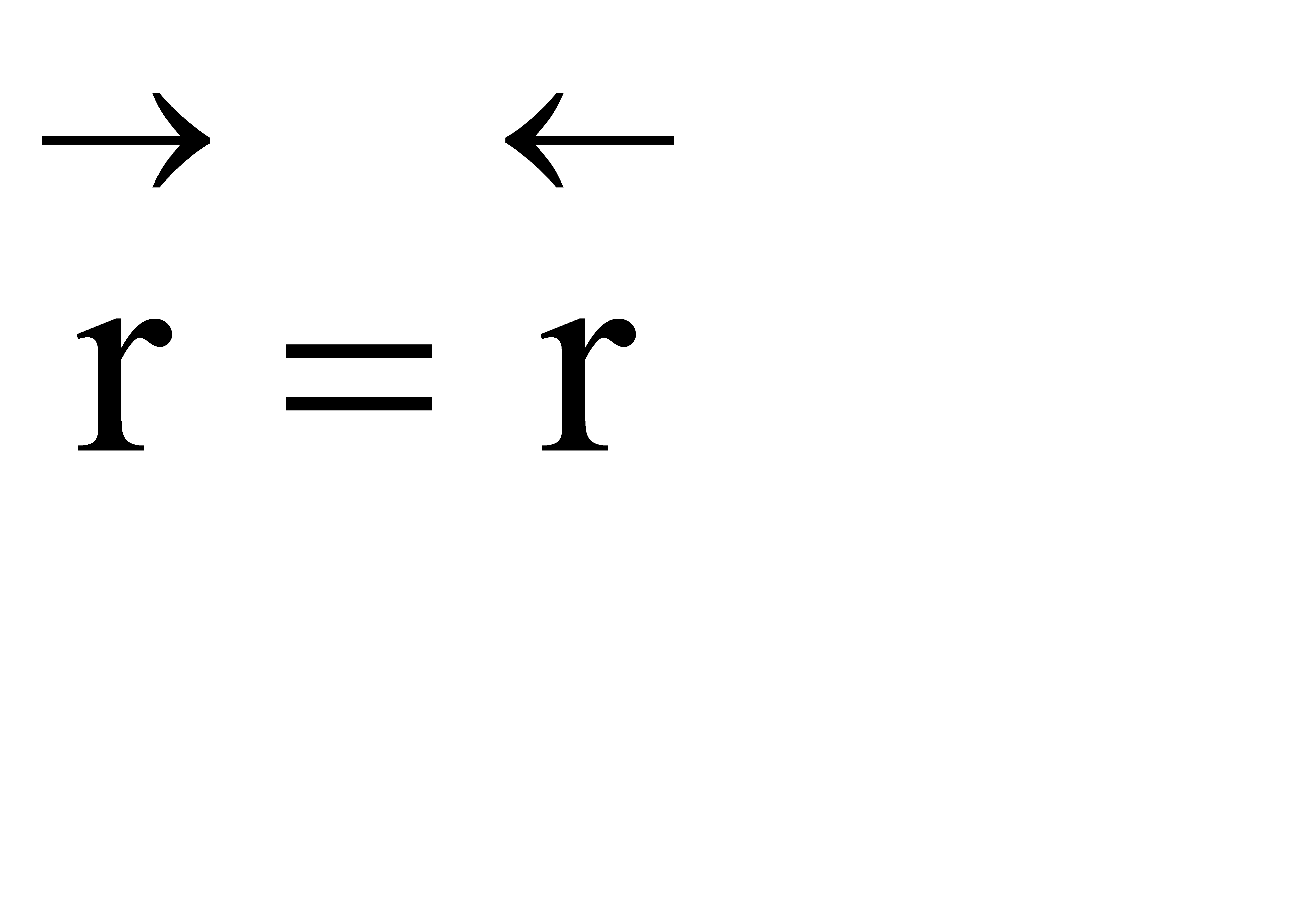 (в момент наступления химического равновесия) равна нулю.
(в момент наступления химического равновесия) равна нулю.
|
|
|
Объекты управления: скорость химической реакции и положение равновесия.
Инструменты управления: кинетические параметры.
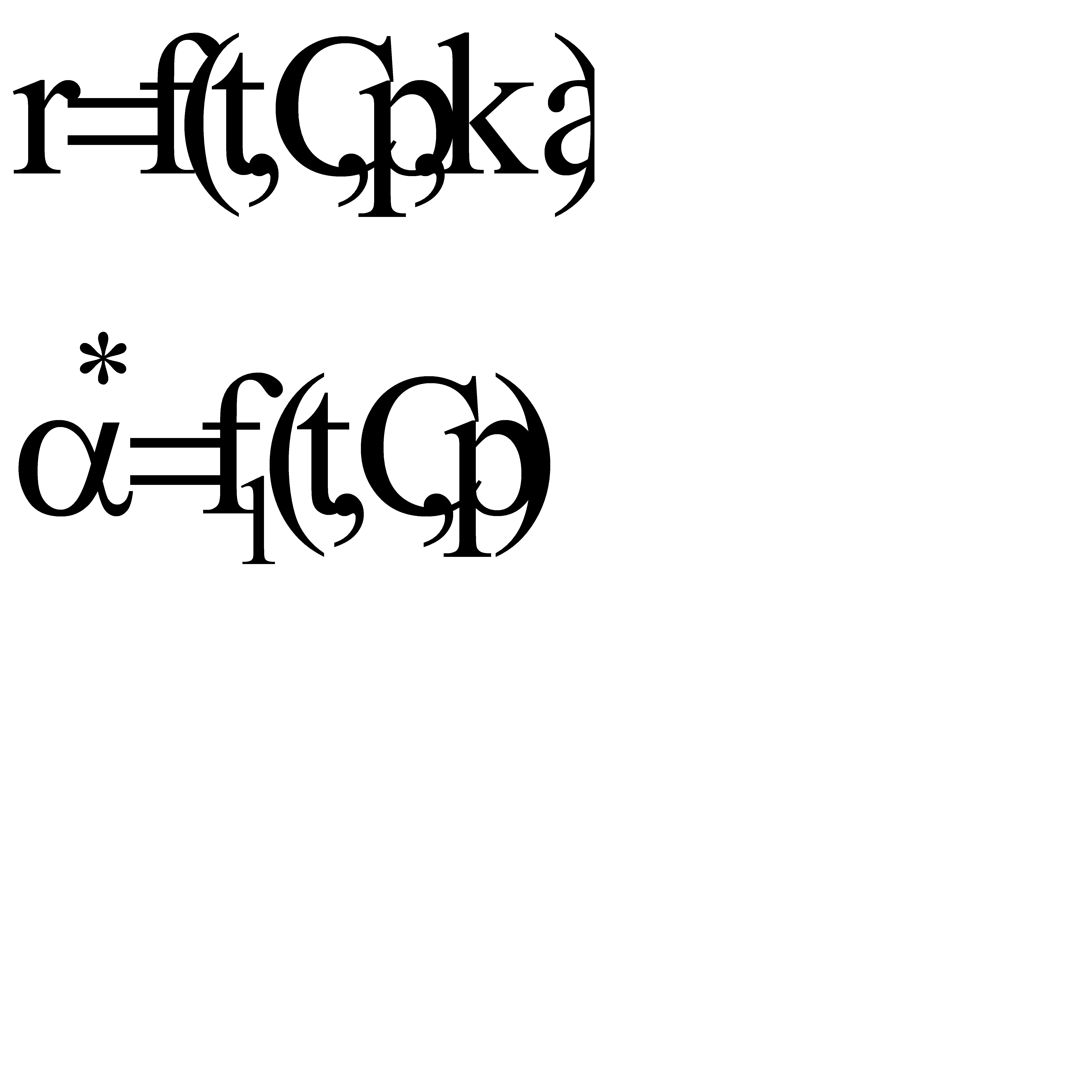
Правила смещения равновесия в обратимых процессах сформулированы химиком Ле-Шателье и состоят в следующем:
«Если на систему, находящуюся в равновесии, воздействовать извне, изменяя какое-нибудь из условий, определяющих равновесие, то равновесие смещается в том направлении, в котором эффект воздействия уменьшается».
Смещение равновесия происходит только в том случае, когда произведенное воздействие неодинаково влияет на скорость прямой и обратной реакции. Например, катализатор всегда одинаково ускоряет как прямую, так и обратную реакцию, и поэтому не оказывает влияния на положение равновесия.
Рассмотрим, как влияет на скорость и положение равновесия изменение таких технологических параметров, как температура, давление, концентрация реагентов.
1) Влияние температуры
При повышении температуры скорость химической реакции увеличивается за счет увеличения константы скорости, причем, чем больше энергия активации процесса, тем больше влияние температуры на скорость. Энергия активации эндотермического процесса всегда больше энергии активации обратного экзотермического процесса на величину теплового эффекта реакции. Покажем это на энергетической диаграмме.
По оси «y» отложим энергию рассматриваемой системы, а по оси «x» - путь или координату реакции. Пусть реакция взаимодействия А+В является экзотермической, ∆Н < 0. Тогда энергия системы в результате реакции будет понижаться; энергетический уровень продуктов С и D будет меньше энергетического уровня исходных реагентов. Разница между энергиями конечного и начального состояния есть тепловой эффект процесса ∆Н.
Чтобы молекулы веществ А и В прореагировали, они должны преодолеть некоторый энергетический барьер. На это затрачивается энергия, называемая энергией активации 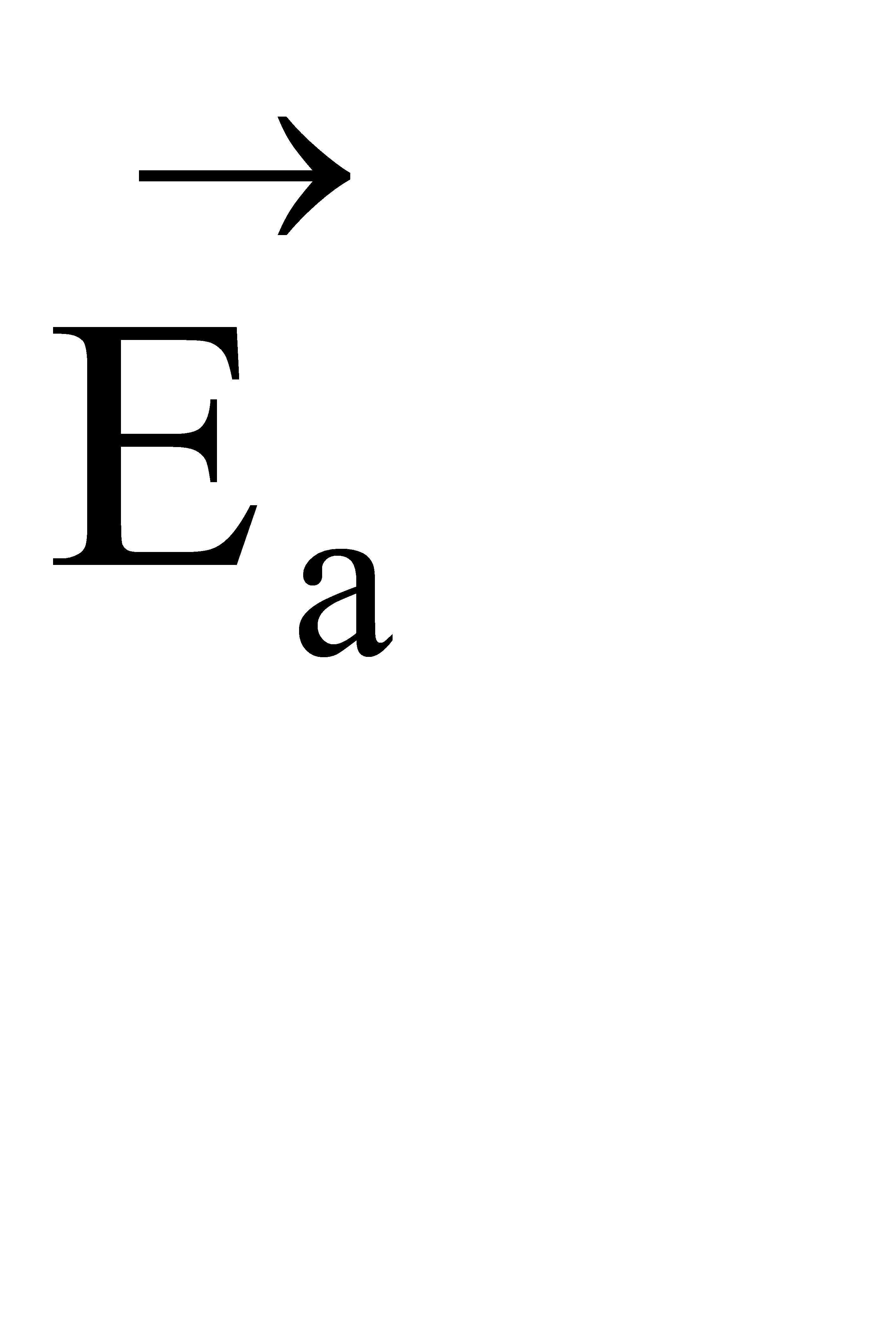 . Для того, чтобы прореагировали вещества C и D, они тоже должны обладать энергией активации
. Для того, чтобы прореагировали вещества C и D, они тоже должны обладать энергией активации 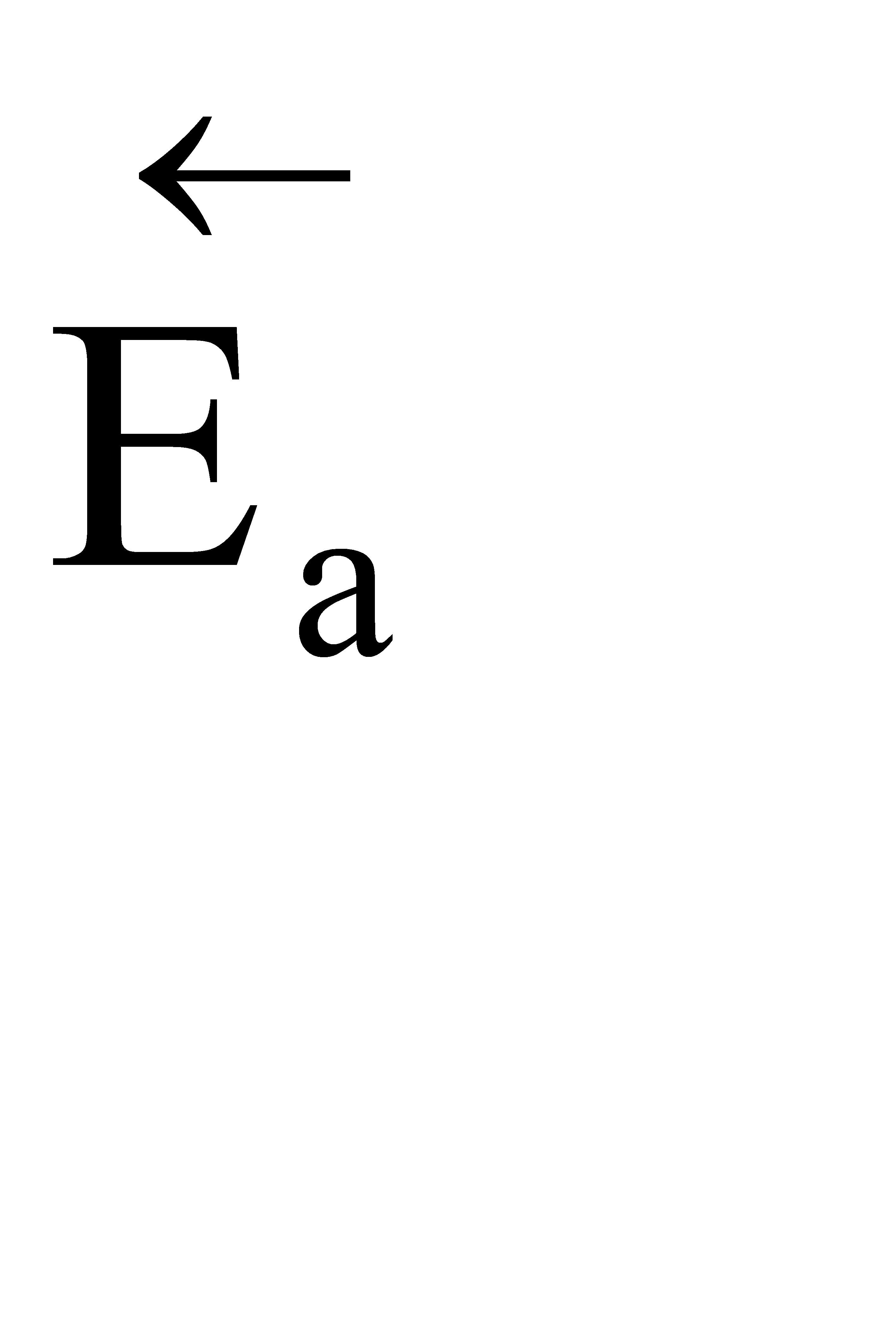 . Как видно из рисунка, энергия активации обратной реакции больше энергии активации прямой реакции
. Как видно из рисунка, энергия активации обратной реакции больше энергии активации прямой реакции 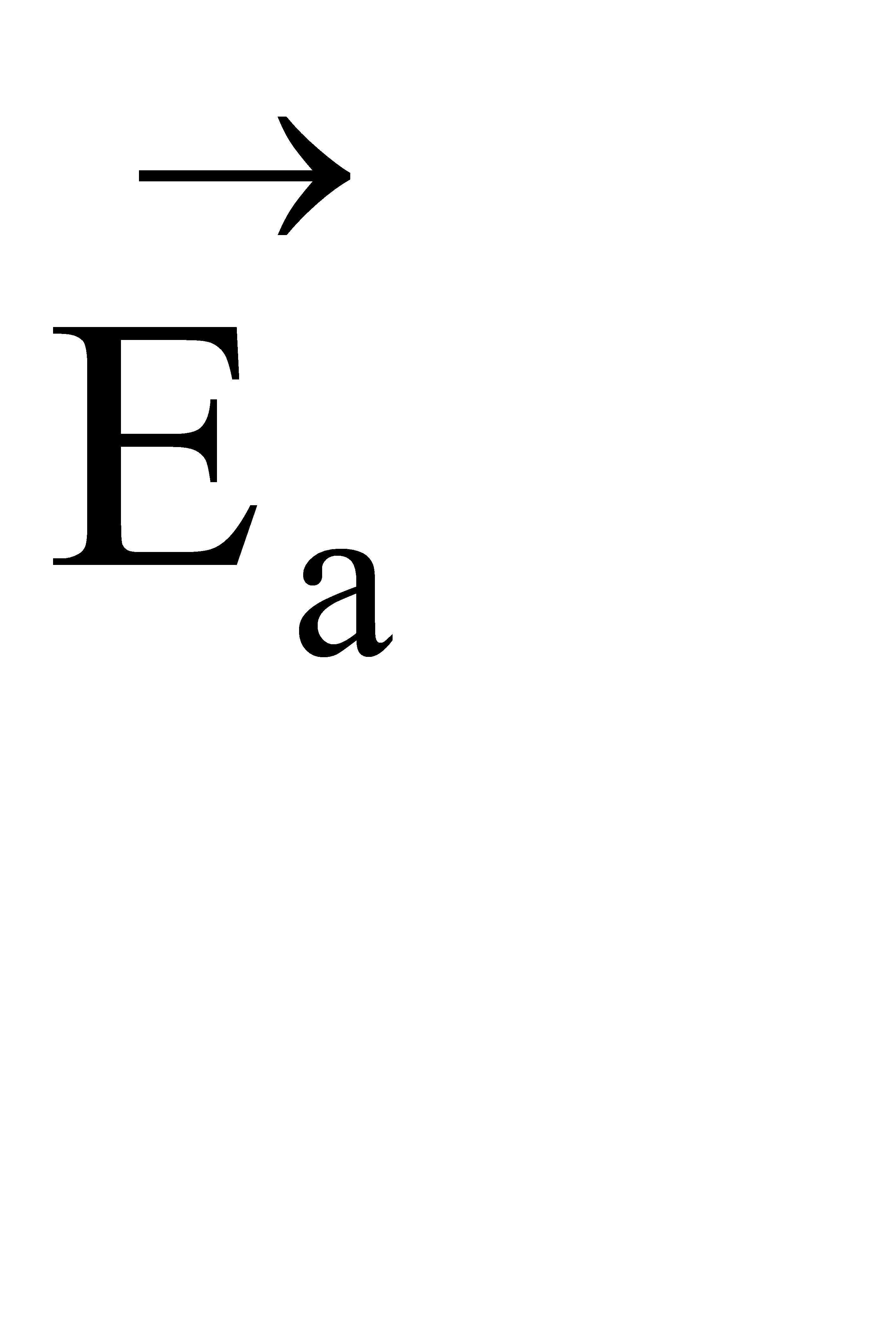 <
< 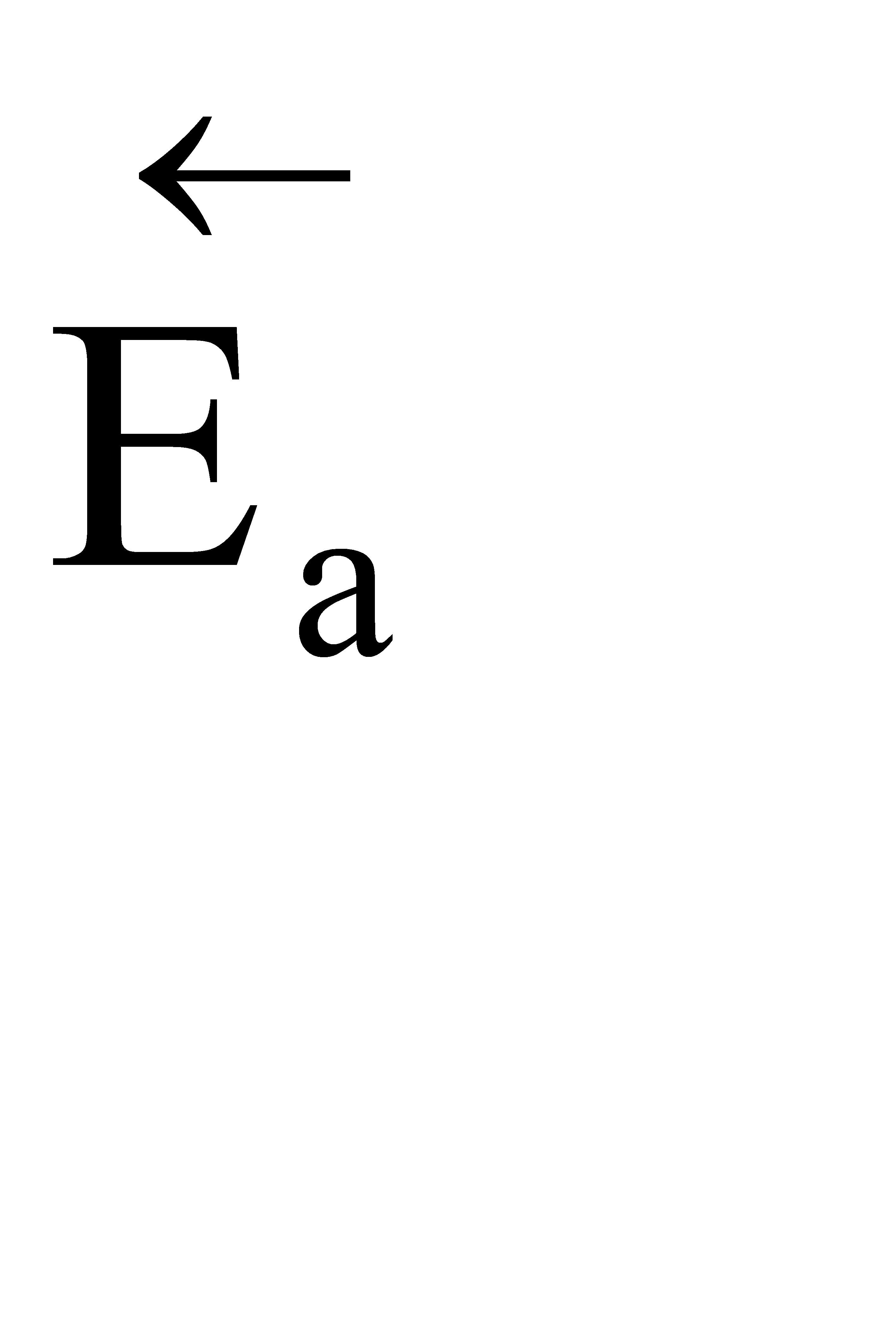 .
.
| энергия |
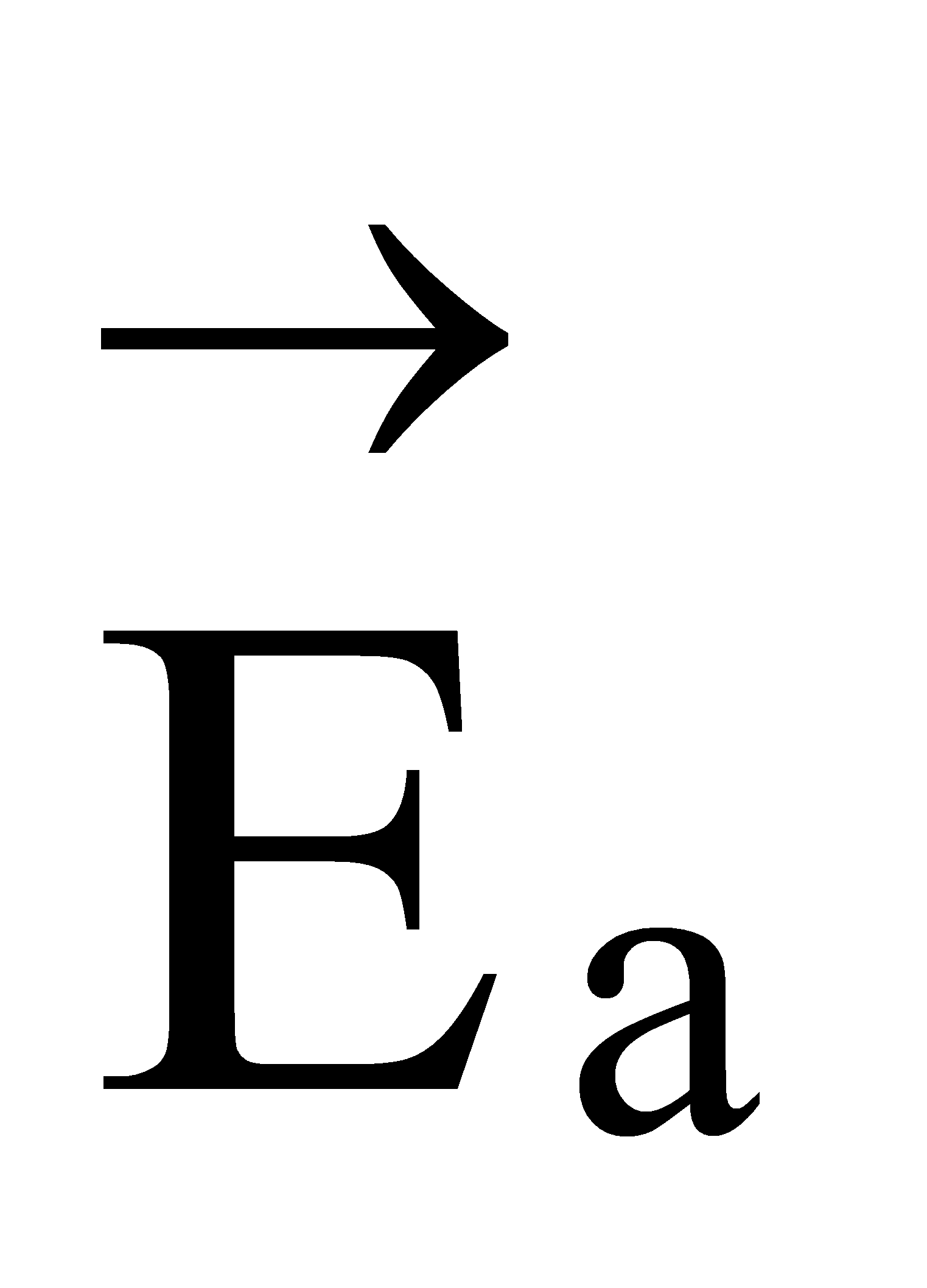
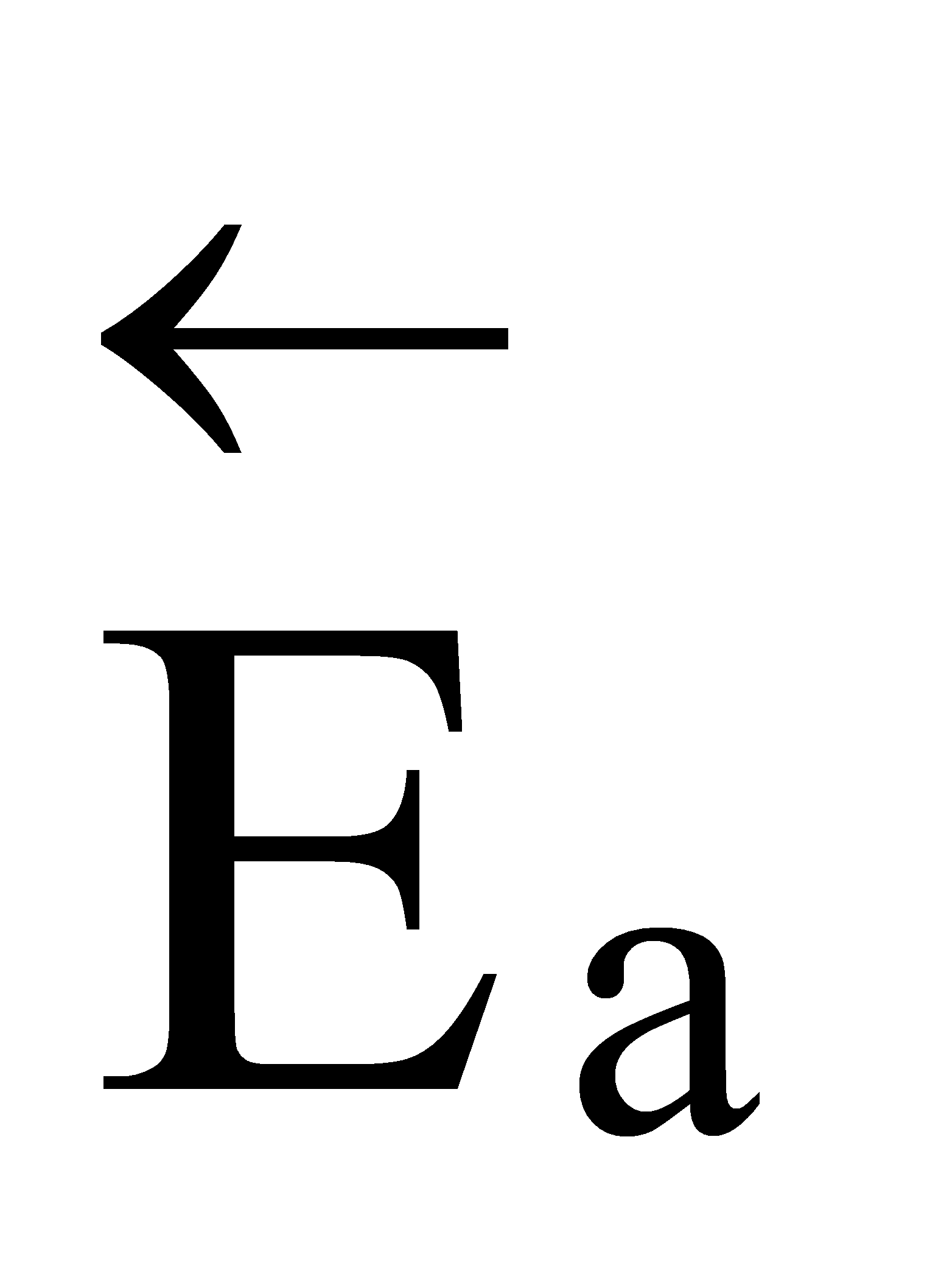
| А+В |
| C+D |
| ∆H |
| путь реакции |
Если реакция взаимодействия А + В будет эндотермической, то получим такую же диаграмму, отличающуюся лишь тем, что энергетический уровень системы А + В ниже, чем уровень энергии системы C + D. Энергия активация прямой реакции будет выше энергии активации обратной реакции 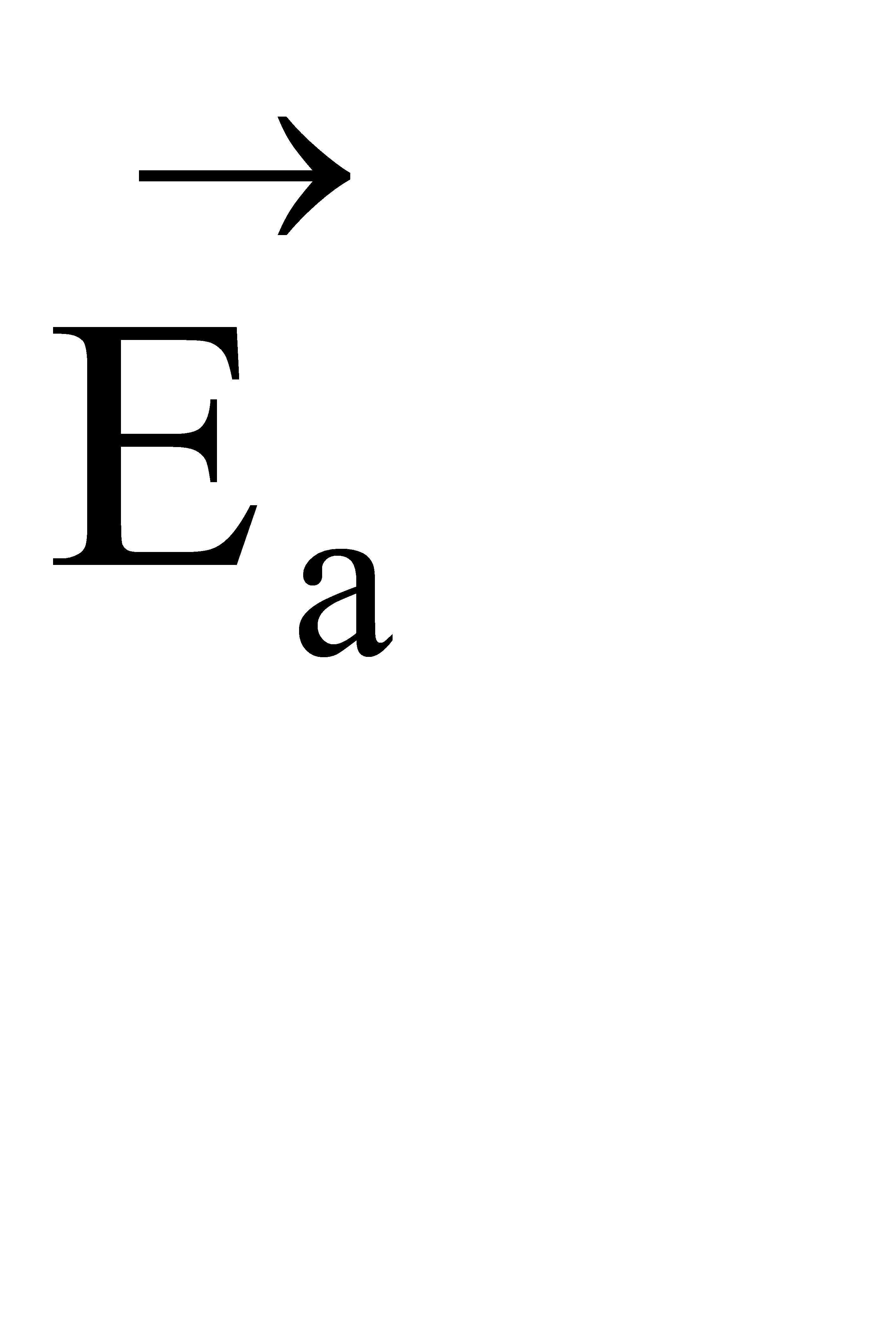 >
> 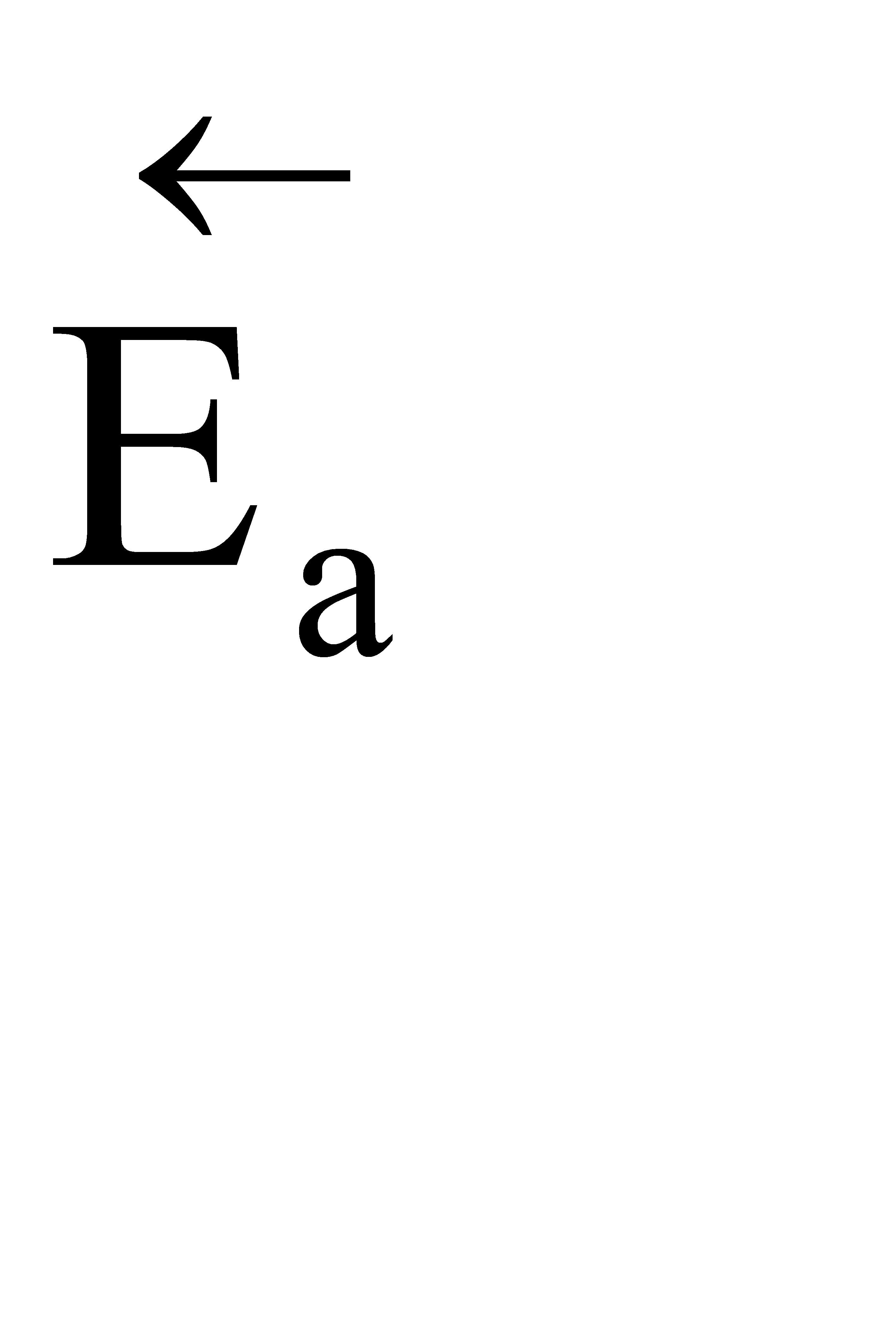 .
.
Таким образом, энергия активации эндотермического процесса всегда больше энергии активации обратного экзотермического процесса на величину теплового эффекта реакции. Следовательно, повышение температуры увеличивает в большей степени скорость эндотермической реакции.
Если реакция образования целевого продукта С происходит с выделением тепла, повышение температуры увеличит в большей степени константу скорости обратной реакции, чем константу скорости прямой реакции; константа равновесия уменьшится, равновесие сместится в сторону образования исходных веществ А и В.
Если ∆Н < 0, при Т↑  ,
, 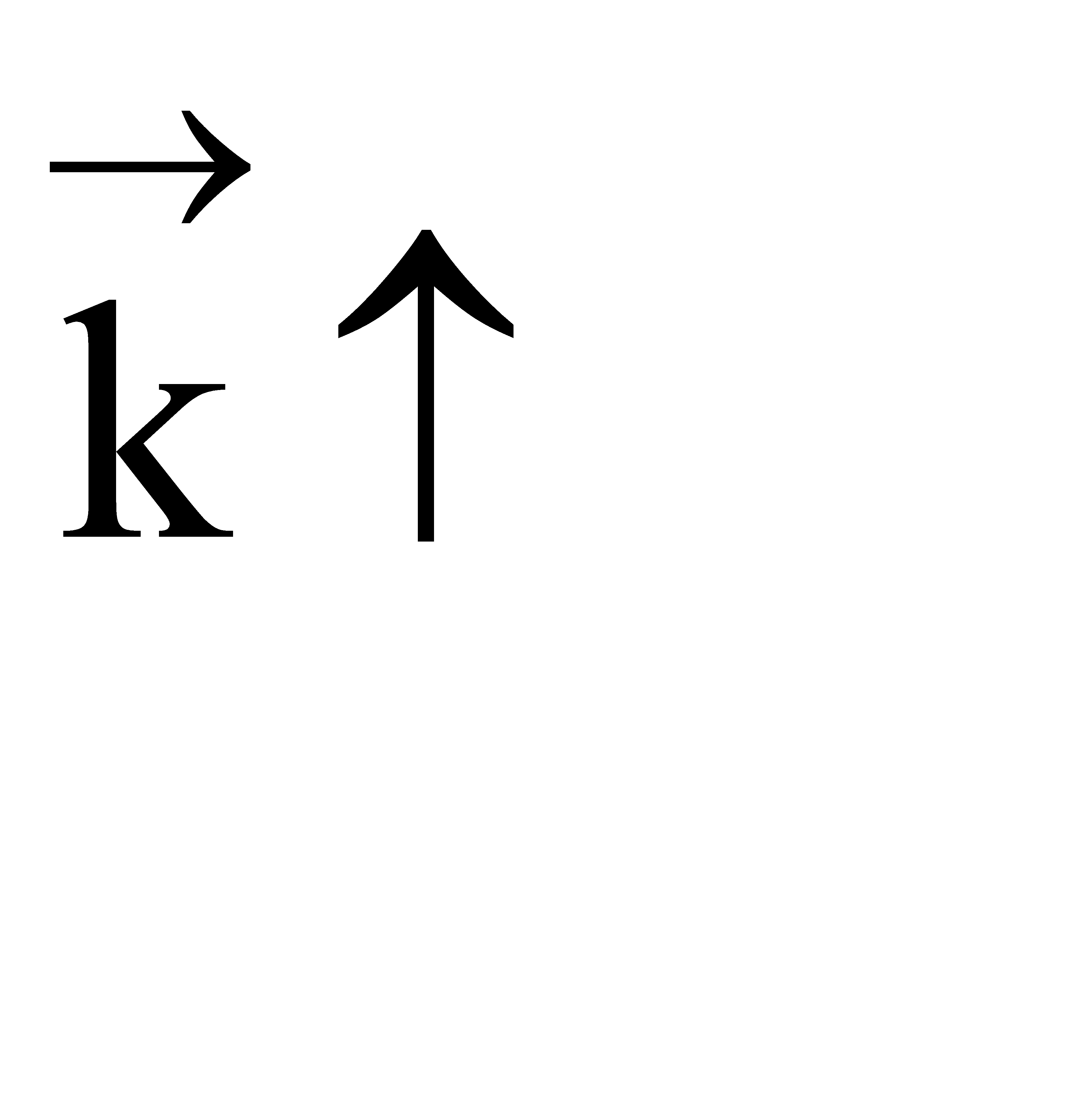
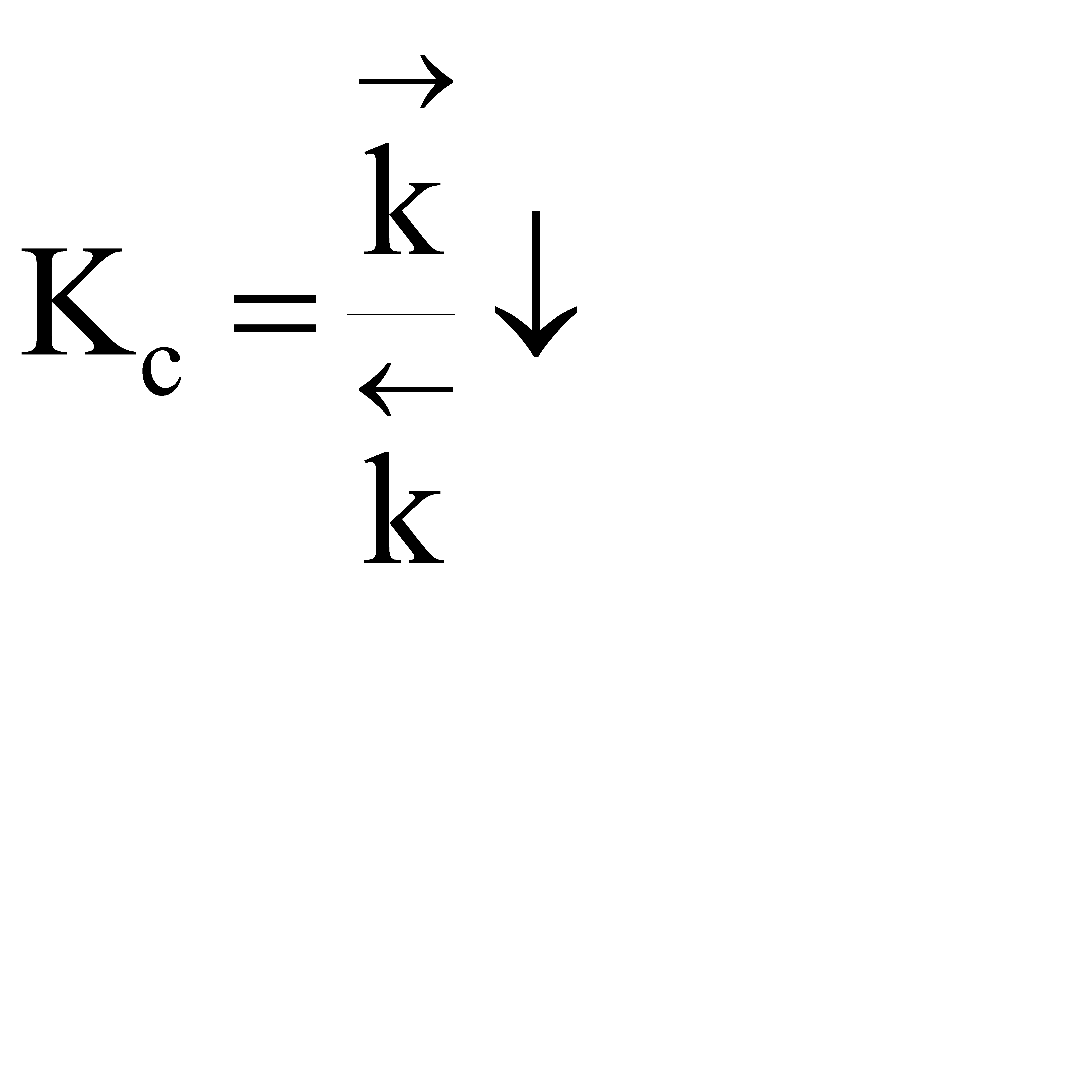
Если прямая реакция эндотермическая, повышение температуры в большей степени увеличит константу прямой реакции; константа равновесия увеличится, равновесие сместится в сторону образования целевого продукта.
Если ∆Н > 0, при Т↑ 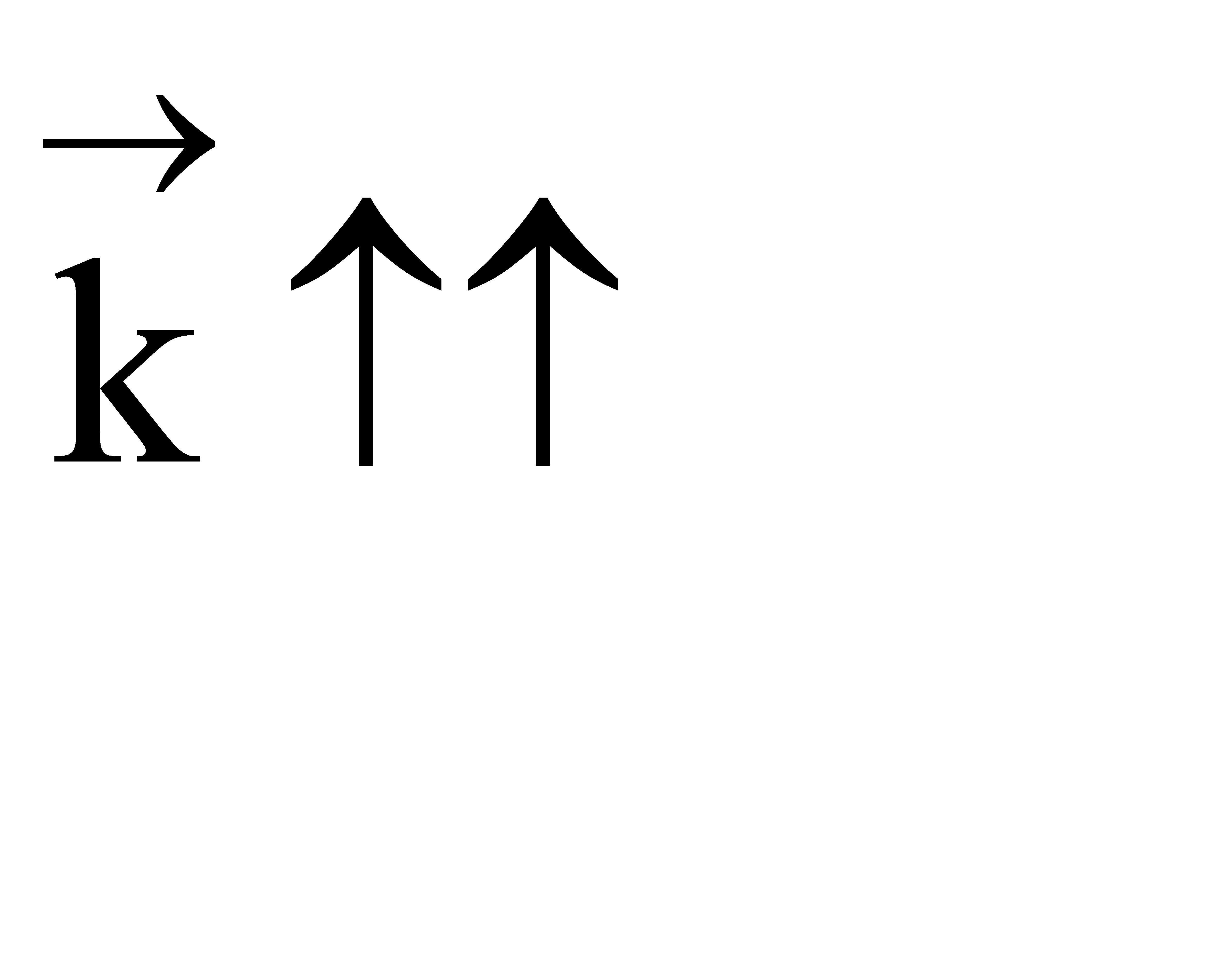 ,
, 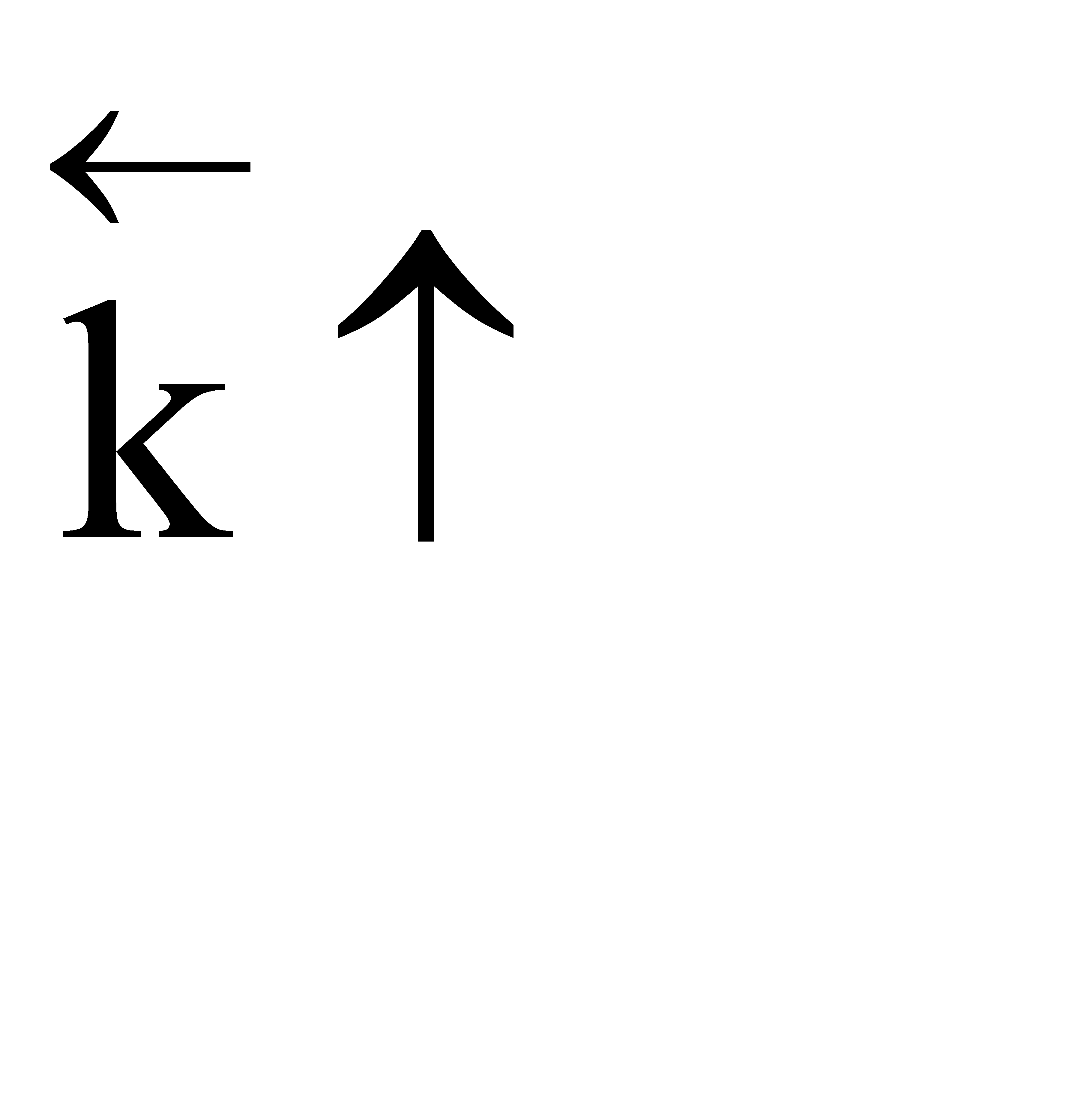 ,
, 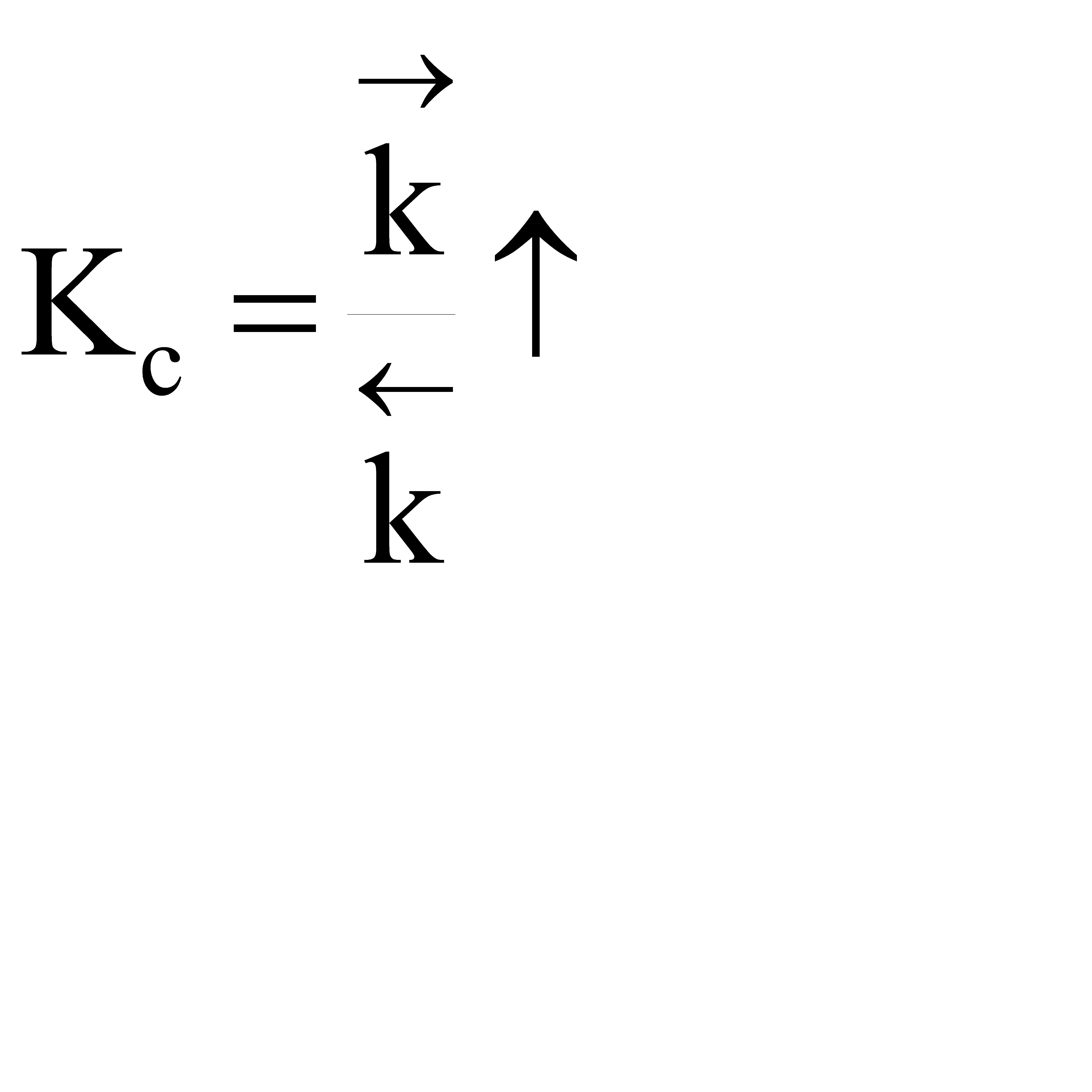 .
.
Смещение равновесия означает изменение величины равновесной конверсии и выхода; в случае простого процесса они синхронно уменьшаются при увеличении температуры в экзотермических процессах и увеличиваются в эндотермических.
y cy9kb3ducmV2LnhtbEyPQUvDQBCF74L/YRnBm93EGjExm1KKeipCW6H0Ns1Ok9Dsbshuk/TfO3rR y4PHG977Jl9MphUD9b5xVkE8i0CQLZ1ubKXga/f+8ALCB7QaW2dJwZU8LIrbmxwz7Ua7oWEbKsEl 1meooA6hy6T0ZU0G/cx1ZDk7ud5gYNtXUvc4crlp5WMUPUuDjeWFGjta1VSetxej4GPEcTmP34b1 +bS6HnbJ534dk1L3d9PyFUSgKfwdww8+o0PBTEd3sdqLVgE/En6VsyRN2R4VzNOnBGSRy//0xTcA AAD//wMAUEsBAi0AFAAGAAgAAAAhALaDOJL+AAAA4QEAABMAAAAAAAAAAAAAAAAAAAAAAFtDb250 ZW50X1R5cGVzXS54bWxQSwECLQAUAAYACAAAACEAOP0h/9YAAACUAQAACwAAAAAAAAAAAAAAAAAv AQAAX3JlbHMvLnJlbHNQSwECLQAUAAYACAAAACEARVxQDBoJAACvRAAADgAAAAAAAAAAAAAAAAAu AgAAZHJzL2Uyb0RvYy54bWxQSwECLQAUAAYACAAAACEAmcmZOt0AAAAFAQAADwAAAAAAAAAAAAAA AAB0CwAAZHJzL2Rvd25yZXYueG1sUEsFBgAAAAAEAAQA8wAAAH4MAAAAAA== ">
| α*, β* |
| Т |
| ∆Н > 0 |
| ∆Н < 0 |
| 100% |
Степень смещения равновесия при изменении температуры зависит от величины теплового эффекта. Чем больше ∆Н, то есть чем больше разница энергий активации прямой и обратной реакции, тем больше смещается равновесие. Если ∆Н ≈ 0, температура почти не влияет на положение равновесия.
Задача управления обратимым процессом заключается в создании условий, при которых равновесие смещено в сторону образования целевого продукта с одновременным обеспечением достаточно высокой скорости достижения равновесия.
Пусть протекает простая необратимая реакция типа 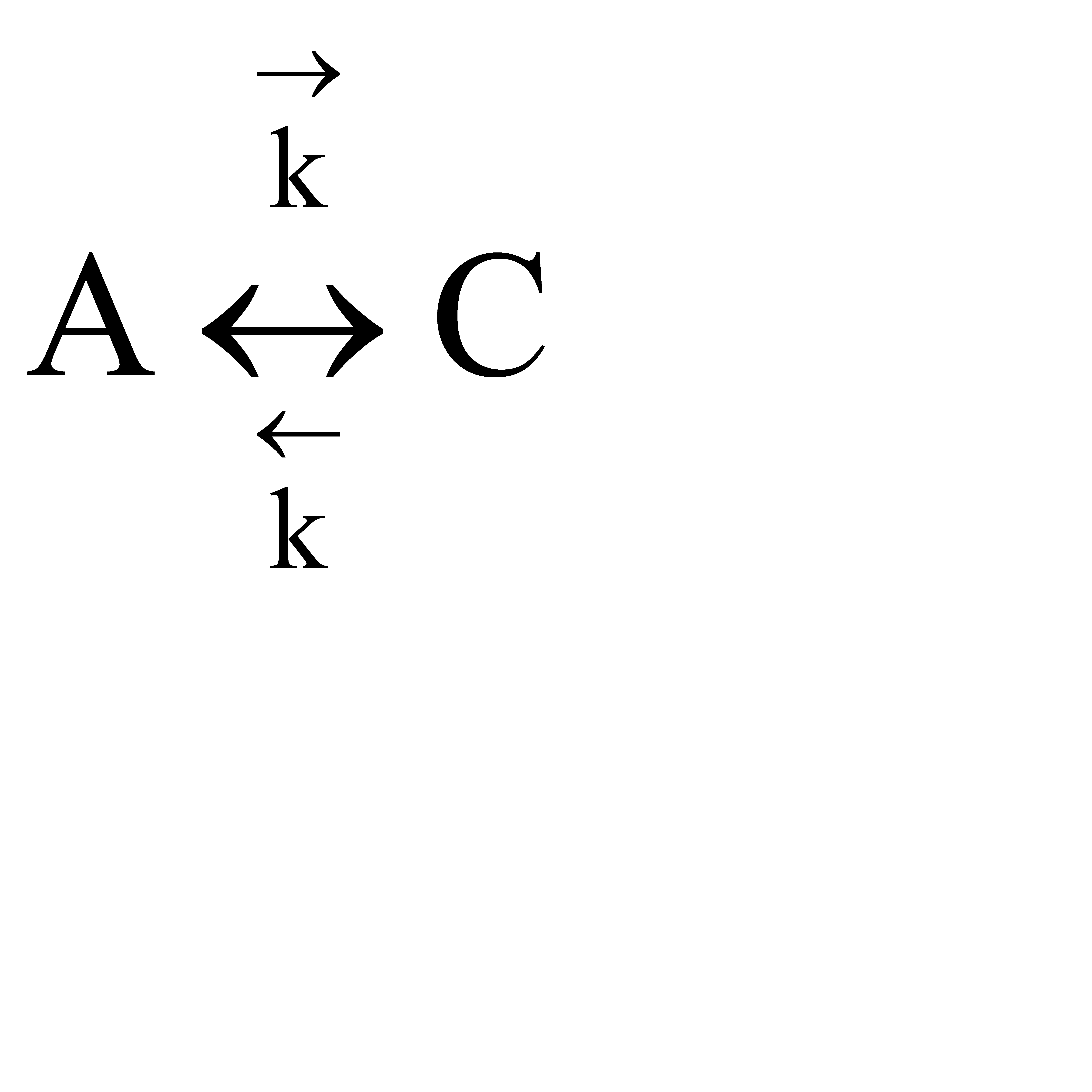 .
.
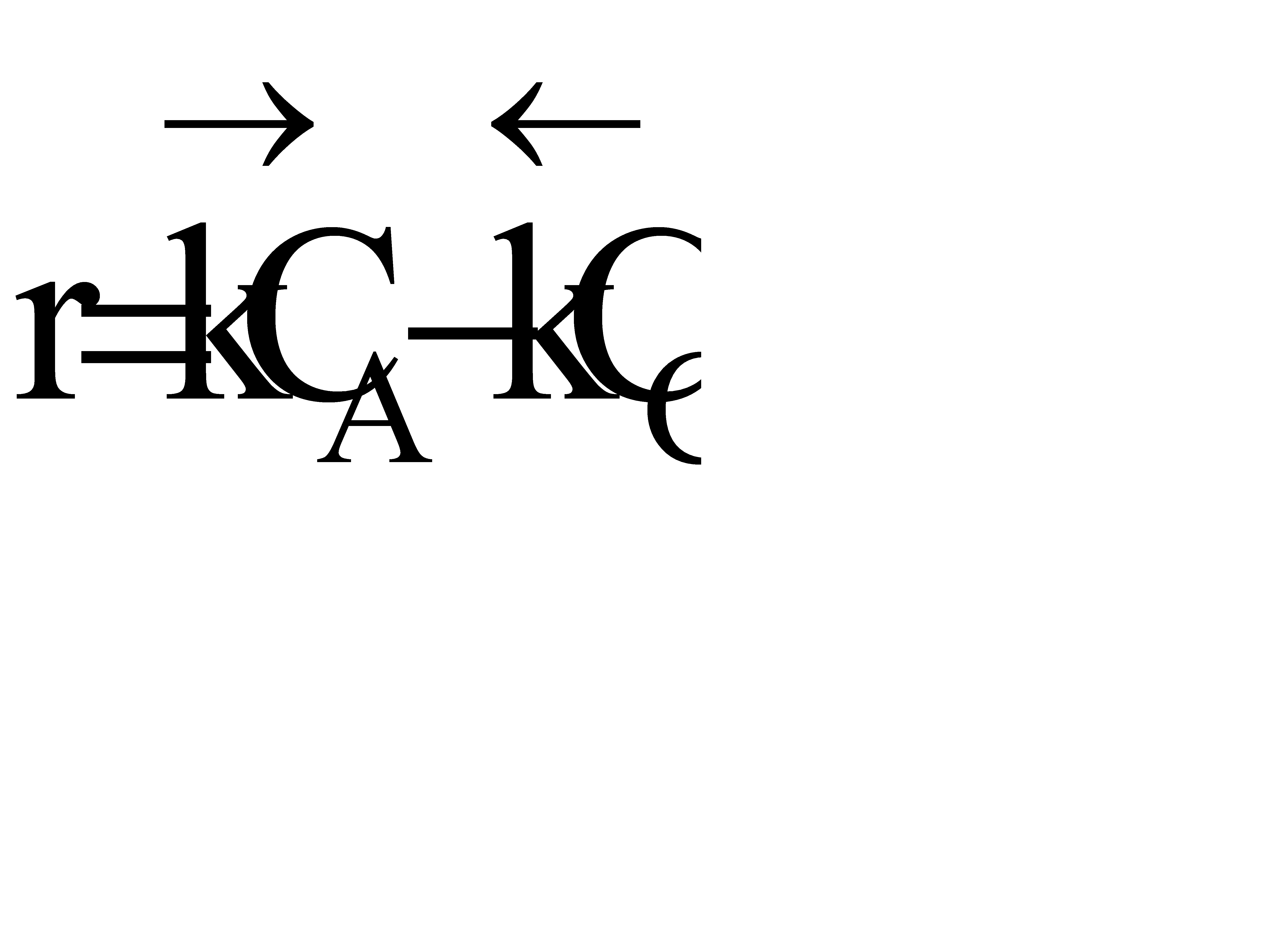
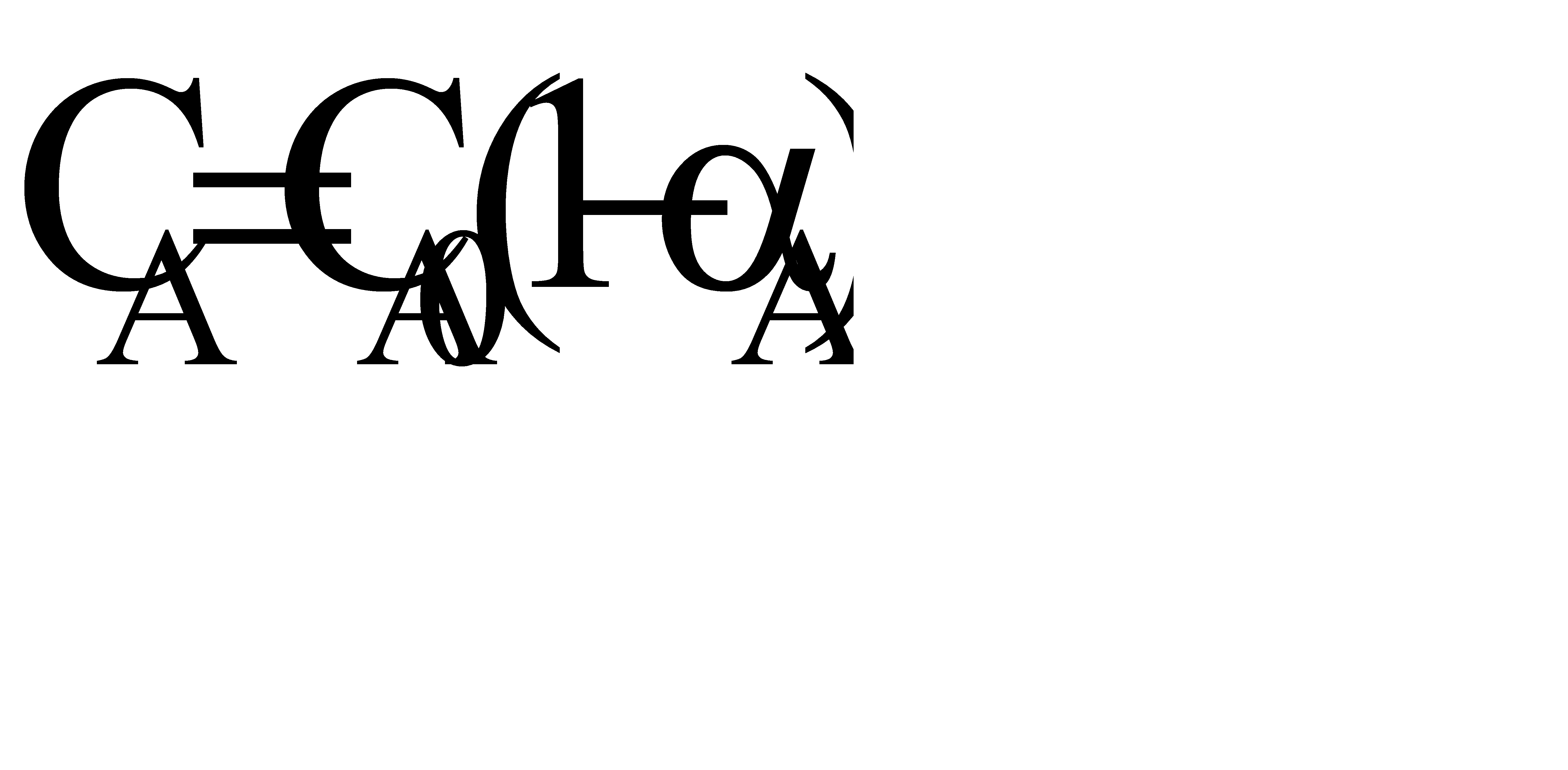
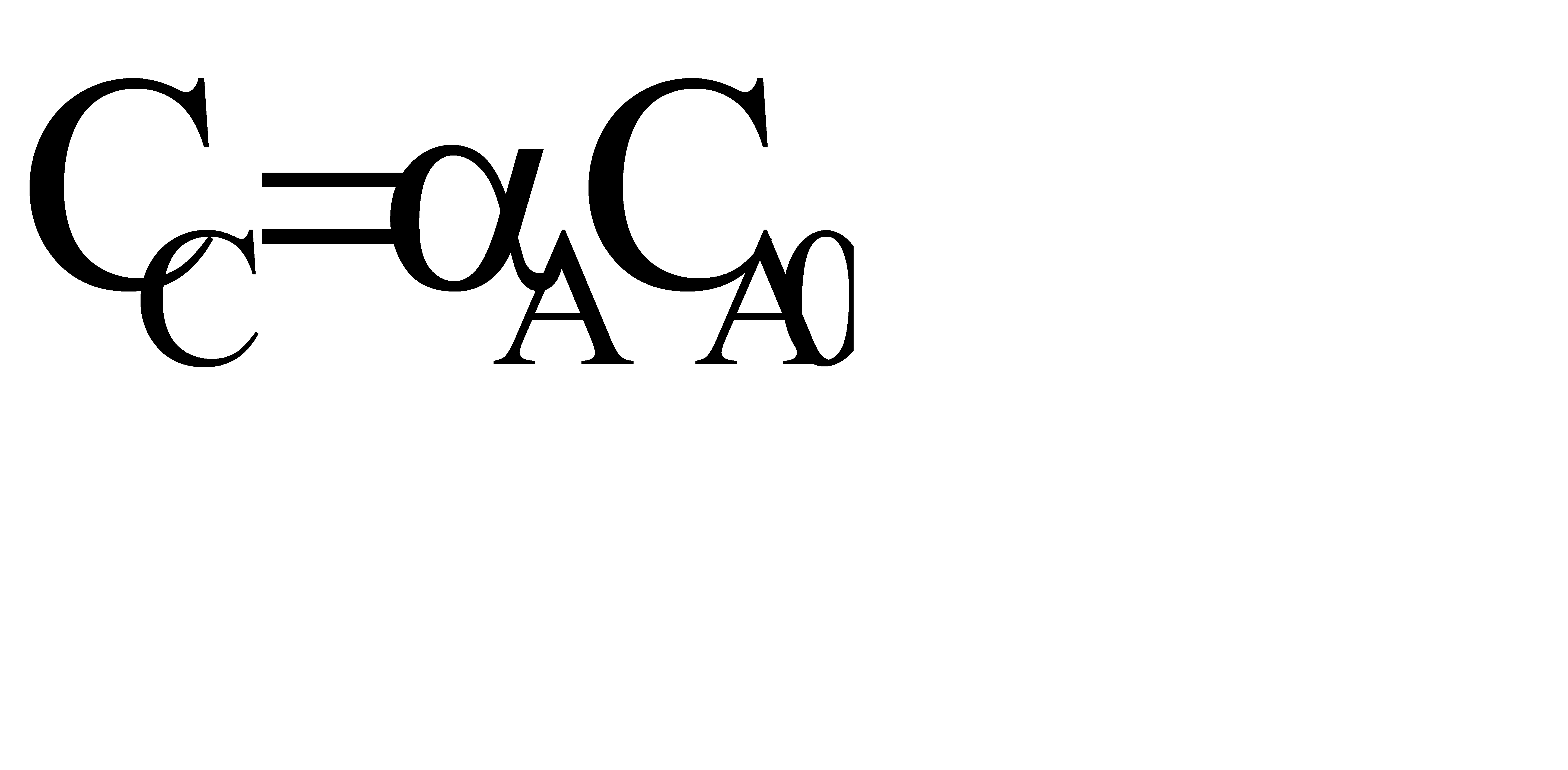
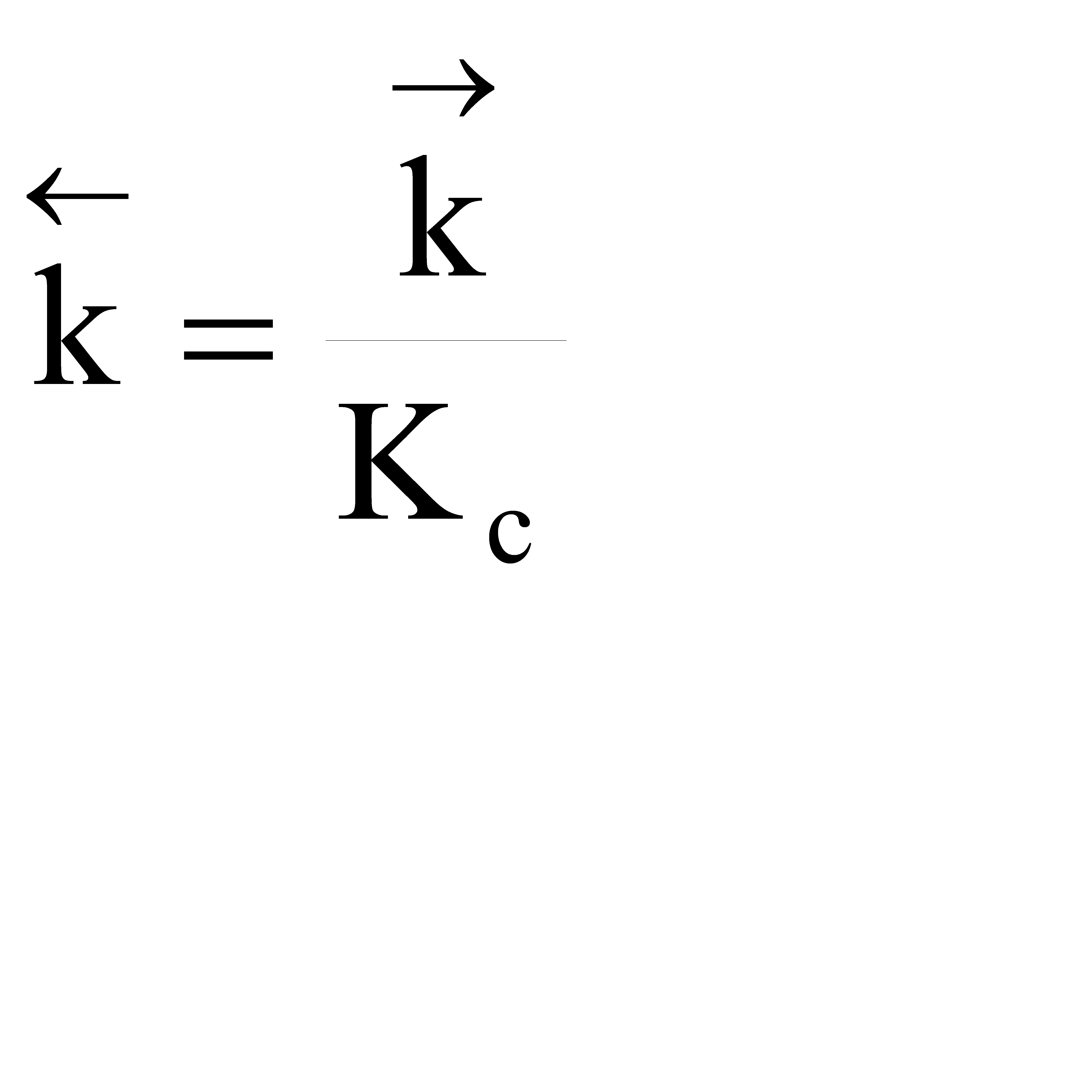
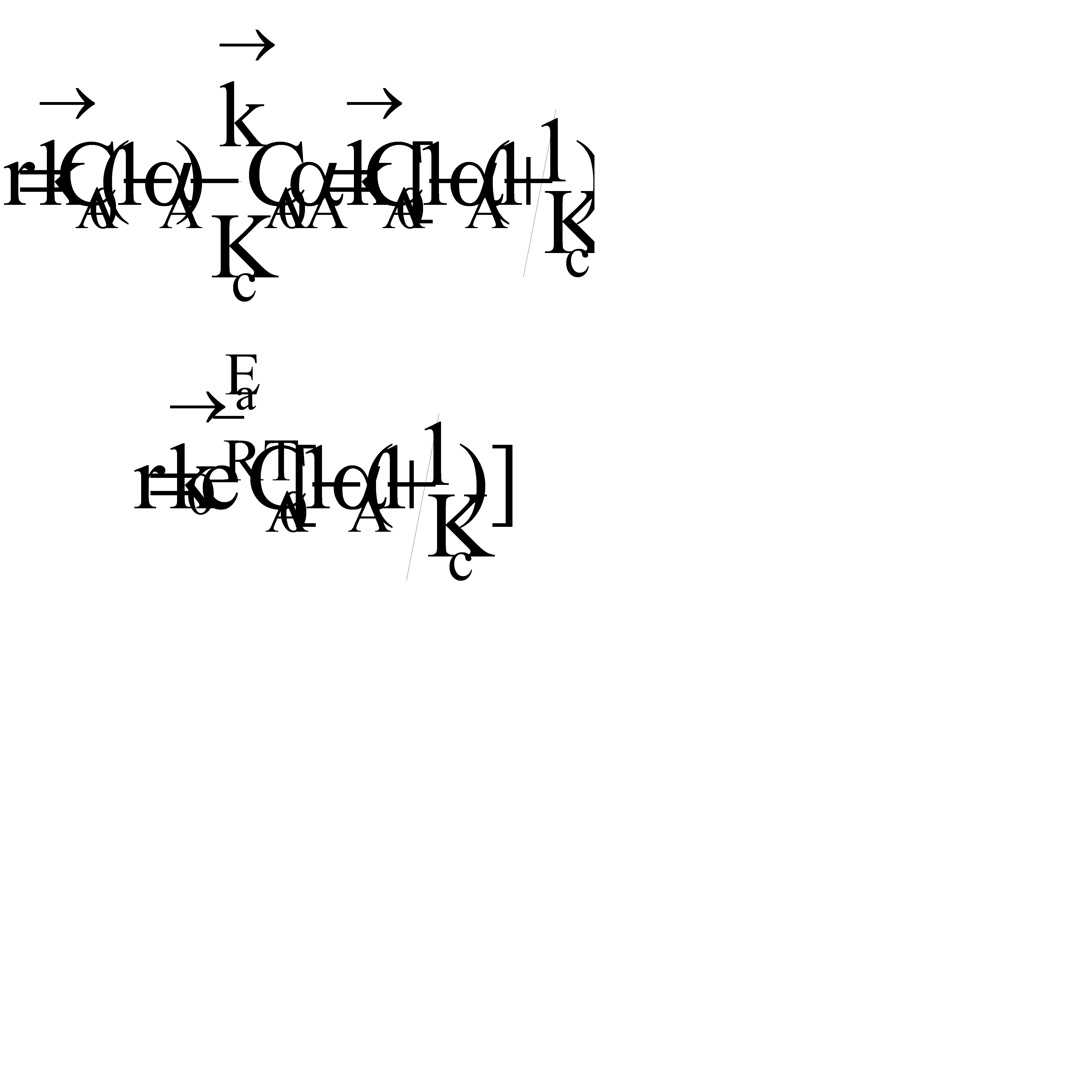
Из уравнения видно, что для некоторой постоянной конверсии αА скорость процесса при повышении температуры должна возрастать за счет увеличения члена 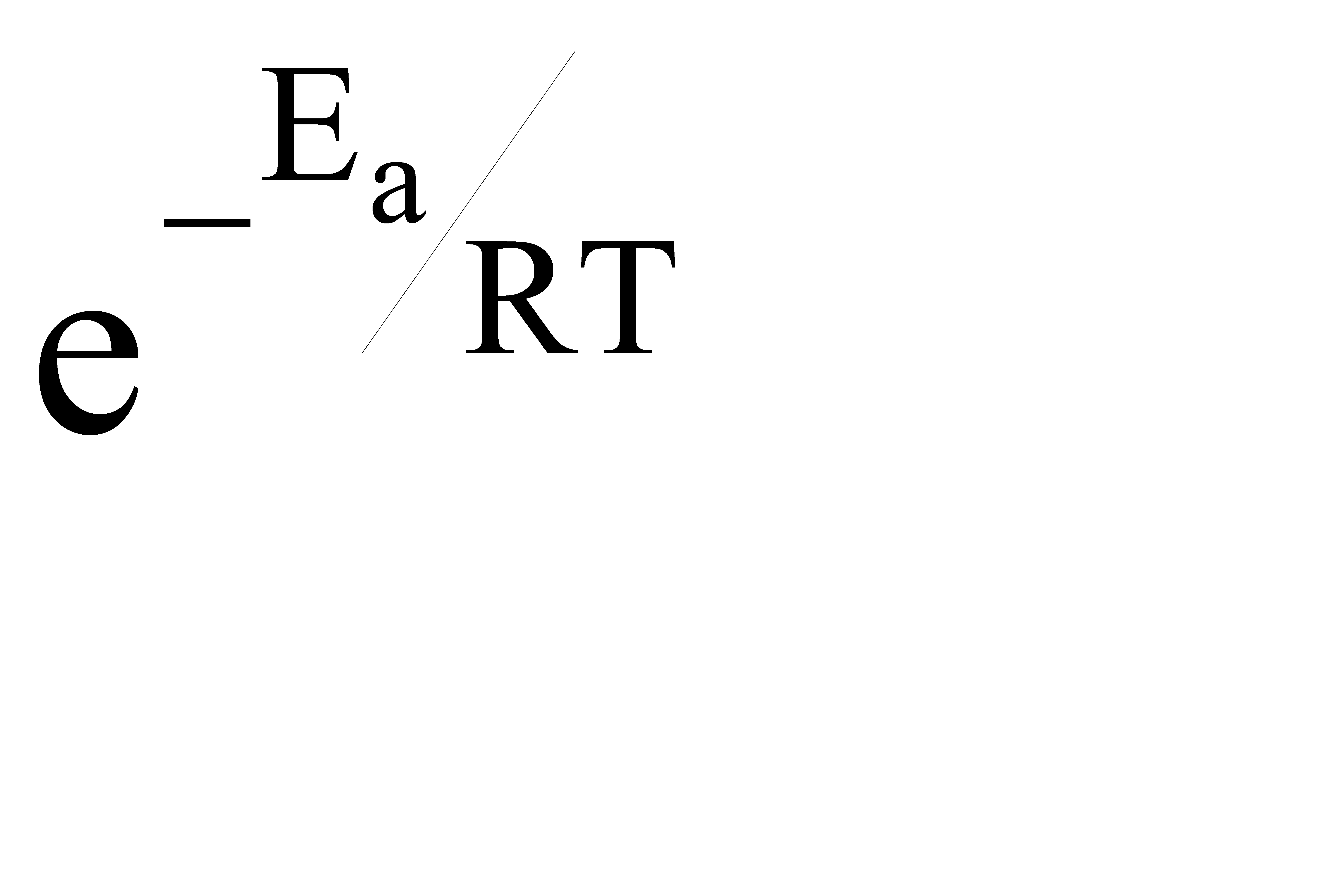 , а с другой стороны, может уменьшаться, если уменьшается константа равновесия Кс, или увеличиваться, если Кс увеличивается.
, а с другой стороны, может уменьшаться, если уменьшается константа равновесия Кс, или увеличиваться, если Кс увеличивается.
При Т↑ 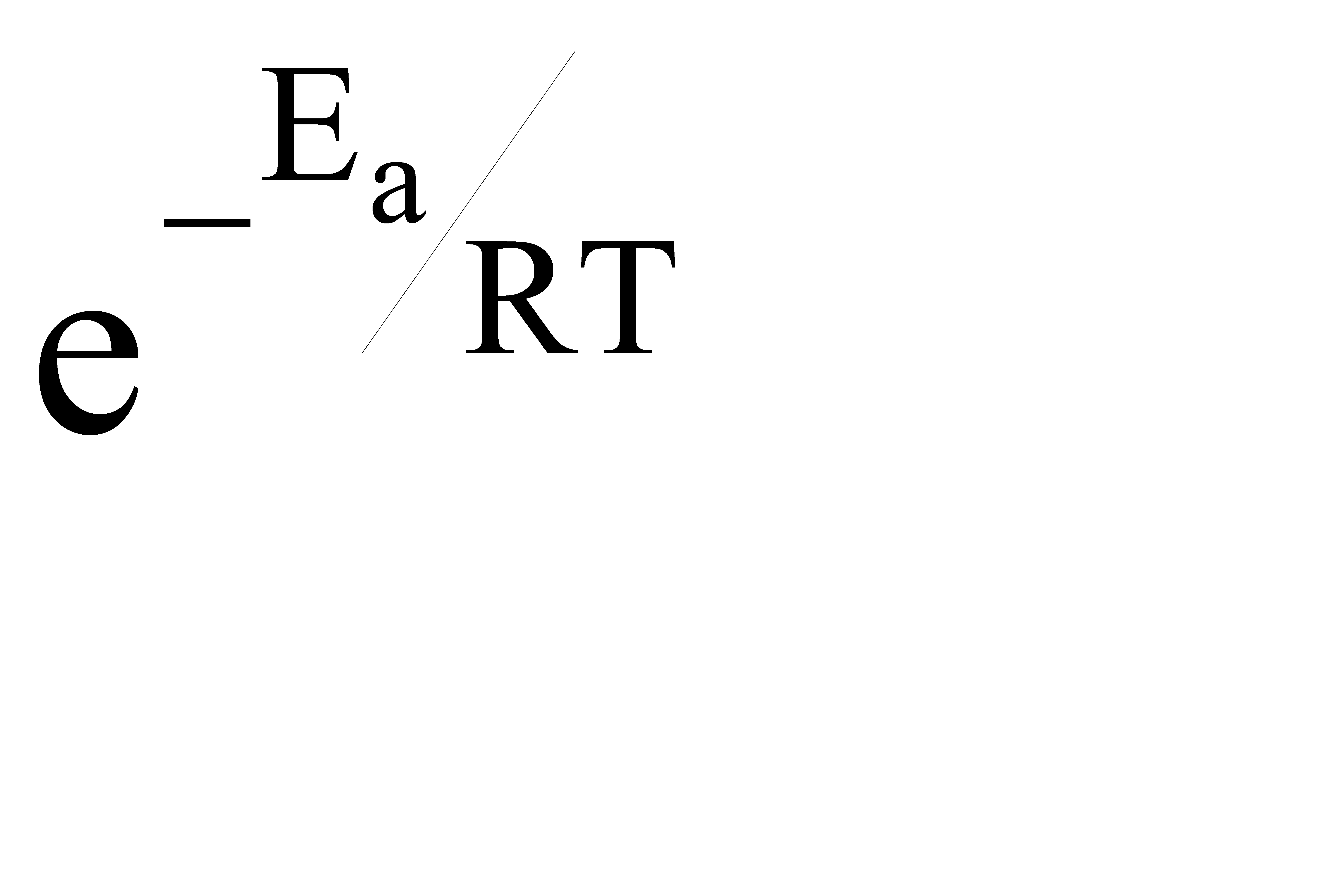 ↑ r↑;
↑ r↑;
если Кс ↓ r↓, если Кс ↑ r↑
Первый случай реализуется в экзотермических реакциях. В обратимых экзотермических реакциях при повышении температуры скорость сначала возрастает за счет увеличения 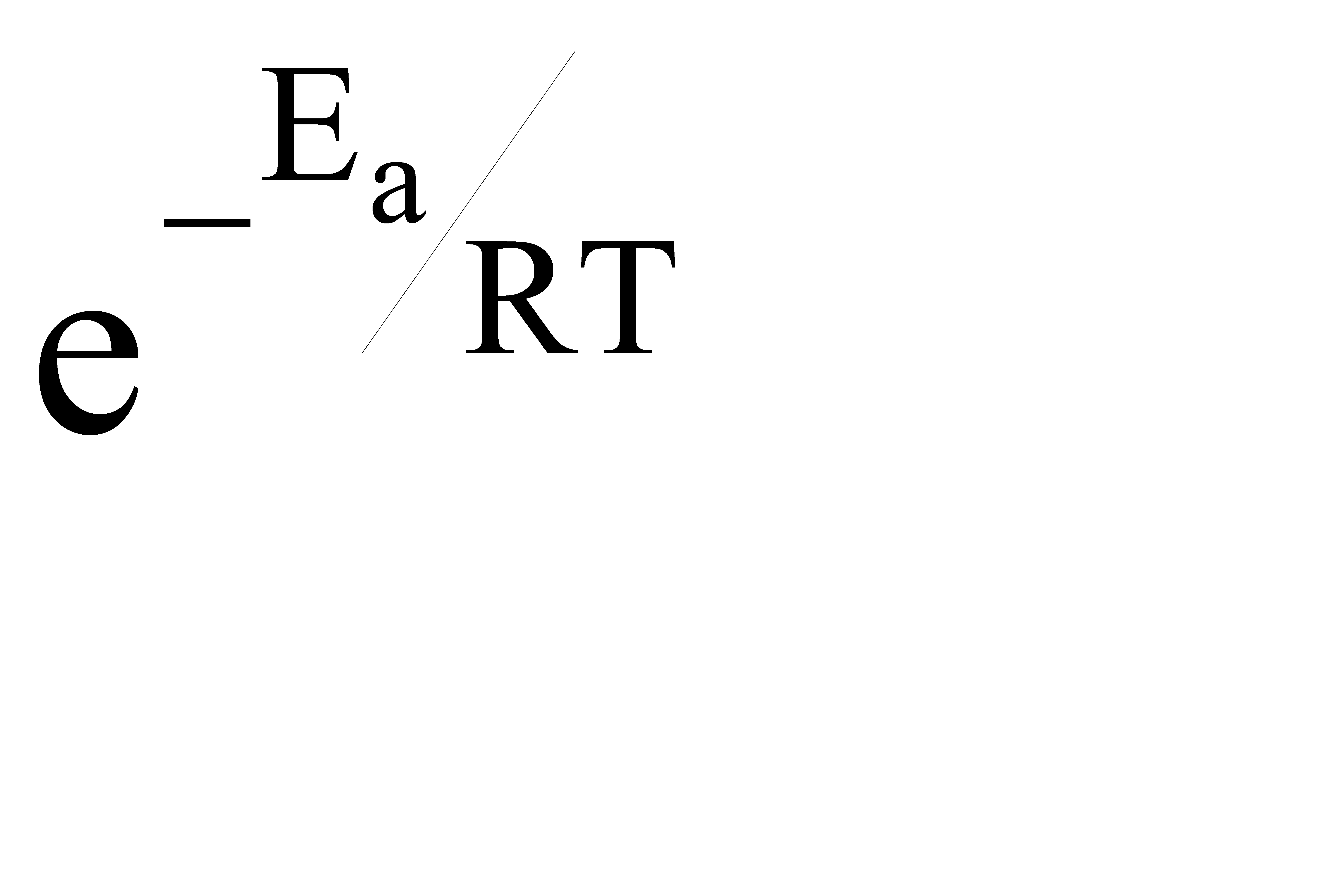 , достигает некоторого максимального значения, а затем начинает уменьшаться за счет уменьшения константы равновесия.
, достигает некоторого максимального значения, а затем начинает уменьшаться за счет уменьшения константы равновесия.
| r |
| T |
| αA=const |
| Tопт. |
| ∆Н < 0 |
В области низких температур при повышении температуры скорость процесса увеличивается за счет увеличения скорости прямой экзотермической реакции; обратная эндотермическая реакция при этих температурах еще практически не протекает. При переходе к более высоким температурам начинает протекать обратная реакция, ее скорость в большей степени возрастает под воздействием температуры, чем скорость экзотермической реакции. В результате суммарная скорость процесса начинает уменьшаться. Температура, при которой достигается максимальная скорость, называется оптимальной.
Из уравнения также видно, что при увеличении конверсии αА скорость процесса уменьшается.
| Tопт.1 |
| Tопт.2 |
| ЛОТ |
| α1 |
| α2 |
| α3 |
| α1< α2 <α3 |
| r |
| Tопт.3 |
| ∆Н < 0 |
| T |
Если α2 > α1, кривая зависимости r =f (T) располагается ниже кривой, соответствующей α1. Если α3 > α2, то соответствующая кривая располагается еще ниже и т.д. Это связано с тем, что для того, чтобы достичь более высоких значений конверсии, требуется больше времени (максимальная конверсия достигается в момент наступления равновесия). Но по мере приближения к равновесию скорость процесса падает и в момент равновесия она равна нулю. Для каждой величины конверсии получается своя кривая зависимости r =f (T), причем, чем выше конверсия, тем ниже расположена эта кривая и тем меньше оптимальная температура. Линия, соединяющая максимумы полученных таким образом кривых, является линией оптимальных температур (ЛОТ). Эта линия показывает, как нужно изменять температуру в ходе процесса для того, чтобы увеличить степень превращения реагентов, работая все время при максимально возможных в этих условиях скоростях процесса.
В простых обратимых эндотермических процессах скорость процесса при повышении температуры возрастает и за счет увеличения члена 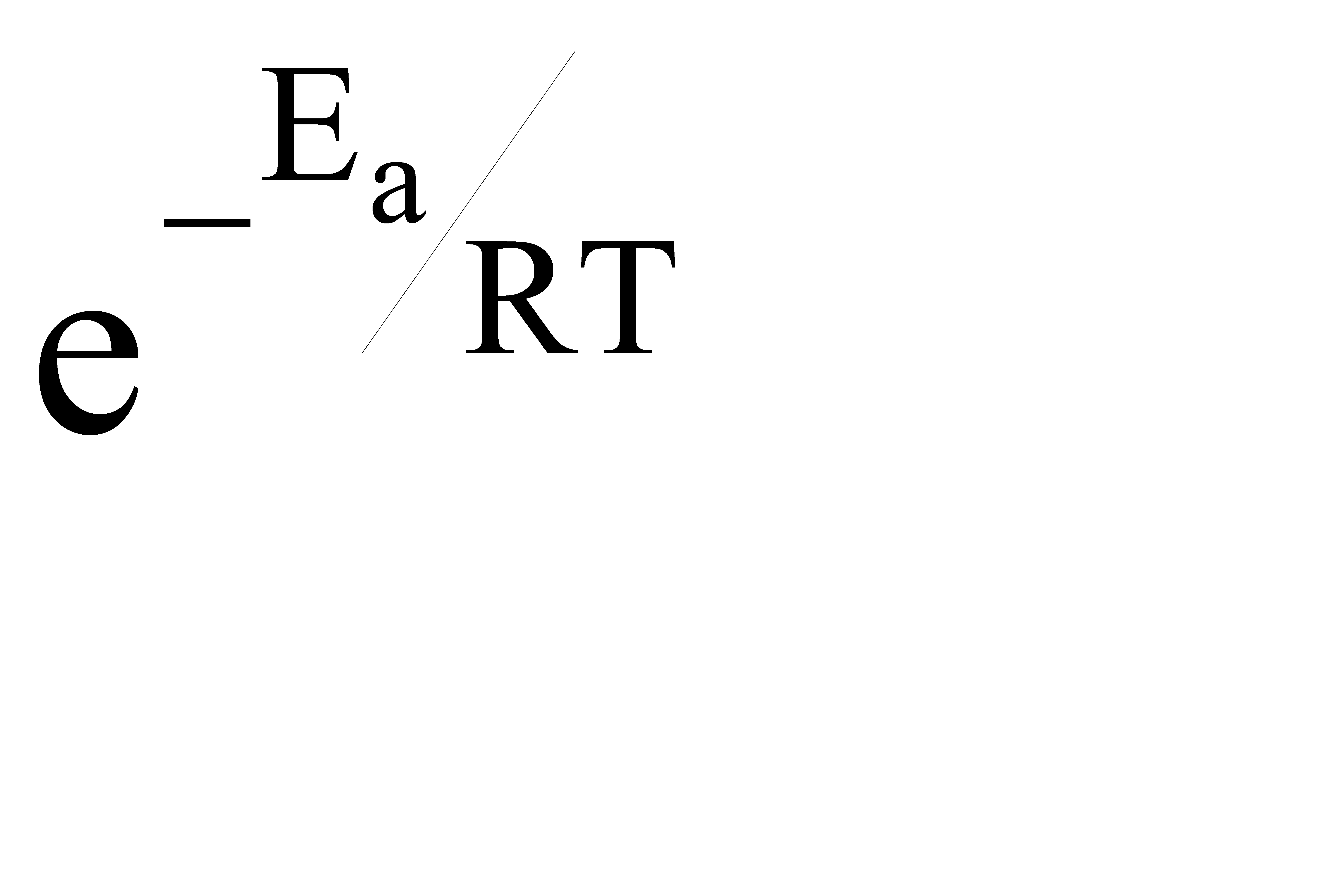 , и за счет увеличения Кс. При увеличении конверсии (при прочих равных условиях) скорость процесса уменьшается.
, и за счет увеличения Кс. При увеличении конверсии (при прочих равных условиях) скорость процесса уменьшается.
| α1 |
| α2 |
| α3 |
| α1< α2 <α3 |
| r |
| ∆Н > 0 |
| T |
Установим зависимость конверсии от температуры α = f (T) для тех же реакций.
Для обратимого экзотермического процесса зависимость α = f (T) при τ = const сначала увеличивается, достигая максимального значения, а затем снижается. Снижение αА связано с достижением равновесной конверсии, которая при повышении температуры в экзотермическом процессе уменьшается за счет смещения равновесия.
| α |
| α* |
| Топт. |
| α = 100% |
| Т |
| ∆Н < 0 |
| τ = const |
Кривая, соответствующая τ2 > τ1, располагается выше, чем τ3 > τ2 – еще выше и т.д. Кривая, соединяющая максимумы, является линией оптимальных температур (ЛОТ).
| α |
| α* |
| Т |
| α = 100% |
| τ2 |
| τ1 |
| τ3 |
| ЛОТ |
| ∆Н < 0 |
| τ1 < τ2 < τ3 |
Таким образом, для обратимого экзотермического процесса не существует единой оптимальной температуры. В начале процесса нужно задавать более высокую температуру для поддержания высокой скорости процесса, а затем температуру следует снижать по ЛОТ, чтобы при достижении более высоких значений конверсии поддерживать максимально возможную скорость процесса.
Для простого обратимого эндотермического процесса вопрос о влиянии температуры решается однозначно: при повышении температуры увеличивается и равновесная и фактическая степень превращения. Однако, и в этом случае есть некоторая оптимальная температура, выше которой процесс вести нерационально, поскольку конверсия увеличивается незначительно.
| Т |
| τ2 |
| τ1 |
| τ3 |
| α* |
| α = 100% |
| ∆Н > 0 |
| τ1 < τ2 < τ3 |
| α |
Для всех кривых зависимости α = f(Т) характер изменения конверсии при невысоких температурах одинаков, поскольку в этих условиях влияние термодинамических факторов (т.е. обратной реакции) незначительно. С повышением температуры влияние термодинамических факторов увеличивается. Степень этого влияния зависит от типа реакции. Для необратимых реакций кривые зависимости α = f(Т) асимптотически приближаются к единице. Для обратимых реакций они ограничиваются кривой равновесной степени превращения, которая для экзотермических процессов с повышением температуры уменьшается, а для эндотермических процессов возрастает.
2) Влияние концентрации участников реакции
Суммарная скорость обратимого процесса равна
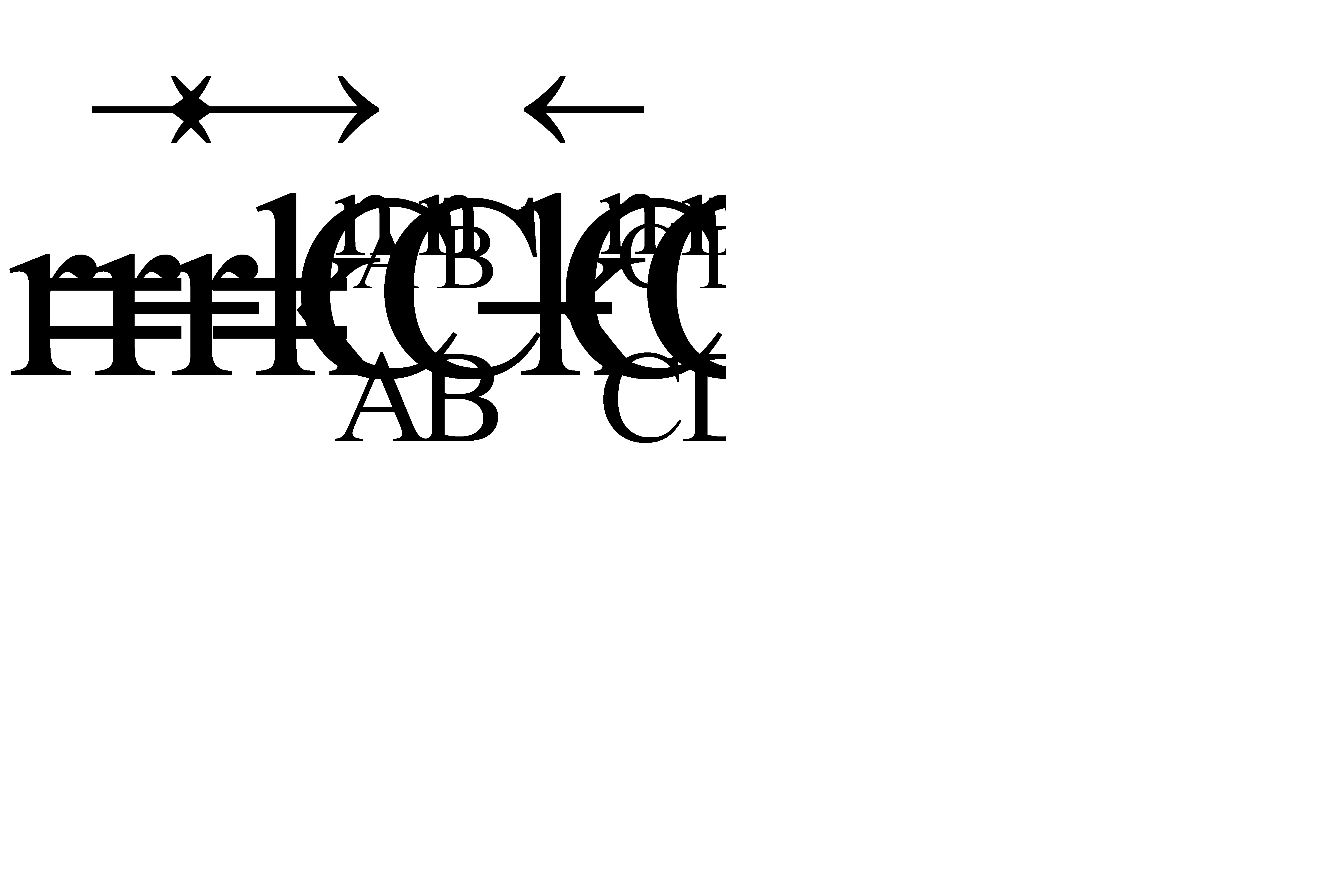
При увеличении начальной концентрации исходных реагентов А и В увеличиваются их текущие концентрации, а, следовательно, скорость прямой реакции и скорость всего процесса в целом (химическое равновесие устанавливается быстрее).
Константа равновесия 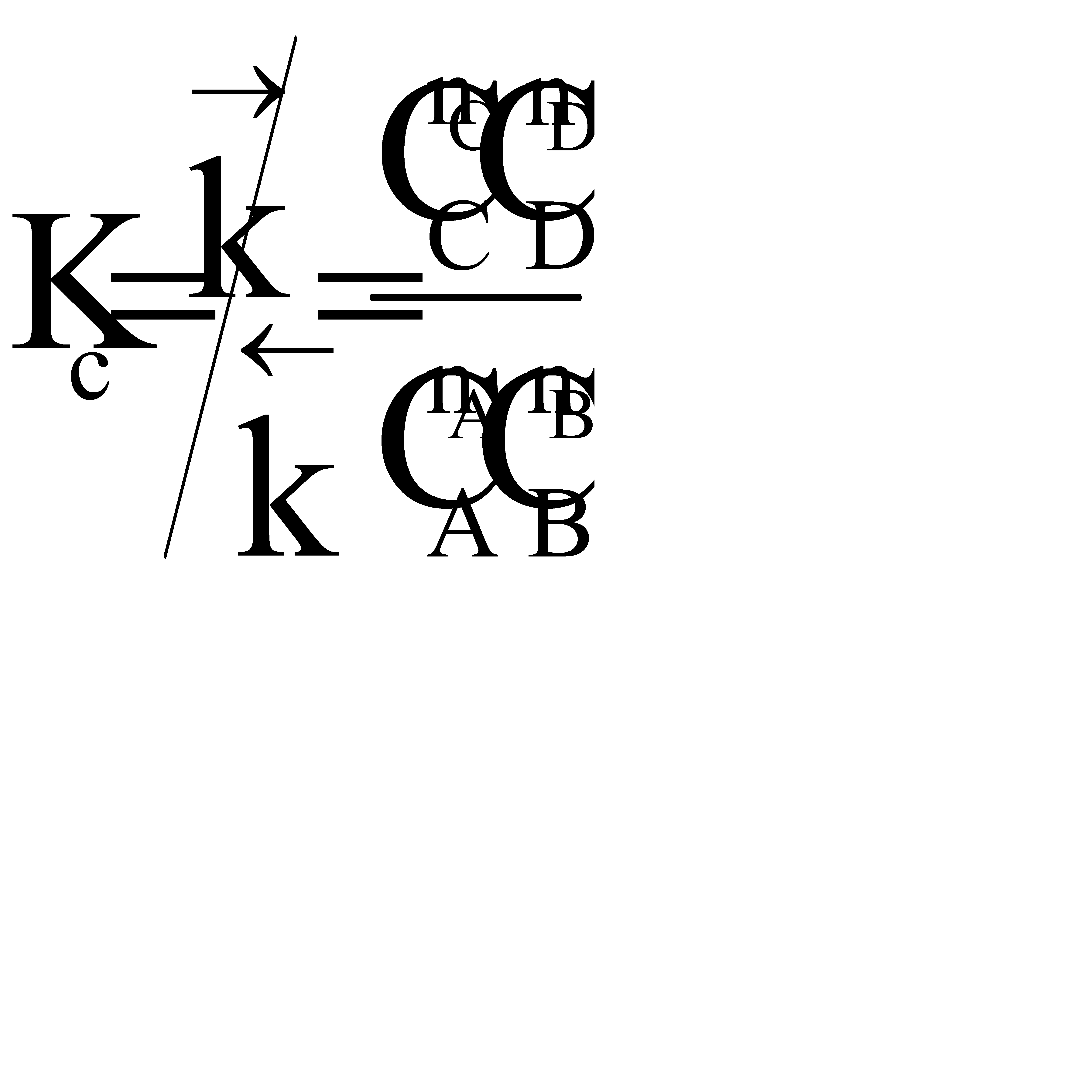 при этом не меняется: во сколько раз увеличивается произведение равновесных концентраций реагентов, во столько раз увеличивается и произведение равновесных концентраций продуктов. Однако равновесный состав смеси будет другой.
при этом не меняется: во сколько раз увеличивается произведение равновесных концентраций реагентов, во столько раз увеличивается и произведение равновесных концентраций продуктов. Однако равновесный состав смеси будет другой.
При увеличении концентрации одного из реагентов увеличивается равновесная конверсия другого реагента, выход целевого продукта увеличивается.
Таким образом, в случае обратимого процесса также целесообразно работать с высококонцентрированным сырьем и можно использовать избыток одного из реагентов. Это позволяет не только поддерживать высокую скорость процесса в течение необходимого времени, но и сдвигает равновесие в сторону образования целевого продукта.
Равновесие обратимого процесса можно сместить вправо также уменьшая концентрацию продуктов С и D , выводя их из реакционной зоны. Константа равновесия Кс при этом также не изменяется: во сколько раз уменьшается произведение концентраций продуктов, во столько же раз уменьшается и равновесная концентрация исходных реагентов. При заданных значениях начальных концентраций реагентов это означает увеличение степени переработки сырья.
Уменьшение концентрации продуктов в реакционной смеси приводит к уменьшению скорости обратной реакции и к увеличению суммарной скорости процесса.
Способы удаления продуктов из зоны реакции могут быть разные. Продукт либо химически связывают вводимым извне веществом, например,
СО + Н2О ↔ Н2 + СО2 СО2 + СаО → СаСО3↓,
либо переводят в другое фазовое состояние (конденсируют или кристаллизуют при охлаждении, испаряют или возгоняют при нагревании и т.д.). В последнем случае, как правило, используют циркуляционную схему процесса.
3) Влияние давления
Скорость обратимого газофазного процесса

зависит от давления, причем тем больше, чем больше отличаются порядки прямой и обратной реакции.
Если реакция протекает без изменения числа молей, скорость обратимого процесса не зависит от давления. Если число молей в результате реакции уменьшается, увеличение давления приводит к увеличению скорости процесса. В противном случае повышение давления вызывает уменьшение скорости установления химического равновесия.
при р↑ r = const, если 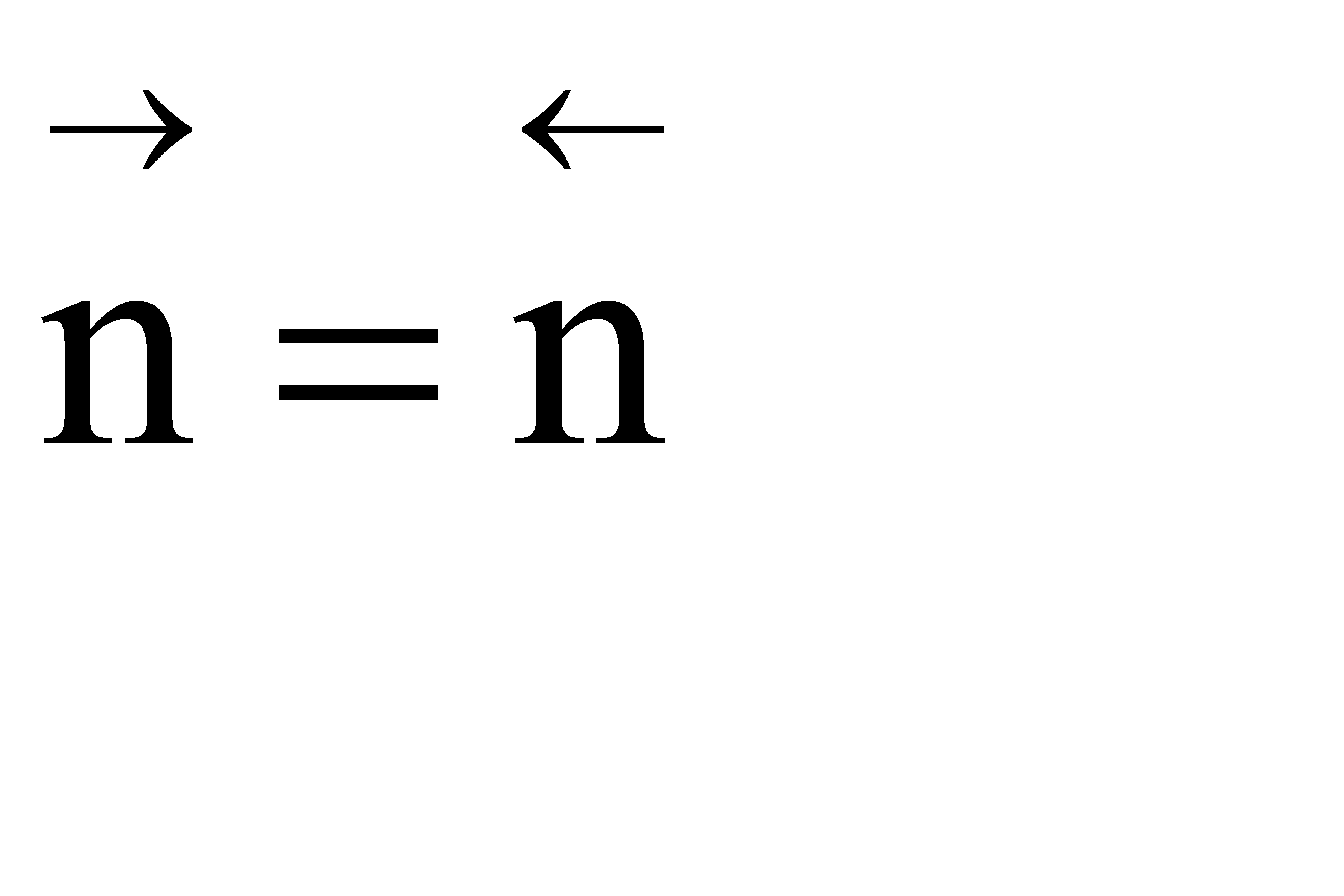 ;
;
r↑, если 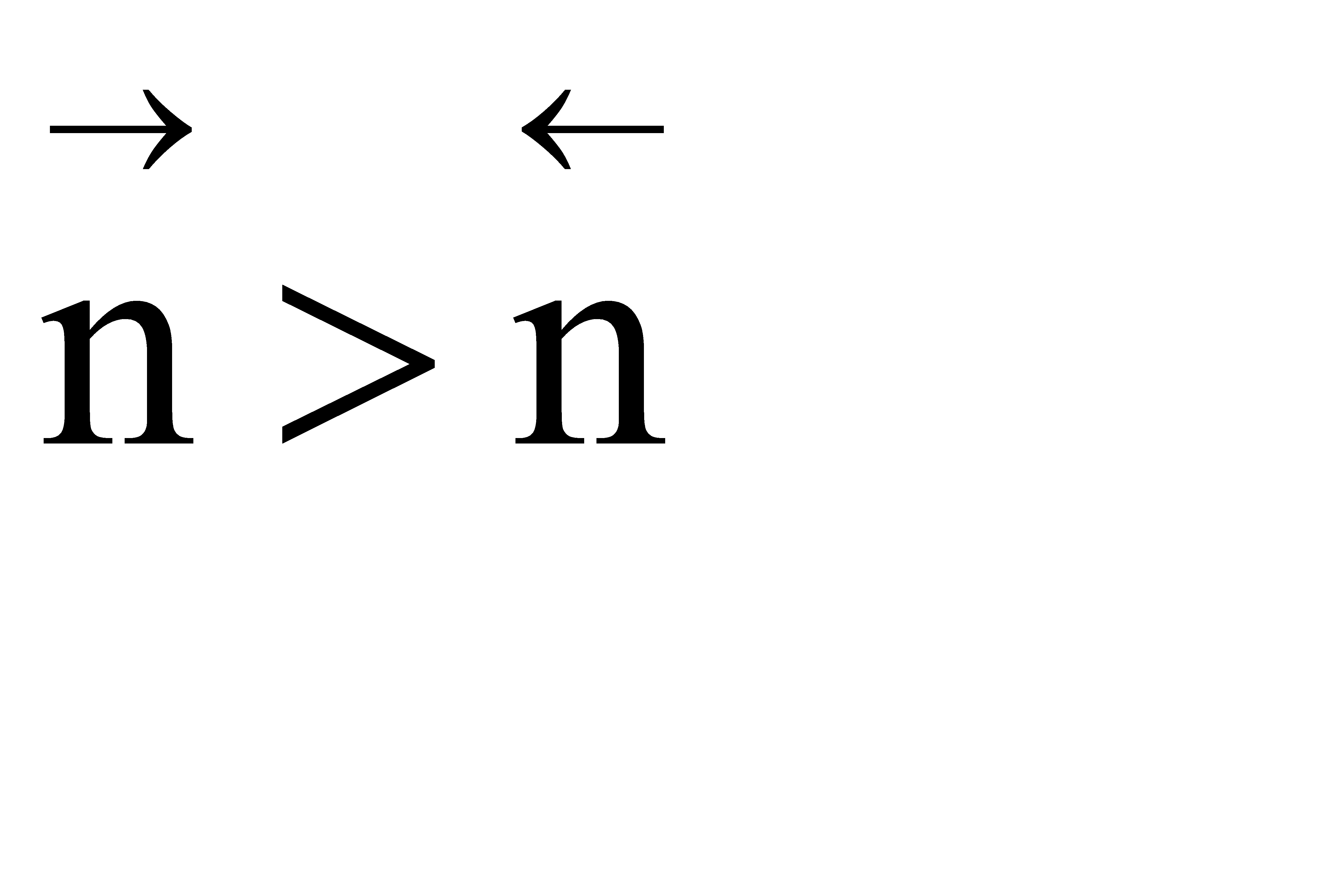
r↓, если 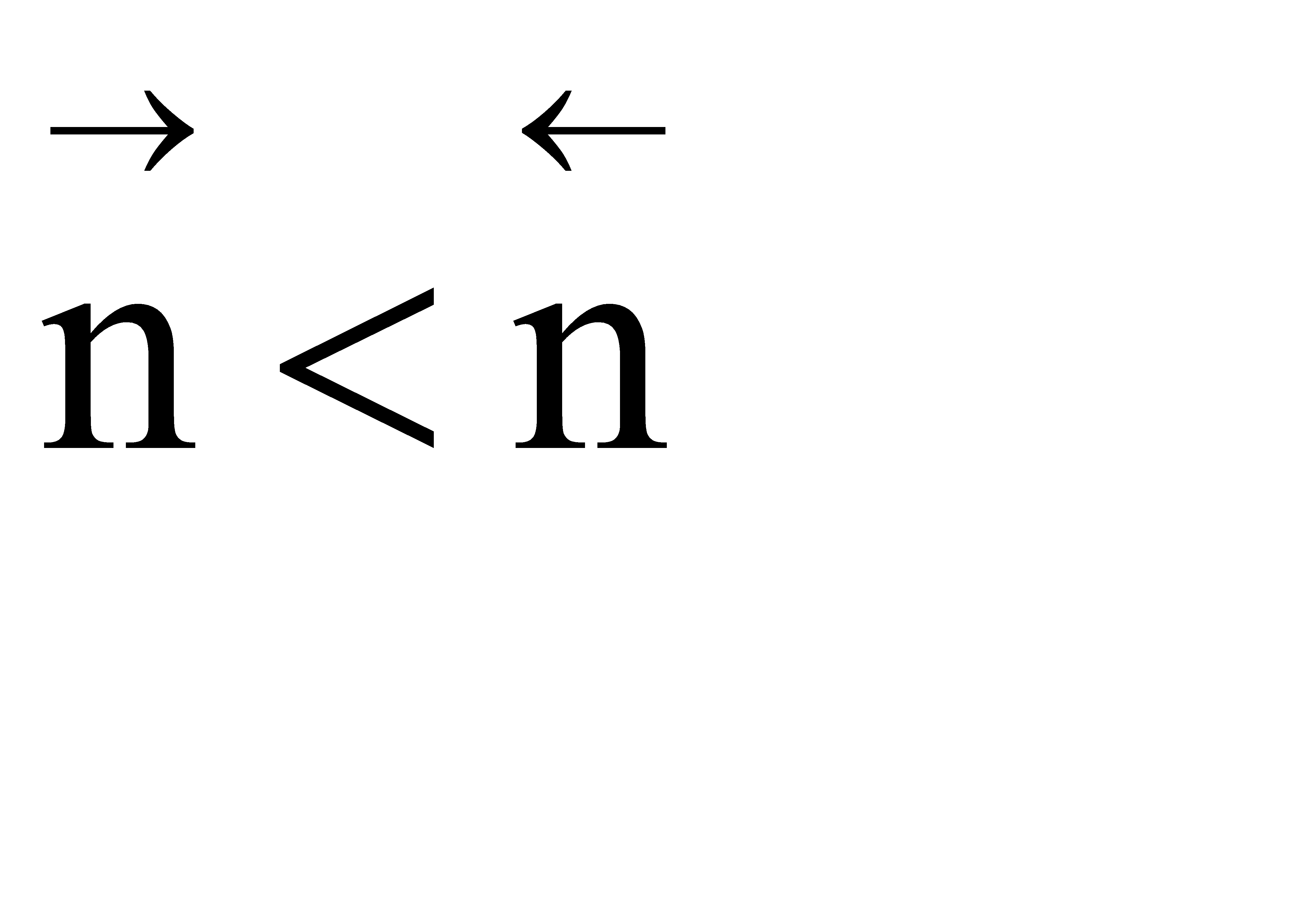
Давление также влияет на положение равновесия. Для анализа этого влияния воспользуемся уравнением 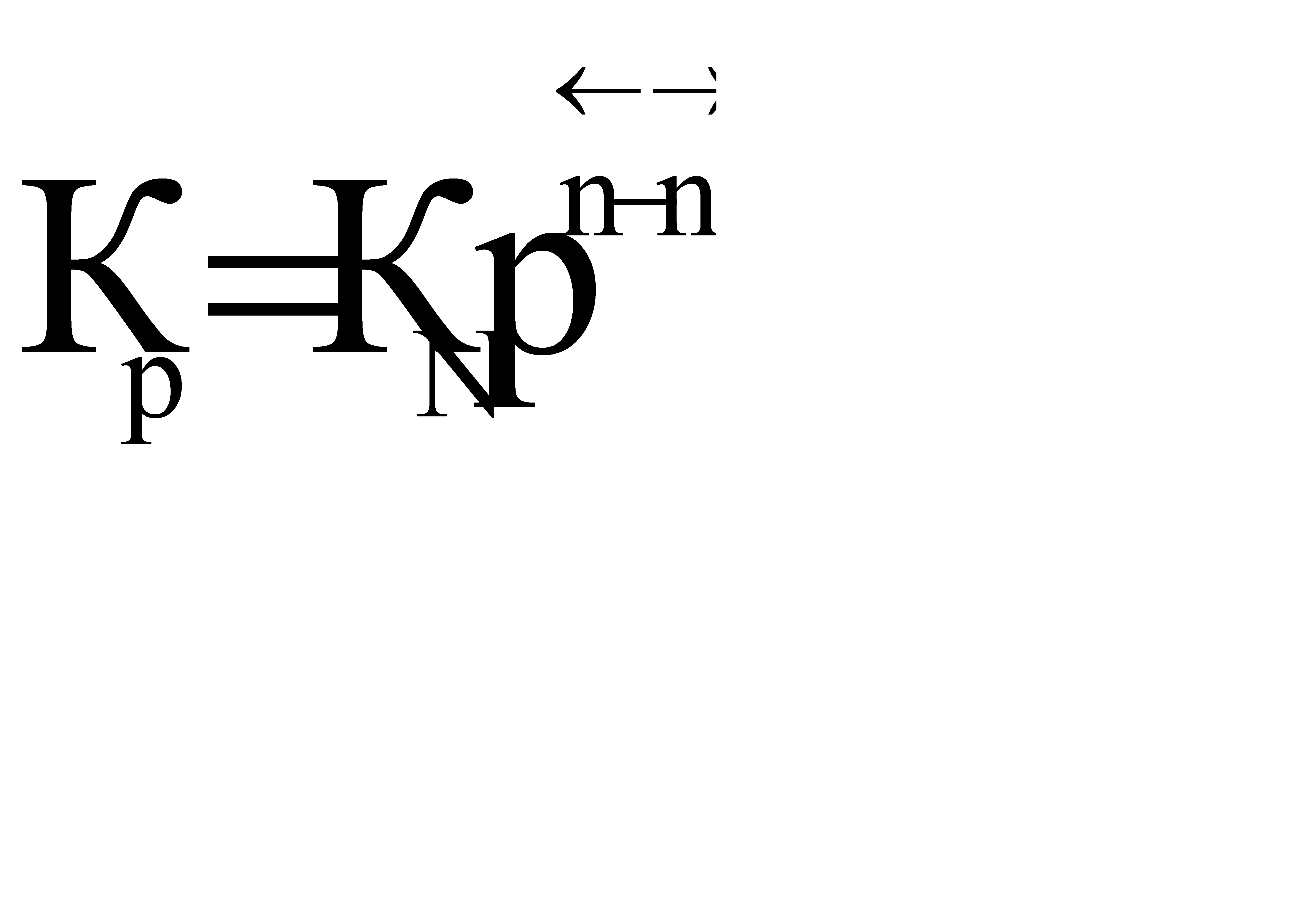 .
.
Константа равновесия КР зависит только от температуры, поэтому при Т = const, КР = const.
Если 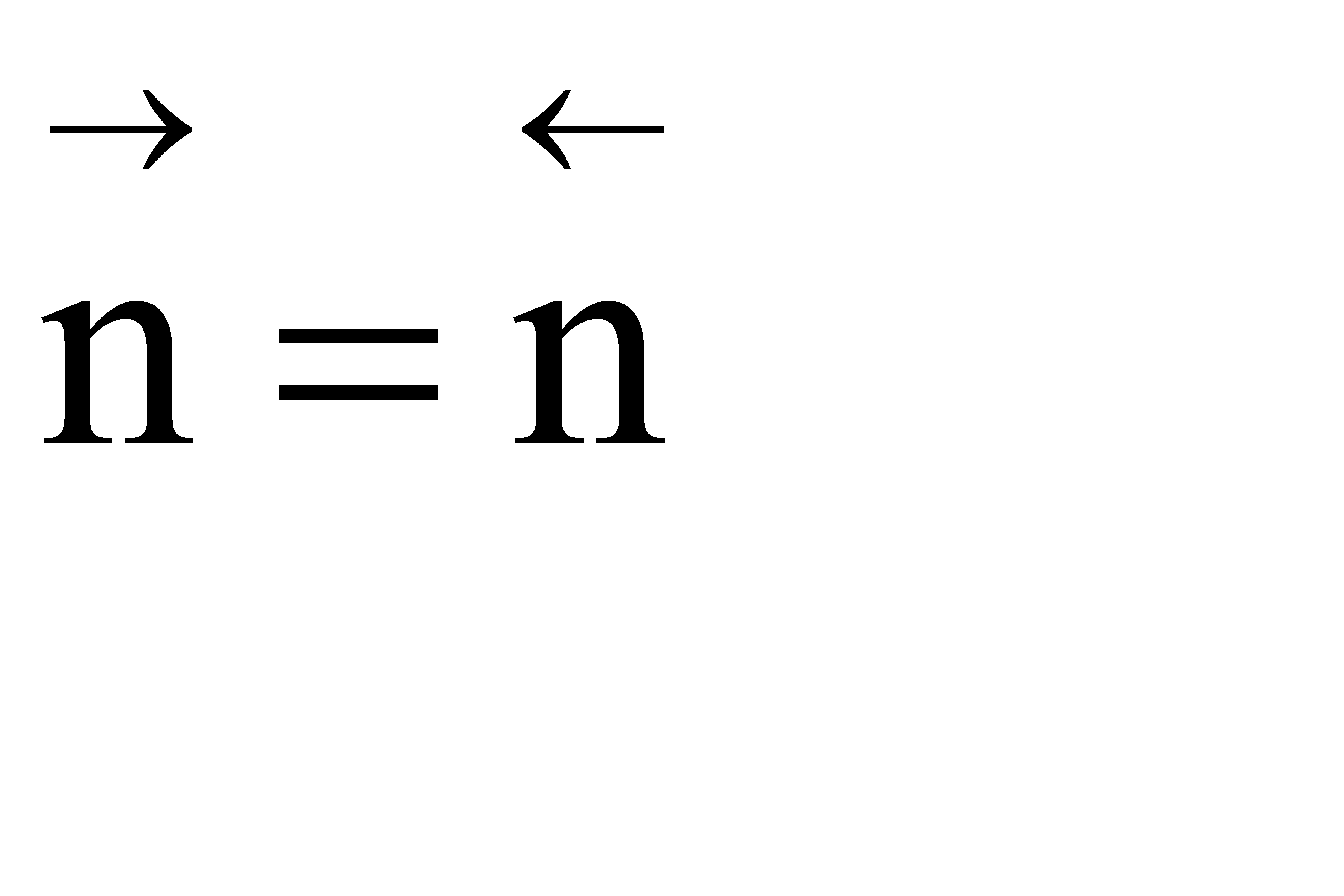 , КР = КN = const. Константа КN не зависит от давления; давление не влияет на положение равновесия, на равновесную конверсию и выход.
, КР = КN = const. Константа КN не зависит от давления; давление не влияет на положение равновесия, на равновесную конверсию и выход.
Если 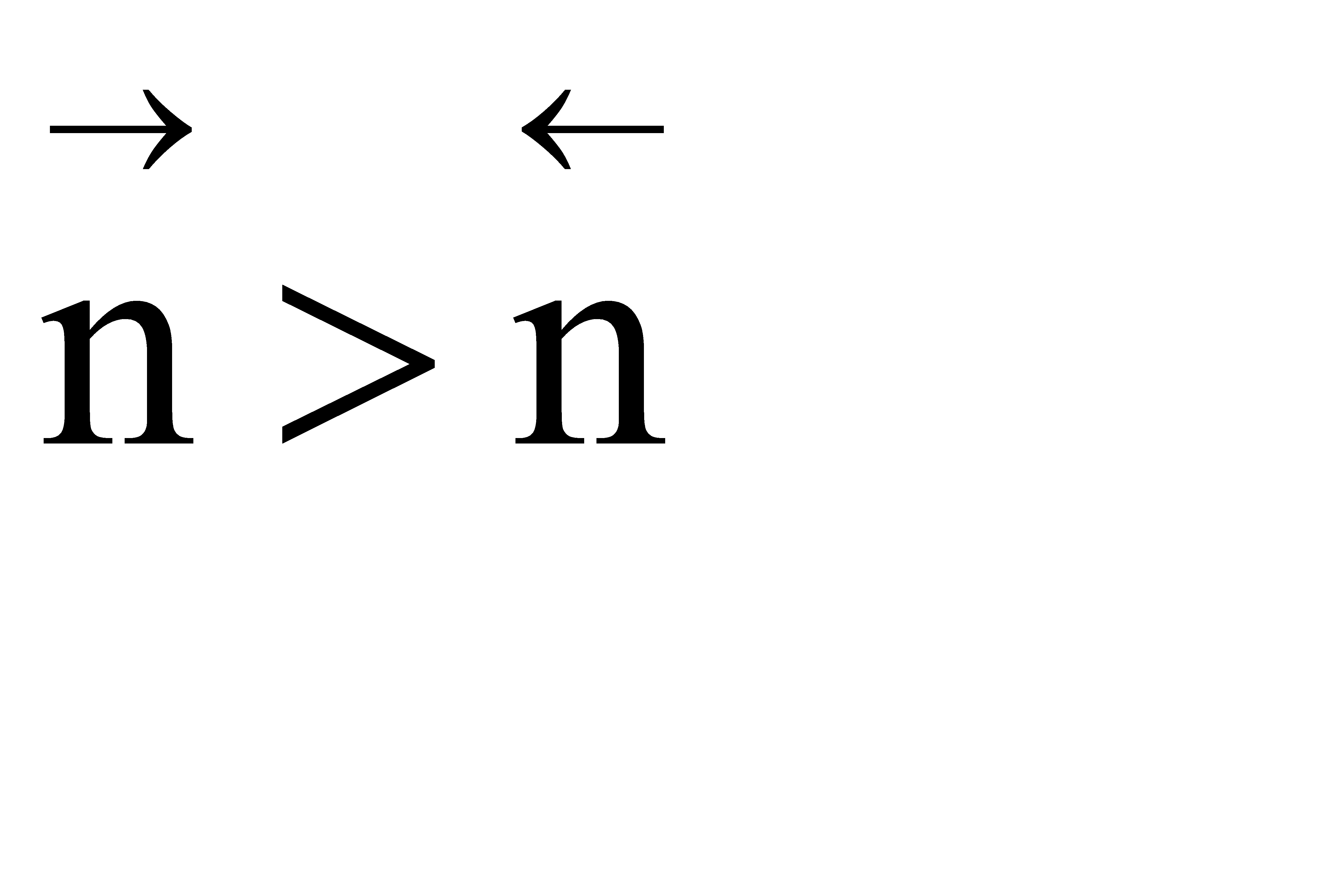 , увеличение давления приводит к уменьшению
, увеличение давления приводит к уменьшению 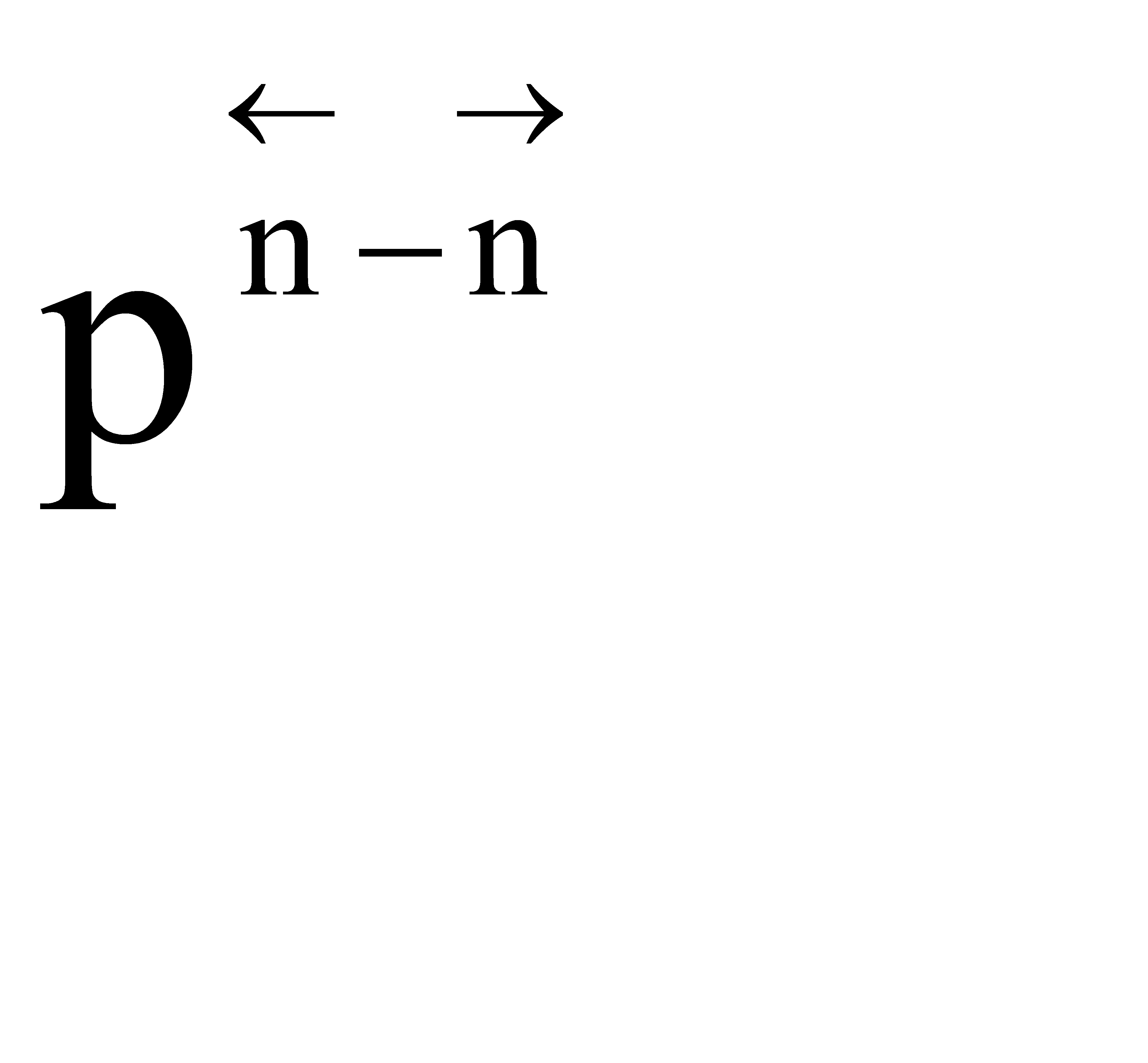 , КN должна увеличиться, равновесие сдвигается в сторону образования целевого продукта.
, КN должна увеличиться, равновесие сдвигается в сторону образования целевого продукта.
Если 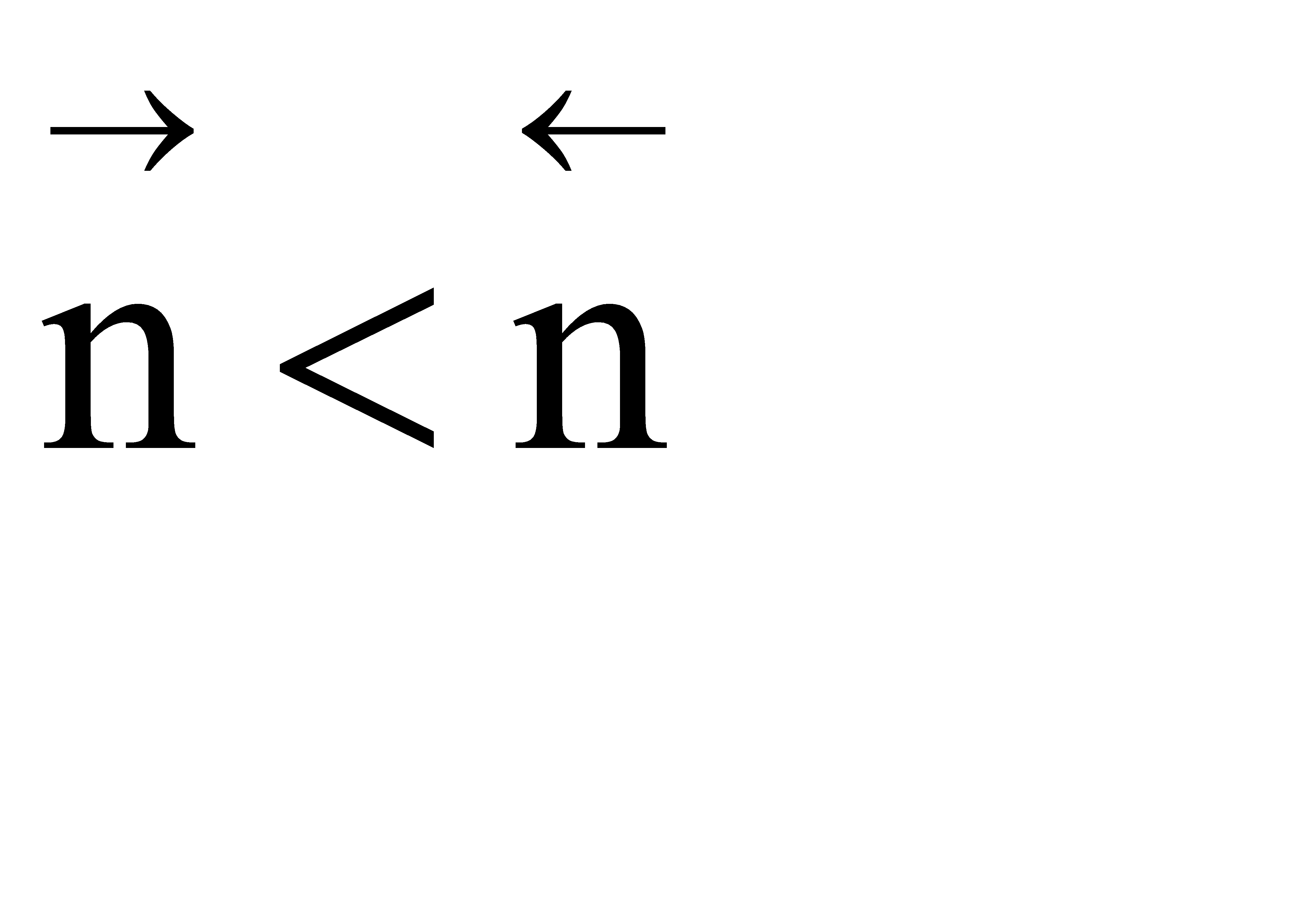 , увеличение давления приводит к увеличению
, увеличение давления приводит к увеличению 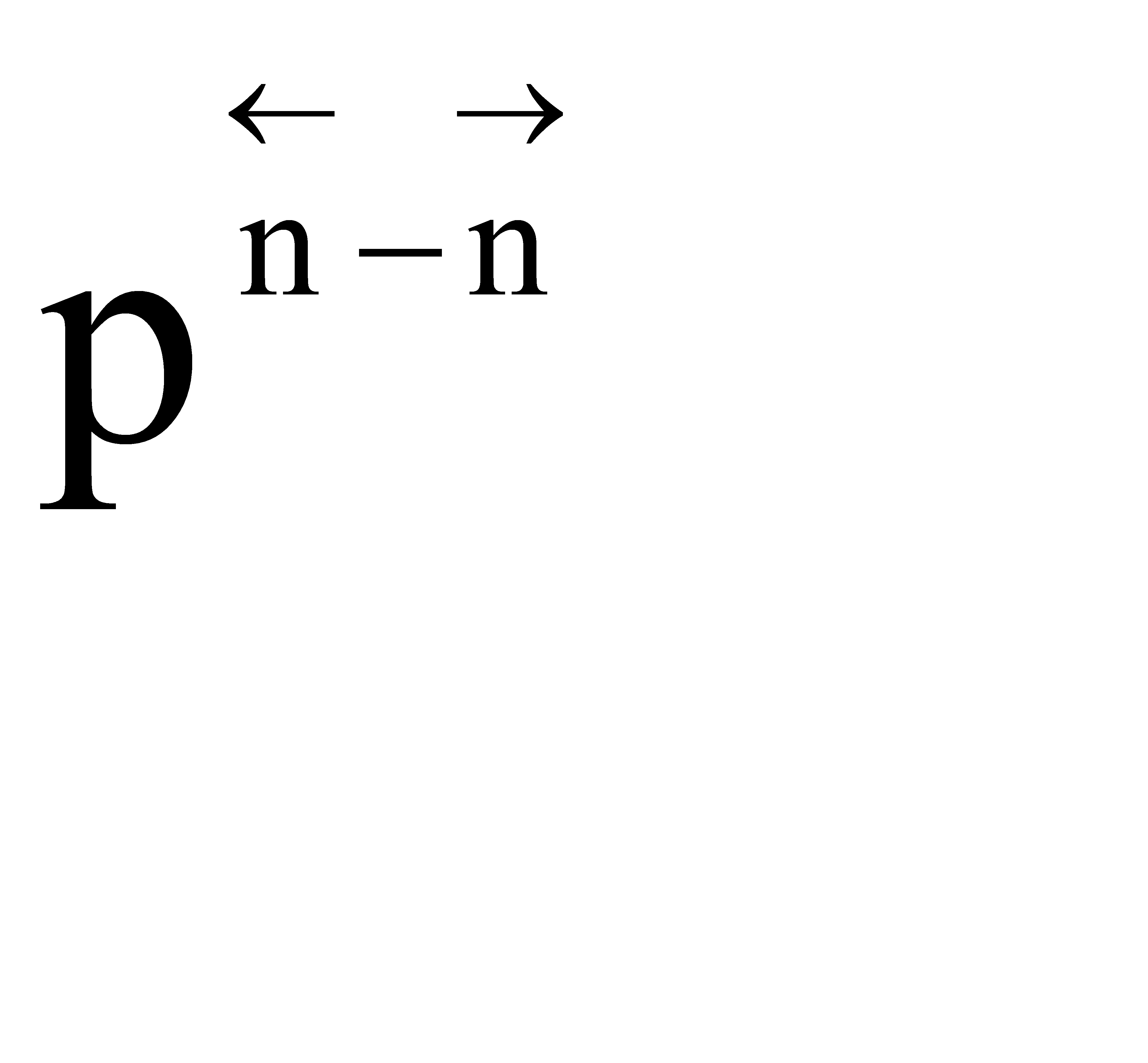 , КN уменьшается, равновесие сдвигается в сторону образования исходных реагентов.
, КN уменьшается, равновесие сдвигается в сторону образования исходных реагентов.
Таким образом, если число молей в результате реакции уменьшается, увеличение давления способствует сдвигу равновесия в сторону образования целевого продукта и увеличению скорости процесса. Если число молей в результате прямой реакции увеличивается, для увеличения скорости процесса и сдвига равновесия в сторону образования целевого продукта нужно уменьшить давление в системе. Если 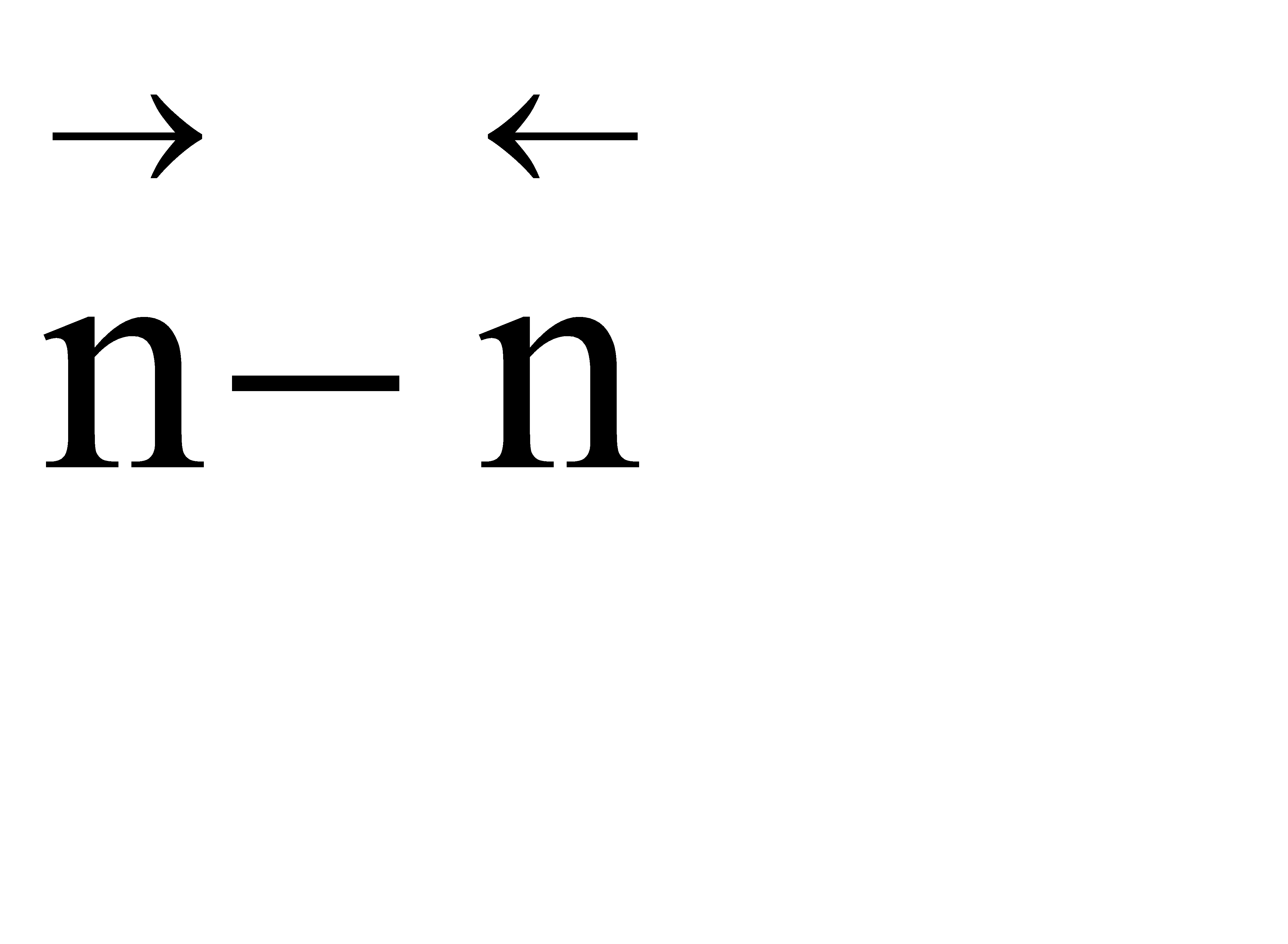 близко к нулю, использовать давление для повышения эффективности процесса нецелесообразно, так как затраты намного превысят полученный эффект.
близко к нулю, использовать давление для повышения эффективности процесса нецелесообразно, так как затраты намного превысят полученный эффект.
Дата добавления: 2020-04-25; просмотров: 529; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
