Чередование зон коагуляции коллоидных растворов. Сущность явления
Перезарядка золей
| С( FeCl3) моль / л | Коагуляция золя | Движ.частиц в эл.поле | Знак заряда частицы |
| 0.0206 | Нет | К аноду | - |
| 0,0833 | Полная | Нет | 0 |
| 0,3333 | Нет | К катоду | + |
| 6,3300 | полная | нет | 0 |
Кинетика коагуляции золей под действием электролитов. Понятие о скрытой ,явной,медленной и быстрой коагуляции
Скрытая коагуляция- первая порция электролита на золь практически не влияет,нет видимых изменений
Явная коагуляция – выражается в помутнении р-ра,изменении окраски, увеличении вязкости, изменении осмотического давления
Медленная коагуляция- увелечение концентрации эл-та ускоряет коагуляцию
Быстрая коагуляция- увелечение концентрации электролита не влияет на скорость коагуляции
Зависимость скорости коагуляции от дзета потенциала и от концентрации электролита
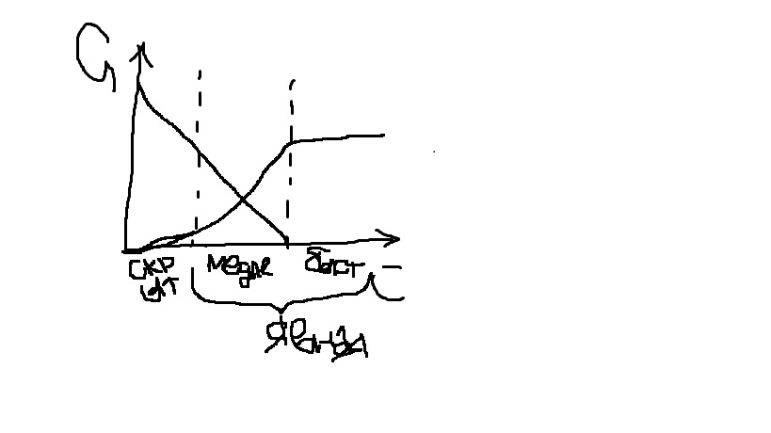
Коагуляция золей смесями электролитов.
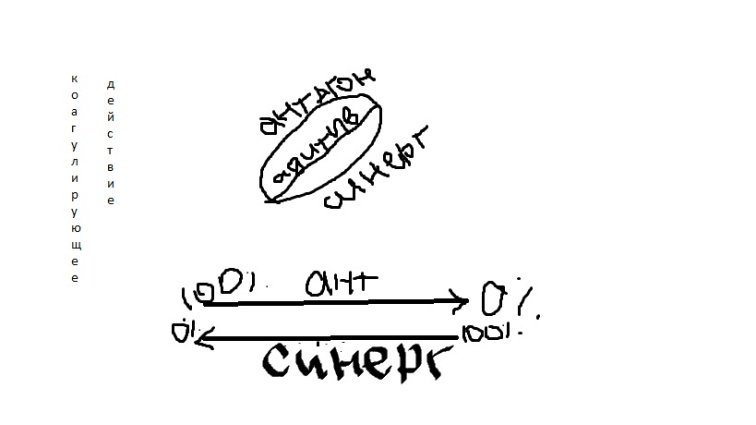
Адивитивность (суммирование)- коагулирующий эффект от двух электролитов равен сумме эффектов каждого из них
Синергизм –один электролит несколько усиливает коагулирующее действие другого
Антагонизм- один электролит ослабляет действие другого
Явление привыкания при коагуляции золей,его механизм
При медленном добавлении электролита или порциями через большие промежутки времени коагуляция может не наступить
Происходит образование новых химических соединений (пептизаторов) которые придают частицам ç- потенциал
|
|
|
Взаимная коагуляция золей. Применение
Происходит ,если смешать два коллоидных раствора, у которых частицы имеют противоположный знак
Применяется: для очистки воды от частиц глины и органических примесей
Al2(SO4)3+ 6h2o= AL(OH)3 + 3 H2SO4
Коллоидная защита. Механизм коллоидной защиты.
При добавлении к гидрофобному золю высокомолекулярных веществ происходит их адсорбция на коллоидных частицах и образование агрегатов обладающих гидрофильными свойствами (белки,углеводы, пав) Коллоидные растворы приобретают свойство обратимости
Количественная характеристика коллоидной защиты
«Золотое Число»
Число мг сухого высокомолекулярного в-ва ,которое нужно добавить к 10 мл красного золя золота,чтобы предотвратить его коагуляцию, при добавлении 1 мл 10% р-ра NaCl
Золотое число условно т.к. на защитное действие в-ва влияет дисперсность золя,молекулярный вес защитного в-ва, значение рН системы
Значение явления коллоидной защиты
-При изготовлении ЛП (протаргол)
- нерастворимы в воде холестерин и другие жироподобные в-ва удержив-ся в крови благодаря коллоидной защите которую оказывают белки крови
-Коллоидная защита препятстсвует образованию желчных,почечных камней,развитию подагры (отложение солей мочевой кислоты в суставах)
|
|
|
Холаты, улохром,муцин –защитное действие по отношению к билирубину ,холестерину
МИКРОГЕТЕРОГЕННЫЕ ДИСПЕРСНЫЕ СИСТЕМЫ
1. Аэрозоли, их виды, размер частиц дисперсной фазы.
Аэрозоль – свободно дисперсная система с газообразной дисперсионной средой, состоящей из твердых или жидких частиц (образуются при взрывах, дроблении веществ, а также в процессах конденсации).
По агрегатному состоянию частиц аэрозоли классифицируют на:
А) Туманы (жидкость+газ) – дисперсная фаза состоит из капель жидкости.
Б) Дымы – конденсационные аэрозоли с твердыми частицами
В) Пыли – твердые частицы, образующиеся путем диспергирования.
Размер частиц дисперсионной фазы – 10-7-10-4 м. В большинстве случаев частицы дисперсной фазы можно наблюдать в световой микроскоп.
2. Конденсационные и дисперсионные методы получения аэрозолей.
Аэрозоли образуются при взрывах, дроблении и распылении веществ, а также в процессах конденсации при охлаждении перенасыщенных паров воды и органических жидкостей. Их можно получить и с помощью химических реакций, протекающих в газовой фазе.
3. Характеристика молекулярно-кинетических и оптических свойств аэрозолей
|
|
|
-Интенсивное броуновское движение.
-Высокое светорассеивание.
-Выраженная агрегативная устойчивость
.Специфические свойства:
-термофорез-движение частиц аэрозоля в направлении области более низких температур.
Фотофорез-перемещение частиц аэрозоля при одностороннем освещении.
Термопреципитация-осаждение частиц аэрозоля на холодных поверхностях за счёт потери частицами кинетической энергии
4. Возникновение зарядов на частицах аэрозолей.
Электрические свойства аэрозолей сильно отличаются от электрических свойств систем с жидкой средой, что объясняется резким различием плотностей и диэлектрических свойств газов и жидкостей. В газовой среде отсутствует электролитическая диссоциация и ДЭС, однако, частицы в аэрозолях имеют заряды, которые возникают при случайных столкновениях частиц друг с другом или с какой-либо поверхностью.
5. Характеристика кинетической и агрегативной устойчивости аэрозолей
Для аэрозолей характерна агрегативная неустойчивость.
Их длительное существование связано с высокой дисперсностью и малой концентрацией. Это значит, что устойчивость аэрозолей лишь кинетическая. ТД факторы устойчивости отсутствуют.
К нарушениям устойчивость аэрозолей приводят следующие процессы: седиментация частиц, коагуляция частиц, влияние температуры
|
|
|
6. Применение аэрозолей для химико-бытовых нужд и в медицине
В медицине аэрозоль используется для распыления антибиотиков, при лечении инфекционных заболеваний. Также аэрозоли применяются для лечения ожогов и других повреждений кожи. Ингаляторы для астматиков, спреи для лечения заболеваний горла и носа. При помощи аэрозоля проводится дезинфекция и дезинсекция помещений. Дезодоранты, спреи для загара, увлажняющие спреи, которые очень хорошо применять летом. А также различные муссы, лаки и пенки для укладки волос – это тоже аэрозоли.
7. Отрицательное влияние аэрозолей на здоровье человека.
В зонах интенсивных пылевых загрязнений возникает ряд специфических заболеваний. К ним, среди прочих, относятся силикоз и асбестоз, приводящие к изменению тканей легких. Воздушная среда производственных помещений, в которой содержатся вредные вещества в виде аэрозолей, оказывает существенное влияние на здоровье работников. Наиболее частым заболеванием, вызываемым действием пыли, является бронхит. В бронхах скапливается мокрота, и болезнь хронически прогрессирует. Наиболее опасны для человека аэрозоли, состоящие из очень мелких частиц (размером от 0,5 до 10 мкм), которые легко проникают в легкие и задерживаются там в альвеолах. Чем мельче частицы пыли, тем дольше они находятся в воздухе в виде аэрозоля и тем легче в процессе дыхания попадают в организм человека.
Пылевые частицы с зазубренными острыми краями (металлическая, минеральная пыль) попадающие в дыхательные пути в большом количестве, могут травмировать слизистые оболочки. Задерживаясь в легких, они приводят к развитию соединительной ткани в воздухообменной зоне и рубцеванию (фиброзу) легких.
8.Очистка воздуха от аэрозолей
Процесс обеспыливания воздуха в общем виде включает следующие основные этапы (элементы):
предотвращение распространения "исходной" аэродисперсной системы в воздухе рабочей зоны и увеличения устойчивости этой системы в направлении строго ограниченной заранее выделенной области (процесс пылеулавливания);
разрушение пылевого аэрозоля, заключающееся в выделении пыли из воздуха (процесс пылеочистки);
дальнейшее снижение устойчивости пылевого аэрозоля, сохранившегося после реализации предыдущих этапов, заключающееся в интенсификации распространения оставшихся в воздухе пылевых частиц и аэрации дисперсной среды в приземном слое атмосферы (процесс рассеивания пыли). Многочисленные способы очистки промышленных газов от механических примесей основаны на применении двух групп методов - механических и физических . К механическим методам очистки газов относятся гравитационная и инерционная сепарация; мокрая очистка (промывка) газов; фильтрация через различные пористые материалы, к физическим - осаждение в электрическом поле и акустическая коагуляция.
9. Суспензии, их виды, размеры частиц, способы получения
Суспензии – микрогетерогенная дисперсная система с жидкой дисперсионной средой и твердой дисперсной фазой, с размерами частиц 10-6 – 10-4 м. Наиболее грубые дисперсные системы – взвеси. По характеру частиц дисперсной фазы различают суспензии гидрофильных и гидрофобных веществ. Суспензии классифицируются по нескольким признакам:
1. По природе дисперсионной среды: органосуспензии (дисперсионная среда - органическая жидкость) и водные суспензии.
2. По размерам частиц дисперсной фазы: грубые суспензии (d > 10-2 см), тонкие суспензии (-510-5< d < 10-2 см), мути (110-5< d < 510-5 см).
2. По концентрации частиц дисперсной фазы: разбавленные суспензии (взвеси) и концентрированные суспензии (пасты).
Получение суспензий. Два основных способа-смешение сухих порошков с жидкостью или измельчениетвердых тел в жидкости (методы диспергирования) и выделение твердой фазы из жидкой среды (методы конденсации). Методы диспергирования требуют затраты энергии на преодоление сил межмолекулярного взаимод. и накопление своб. поверхностной энергии образовавшихся частиц. Измельчение твердых телосуществляют раздавливанием, истиранием, дроблением, расщеплением мех. способом с помощью дробилок, ступок и мельниц разл. конструкции (шаровых, вибро-, струйных, коллоидных), ультразвуком, а также электрич. методами. При получении суспензий методами конденсации частицы твердой фазы выделяются из пересыщенных жидких р-ров, к-рые образуются при охлаждении, изменении растворяющей способности среды (метод замены р-рителя), вследствие хим. р-ций (окисления, восстановления, гидролиза, двойного обмена), приводящих к образованию малорастворимых соединений [BaSO4, AgI, CaCO3, Al(OH)3 и др.]
10. Сравнение свойств суспензий со свойствами коллоидных растворов.
Способы получения и стабилизации суспензий во многом сходны с таковыми для коллоидных растворов. Резко различаются суспензии от коллоидов в кинетических и оптических свойствах. Явление диффузии и осмоса не свойственны суспензиям. В большинстве суспензий частички твердой фазы не участвуют в броуновском движении. Прохождение света через суспензию не вызывает опалесценцию.
11. Факторы, обусловливающие низкую кинетическую устойчивость суспензий.
Седиментационная устойчивость суспензий обычно очень мала из-за крупных размеров частиц. В суспензиях твердые частицы могут находиться во взвешенном состоянии непродолжительное время, оседая под действием силы тяжести. Процессам облигации (агрегации?) частиц в суспензиях способствуют силы притяжения различной природы.
12. Агрегативная устойчивость суспензий. Факторы, определяющие устойчивость
Агрегативная устойчивость суспензий – это результат действия сил различной природы, препятствующих слипанию частиц:
1) Отталкивания частиц обусловлено ДЭС.
2) Энтропийного отталкивания, проявляющегося, когда частицы сближаются друг с другом на такие расстояния, при которых адсорбированные на них молекулы ПАВ начинают задевать друг друга УВ-цепями, находящимися в состоянии микроброуновского движения.
3) Отталкивания, обусловленные сольватными (сольватационными?) оболочками. Этот вид отталкивания возникает между частицами, если на их поверхности адсорбируются молекулы растворителя, образуя сольватный слой, толщиной в 1-2 молекулярных диаметра. Образующиеся сольватированные суспензии агрегативно устойчивы без специальных методов стабилизации.
13. Способы стабилизации суспензий.
Стабилизацию суспензий можно производить полимерами, при этом возрастает не только агрегативная устойчивость, но и замедляется седиментация.
Увеличение концентрации дисперсной фазы до предельно возможной величины в агрегативно-устойчивых суспензиях приводит к образованию высоко концентрированных суспензий, называемых пастами.
Пасты агрегативно устойчивы в присутствии достаточного количества сильных стабилизаторов, когда частицы дисперсной фазы в них хорошо сольватированы и разделены пластами жидкости, служащими дисперсионной средой.
14. Практическое значение суспензий
Суспензии имеют большое практическое значение, даже значительно большее, чем золи. Только лакокрасочная, полиграфическая и текстильная промышленность потребляют огромное количество суспензий пигментов и красящих веществ, диспергированных в воде или углеводородах. Угольные и графитовые суспензии широко применяются для предотвращения образования накипи в котлах. Здесь частички используются как центры кристаллизации солей. Бурение скважин сопровождается закачкой в них глинистых суспензий.
15. Эмульсии. Размеры частиц дисперсной фазы. Виды эмульсий в зависимости от концентрации и природы компонентов.
Эмульсии – свободно-дисперсные системы, в которых дисперсионная среда и дисперсная фаза являются жидкостями. Образующие эмульсию жидкости не смешиваются или ограниченно смешиваются. Жидкость, являющаяся дисперсной фазой, находится в диспергированном состоянии в виде капель размером от 10-7 до видимых невооруженным глазом.
В зависимости от концентрации:
а) Разбавленные ( с концентрацией дисперсной фазы не более 0,1%)
б) Концентрированные ( с концентрацией дисперсной фазы от 0,1 до 74%)
в) Высококонцентрированные ( с концентрацией дисперсной фазы больше 74%)
В зависимости от полярности фаз:
а) прямые – эмульсии первого рода, которые состоят из полярной дисперсионной среды (вода) и неполярной дисперсной фазы (масло), т.е. масло в воде
б) обратные – эмульсии второго рода (неполярная дисперсионная среда – масло и дисперсная фаза – полярная – вода, т.е. вода в масле.
16. Характеристика устойчивости эмульсий
Т.к. эмульсии – гетерогенные системы с большой удельной поверхностью раздела, в следствие раздробленности одной из фаз, они ТД устойчивы. В эмульсиях самопроизвольно протекает процесс сливания капель – коалесценция. При этому могут образовываться агрегаты капель, которые не сливаются, а сохраняют свою индивидуальность и при определенных условиях вновь расходятся. Такой процесс – обратная коалесценция. Седиментационная устойчивость определяется их дисперсностью, различием плотностей жидкостей, составляющих фазы, вязкостью среды. Устойчивость эмульсий против коалесценции связана с концентрацией дисперсной фазы. Разбавленные эмульсии могут существовать длительное время, концентрированные нуждаются в применении эмульгаторов.
17. Стабилизация эмульсий. Роль эмульгаторов и их виды.
Эмульгаторы – растворимые ПАВ или ВМС или нерастворимые порошкообразные вещества, добавление которых к эмульсиям делает их устойчивыми.
Механизм стабилизирования эмульсий различен, однако имеются некоторые закономерности, которые характеризуются правилом. Гидрофильные эмульгаторы (некоторые ПАВы), лучше растворяющиеся в воде или порошки, избирательно смачивающиеся водой, стабилизируют прямые эмульсии. Гидрофобные эмульгаторы, лучше растворяющиеся в масле, чем в воде, стабилизируют обратные эмульсии. Т.е., молекулы или частицы эмульгатора должны располагаться преимущественно со стороны дисперсионной среды, т.е. главным образом на наружной поверхности эмульсии.
Эффективность любого эмульгатора определяют по двум основным показателям:
А) по устойчивости эмульсии, стабилизированной данным эмульгатором
Б) по максимальному количеству эмульсии, которое может быть стабилизировано определенной порцией эмульгатора.
18. Методы определения типа эмульсий.
Существует ряд методов:
а) Разбавление или смешение определенного объема или капли эмульсии с водой или «маслом». Если наблюдается смешение капель эмульгатора с водой, то эмульсия – прямая и наоборот
б) Избирательное окрашивание одной из фаз эмульсии: водорастворимый краситель окрашивает водную фазу, а жирорастворимый окрашивает "масло»
в) применение инструментальных физико-химических методов, например, измерение электропроводности. Высокие значения электропроводности указывают на прямой тип эмульсии, обратные эмульсии имеют малые электропроводности.
19. Обращение фаз эмульсий
Переход эмульсии первого рода в обратную и наоборот. Определяющим фактором является форма молекул ПАВ, которые рассматриваются как молекулярные клинья – один конец молекулы широкий, а другой – узкий. Клинья располагаются на межфазной поверхности и изгибают ее так, что поверхность раздела по отношению к одной фазе выпуклой, другая – вогнутой. Она обращена к жидкости, служащей дисперсной фазой.
Практическое обращение фаз эмульсий можно вызвать:
1) изменением соотношения объема фаз
2) перенесением эмульсии в сосуд из другого материала
3) воздействием на эмульсию химическими реагентами.
20. Методы эмульгирования и деэмульгирования.
Эмульсии можно получать методами конденсации и диспергирования. Наибольшее практическое применение имеют методы диспергирования. Это механическое диспергирование двух жидкостей в присутствии эмульгатора путем встряхивания, перемешивания, вибрационного воздействия.
К разрушению эмульсий ведут 3 процесса:
а) коалесценция при недостаточной агрегативной устойчивости. Процесс необратим
б) коагуляция или коогуляция – процессы обратимые
в) седиментация – высаливание или оседание капель дисперсной фазы.
21. Медико-биологическое значение эмульсий
В жизни человека эмульсии занимают особое место. С первого дня жизни человек получает жиры, необходимую часть питания, в виде эмульсии – молоко матери. Поскольку жиры нерастворимы в водной среде, составляющей основу жизнедеятельности организма, поэтому организм может хорошо усваивать только эмульгированные жиры – молоко, сметану, сливки, сливочное масло. Другие жиры, потребляемые с пищей (растительное масло, животные жиры) в организме переводятся в эмульгированное состояние.
Процесс превращения грубых дисперсий жиров, образовавшихся при пережевывании пищи, в высокодисперсные эмульсии происходит в двенадцатиперстной кишке. Сюда, кроме желчи, выделяется секрет поджелудочной железы и кишечный сок, которые содержат большое количество NаHCO3. При его взаимодействии с кислой пищевой кашицей, поступающей из желудка (pH ≈ 1,7), выделяется углекислый газ, перемешивающий и диспергирующий пищевую кашицу – происходит эмульгирование. Образовавшиеся мелкие капли жира адсорбируют на своей поверхности ПАВ – желчные кислоты и это предохраняет капли от коалесценции. Образуется высокоустойчивая жировая эмульсия с размером частиц ~ 5·10‾5 м. При эмульгировании резко увеличивается поверхность жиров, что облегчает их взаимодействие с ферментами, ускоряет гидролиз и всасывание.
22. Понятие о коллоидных ПАВ?????
Молекулы мыла и детергентов представляют собой длинные УВ цепи (8-21 атомов углерода), на одном конце которых находятся диссоциирующие или ионогенные группы, поэтому детергенты в зависимости от заряда ионогенной группы разделяют на?
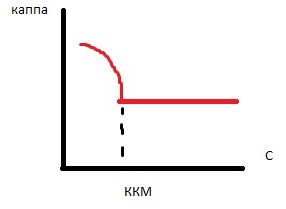
23. ККМ. Факторы, влияющие на ее величину. График
Важнейшей характеристикой полуколлоидной системы служит ККМ – минимальная концентрация растворенного детергента, при которой можно обнаружить коллоидно-дисперсную фазу. Выражается в % или моль/л.
В результате изучения ККМ, в растворах различных ПАВ установлены следующие закономерности:
а) ККМ зависит от строения УВ части молекулы и полярных групп
б) в случае одинаковых полярных групп, меньшее значение ККМ соответствует соединению, неполярная часть которого содержит большее число углеродных атомов.
Факторы:
1.строение углеводородного радикала в молекуле ПАВ;
2.характер полярной группы;
3.наличие в растворе электролитов;
4.температура
24. Сущность солюбилизации. Ее применение
Солюбилизация – самопроизвольное растворение в воде в присутствии добавок коллоидных ПАВ веществ, которые обычно в воде не растворяются. Процесс солюбилизации можно рассматривать как распределение труднорастворимого вещества между истинным раствором и мицеллами ПАВ. Очевидно, что абсолютно нерастворимые вещества не будут и солюбилизироваться, так как их переход от частиц или капель в мицеллы должен происходить через молекулярный раствор. Для водных растворов характерна солюбилизация маслоподобных гидрофобных веществ – углеводородов, дисперсных красителей и др. веществ, которые хорошо растворяются в углеводородных жидкостях и трудно растворяются в воде. Для растворов ПАВ в неполярных растворителях характерна солюбилизация воды и водных растворов различных веществ. Солюбилизация водонерастворимых веществ происходит и в организме человека и многих животных, что обеспечивает транспорт таких веществ по кровеносной системе между различными частями организма.
25. Понятие о липосомах
В системе вода-фосфолипид при встряхивании, перемешивании образуются мицеллы – липосомы. Молекулы фосфолипидов образуют в липосомах бислойную мембрану, в которой полярные группы обращены к воде, а неполярные друг к другу. С помощью липосом можно изучать проницаемость мембран и влияние на нее различных факторов. Липосомы используют для направленной доставки лекарственного вещества к тем или иным органам или зонам поражения. С помощью липосом можно транспортировать лекарственные вещества внутрь клеток. Липосомные мембраны используют в иммунологических исследованиях при изучении взаимодействия между антигеном и антителом.
ПАВ
Дата добавления: 2020-04-25; просмотров: 578; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
