ЧАСТЬ 2. МЕТАЛЛИЧЕСКИЕ МАТЕРИАЛЫ
Кристаллическое строение металлов и сплавов
Металлы и их сплавы относятся к поликристаллическим телам, которые характеризуются закономерным периодическим расположением атомов или ионов в пространстве. Если соединить атомы воображаемыми линиями в трёх взаимно перпендикулярных направлениях, то получится пространственная кристаллическая решётка. Её наименьшим структурным образованием является элементарная ячейка, контур которой представляет собой составленное из атомов геометрическое тело, например, куб или шестигранную призму.
|
| ||||||
| А | б | в | ||||
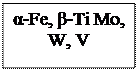

Рис. 2.1. Типы кубических решёток: простая (а), объёмноцентрированная (б), гранецентрированная (в) и примеры металлов, имеющих такие решётки
Кубическая решётка может быть простой, т.е. такой, в вершинах которой находятся атомы (ионы); объёмноцентрированной (ОЦК), у которой один атом расположен в центре куба; гранецентрированной, у которой атомы расположены в центрах граней (ГЦК) (рис. 2.1.). Кристаллические решётки характеризуются параметром (межатомное расстояние, измеряемое между двумя соседними плоскостями), координационным числом (количеством атомов - соседей, находящихся на ближайшем расстоянии от данного атома) и плотностью упаковки.

а б
Рис. 2.2. Типичные плотноупакованные структуры в металлах:
|
|
|
А – гексагональная (ГП) и б – гранецентрированная (ГЦК)
Плотноупакованной называется кристаллическая решётка, в которой при данном параметре достигается максимальная концентрация узлов в единице объёма. Плотноупакованной является гранецентрированная решётка, а также гексагональная плотноупакованная решётка (ГПУ) (рис. 2.2). Типы кристаллических решёток определяются при помощи рентгеноструктурного анализа.
Существуют кристаллы, которые могут иметь различные кристаллические решётки в зависимости от температуры (две или несколько). Такое явление называется полиморфизмом или аллотропией. Наибольшее значение полиморфизм имеет в переходных металлах, применяемых в технике. К ним относятся: железо, кобальт, скандий, титан (по две модификации), марганец (четыре модификации). Модификации металлов обозначаются малыми греческими буквами; при этом низкотемпературная модификация обычно обозначается α. Например, для железа – α и γ; для титана – α и β (табл. 2.1).
Таблица 2.1.
Кристаллические структуры переходных металлов 4-го периода*
| Группы элементов | |||||||
| III | IV | V | VI | VII | VIII | ||
| Sc | Ti | V | Cr | Mn | Fe | Co | Ni |
| ОЦК ГП | ОЦК ГП | ОЦК | ОЦК | ОЦК ГЦК Сложная куб. Сложная ОЦК | OЦК ГЦК ОЦК | ГЦК ГП | ГЦК |
* ОЦК-объемноцентрированная, ГЦК - гранецентрированная, ГП- плотноупакованная гексагональная
|
|
|
Объёмноцентрированные кристаллические решётки имеют: α - железо, β - титан, ванадий, хром, молибден, вольфрам; гранецентрированные решётки имеют: γ - железо, никель, алюминий, медь; гексагональные плотноупакованные имеют: магний, α - титан, цинк. Кристаллические решётки представляют собой идеальную, совершенную структуру кристалла.
Для всех кристаллов характерна а низотропия свойств, причиной которой являетсяразличие в расположении атомов в различных кристаллографических направлениях.
Анизотропия свойств – различие свойств кристаллов в разных кристаллографических направлениях. Анизотропия проявляется при измерении как физических, так и механических и других характеристик. Однако существуют свойства и не зависящие от кристаллографического направления. Например, такие физические характеристики как плотность и теплоемкость. Большинство же характеристик – модуль упругости Е, электросопротивление ρ, коэффициент диффузии D и др., зависят от выбора кристаллографического направления, в котором они измеряются.
|
|
|
Измерить свойства возможно на объектах, которые имеют определенный материальный объем: размеры - от нескольких миллиметров до десятков сантиметров. Эти объекты, имеющие строение, идентичное кристаллической ячейке, носят название монокристаллы.
Сплавом называют вещество, полученное при сплавлении и последующем затвердевании смеси двух или нескольких металлов или металлов и неметаллов.
Химические элементы, составляющие сплав, называются компонентами. Компонент - это химически индивидуальное вещество.Суммарное содержание всех компонентов в сплаве составляет 100 %. Компонентыделятся на четыре группы:
1) металл основы (металл - растворитель), на базе которого формируется сплав, т.е. в который вводятся другие элементы; концентрация металла-растворителя составляет не менее 50 % .
2) легирующие компоненты – химические элементы, специально вводимые в сплав для получения определённых свойств.
3) микродобавки – химические элементы, вводимые в сплав в небольших количествах для улучшения свойств; их содержание составляет от 0,001 % до 0,05 %.
4) примеси – химические элементы, присутствующие в сплаве как «остаток» от металлургического производства. Например, в сталях примесями являются сера, фосфор, марганец, кремний, мышьяк и газы; а в алюминиевых сплавах – натрий и кальций. Содержание примесей составляет от 10-4 до 10-1 %.
|
|
|
Количественной характеристикой химического состава является концентрация легирующих компонентов, % масс. В зависимости от концентрации легирующих компонентов сплавы подразделяют на низко - средне - и высоколегированные (суммарное содержание легирующих элементов составляет ≤ 5 ≤ 10 и > 10 % соответственно).
Фаза – часть сплава, отделенная поверхностью раздела, отличающаяся непрерывностью химического состава, кристаллической структуры и свойств по всему объему и скачкообразным изменением всех указанных параметров при переходе через границу.
Таким образом, признаками любой фазы являются: кристаллическая решётка; химический состав; граница раздела, обособляющая фазу от других фаз сплава.
В твёрдом состоянии в сплавах различают два вида твёрдых фаз – твёрдые растворы и промежуточные фазы (ПФ). В сплавах могут также присутствовать специфические смеси фаз, особенность которых состоит в том, что они образуются (при охлаждении) одновременно при постоянной температуре. Эти фазовые смеси могут состоять из твёрдых растворов, промежуточных фаз и чистых металлов. Они носят название эвтектические и эвтектоидные смеси.

Рис. 2.3. Схема относительных размеров и расположения интерметаллических фаз (Ф) в сплавах: Фперв– фазы, образовавшиеся при кристаллизации; Фвтор – фазы, образовавшиеся при горячей деформации; Фстар – фазы, образовавшиеся при старении; Фэвт – фазы, образовавшиеся при кристаллизации по эвтектической реакции
При микроструктурном анализе возможно выявить эти виды фаз. На рис. 2.3. показана схема микроструктуры сплавы с различными промежуточными фазами. Белое поле с границами (см. далее разделы «зёрна и границы зёрен») – это твёрдый раствор. Промежуточные фазы крупных размеров, образовавшиеся при кристаллизации, обозначены Фперв. Промежуточные фазы более мелких размеров, образовавшиеся при горячей обработке давлением обозначены Фвтор, а дисперсные частицы ПФ, образовавшиеся при термообработке обозначены Фстар. Частицы этих фаз находятся внутри твёрдого раствора.
Пластинчатые образования в одном из зёрен представляют собой эвтектодную смесь из двух фаз, Фэвт.
Твёрдые растворы. В том случае, когда легирующий компонент растворяется в металле - основе, не меняя его кристаллическую решётку, образуется новая фаза твердый раствор.
Твердый раствор – фаза сплава, кристаллическая решетка которой не отличается от кристаллической решетки металла - основы; а концентрация легирующих компонентов изменяется в широких пределах.
Твёрдые растворы занимают основное пространство сплава, т.е. они являются матричными фазами. Твердые растворы классифицируют по нескольким признакам, одним из которых является положение атома легирующего элемента в кристаллической решётке: это – твёрдые растворы внедрения и замещения.



Атом легирующего элемента
а б в
Рис. 2.4. Схема различных типов твёрдых растворов: а – твёрдый раствор
внедрения;
Дата добавления: 2020-01-07; просмотров: 226; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!

