ОПУХОЛЕВЫЕ ЛИМФАТИЧЕСКИЕ УЗЛЫ
Ультразвуковое исследование, в основном, рассматривается в качестве исследования первой линии в диагностике метастатических поражений, лимфом, особенно в поверхностных зонах. Лимфоузлы являются наиболее частым местом метастатического распространения. Чувствительность в обнаружения региональных ЛУ-метастазов в B-режиме зависит от первичной опухоли, размера, толщины коркового слоя и эхогенности ворот (смотри рис. 7A-F). ЛУ-метастазы в основном круглые и гипоэхогенные как кисты, а эхогенные ворота утрачены. Чувствительность для обнаружения кровоснабжения ЛУ и перфузии зависит от ультразвукового метода. Цветной Допплер и B-поток может определить большие сосуды, кровоснабжающие ЛУ. В случаях ранней стадии лимфатической опухоли, центральные сосуды все еще различимы, в то время как опухолевый узел формирует собственную сосудистую сеть. Наряду с нормальными центральными сосудами, опухолевые сосуды будут внедряться в ЛУ с его периферии. Так как опухолевые сосуды в определенной степени негерметичны, интранодальное давление будет отличаться между различными стадиями процесса. Кроме того известно, что неоангиогенез принимает участие и в образовании лимфатических сосудов (лимфангиогенеза за счет сосудистого эндотелиального фактора роста С). Предполагается, что лимфангиогенез в сторожевом ЛУ способствует распространению опухоли в отдаленные места. Способствует ли лимфангиогенез дренажу из опухоли и таким образом уменьшению интранодального давления пока не ясно.
|
|
|
Диагностическая точность УЗИ в установки стадии процессе в брюшной полости ниже, чем у КТ и МРТ, особенно в области грудной клетки.
Регионарные ЛУ расположены вдоль магистральных сосудов и органоснабжающих сосудов. В случае лимфатического распространения, опухолевые клетки входят в ЛУ через афферентный лимфатический сосуд и начинают расти там, где они попали в корковый слой, таким образом, образование новых сосудов начинается от коры (Рис. 17).
При стадировании пациентов с опухолями, знание лимфатических путей из первичной опухоли является обязательным. Трансортировние через лимфатическую систему является наиболее распространенным путем для начального распространение рака. Первоначальный маршрут опухолевых клеток у большинства пациентов с меланомой или раком молочной железы проходит через лимфатические сосуды в региональные узлы. Опухолевые клетки могут, собенно при меланоме, оставаться в пределах лимфатического сосуда и начинать там расти (транзитные метастазы, рис. 18).
Место раковой инфильтрации в ЛУ при раке груди зависит от квадранта расположения
|
|
|
опухоли. Опухоли верхнего наружного квадранта распространяются на ЛУ подмышечной впадины в 75%. Другие места распространения метастазов в начале заболевания над- и подключичные ЛУ и межгрудные ЛУ (ЛУ Роттера).
Применяя функции B-режима, негативная прогностическая ценность низкая при обнаружении метастазов в ЛУ при раке груди. Сравнивая биопсию сторожевого узла с диссекцией у пациентов с раком молочной железы, чувствительность метода составила от 71% до 100%. Тонкоигольная аспирация подозрительных подмышечных ЛУ при раке молочной железы имеет чувствительность только 42%. Причины неудовлетворительных результатов объясняются лимфоваскулярной инвазией и выбора методики тонкоигольной пункции. Поэтому отрицательный результат не исключает подмышечных метастазов. Отрицательный индекс Solbiati, фиксированный в В-режиме, и интранодальная ангиоархитектоника являются причиной нераспознавания опухоли-инфильтрата подмышечных ЛУ. Рис. 19 отражает то, что одного графического критерия зачастую недостаточно для диагностики и при этом, очень важно решить, какой ЛУ взять для биопсии.
У пациентов с меланомой или других опухолей кожи, таких как карцинома Меркеля, региональные ЛУ необходимо тщательно обследовать; при опухоли дистальнее локтя или колена, изгиб локтя или подколеая ямка также должны быть исследованы. Метастатические ЛУ шеи наиболее часто встречаются при раке головы и шеи, раке легких, меланоме, раке молочной железы и лимфомах. Меланома преимущественно распространяется через лимфатические сосуды, что делает первый региональный узловой бассейн важнейшим направлением исследования. Кистозные или кальцинозные изменения увеличивают вероятность канцерозных ЛУ. Крошечные кальцификаты или кистозные изменения в ЛУ в области шеи всегда подозрительны на наличие метастазов рака щитовидной железы, но они не являются специфичными (Рис. 20 и 21).
|
|
|

Рис. 15. (A, B) Два крошечных, округлой формы ЛУ. (А) Реактивные ЛУ с правильно ветвящимися центральными сосудами при терапии интерфероном. (B) ЛУ-метастазы с сосудами по периферии.

Рис. 16. (A, B) Круглой формы ЛУ с правильным ветвлением центральных сосудов и сосудов его капсулы (метастазы меланомы). (C, D) Реактивные, болезненные ЛУ с эхонегативной утолщенной корой, эхогенными воротами и индекс Solbiati ниже, чем 2.
Таблица 1. Лимфатические характеристики лимфоузлов в В-режиме
| КРИТЕРИЙ | РЕАКТИВНЫЕ ЛУ | ЛИМФОМЫ | МЕТАСТАЗЫ |
| Размер | Измерение наибольшего ЛУ в соответствующих региональных местах расположения ЛУ в 2-х плоскостях сканирования (динамическое наблюдение!) | Измерение наибольшего ЛУ в соответствующих региональных местах расположения ЛУ в 2-х плоскостях сканирования (динамическое наблюдение!) | Измерение наибольшего ЛУ в соответствующих региональных местах расположения ЛУ в 2-х плоскостях сканирования (динамическое наблюдение!) |
| Форма | Овальной формы (длина: ширина> 2) | От овальной к круглой | В основном круглая |
| Количество | От 1 до нескольких | От нескольких до множества в разных областях | От нескольких до множества, местнорегионарные ЛУ |
| Расположение | В основном 1 или несколько ЛУ в области ЛУ 1-го порядка | В основном ЛУ в одной или в разных областях | В основном 1 или несколько регионарных узлов разного порядка, но не все регионарные узлы |
| Пространственное расположение | Размер и количество увеличиваются в направлении очага поражения | Хаотичное, цепочки или пакеты узлов | Вдоль дренирующей сети ЛУ |
| Эхогенность | Эхонегативная кора | От эхонегативной до кистозной картины | Эхонегативные |
| Структура | Сохранена (кроме: абсцессов, ТВ, саркоидоза) | От сохраненной до разрушенной | Полностью или частично разрушена |
| Кора | Утолщена концентрически или эксцентрически | Утолщена концентрически или эксцентрически | Инфильтрирована, больше в узелках |
| Ворота | Эхогенные | Истончены или отсутствуют | Сдавлены, часто отсутствуют |
| Край | Острый, неопределенный при абсцедировании | Острый | Острый, неопределенный при окружающем отеке |
| Абдоминальное распространение | Лимфотропные вирусы (мононуклеоз), саркоидоз, ТВ (печень, селезенка) | Чаще при НХЛ, инфильтрация всех органов возможна (печень, селезенка, почки, железы). Нехарактерно для лимфомы Ходжкина | Возможно, чаще печень и абдоминальные ЛУ |
ТВ – туберкулез, НХЛ – неходжкинская лимфома.
|
|
|
Таблица 2. Характеристики лимфатических узлов в сосудистом режиме (перфузии).
| РЕЖИМ | ЗЛОКАЧЕСТВЕННЫЕ ЛИМФОМЫ/ РЕАКТИВНЫЕ ЛУ | МЕТАСТАТИЧЕСКИЕ ЛУ |
| Цветовая дуплексная сонография В-поток | От гипо до гиперваскуляризации Сохраненная ангиоархитектоника. Древовидное ветвление сосудов часто до капсулы. Ампутация ворот при высокой плотности опухоли или воспалительном отеке. Центральные сосуды ворот. Артериальный и венозный кровоток регистрируется. | Преимущественно гиповаскуляризация, кроме случаев гиперваскуляризированной первичной опухоли. Изредка ангиоархитектоника подмышечных лимфоузлов при раке молочной железы может быть сохранена. Преимущественно хаотичное строение сосудов. Часто периферическое кровоснабжение. В основном только артериальный поток или его отсутствие в центре узла. |
| Сонография, усиленная контрастом | Центробежный поток. Полная или только центральная васкуляризация. Усиление только в пределах ЛУ, кроме местного абсцесса | В основном центростремительный поток, интранодальная ишемия/ может быть некроз Усиление может выходить за край ЛУ, когда опухоль прорастает капсулу. |

Рис. 17. (А-D) Метастазы в лимфатических узлах из плоскоклеточного рака легких. Образец центростремительного накопления контраста, типичный для злокачественной трансформации ЛУ.
Отрицательный результат при сонографии ЛУ недостаточно достоверный для стадирования пациентов при небольшой раковой опухоли для постановки диагноза, при этом по-прежнему рекомендуется диссекция ЛУ. Сонография является наиболее удобным методом для определения течения послеоперационного периода, в отношении изменения размера метастазов.
Высокодифференцированные опухоли также характеризуется богатой внутриопухолевой васкуляризацией и часто отражают васкуляризацию первичной опухоли. Поэтому гиперваскуляризованные ЛУ можно найти у пациентов с раком щитовидной железы, яичников, молочной железы, почек и других локализаций, у которых опухоль также гипирваскуляризована (см. Таблицы 1 и 2).
Экстравазация жидкости в окружающую жировую ткань вызывает постоянный поток опухолевых клеток в окружающие мягкие ткани. Если планируется хирургическое вмешательство, то этот факт должен быть учтен и уровень резекции должен включать отечные ткани вокруг злокачественного ЛУ.

Рис. 18. (А) Подкожное метастазирование злокачественной меланомы изображаемое в с-плоскости с перевернутой серой шкалой. Эфферентные лимфатические сосуды инфильтрированы транзитными метастазами. Подкожные вены можно увидеть вблизи опухоли. (В) Гиперваскуляризация из транзитных метастазов.
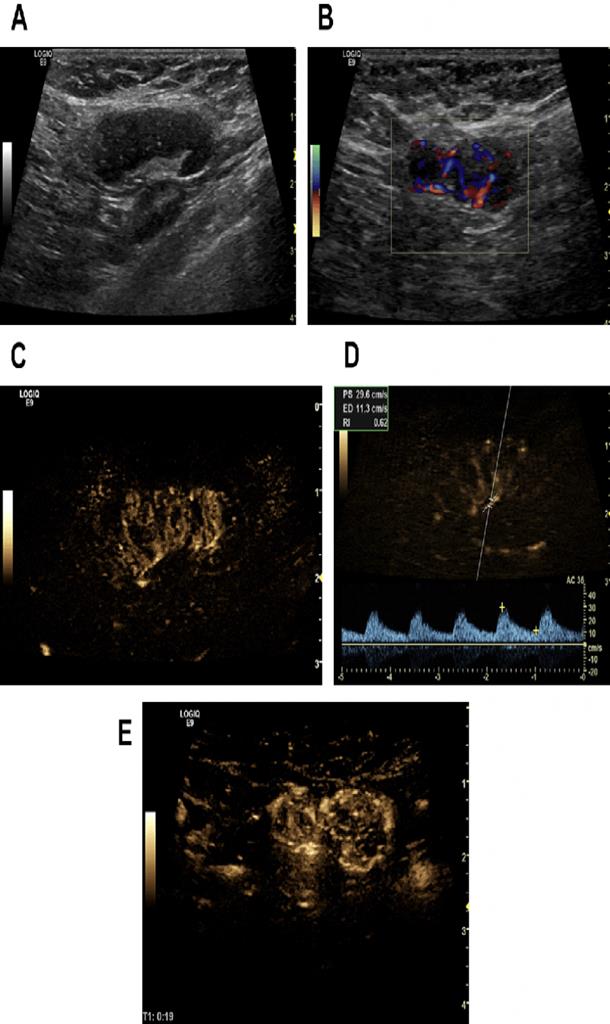
Рис. 19. (А-E) 55-летняя женщина со случайный находкой – увеличенными подмышечными ЛУ. Хотя они и овальной формы (А), с правильным ветвлением сосудов на цветном допплеровском и B-потоковом изображении (B, C), а также низким индексом резистивности 0,62 (D), ЛУ имеют утолщенную кору, что стало показанием к биопсии. На B-потоковом изображении при УЗУК обнаружены расширенные периферические вены (Е). Иммуногистохимия подтвердила метастаз протоковой аденокарциномы молочной железы.
ЛИМФОМЫ
Существует 2 типа лимфом: Ходжкина и неходжкинская лимфома (НХЛ). Описано четыре гистологических подтипа лимфомы Ходжкина: лимфоидное доминирование, смешанноклеточная, лимфоидное истощение и нодулярный склероз (Рис. 22 и 23). Нодулярный склероз наиболее распространенный подтип до 70%, в тоже время лимфоидное истощение – самый редкий подтип.

Рис. 20. (A) Папиллярная опухоль щитовидной железы с кальцификатами (B) Метастатические ЛУ у того же пациента с такими же микрокальцификатами. (C, D) Подключичные узлы у другого пациента с микрокальцификатами. Гистологически – лимфома Ходжкина.
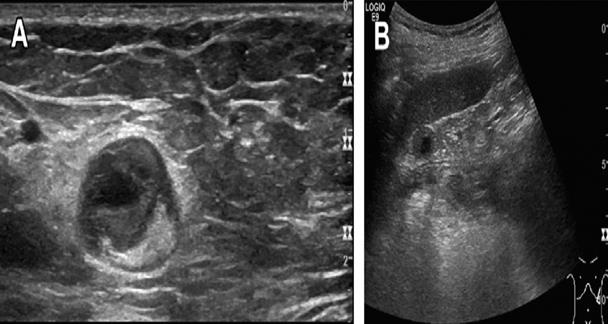
Рис. 21. (А) Центральный кортикальный некроз ЛУ – метастаз в пах (меланома), кистозная область в воротах селезенки. (В) Центральный некроз метастаза в ЛУ при раке толстой кишки в воротах селезенки.

Рис. 22. (А) Лимфома Ходжкина шеи (нодулярный склероз), (В) Цветной допплер показывает гиперваскуляризацию (С) Кор-биопсия под УЗИ контролем, определены клетки Рида-Штемберга.

Рис. 23. (А, В) Большая Ходжкинская инфильтрация паховых ЛУ. Опухолевые сосуды имеют правильное деление, ЛУ кровоснабжается центральными сосудами.

Рис. 24. (А-С) НХЛ. (А) Эхонегативный ЛУ с окружающим отеком. (В) В-поток – правильное деление сосудов. (С) Окраска СD31 демонстрирует большие сосуды и мелкоклеточную опухолевую инфильтрацию.

Рис. 25. Парааортальная инфильтрация НХЛ. (С,D) Множественные узлы НХЛ шеи, цветной допплер указывает на гиперваскуляризацию.

Рис. 26. (А) Паховые ЛУ поражены НХЛ. (В) Допплер – большие центральные сосуды, нет периферических сосудов (ампутация ворот). (С) УЗУК – показаны мелкие сосуды, но также нет периферических субкапсулярных сосудов.

Рис. 27. Местный рецидив опухоли через 2 мес. после лимфодиссекции метастаза меланомы (А) Подкожные гиперваскуляризированные метастазы (4 мм) (В) Изображение в с-плоскости – метастазы, прилежащие к рубцу.

Рис. 28. (А, В) 35-летный мужчина после подмышечной лимфодиссекции по поводу меланомы. (А) Подозревается гематома. (В) Диффузное гипернакопление контраста без признаков воспаления. Кор-биопсия подтвердила диффузную опухолевую инфильтрацию.
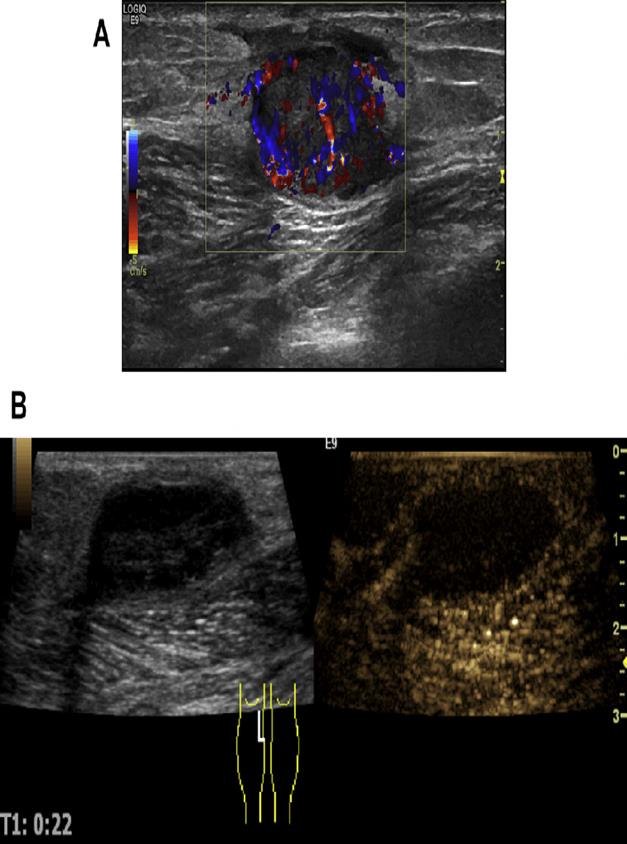
Рис. 29. (А) Транзитные метастазы (меланома) – богатая хаотичная васкуляризация до местной химиотерапии. (В) УЗУК – аваскулярный узел через 2 недели после терапии.
НХЛ развивается из В-клеток (90%), T- клеток (10%), клеток-киллеров (1%). НХЛ также различают в зависимости от скорости роста: медленный и агрессивный. Медленный и агрессивный рост НХЛ одинаково встречаются у взрослых. У детей – чаще всего агрессивный рост. Для окончательного диагноза у пациентов с лимфомой необходима гистология. Некоторые исследователи предпочитают кор-биопсию, как первый диагностический этап, с чувствительностью 89% и специфичностью 97%, другие – первичную диссекцию ЛУ.
Рис. 24 отражает случай кожной Т-клеточной лимфомы с поражением опухолевыми клетками подмышечных ЛУ. Экстранодальное распространение характерно больше для НХЛ, чем для лимфомы Ходжкина – 20-40% и 4-5% соответственно. Экстранодальное распространение характерно больше для пациентов с иммунодефицитом, чем для пациентов с первичными проявлениями. Так как лимфома поражает почти все органы и ткани, диференциальный диагноз многообразен. В большинстве случаев ЛУ эхонегативные или даже кистозные, могут быть выстроены в линию или цепочку, отечные и безболезненные (Рис. 25C, D). Некоторые ЛУ могут утратить свою структуру, когда в других могут определяться кора и ворота. В В-режиме могут определяться только незначительные изменения коры.
В других случаях множественные кистозные образования вокруг аорты могут имитировать аневризму аорты или ретроперитонеальный фиброз (см. Рис. 25A, B).
Абдоминальная лимфома может быть определена интроперитонеально, ретроперитонеально и имеет те же параметры, что и поверхностная, за исключением того, что при этом желательно использовать датчики меньшей частоты.
Лимфоматозный ЛУ выглядит как реактивный и лишь обильная васкуляризация, при отсутствии инфекции, может наводит на мысль о лимфоме. Фокальная инфильтрация может быть причиной эхонегативного, гиперваскуляризированного кортикального утолщения (см. Табл. 1 и 2).
Не существует четких сонографических критериев, позволяющих дифференцировать увеличенные реактивные ЛУ от НХЛ. Как и в случае малигнизации, лимфома характеризуется высокой микрососудистой плотностью (МСП), особенно агрессивные лимфомы имеют очень высокую МСП. Как и при малигнизации это говорит о плохом прогнозе. Однако, даже УЗУК не всегда определяет микрососудистую плотность, так как повышенное интерстициальное давление может препятствовать этому. На сегодня нет данных о том, что УЗУК может выявлять различные типы НХЛ.
В большинстве случаев допплер отражает богатую сосудами лимфоидную ткань с хорошо видимыми артериями и венами. Нормальная структура сохранена, особенно при НХЛ с низкой агрессивностью. В противоположность канцероматозным узлам, сосудистая сеть не разрушена и отсутствует неоваскуляризация. Цветной допплер и УЗУК могут выявить нарушение ветвления сосудов и сосудистую ампутацию (Рис. 26).
Хотя большинство измененных ЛУ при НХЛ имеют типичную структуру в серой шкале, все же некоторые имеют перинодулярную инфильтрацию, такую как при воспалительном отеке мягких тканей.
Сонографически выявленные, увеличенные ЛУ без опухолевого анамнеза – задача для исследователя. Существует множество перекрещивающихся сонографических признаков между воспалительными и НХЛ ЛУ. Комбинация нескольких признаков и клиническая картина помогаю поставить правильный диагноз.
Дата добавления: 2019-11-25; просмотров: 283; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
