ВРОЖДЕННЫЕ ГЕМОЛИТИЧЕСКИЕ АНЕМИИ, ОБУСЛОВЛЕННЫЕ ГЕНЕТИЧЕСКИМИ (НАСЛЕДСТВЕННО-СЕМЕЙНЫМИ) ФАКТОРАМИ
ВРОЖДЕННАЯ (СЕМЕЙНАЯ) СФЕРОЦИТАРНАЯ ГЕМОЛИТИЧЕСКАЯ АНЕМИЯ (БОЛЕЗНЬ МИНКОВСКОГО—ШОФФАРА), НАСЛЕДСТВЕННЫЙ СФЕРОЦИТОЗ
Врожденная офероцитарная гемолитическая анемия представляет собой семейное заболевание, наследуемое по доминантному типу.
Хотя болезнь имеет врожденный характер, но в силу своего длительно латентного течения она выявляется обычно в более поздние периоды жизни. При этом желтуха иногда является единственным симптомом, по поводу которого больной обращается к врачу. Именно к этим лицам относится известное выражение Chauffard: «Они более желтушны, чем больны».
В последнее время благодаря улучшившейся диагностике болезнь стала чаще выявляться в раннем детском возрасте.
Среди членов одной семьи наряду с больными гемолитической болезнью встречаются лица, находящиеся в латентной стадии заболевания с едва заметными признаками гемолиза — еле уловимой субиктеричностью покровов — при наличии характерных изменений со стороны крови (микросфероцитоз эритроцитов и др. — см. ниже).
Нередко заболевание выявляется под влиянием интеркуррентного внешнего фактора (инфекция, охлаждение, переутомление и т. п.), вызывающего обострение гемолиза.
Клиническая картина. Центральное место в клинической картине принадлежит гемолитическому синдрому, который проявляется тремя кардиальными признаками: желтухой, спленомегалией и анемией.
|
|
|
Первоначально единственным симптомом является желтуха, не сопровождающаяся никакими другими патологическими проявлениями. В дальнейшем развивается спленомегалия, а еще позднее — анемия. Огромный распад и регенерация кровяных клеток в период роста приводят к недостатку материала, необходимого для нормального развития организма, в результате чего наблюдается общая отсталость развития (спленогенный инфантилизм).
В дальнейшем могут присоединиться симптомы, связанные с анемизацией больного: адинамия, вялость, головокружение, сердцебиения и пр.
Желтуха изменяется в своей интенсивности, обостряясь в период гемолитических кризов.
Содержание «непрямого» билирубина в крови не достигает особенно высоких цифр; обычно оно колеблется в пределах 2—3 мг% и даже в периоды обострения не превышает 6 мг%. Перехода этого билирубина в мочу не наблюдается — этим гемолитическая желтуха отличается от механической желтухи. Отсюда название этого вида желтухи: ахолурическая, т.е. желтуха без наличия желчных пигментов и желчных кислот в моче.
Значительная часть билирубина, поступающего в кишечник, восстанавливается в уробилин. Приток большого количества уробилина из кишечника по воротной вене в печень вызывает функциональную перегрузку последней, вследствие чего часть уробилина поступает неизмененной в ток крови (уробилинемия) и выделяется из организма с мочой (уробилинурия).
|
|
|
Большая часть уробилина выделяется из организма с калом; количество стеркобилина превышает норму в 10—25 раз, доходя до 3000 мг в сутки (рис. 49).
Спленомегалия развивается вторично в связи с тем, что повышенный гемолиз эритроцитов в селезенке приводит к ее гиперплазии. Размеры селезенки меняются соответственно интенсивности гемолитического процесса, который протекает циклически. В тех случаях, когда болезнь проявляется в раннем возрасте, селезенка достигает огромных размеров; вес ее доходит до 3,5 кг (рис. 50). Случаи без выраженной спленомегалии представляют исключение. В связи с увеличением селезенки больные испытывают тягостное ощущение в левом подреберье.
Печень при гемолитической желтухе увеличивается в меньшей степени. Гемолитическая болезнь нередко осложняется приступами печеночной колики вследствие образования пигментных камней в желчном пузыре и желчных протоках. По данным некоторых клиник, у 60% больных гемолитической болезнью, которым производится операция удаления селезенки, в желчном пузыре обнаруживают пигментные камни. В связи с приступами печеночной колики и вторичным застоем желчи в печени у больных могут наблюдаться симптомы ангиохолецистита и паренхиматозного гепатита с появлением «прямого» билирубина в крови.
|
|
|
Обострениям болезни обычно предшествуют различные экзогенные факторы, как интеркуррентные инфекции, травмы, у женщин беременность.
При обострениях обычно повышается температура. Повышение температуры неинфекционного характера; оно связано с интенсивными процессами распада крови. Отмечается наклонность к носовым кровотечениям.
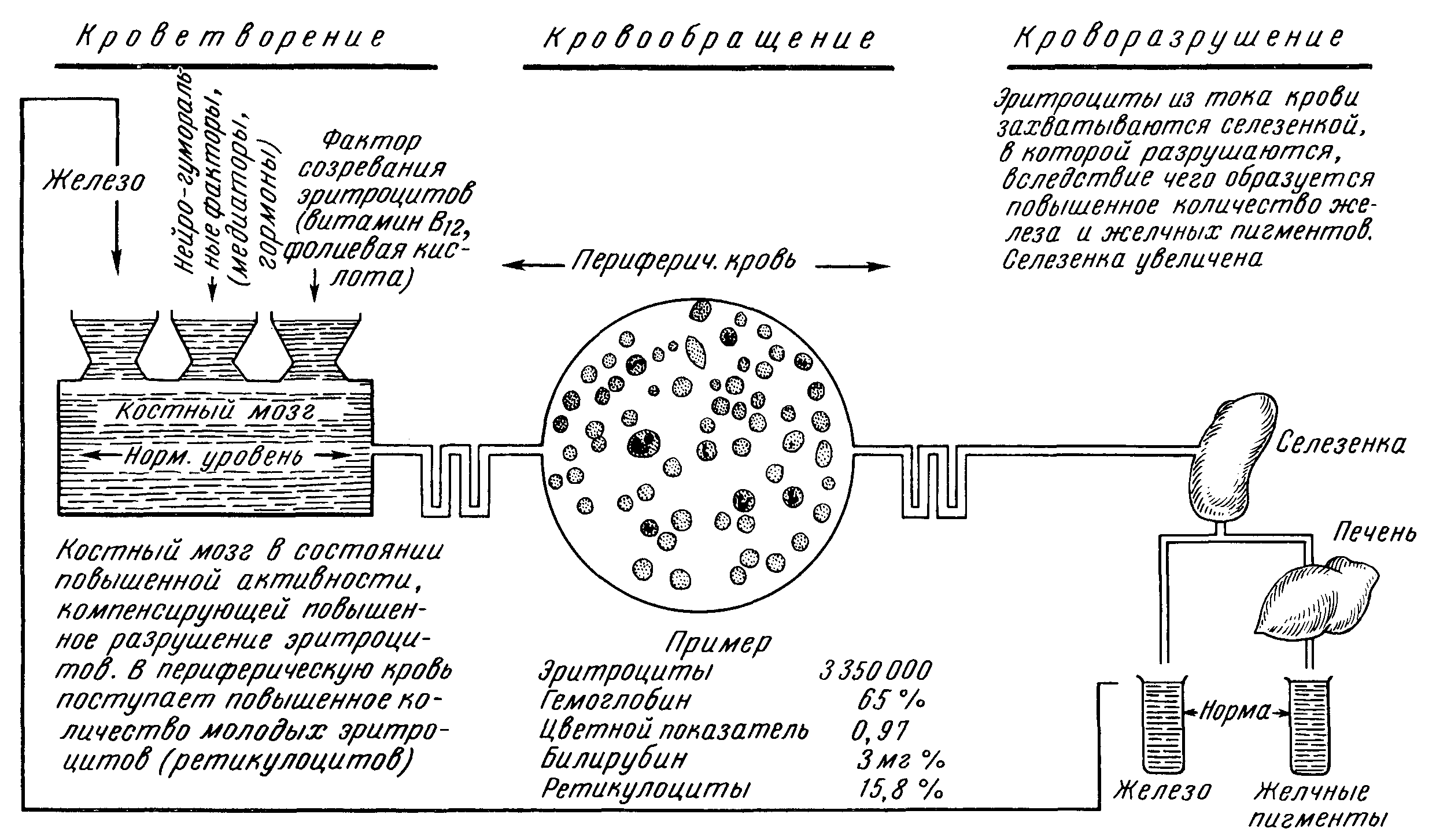
Рис. 49. Кроветворение и кроворазрушение при гемолитической болезни.
Нередко наблюдаются трофические язвы голени, не поддающиеся обычному лечению, но заживающие после спленэктомии.
Патогенез этих язв следует связывать с процессами аутоагглютинации и распада нестойких эритроцитов в дистальных капиллярах конечностей, где в силу замедленного кровотока для сфероцитов создаются такие же условия, как в селезеночном кровообращении. В результате тромбирования капилляров распадающимися массами эритроцитов нарушается кровоснабжение конечностей и возникают язвы.
|
|
|
В качестве симптомов, сопутствующих врожденной гемолитической болезни, описывается так называемый башенный или круглый череп с плоским седловидным носом, увеличенной дистанцией между углами глаз, узкими глазными щелями, микрофтальмией и высоким стоянием неба. Рентгенограммы костей черепа обнаруживают увеличение костномозговых диплоических пространств за счет уменьшения компактного вещества. Указанные изменения лицевого скелета отмечаются только в тех случаях, когда болезнь развивается в детском возрасте, и носят вторичный характер. Они являются следствием неправильного окостенения швов основания черепа, наступающего в результате повышенной активности и гиперплазии костного мозга в связи с усиленным гемолизом.
Картина крови. При врожденной гемолитической желтухе картина крови характеризуется патологической триадой со стороны эритроцитов: 1) микросфероцитозом, 2) ретикулоцитозом и 3) пониженной осмотической резистентностью.
При микроскопировании препаратов крови создается впечатление о малых размерах эритроцитов. Действительно, при измерении окулярмикрометром обнаруживается уменьшение диаметра большинства эритроцитов. Эритроцитометрическая кривая дает отклонение влево, т. е. в сторону микроцитоза, с более широким основанием, чем в норме, что объясняется присутствием единичных макроцитов (рис. 51). Однако при определении объема эритроцитов при помощи гематокрита получаются нормальные и даже повышенные цифры (до 128 мкм3 вместо нормальных 88 мкм3), что противоречит истинному микроцитозу. Кажущиеся малые размеры эритроцитов объясняются своеобразной сферической формой последних (так называемый сфероцитоз). Сфероциты имеют вид шарообразных, толстых и интенсивно окрашенных эритроцитов без центрального просветления.

Рис. 50. Больная О-ва. Врожденная микросфероцитарная гемолитическая анемия.
Другой отличительной особенностью врожденной гемолитической желтухи является резко пониженная резистентность эритроцитов по отношению к гипотоническим растворам поваренной соли. Начало гемолиза (минимальный гемолиз) соответствует 0,60—0,70 (вместо 0,48 в норме), конец (максимальный гемолиз) — 0,40 (вместо 0,32 в норме).
Наблюдения последних лет устанавливают тесную взаимосвязь обоих явлений — сфероцитоза и пониженной осмотической резистентности эритроцитов и их общую зависимость от условий среды. Как известно, двояковогнутая форма эритроцита поддерживается нормальным состоянием его оболочки. Когда под воздействием гипотонического солевого раствора или какого-либо лизина оболочка эритроцита повреждается, последний набухает и изменяет свою двояковогнутую форму на сферическую. При этом объем эритроцита увеличивается. Установлено, что и нормальные, имеющие двояковогнутую форму эритроциты под воздействием лизолецитина (весьма активный липоидный гемолизин, образующийся в селезенке и обнаруживаемый в нормальной сыворотке крови) набухают, увеличиваются в объеме (до 120 мкм3) и становятся сферичными. По достижении известного критического объема сфероцита его растянутая до предела оболочка становится проницаемой и лопается — наступает эритролиз.

Рис. 51. Кривые диаметров эритроцитов при врожденной микросфероцитарной гемолитической анемии.
В свете указанных данных сфероцитоз эритроцитов следует рассматривать как начальную стадию эритролиза.
Регенераторные симптомы со стороны эритроцитов достигают необычайной интенсивности в периоды гемолитических кризов. В эти периоды наблюдаются в большом количестве полихроматофильные эритроциты и даже нормобласты; количество ретикулоцитов превышает 50%; в отдельных случаях почти 100% эритроцитов являются ретикулоцитами (при учете и ретикулоцитов V группы (табл. 26).
Напомним, что ретикулоциты имеют нормальные и даже чуть увеличенные плоскостные размеры: 7,5—8,5 мкм и больше в диаметре при нормальной толщине. Следовательно, ретикулоциты являются как бы антиподами микросфероцитов, это — макропланоциты.
Между сфероцитозом и ретикулоцитозом не наблюдается параллелизма — напротив, в начальной фазе гемолитического криза, по мере того, как большинство эритроцитов становится сферическим, количество ретикулоцитов в периферической крови снижается. Обратная картина имеет место в конечной фазе гемолитического криза: в результате массивного распада эритроцитов отмечаются исчезновение сфероцитоза и повышение ретикулоцитоза как ответной реакции на повышенный распад крови. Соответственно динамике морфологических особенностей эритроцитов изменяется их осмотическая резистентность, понижаясь по мере сферуляции эритроцитов и повышаясь по мере их планизации.
Со стороны белой крови больших изменений не наблюдается: в течение гемолитических кризов возникает незначительный лейкоцитоз (до 10000—15000) с нейтрофилезом.
Количество тромбоцитов обычно варьирует в пределах нормы; иногда отмечается гипотромбоцитоз (ниже 100 000 в 1 мм3).
Костномозговое кроветворение. По данным стернальных пунктатов, оно обнаруживает чрезвычайно интенсивную реакцию нормобластического типа. Эритронормобласты составляют абсолютное большинство — до 60—70% всех костномозговых клеток. Вымывание эритроцитов из костного мозга совершается в ускоренном темпе, благодаря чему в периферическую кровь поступают главным образом незрелые формы эритроцитов — полихроматофилы и ретикулоциты первых групп. Гиперплазия эритробластических элементов костного мозга наблюдается не только в плоских костях и эпифизах длинных костей, но и в диафизах последних. Развивается экстрамедулярный эритропоэз в селезенке и в других органах (по данным пункционных биопсий).
Вслед за ретикулоцитарным кризом, когда большая часть нормобластов теряет ядра и поступает в периферическую кровь в виде ретикулоцитов, в костном мозгу обнаруживаются лишь родоначальные формы эритропоэза — базофильные эритробласты. В этой стадии костномозговой пунктат несколько напоминает картину «синего» костного мозга при обострении пернициозной анемии. Однако это сходство только кажущееся, так как при гемолитической анемии «синие» эритробласты переходят в нормобласты, а при пернициозной анемии — в мегалобласты. Последовательность изменений периферической крови и костного мозга при гемолитическом кризе может быть выражена в виде схемы.
Гемолитический криз
| Гематологические данные | Начальная фаза | Конечная фаза |
| Периферическая кровь | ||
| Ретикулоцитоз | + | +++ |
| Сфероцитоз | +++ | + |
| Понижение резистентности эритроцитов | +++ | ± |
| Костный мозг | ||
| Нормобластоз | +++ | + |
| Эритробластоз | + | +++ |
Наблюдения показывают, что анемия достигает особенно резкой степени в том случае, когда гемолитический криз не сопровождается ответной ретикулоцитарной волной, а в стернальном пунктате вместо эритробластоза обнаруживается картина острой эритробластопении — так называемый апластический (Gasser), вернее, арегенераторный (А. Г. Алексеев) криз. Отличием арегенераторного состояния от истинной аплазии костного мозга (эритробластофтиза) является его принципиально обратимый характер.
«Декомпенсация» гемолитического процесса, выражающаяся в развитии малокровия, возникает в связи с усилением распада крови и тормозящего влияния селезенки на костный мозг (вторичный гиперспленизм). В пользу такого предположения свидетельствует тот факт, что параллельно с развитием анемии снижается количество лейкоцитов и кровяных пластинок.
При гистологическом исследовании селезенки отмечается резкое кровенаполнение пульпы, тогда как венозные синусы бедны кровью. Основа пульпы, так называемые тяжи Бильрота, буквально нафарширована эритроцитами, которые захватываются селезеночными макрофагами. В результате повышенного гемолиза освобождается ,большое количество железосодержащего пигмента — гемосидерина, который откладывается в тканях (главным образом в той же селезеночной пульпе). Одновременно образуются безжелезистые продукты распада гемоглобина; по венозным синусам и селезеночной вене они поступают в печень в виде динамического (т.е. связанного с глобулина-ми) билирубина, который дает непрямую реакцию ван ден Берга.
Аналогичные, хотя и менее выраженные проявления эритрофагоцитоза и эритролиза с образованием гемосидерина и билирубина обнаруживаются также в купферовых клетках печени, костном мозгу, лимфатических узлах.
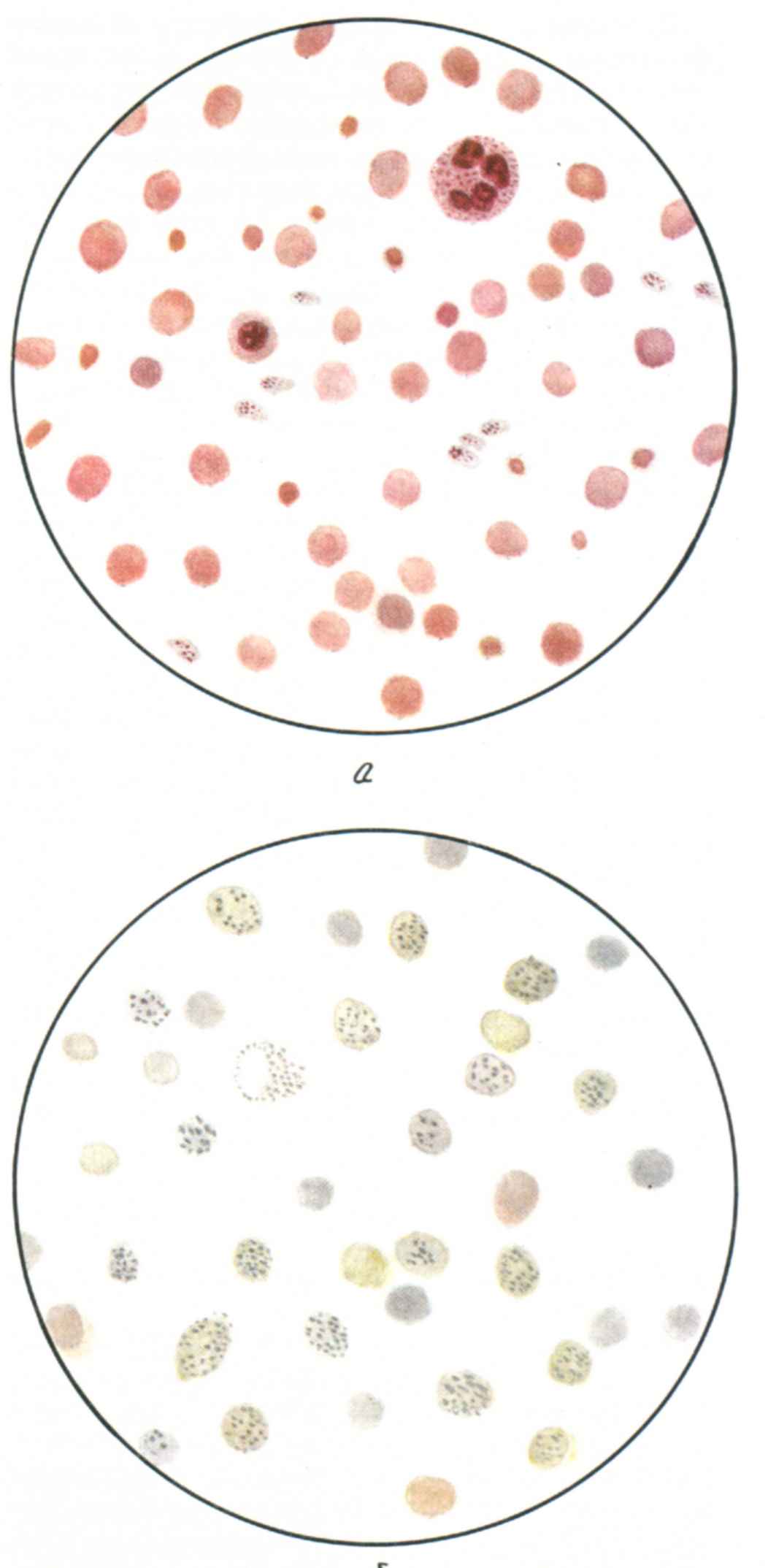
Табл. 26 а. Картина крови при микросфероцитарной форме гемолитической болезни. Преобладают микросфероциты. Ретикулоциты периферической крови в огромном количестве.
Патогенез. Основным патогенетическим фактором врожденной микросфероцитарной гемолитической болезни является повышенный распад ненормальных эритроцитов, вследствие чего нарушается физиологическое равновесие между эритропоэзом и эритролизом. В настоящее время не подлежит сомнению, что гемолиз в этих случаях является не внутрисосудистым, а внутриклеточным — он происходит в органах ретикуло-гистиоцитарной системы, главным образом в селезенке и в меньшей степени в купферовых клетках печени, костном мозгу и лимфатических узлах.
Согласно нашим наблюдениям (1949—1952), эритроциты в крови селезеночной вены (добытой во время спленэктомии) у больных сфероцитарной гемолитической анемией обладают более высокой осмотической резистентностью по сравнению с эритроцитами периферической крови. Этот факт подтверждает «отсеивающую» роль селезеночного фильтра, заключающуюся в том, что в селезенке происходит распад подготовленных к гемолизу осмотически нестойких сфероцитов.
Повышенное разрушение сфероцитов в селезенке обусловливается физическими особенностями последних — их пониженной осмотической и механической резистентностью. Толстые, набухшие эритроциты агглютинируются и с большим трудом проходят через узкие устья венозных синусоидов. Они задерживаются в селезеночной пульпе, где подвергаются воздействию селезеночного гемолизина — лизолецитина и захватываются селезеночными макрофагами. Последнее доказывается опытами с перфузией крови через экстирпированную селезенку непосредственно после операции — в селезеночной пульпе оказалось гораздо больше сфероцитов, чем в периферической крови.
Неполноценность эритроцитов при врожденной гемолитической болезни доказывается данными, согласно которым в сфероцитах понижено содержание гидрофильных коллоидов, солей калия и липоидного фосфора (лецитина). По данным Young и соавторов, основной генетический дефект эритроцитов при наследственном сфероцитозе заключается в нарушении ресинтеза аденозинтрифосфорной кислоты (АТФ) и (или) других фосфорных соединений, необходимых для поддержания нормальной двояковогнутой формы эритроцитов. По мнению Dacie, в основе врожденной неполноценности эритроцитов имеется еще мало изученная ферментная недостаточность, приводящая к расстройству внутриклеточного метаболизма углеводов и липоидов. Возможно, что пониженная осмотическая стойкость эритроцитов, вызывающая их преждевременную сферуляцию с последующим лизисом, связана с большей степенью потери липидов вызревающими эритроцитами.
Как показали японские исследователи (Nakao и соавторы), между энергетическим обменом эритроцитов и их формой существует тесная связь, осуществляемая за счет АТФ.
При наличии 50% исходного количества АТФ эритроциты сохраняют форму диска; при падении уровня АТФ ниже 10% от нормального эритроциты теряют ионы калия и становятся сферичными.
Существует предположение, что снижение уровня АТФ происходит в силу его ускоренного распада вследствие повышенной активности аденозинтрифосфатазы (АТФ-аза) — фермента, обеспечивающего проницаемость оболочки эритроцитов для ионов калия.
По данным современных авторов, в мембране эритроцитов содержатся актомиозиноподобные белки, обладающие контрактильной функцией и АТФ-азной активностью. На основании этого высказывается предположение, что нарушенный транспорт катионов при наследственном сфероцитозе связан с мутантным белком, а сферическая форма эритроцитов является результатом измененных контрактильных свойств данного белка.
Сфероцитоз и пониженная осмотическая стойкость эритроцитов при гемолитической болезни сохраняются и после оперативного удаления селезенки. Этим фактом, отмеченным нами (1949) и многократно подтвержденным другими авторами, опровергается учение о гиперспленизме как первичной причине гемолиза.
Продолжительность пребывания эритроцитов в циркулирующей крови при гемолитической болезни резко уменьшена. Средний срок пребывания эритроцитов в кровеносном русле может составить всего 12—14 дней (вместо нормальных 120—125 дней). Следовательно, для поддержания нормального состава крови при таком интенсивном ее распаде костный мозг должен обновить весь клеточный состав крови в предельно короткий срок — в течение 2 недель. В редких случаях гемолитической болезни повышенная эритропоэтическая функция костного мозга настолько перекрывает распад эритроцитов, что развивается даже полиглобулия. Когда же повышенная регенерация кровяных элементов в костном мозгу не в состоянии компенсировать массовое разрушение эритроцитов в селезенке, развивается малокровие.
Итак, основная роль в патогенезе семейной гемолитической болезни принадлежит врожденной неполноценности, resp. пониженной осмотической стойкости эритроцитов, приводящей через стадию сфероцитоза к их ускоренному разрушению в селезенке. Это положение, в частности, доказывается перекрестными опытами Dacie и Mollison, которые показали, что эритроциты здорового донора, перелитые больному со сфероцитозом, сохраняют нормальную продолжительность жизни (120 дней). Напротив, эритроциты-сфероциты больных врожденной гемолитической болезнью, в том числе больных в стадии клинической ремиссии после спленэктомии, перелитые здоровому реципиенту, быстро, в течение 14—20 дней, подвергаются полному разрушению. Те же эритроциты-сфероциты, перелитые здоровому человеку, у которого в связи с травмой была удалена селезнка, еще 32 дня спустя обнаруживаются в крови реципиента в большом количестве (Schrumpf). Таким образом, в силу создающихся после спленэктомии новых условий среды в организме срок пребывания малоустойчивых сфероцитов в кровяном русле значительно возрастает, приближаясь к нормальному сроку пребывания их в периферической крови. Поэтому, невзирая даже на некоторое викарное усиление кроворазрушающей функции других органов ретикуло-гистиоцитарной системы после спленэктомии, явления гемолитической желтухи и анемии резко уменьшаются и наступает практическое выздоровление.
Диагноз. Диагноз врожденной гемолитической болезни представляет порой известные трудности. Наиболее типичные проявления гемолиза — желтушность склер .и покровов — не всегда ярко выражены и могут быть не замечены врачом, особенно если осмотр больного производится при искусственном освещении. Для распознавания желтухи в вечернее время рекомендуется осматривать больного при свете синей лампы. Еще лучше пользоваться на приеме больных лампой дневного света.
Течение болезни циклическое; оно характеризуется чередованием обострений (кризов) и ремиссий.
Прогноз. Прогноз для жизни обычно благоприятный. Случаи смерти от обострения гемолитического процесса в период арегенераторного криза сравнительно редки. Смерть при гемолитической болезни может наступить от холангита (в связи с калькулезным холециститом) или от интеркуррентных инфекций. Своевременная спленэктомия резко снизила летальность.
Лечение. Единственным эффективным терапевтическим мероприятием при врожденной форме гемолитической болезни является спленэктомия. В принципе следует согласиться с положением, высказанным Cazal, что каждый случай врожденной гемолитической болезни показан для оперативного вмешательства (с точки зрения профилактики возможных осложнений). Практически, однако, доброкачественное течение болезни, а также, хотя и редкие, летальные исходы от операций ограничивают показания к операции. Спленэктомия безусловно показана при резкой анемизации и частых кризах, при инфарктах селезенки и приступах печеночных колик.
Спленэктомия срочно показана при остром гемолитическом кризе, вызванном внутриклеточным (селезеночным) гемолизом; чем больше анемизирован больной, тем неотложнее операция. Последнюю следует обязательно производить под защитой переливания крови.
Эффект спленэктомии проявляется немедленно, через несколько часов после удаления селезенки; уже на операционном столе количество эритроцитов циркулирующей крови увеличивается на 1 000 000 и более, что объясняется поступлением депонированной в селезенке крови в общее кровяное русло. Получающаяся таким образом «аутотрансфузия» не исключает необходимости дополнительного переливания крови после операции.
Спленэктомия приводит к быстрому исчезновению симптомов болезни — желтухи и анемии.
По выражению П. А. Герцена, «триумфом спленэктомии можно назвать результаты, полученные при гемолитической желтухе».
После спленэктомии в крови появляются сидероциты, причем этот симптом становится пожизненным; другие изменения крови, наступающие после спленэктомии: — гиперлейкоцитоз и особенно гипертромбоцитоз — носят временный характер.
У больных микросфероцитарной гемолитической анемией, подвергнутых спленэктомии, как правило, наступает полное клиническое выздоровление (исчезновение желтухи и анемии), хотя эритроциты пожизненно сохраняют патологические качества. У некоторых больных в течение ряда лет после произведенной спленэктомии эритроциты оказываются еще менее стойкими и более сферичными, чем до операции (наши наблюдения, рис. 52, табл. 27).
Факт прекращения повышенного гемолиза в организме после спленэктомии объясняется удалением органа, играющего главную роль в процессах кровяного распада.
Выключение селезеночного фильтра (в результате спленэктомии) способствует сохранению в кровеносном русле наименее устойчивых форм эритроцитов—сфероцитов, которые до операции задерживались в селезенке и, подвергаясь распаду, «выходили в тираж».
Иногда наблюдаются рецидивы болезни, однако в меньшей степени, чем до спленэктомии, ибо сохранившиеся в других органах ретикуло-гистиоцитарные элементы не в состоянии возместить выпавшую гемолитическую функцию селезенки. Патогенез рецидивов объясняется обычно викарной гиперплазией сохранившихся добавочных селезенок.
Переливание крови (эритроцитарной массы) при врожденной гемолитической анемии следует считать показанным в случае тяжелого гемолитического криза, при подготовке больного к операции (когда больной резко анемизирован) и в послеоперационном периоде. Гемотрансфузии нужно производить с обязательным учетом резус-совместимости.
При упорно рецидивирующих печеночных коликах показана спленэктомия (не холецистэктомия!), так как в связи с нормализацией повышенного гемолиза прекращается образование пигментных камней и исчезают симптомы псевдохолелитиаза. В случае показаний к холецистэктомии, диктуемых осложнением истинной желчнокаменной болезнью или холециститом, операция удаления желчного пузыря сочетается со спленэктомией.
После операции показано санаторно-курортное лечение минеральными водами (Железноводск).
Дата добавления: 2019-11-25; просмотров: 188; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
