Глава 6. ЭКОЛОГИЯ МИКРООРГАНИЗМОВ
Термин «экология» образован двумя греческими словами: oikos – дом и logos – наука. Экология – это всеобщая наука о биосфере, которая в настоящее время приобрела особое значение. По Э. Геккелю, предложившему в 1866г. этот термин, экология – это наука об отношениях организмов и окружающей среды.
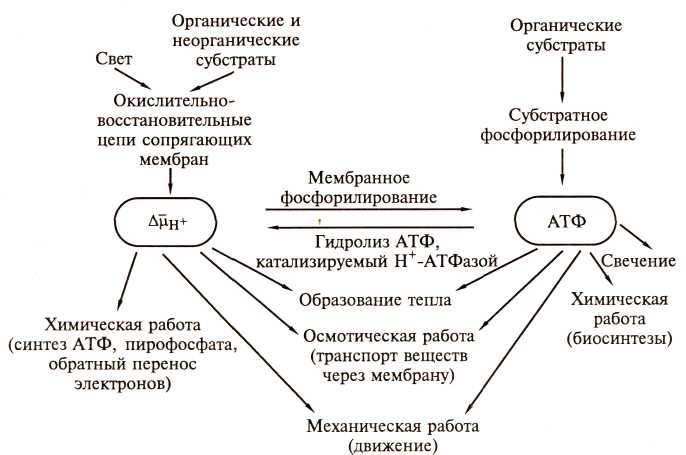
Рис. 30. Преобразование энергии в клетке прокариот (по Скулачеву В.П., 1980)
Степень приспособляемости вида к изменениям условий среды называют экологической валентностью. Экологической валентностью вида микроорганизмов также называют его способность заселять среду проявляющуюся определенными изменениями экологических факторов.
Таким образом, экология микроорганизмов – наука о взаимоотношениях микроорганизмов друг с другом и с окружающей средой.
Поскольку вероятность размножения некоторых патогенных микроорганизмов в окружающей среде не вызывает в настоящее время сомнений, возникают естественные вопросы: как они могут размножаться в столь различных условиях обитания, включающих организмы теплокровных животных и человека, с одной стороны, и объекты окружающей среды – с другой, какие генетико-биохимические механизмы определяют столь большие адаптационные возможности бактерий, такую широкую их метаболическую пластичность?
В современный период знания по экологии пополнились своеобразными научными фактами о механизмах выживания патогенных микроорганизмов в абиотических и биотических объектах окружающей среды, что дает новое объяснение теоретических положений эпизоотического процесса. Так, сравнительно недавно эпизоотологию признавали единственным источником возбудителя инфекции организм животного. Открытия последних лет, касающиеся механизмов выживания патогенных микроорганизмов в водной среде, в корне меняют это представление. Эти и другие вопросы пока не находили отражения в традиционных курсах и учебных пособиях.
|
|
|
6.
Влияние факторов внешней среды на микроорганизмы
Микроорганизмы находятся в тесной зависимости от условий окружающей среды. Благоприятные условия способствуют проявлению жизнедеятельности микроорганизмов, а неблагоприятные факторы могут привести к их гибели или изменчивости свойств. Факторы внешней среды принято делить на: 1) физические, 2) химические и 3) биологические.
Влияние физических факторов
Из физических факторов наибольшее влияние на микроорганизмы оказывают температура, влажность, излучение.
Температура
Жизнь организмов определяется температурой больше, чем каким-либо фактором внешней среды, в связи с тем, что все организмы построены из химических компонентов и все процессы жизни происходят на основе химических реакций, подчиненных законам термодинамики. Температура действует не только на скорость химических реакций, но также является причиной структурной перестройки протеинов, фазовых перемещений жиров, изменения структуры воды. Температурная амплитуда биохимической активности относительно мала в связи со специфическими свойствами биомолекул.
|
|
|
По отношению к температурным условиям микроорганизмы разделяют на мезофильные, психрофильные и термофильные. Деление бактерий на указанные группы довольно условно, так как температурные диапазоны их роста значительно перекрываются (рис. 31).
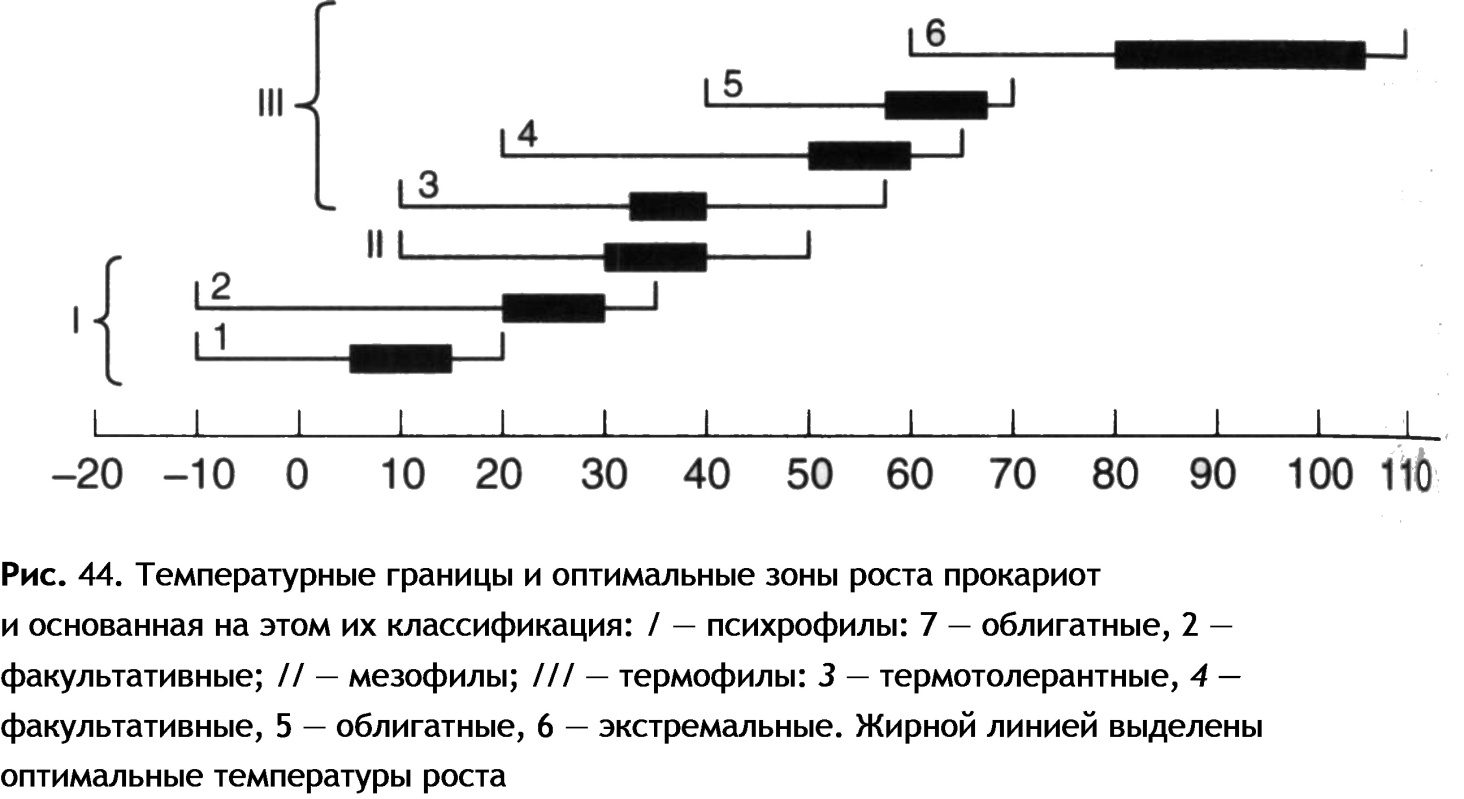
Рис. 31. Температурные границы и оптимальные зоны роста прокариот и основанная на этом их классификация: I. Психрофилы: 1 – облигатные; 2 – факультативные. II. Мезофилы. III.Термофилы: 3 – термотолерантные; 4– факультативные; 5 – облигатные; 6 – экстремальные. Жирной линией выделены оптимальные температуры роста (по Гусеву М.В. и Минеевой Л.А., 2003)
Большинство известных видов относится к мезофилам, у которых оптимальные температуры роста лежат между 30 и 40 °С, а температурный диапазон, в котором возможен рост находится между 10 и 45–50 °С. типичным мезофилом является E. сoli: нижняя граница роста +10 °С, верхняя +49 °С, оптимальная температура +37 °С при росте на богатой среде.
|
|
|
Психрофилы и факторы, определяющие возможность роста при низких температурах. Область температур роста психрофилов лежит в пределах от –10 до +20 °С и выше. В свою очередь психрофилы делятся на облигатных и факультативных.
Основное различие между подгруппами заключается в том, что облигатные психрофилы не способны к росту при температуре выше 20 °С, а верхняя температурная граница роста факультативных форм намного выше. Различаются они также и оптимальными температурными зонами роста, находящимися у облигатных психрофилов значительно ниже, чем у факультативных. Принципиальное же сходство между ними – способность к росту при 0 °С и минусовых температурах.
Термофилы и механизм термофилии. Группу термофилов делят на 4 подгруппы:
1. термотолерантные виды растут в пределах от 10 до 55–60 °С, оптимальная область лежит при 35–40 °С.
2. Факультативные термофилы имеют максимальную температуру роста между 50 и 65 °С, но способны также к размножению при комнатной температуре (20 °С).
3. К облигатным термофилам относят виды, обнаруживающие способность расти при температурах около 70 °С и не растущие ниже 40 °С.
|
|
|
4. Наконец, недавно обнаружены прокариоты, выделенные в подгруппу экстремальных термофилов. Для них характерны следующие температурные параметры: оптимум в области 80–105 °С, минимальная граница роста 60 °С и выше, максимальная – до 110 °С. К экстремальным термофилам относятся организмы из группы архебактерий, не имеющие аналогов среди мезофилов, например представители родов Thermoproteus, Pyrococcus, Pyrodictium и др.
Появились публикации об обнаружении бактерий, способных расти при температуре воды 250–300 °С и давлении 265 атм (при этом давлении вода в жидком состоянии может находиться до 460 °С). Эти бактерии выделены из проб воды поднятых с глубины 2560 м над поверхностью Тихого океана, где предположительно они существуют в горячих струях, выбрасываемых на дне океана так называемыми «черными гейзерами». Давление в районе обнаружения бактерий около 250 атм, а температура воды может быть выше 350 °С. в связи с этим исследователи начинают переоценивать границы условий, при которых способны развиваться прокариоты. Высказывается предположение, что прокариоты могут существовать везде, где есть вода в жидком состоянии и достаточное количество питательных веществ.
Высокая температура вызывает коагуляцию структурных белков и ферментов микроорганизмов. Большинство вегетативных форм гибнет при 60 °С в течении 30 мин, а при 80–100 °С – через 1мин. Для сохранения жизнеспособности относительно благоприятны низкие температуры (например, ниже 0 °С), безвредные для большинства микробов. Бактерии выживают при температуре ниже –100 °С; споры бактерий и вирусы годами сохраняются в жидком азоте. Простейшие и некоторые бактерии (спирохеты, риккетсии и хламидии) менее устойчивы к температурным воздействиям.
Воздействие высоких температур широко используется в лабораторной микробиологии – частной практике. Стерилизация (sterilis –бесплодный) объектов проводится методами автоклавирования, кипячения, тиндализации, пастеризации, фламбирования, стерилизации сухим жаром, паром без давления.
В хирургической практике стерилизуют инструменты, растворы, перевязочный материал.
Холодоустойчивость микроорганизмов
Организмы, способные образовывать тепло внутри своего тела с помощью различных физиологических и биохимических механизмов, называют эндотермными (эндотермы), а организмы, температура тела которых полностью зависит от температуры окружающей среды, т. е. определяется внешними источниками тепла – эктотермными (эктотермы).
Поддержание постоянства метаболизма у эктотермных организмов при смене температуры обитания названо температурной компенсацией. Генетико-биохимическая адаптация эктотермных организмов к изменению температурных условий обитания достигается разными путями: регуляцией экспрессии генов, изменениями функциональной активности ферментов, заменой одних изоферментов другими, изменениями концентрации ферментов в клетках и тканях и подвижностью жидкокристаллического состояния мембран.
Патогенные бактерии при выведении из теплокровного организма попадают в окружающую среду, где температура значительно ниже и перепад ее для бактерий может составлять до 30–35°С. С учетом узкого диапазона активности ферментов, становится понятным, что в этих изменяющихся условиях один фермент не способен функционировать. Эктотермные организмы могут синтезировать несколько форм ферментов, сходных по функции, но отличающихся молекулярной массой и приспособленностью к различным температурам. Синтез этих форм кодируется разными генными локусами и тогда они называются изоферментами (изозимами).
Возможен ли рост патогенных бактерий при низких температурах? Считалось, что патогенные микроорганизмы, будучи паразитами теплокровных животных и человека, температурный оптимум которых лежит в пределах 36–39°С, не могут размножаться при низких температурах и в связи с этим не способны обитать в окружающей среде. Почти все патогенные бактерии относятся к мезофилам. Однако большое количество видов бактерий, способных вызывать болезни животных, имеют широкий температурный диапазон роста (от 0 до 43–45°С). Например, Jersinia pestis может расти как при –2°С, так и при +40°С. J.pseudotuberculosis – от 0° до 40°С, L.monocytogenes – от 4 до 40°С, J.interocolita – от 0,5 до 42°С, B.anthracis способна к споруляции от 4 до 20 и 37°С и размножаться при 8°С. Возбудитель холеры размножается при 5°С, возбудитель туберкулеза – при 20–40°С.
Обнаружение патогенных бактерий (сальмонелл, шигелл, иерсиний, стафилококков, псевдомонад, клостридий, бацилл, листерий, клебсиелл, эшерихий, микобактерий) в почве, воде, иле, животных и растительных остатках позволяют проследить определенную закономерность: при понижении температуры ниже 20°С и при наличии достаточной влажности жизнеспособность перечисленных бактерий увеличивается многократно. Не образующие спор бактерии не способны длительно сохраняться при низкой температуре в окружающей среде без активного роста.
Таким образом, нет сомнений в том, что большое количество видов патогенных бактерий могут размножаться при биологически низкой температуре. Однако оптимум роста таких микроорганизмов. т. е. когда скорость размножения клеток наибольшая, сдвинут все же в сторону более высоких температур (22–30 °С).
Для факультативных паразитов, способных обитать не только в организме теплокровных, но и в окружающей среде, низкая температура столь же естественна, как и температура 37–39 °С.
Снижение температуры часто является причиной возникновения у бактерий способности к прототрофному питанию. В таких условиях проявляются сапрофитические свойства чумного микроба, позволяющие ему длительно сохраняться в окружающей среде. B. anthracis при перенесении штаммов, культивируемых на питательных лабораторных средах при температуре 37 °С, непосредственно в бурую лесную почву, где они росли при температуре 10–12 °С, они изменяли свои биохимические свойства. «Природный» субстрат и низкая температура индуцировали у B. anthracis синтез протеаз и лецитиназы, которые не свойственны микробу при высокой температуре.
Определение активности каталазы интактных микробных клеток Y. enterocolitica, L. monocitogenes, S. auereus, P. aeruginosa, E. coli, S. typhimurium, выращенных при 10 и 37 °С позволило установить, что низкая температура в 2–8 раз усиливает активность фермента – в зависимости от вида бактерий. Усиление каталазной активности при низкой температуре является общей закономерностью.
Анализ «холодовых» и «тепловых» вариантов культур по тесту коагуляции плазмы показал, что культуры, выращенные при 10 °С на МПБ коагулировали плазму в первые 30–60 мин. в то время как их «тепловые» варианты, выращенные при 37 °С, – лишь за 4–6 ч.
Температура оказывает регулирующее влияние на ряд свойств возбудителей. Основными свойствами бактерий, детерминируемыми хромосомным генетическим аппаратом, которые усиливаются при низкой температуре и реализуются на этапе инициации инфекции, являются подвижность, хемотаксис, высокий адгезивный потенциал, клеточная и тканевая инвазивность. При относительно высокой температуре обитания вне теплокровного организма эти свойства бактерий ослабляются.
Влажность
Важнейшим фактором поддержания жизни в микробной клетке является вода, в растворах которой протекают все процессы, составляющие жизнь. Нет другого природного тела, которое могло бы сравниться с водой по месту и значимости в процессах жизнедеятельности. Вода обладает совершенно уникальными свойствами, делающими ее неизменной составной частью организмов.
В условиях дефицита влаги некоторые бактерии образуют гидрофильные слизистые капсулы, активно поглощающие влагу.
При высушивании микроорганизмов часть клеток погибает. Клетки же, перенесшие высушивание, переходят в состояние анабиоза. Возможность сохранения бактериями жизнеспособности при высушивании определяется множеством факторов, в том числе зависит от температуры, рН, солевого состава среды и т.п. Обычно формы с мелкими клетками устойчивее, чем крупноклеточные формы; кокки устойчивее палочек. Клетки с толстой клеточной стенкой, в том числе большинство грамположительных бактерий, устойчивее к высушиванию, чем грамотрицательные бактерии и тем более микоплазмы. Особенно высокой устойчивостью к высушиванию характеризуются микобактерии, клетки которых окружены массивными клеточными стенками, содержащими большое количество липидов. Бактериальные цисты и споры устойчивее к высушиванию, чем вегетативные клетки.
Во время длительного сухого хранения в хромосомном аппарате происходят некоторые генетические сдвиги, что приводит к снижению жизненности и накоплению мутаций. На ряде микроорганизмов было доказано, что споры и суспензии бактерий выдержали без воды в течение 5 дней ультравысокий вакуум, приближающийся к тому, который имеется в межпланетном пространстве.
Успешное оживление после быстрого глубокого охлаждения при температуре –182 °С кусочков листьев, простейших и сперматозоидов позволило разработать фундаментальную теорию витрификации тканей, клеток и организмов. Гибель клеток происходит не в процессе охлаждения и витрификации, а в процессе согревания и девитрификации.
Витрификацию выдерживают только немногие мелкие организмы, быстрое охлаждение которых позволяет избегать кристаллизации воды в их теле при охлаждении и оттаивании, что нашло подтверждение в опытах с культурами бактерий кишечной флоры.
Высушиваниеиспользуется в различных технологических процессах для сохранения кормов, продуктов питания. При изготовлении биологических препаратов и сохранения чистых культур микроорганизмов пользуются методом лиофилизации (быстрое замораживание с последующим высушиванием под низким давлением).
Действие излучения
Солнечный свет может вызывать сильный антимикробный эффект. Так, более 99,9 % клеток штамма Escherichia coli с нарушенными репарационными механизмами погибают после облучения солнечным светом в течение трех минут. При этом более 80 % летальных повреждений связаны с действием света длиной волны менее 312 нм. Действие видимого света ответственно менее чем за 1 % летальных повреждений. Видимый свет длиной волны 450 нм индуцирует замены пар оснований и мутации сдвига рамки у E. coli. Световые волны длиной 550 нм и особенно 410 нм вызывают фотолизис клеток Myxococcus xanthus. Эффект определяется поглощением света железопорфиринами.
Ультрафиолетовые лучи и ионизирующее излучение
Ближний ультрафиолет (УФ) – излучение с длинной волн 400–320 нм – даже в невысоких дозах оказывает на бактерий определенное действие. Так, при освещении ближним УФ подвижных клеток E. coli или Salmonella typhimurium сначала наблюдается увеличение частоты кувырканий клеток, т. е. репеллентный эффект, но затем кувыркания полностью прекращаются и в конце концов наступает паралич жгутиков, т. е. свет нарушает механизмы движения и таксиса. В сублетальных дозах ближний УФ вызывает замедление роста культур, главным образом, за счет удлинения лаг-фазы. Скорость деления клеток также несколько снижается, подавляется способность бактерий поддерживать развитие фага и угнетается индукция ферментов. Эти эффекты определяются в основном поглощением УФ- лучей 4-тиоуридином – необычным основанием присутствующим в 8-й позиции у многих тРНК прокариот (но не у эукариот). Возбужденный светом 4-тиоуредин образует сшивки с цитозином, находящимся в 13-ом положении в тРНК, что препятствует связыванию тРНК с аминокислотами и приводит к увеличению образования гуанозинттрафосфата на рибосомах и к приостановке синтеза РНК соответственно и белка.
Средний УФ – это излучение с длинами волн 320–290 нм и дальний УФ – излучение с длинами волн 290–200 нм. Биологические эффекты действия среднего и дальнего УФ сходны.
УФЛ широко применяются в производственной деятельности человека для обеззараживания воздуха помещений (родильные дома, операционные, животноводческие помещения, промышленные цеха производства антибиотиков, лабораторные боксы), воды, отходов производств.
Ионизирующее излучение составляет определенный компонент естественной радиации, определяемый нестабильными изотопами, постоянно находящимися в почве, атмосферных осадках. В областях залегания радиоактивных минералов естественный фон радиации повышен. Изотопы могут попадать в живые организмы и тогда они подвергаются внутреннему облучению. Бактерии иногда способны накапливать некоторые элементы в очень больших количествах.
Ионизирующее излучение возникает также под влиянием космических лучей. Ионизирующие излучения также вызывают повреждения ДНК, которые принято подразделять на прямые и опосредованные, возникающие в связи с образованием свободных радикалов. Повреждения преимущественно представляют собой одноцепочечные или двухцепочечные разрывы молекулы ДНК.
В некоторых случаях удается обнаружить связь радиоустойчивости бактерий с особенностями ее местообитания. Так, микроорганизмы, выделенные из радоновых минеральных источников, оказываются в 3–10 раз более резистентными к радиации, чем организмы тех же видов, выделенные из нерадиоактивной воды. В охладительных системах ядерных реакторов, где средняя доза излучения превышает 106 ФЭР (физический эквивалент рентгена), обитают разные бактерии, в частности представители рода Pseudomonas.
Ионизирующее излучение используется для стерилизации биопрепаратов, перевязочного материала, инструментов.
Действие лазера вызывает у микроорганизмов в зависимости от дозы облучения изменения морфологических и биохимических свойств, вплоть до утраты жизнеспособности. Гибнут бактерии при воздействии лазера длинной волны около 700 нм с энергией 200 Дж. При этом происходит денатурация белка и повреждение нуклеиновых кислот.
Ультразвук. Поскольку бактерии обладают относительно малой массой и жесткой оболочкой, низкочастотные колебания (зона звуковых колебаний 100–10000 Гц) действует на них в очень слабой степени. Если же бактерии погрузить в жидкость, в которой распространяются высокочастотные колебания (т. е. ультразвук), то бактерии разрушаются и погибают. Ультразвуковые колебания обычно создают в жидкостях при помощи вибрирующих никелевых или кварцевых дисков. Существует мнение, что в большинстве случаев разрушение клеток при ультразвуковом воздействии, по-видимому, обусловлено образованием внутри клетки пены, состоящей из мельчайших пузырьков газа, находящегося обычно в растворенном состоянии в протоплазме или в жидкости на поверхности бактериальной клетки.
Бактерицидный эффект ультразвука уменьшается, если подавляется кавитация (разрыв жидкости), что происходит при дегазации, погружения объекта в гель или другую вязкую среду. Бактерицидный эффект ультразвука, напротив, усиливается при насыщении озвучиваемой эмульсии углекислотой, азотом, кислородом, воздухом, так, как это усиливает кавитацию.
Действие ультразвуковых волн не сводится только к механическим повреждениям клеток. В результате ультразвукового воздействия наблюдаются биохимические и функциональные изменения, не приводящие к гибели организма. Так, под воздействием УЗ могут высвобождаться в клетке биологически активные вещества (витамины, ферменты и пр.), а также появляться нехарактерные микроорганизму ферменты: у Saccharomyces globosus после 30 мин. воздействия УЗ частотой в 740 кГц появляется инвертаза, отсутствующая у неозвученных клеток, изменяется чувствительность к антибиотикам – у S. haemoliticus, подвергнутого воздействию ультразвука частотой в 800 кГц в течении 10 мин., чувствительность к пенициллину возрастает в 2–5 раз.
Ультразвук используют для получения отдельных клеточных компонентов, для изучения их структуры и функций, для стерилизации субстратов, повреждающихся при тепловой обработке.
К УЗ чувствительны все микроорганизмы, в том числе и споровые. Но по степени чувствительности к этому фактору они значительно отличаются. Так, УЗ легко разрушаются Salmonella typhimurium, Lactobacterium casei, Proteus vulgaris, Pseudomonas fluorescens, S. aureus, Bacillus anthracis. Несколько более устойчивы Sarcina urea, Saccharomyces cerevisiae, Acetobacter suboxydans. Среди патогенных форм наибольшую устойчивость к УЗ выявили Mycobacterium tuberculosis.
Магнитное поле
Все живые организмы находятся в области магнитного поля Земли. Воздействие дополнительными более мощными полями иногда приводит к стимуляции их роста. Так, воздействие магнитным полем напряженностью в 12, 103 А/м приводило к некоторому ускорению роста Pseudomonas aeriginosa, Staphilococcus epidermidis, Halobacterium salinarium. В магнитном поле напряженностью в 24, 103 или 50, 103 А/м наблюдали их угнетение. Замедление роста Micrococcus denitrificans наблюдали при 40, 104–64, 104 А/м, Staphilococcus aureus и Serratia marcescens – при 120, 104А/м. Действие переменных магнитных полей обычно более эффективно, чем постоянных. В естественной среде обитания бактерий магнитные поля такой напряженности не встречаются.
Молекулярный кислород
Молекулярный кислород явился мощным экологическим фактором, его накопление в атмосфере вызвало прогрессивную эволюцию одних организмов и гибель других.
Кислород широко распространен в природе, находясь как в связанном, так и в свободном состоянии. В первом случае он входит в состав молекул воды, органических и неорганических соединений. Во втором – присутствует в современной атмосфере в виде молекулярного кислорода (О2), объемная доля которого составляет 21 %. Кислород является обязательным химическим компонентом любой клетки. Подавляющее большинство организмов удовлетворяет свои потребности в этом элементе, используя обе формы кислорода.
Среди прокариот существуют значительные различия в отношении к молекулярному кислороду. По этому признаку они могут быть разделены на несколько групп (рис. 32). Прокариоты, для роста которых О2 необходим, называют облигатными (обязательными) аэробами. К ним относится большинство прокариотных организмов. Среди облигатных аэробов обнаружены существенные различия в отношении к уровню молекулярного кислорода в среде. Некоторые представители этой группы не способны к росту при концентрации О2, равной атмосферной, но могут расти, если содержание О2 в окружающей среде будет значительно ниже (порядка 2 %). Такие облигатно аэробные прокариоты получили название микроаэрофилов.
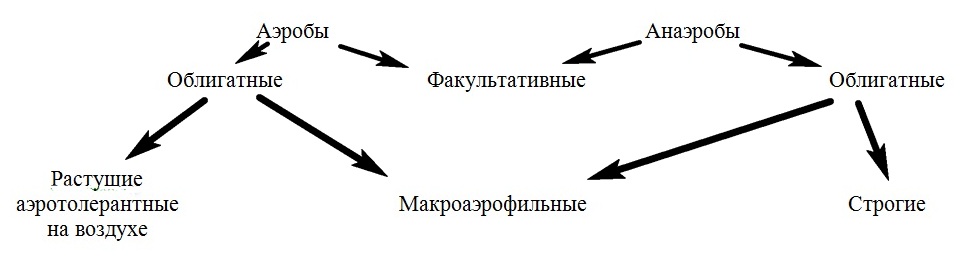
Рис. 32. Группы прокариот в зависимости от отношения к молекулярному кислороду
Облигатные аэробы (aeros – воздух) для осуществления процессов метаболизма нуждаются в молекулярном кислороде. Они не способны получать энергию путем брожения. Их ферменты осуществляют перенос электронов от окисляемого субстрата к кислороду. Аэробы развиваются, как правило на поверхности питательных сред. К облигатным аэробам относятся B. subtilis, микрококки и др.
Облигатные анаэробы не используют молекулярный кислород. Более того, он для них токсичен. Многие ферменты этих бактерий денатурируются при контакте с молекулярным кислородом.
Губительное воздействие кислорода на облигатные анаэробы обусловлено тем, что в живой клетке в присутствии кислорода образуется нероксид водорода, который в больших концентрациях ядовит для бактериальной клетки. облигатные анаэробы погибают при концентрации Н2О2 0,0003 %, тогда как аэробы выдерживают до 0,015 %, т. е. в 50 раз больше. Для обезвреживания пероксида водорода клетки аэробных бактерий вырабатывают фермент каталазу, разлагающую Н2О2 на воду и молекулярный кислород. Благодаря наличию каталазы Н2О2 не накапливается в клетках. У анаэробов и факультативных анаэробов каталаза отсутствует, что и является одной из причин их неспособности жить в аэробных условиях.
Значительное количество представителей анаэробных бактерий относится к роду Clostridium (C. tetani – возбудитель столбняка, C. botulinum – ботулизма, C. perfringens – возбудитель газовой гангрены). Они широко распространены в почве, озерных отложениях. Облигатные анаэробы принадлежат также к родам Methanobacterium, Bacteroides.
Факультативные анаэробы могут жить как при наличии, так и в отсутствии кислорода. Типичными представителями этой группы являются кишечная палочка, стрептококк, стафилококк. Кишечная палочка на среде с углеводами развивается как анаэроб, сбраживая сахара, а затем начинает использовать кислород, как типичный аэробный организм, окисляя до СО2 и Н2О образовавшиеся продукты брожения (например, молочную кислоту).
Степень аэробности или анаэробности среды может быть охарактеризована количественно при помощи окислительно-восстановительного потенциала. Окислительно-восстановительный потенциал выражают символом rH2. это индекс аналогичный рН. Но рН выражает степень кислотности и щелочности, а rH2 –степень аэробности и анаэробности. Это отрицательный логарифм концентрации атомов водорода в среде.
В водном растворе, полностью насыщенным кислородом, rH2 =41, а в условиях полного насыщения среды водородом rH2 =0. таким образом, шкала от 0 до 41 характеризует любую степень аэробности.
Облигатные аэробы, не способные существовать без свободного кислорода, не могут жить при низких значениях rH2. нижним пределом для них является окислительно-восстановительный потенциал порядка 10. однако и величины rH2 выше 30 для этих организмов не благоприятны. Облигатные аэробы защищаются от чрезмерного окисления выделением в среду сильных восстановителей.
Облигатные анаэробы жизнедеятельны при rH2 не выше 18–20. Однако при этих показателях они уже не размножаются, а осуществляют обмен веществ, приводящий к выделению в среду восстановителей для снижения окислительно-восстановительного потенциала. Размножаться анаэробы могут лишь при значениях rH2 не выше 3–5. факультативно анаэробные микроорганизмы сохраняют метаболическую активность в широком диапазоне rH2 – от 0 до 30.
Степень аэробности среды учитывается при культивировании микроорганизмов. При солосовании (консервировании) кормов искусственно создается анаэробные условия для обеспечения метаболических преимуществ бактериям молочнокислого и уксуснокислого брожений. Чрезмерная аэрация промышленных стоков животноводческих ферм позволяет активизировать окисление органического вещества стоков, в том числе и содержащихся в них микроорганизмов.
Влияние химических веществ
Концентрация ионов водорода
Кислотность среды является важным фактором, определяющим существование в ней прокариот. Концентрация ионов водорода в окружающей среде действует на микроорганизм или непосредственно, или косвенно, через влияние на ионное состояние и доступность многих ионов и метаболитов, стабильность макромолекул. Так, например, при низких значениях рН растворимость таких катионов, как Cu2+, Mo2+, Mg2+, Al3+, возрастает и достигает токсичных уровней. Наоборот, при высоких значениях рН растворимость многих катионов необходимых клетке (Fe3+, Ca2+, Mg2+, Mn2+), резко понижается, и они становятся недоступными для организма. От значения рН зависит состояние веществ в окружающей среде. Многие органические кислоты в кислой среде находятся в недиссоциированной форме и легко проникают в клетку, становясь токсичными для нее.
Значение рН, как известно, определяет кислотность и щелочность растворов и представляет собой отрицательный логарифм концентрации ионов водорода. Концентрация ионов водорода в чистой пресной воде 10-7 г* ион\л и, следовательно, рН пресной воды 7. Те значения рН, которые меньше 7, относят к кислотным, а те, которые выше 7, – к щелочным. Следует помнить, что рН – логарифмическая функция, поэтому раствор, который имеет рН 5, будет в 10 раз «кислее» раствора с рН 6.
Кислотность природных субстратов различна:
| Желудочный сок | 1 |
| Черноземные и каштановые почвы, сок креветки | 2 |
| Пресная вода | 7 |
| Щелочные почвы, экскременты животных, разлагающийся белок | 9 |
| Насыщенный раствор извести | 12 |
Границы значений рН, оптимальных для роста различных представителей прокариот, находятся в пределах приблизительно от 1 до 11. В зависимости от отношения к кислотности среды прокариоты могут быть разделены на несколько групп (см. рис. 33).
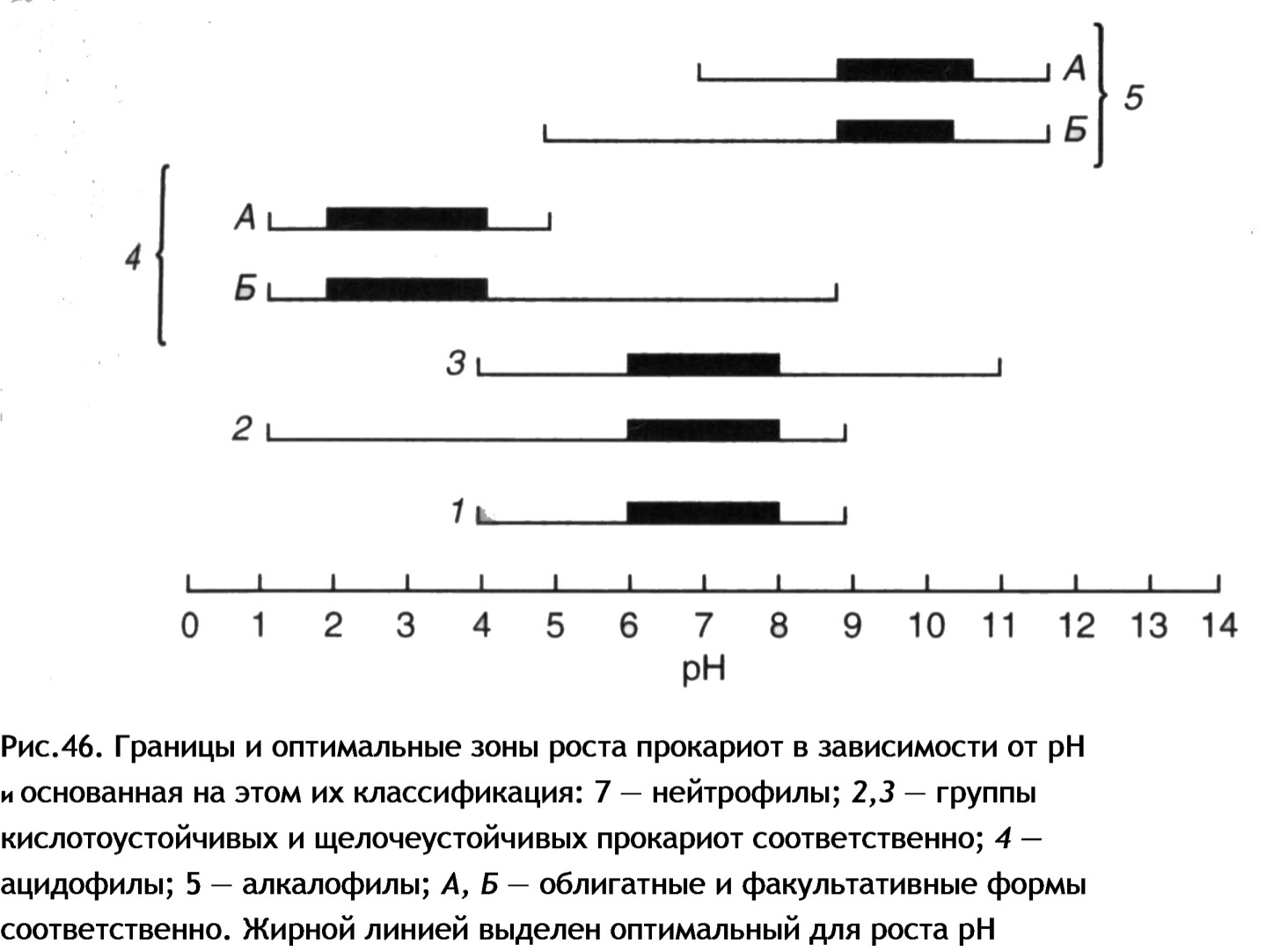
Рис. 33. Границы и оптимальные зоны роста прокариот в зависимости от рН и основанная на этом их классификация: 1 – нейтрофилы; 2, 3 – группы кислотоустойчивых и щелочеустойчивых прокариот соответственно; 4 – ацидофилы; 5 – алкалофилы; а, б – облигатные и факультативные формы соответственно. Жирной линией выделен оптимальный рН роста (по Гусеву М.В. и Минеевой Л.А., 2003)
Для подавляющего большинства прокариот оптимальной является среда, близкая к нейтральной. Такие организмы называют нейтрофилами.Однако рост многих нейтрофилов возможен в средах, значение рН которых лежит в диапазоне от 4 до 9. Типичными нейтрофилами являются штаммы Streptococcus faecalis и многие патогенные бактерии. Многие нейтрофилы способны расти или выживать при значениях рН, лежащих за пределами указанного диапазона. Такие прокариоты считаются кислото- или щелочеустойчивыми – толерантными. К кислотоустойчивым относятся многие грибы, микобактерии. Щелочетолерантны, т. е. устойчивы к значениям рН близким к 9–10, многие из энтеробактерий.
У некоторых видов бактерий адаптация к определенным значениям рН среды привела к тому, что оптимум рН для роста переместился в кислую (рН 4 и ниже) или щелочную (рН от 9 и выше) области. Такие прокариоты названы соответственно ацидо- или алкалофильными (кислото- или щелочелюбивыми) соответственно.
Способность к росту при низких или высоких значениях рН обеспечивает организму определенные преимущества, так как в этих условиях мала конкуренция со стороны большинства других организмов. Однако некоторые бактерии – облигатные формы – не просто переносят высокие концентрации Н+ или ОН`, но и нуждаются в этих ионах для роста и стабильности, т. е. это результат эволюционной адаптации.
В природе можно наблюдать развитие бактерий при рН от 1 до 11, тогда как диапазон значений рН их цитоплазмы варьирует в гораздо более узких пределах. Большинство типов белков и других макромолекул бактериальной клетки стабильны и активны в ограниченном диапазоне значений рН, близком к 7,0. Это справедливо и в отношении ферментов, изолированных из облигатных алкалофилов и ацидофилов. Поэтому для осуществления процессов жизнедеятельности бактерий необходимо поддержание стабильного значения рН внутри клетки (рНi), несмотря на изменения рН в окружающей среде (рН0) в более или менее широком диапазоне.
У всех известных ацидофилов значение рНi поддерживается около 6,5, у нейтрофилов – 7,5 и у алкалофилов – 9,5.
Коррекция рН среды проводится в микробиологической практике для создания благоприятных условий существования тех или иных культивируемых микроорганизмов.
Соединения и ионы, токсичные для бактерий
Полное отсутствие в среде токсических для организма веществ является событием, по всей видимости, крайне редким. Многие вещества могут быть полезными, индифферентными или вредными в зависимости от их концентрации в среде и конкретных условий существования организма. Есть и вещества, например, соли золота, урана, ртути и др., для бактерий не только бесполезные, но и угнетающие их даже в очень низких концентрациях.
Действие токсических для бактерий соединений может быть бактериостатическим или бактерицидным.
Бактериостаз (греч. bacterion – палочка, stasis – стояние на месте) – задержка роста и размножения бактерий, вызванная действием неблагоприятных химических или физических факторов. Прекращение действия фактора приводит к возобновлению роста и деления, хотя при длительном его воздействии может начаться гибель клеток, т. е. фактор проявляет бактерицидность (лат. caedere – убивать). Во многих случаях вещество в невысоких концентрациях обладает бактериостатическим, а в высоких бактерицидным действием. Присутствие в природных средах соединений, токсических для бактерий, приводит к уменьшению их видового разнообразия и появлению устойчивых форм.
Степень токсичности вещества для данной бактерии выражается через пороговую концентрацию, после достижения которой вещество становится бактерицидным, а также определяется его «концентрационной экспонентой» – n. После достижения пороговой концентрации токсичного вещества наблюдается полулогарифмическая зависимость степени отмирания клеток бактерий от времени, log числа погибших клеток находится в линейной зависимости от времени воздействия. Концентрационная экспонента n рассчитывается по формуле:
n = 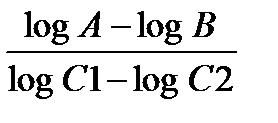 ,
,
где С1 – большая и С2 – меньшая концентрация вещества, А – время гибели определенной части клеток при концентрации С2, В – то же при концентрации С1.
Показатель n характеризует вещество, а не организм: n фенола 6, формальдегида и сулемы 1, этанола 9. Для фенола при n 6 разведение в 3 раза означает падение активности в 36, т. е. в 729 раз. Различия в чувствительности разных бактерий к определенному веществу зависят главным образом от значений их пороговых концентраций.
Химические вещества и физические факторы используются для воздействия на микроорганизмы с целью полного обеспложивания (стерилизации) объекта (субстрата) или для уменьшения числа микроорганизмов в/на объекте.
Система мер, полностью предотвращающих проникновение микроорганизмов в макроорганизм при ранениях, хирургических вмешательствах, называется асептикой. Обезвреживание микроорганизмов в ранах при помощи химических средств (раствора йода, перекиси водорода, калия перманганата, бриллиантового зеленого и др.) называется антисептикой (от греч. anti – против, septicos – гнилостный). Под дезинфекцией понимают комплекс мер, направленных на уничтожение на объектах внешней среды или удаления из них патогенных и условно-патогенных микроорганизмов. Для дезинфекции используют химические средства неспецифического действия, применяемые для обработки помещений, оборудования и различных предметов. Дезинфекция позволяет уменьшить число патогенных микроорганизмов на объектах внешней среды. Стерилизацией называют уничтожение всех видов и форм микроорганизмов в/на объекте.
В качестве химических средств асептики и антисептики, дезинфекции и стерилизации применяют кислоты, щелочи, окислители, хлорсодержащие препараты, органические соединения, соли тяжелых металлов, газы, галогены, красители, поверхностно-активные вещества, спирты и другие химические вещества и их смеси.
Антисептики (греч. anti – противо, septicos – гнилостный) – бактерициды, используемые в практической деятельности человека. Антисептики применяют в ветеринарии при лечении ран, в пищевой промышленности для защиты продуктов от порчи, для предохранения от гниения деревянных сооружений и т.п.
Антисептики относятся к различным группам органических и неорганических веществ. Окислители действуют на сульфгидрильные группы ферментов, окисляют активные группы белков.
Высокотоксичны для бактерий сильные окислители, многие из которых используют в качестве антисептиков. Это перекись водорода, перманганат калия, галогены, озон, оксид этилена и др. Для обеззараживания питьевой воды широко применяют озон и хлор. Хлор гидролизуется в воде с образованием хлорноватистой кислоты НОCl, которая обладает сильными бактерицидными свойствами.
Катионные антисептики – это разнообразные соединения, в молекулах которых присутствуют сильноосновные группы, связанные с липофильными участками. Уже в невысоких концентрациях эти вещества нарушают функции мембран, в частности работу мембранного АТФазного комплекса. Хлоргексидин, относящийся к этой группе веществ, находит практическое применение в ветеринарии.
Фенолыи их замещенные производные широко применяют как дезинфектанты, в меньших концентрациях – в качестве антисептиков. Препараты денатурируют белки и нарушают структуру клеточной стенки. От применения собственно фенола отказались давно вследствие его токсичности, но его производные (например, гексахлорофен, резорцин, хлорофен, тимол, салол) применяют часто.
Газы как дезинфектанты известны с глубокой древности. Двуокись серы еще в античности широко применяли для обработки складов и предохранения пищевых продуктов от порчи. Не менее широкое распространение получила дератизация двуокисью серы. Для уничтожения спор микроорганизмов при стерилизации инструментов из пластмасс применяют окиси этилена и пропилена под давлением при 30–60 °С. Метод позволяет эффективно уничтожить большинство микроорганизмов, в том числе в тканях и жидкостях (кровь, гнойное отделяемое). Механизм действия связан со способностью окиси этилена алкилировать белки. В частности, повреждению подвергаются сульфгидрильные группы вегетативных форм и карбоксильные группы оболочек спор.
Бактериостатическим, а при высоких концентрациях бактерицидным действием обладаюткрасители(риванол, бриллиантовая зелень, трипафлавин). Они задерживают рост бактерий за счет сродства к фосфорнокислым группам нуклепротеидов. Чувствительность различных форм бактерий к определенным красителям может существенно различаться, поэтому среды с красителями, например генцианом фиолетовым, метаниловым желтым, ализарином, оранжевым G и др., являются селективными и их используют в качестве диагностических и дифференциальных при выделении определенных бактерий.
Ионы тяжелых металлов в невысоких концентрациях стимулируют развитие тех или иных микроорганизмов, так как являются для них необходимыми микроэлементами, входящими в состав тех или иных ферментов. Стимуляцию развития микроорганизма иногда можно наблюдать и при невысоких концентрациях солей свинца, кадмия и других металлов, очевидно, не являющихся необходимыми микроэлементами. Например, кадмий в концентрации 20 частей на миллион стимулировал рост Lactobacillus acidophilus и в концентрации 5–10 частей на миллион – рост Streptococcus faecalis; хотя при концентрации 40 частей угнетал развитие обеих этих бактерий. Стимуляция метаболизма микроорганизмов невысокими концентрациями токсических соединений может объясняться так называемым эффектом Арндт-Шульца, заключающимся в том, что аккумуляция яда в нелетальных концентрациях на поверхности клетки изменяет проницаемость мембраны, нарушает ее барьерные функции, что определяет свободное поступление пищи в клетку и соответственно усилением метаболизма.
Действие ионов тяжелых металлов зависит от состава среды и природы соответствующих солей. Токсичность в сильной степени зависит от того, присутствует ли металл в виде свободного иона в растворе или в составе в основном недиссоциированной соли, а также входит ли данный элемент в состав органических или неорганических комплексных соединений.
Ионы тяжелых металлов способны соединяться с белками, нуклеотидами, коферментами, фосфолипидами, порфиринами, т. е. практически со всеми классами веществ, участвующих в метаболизме клетки. Ингибирование тяжелыми металлами активности металлоферментов может быть связано с замещением специфического катиона. Они обладают также олигодинамическим действием по отношению ко многим бактериям за счет действия положительно заряженных ионов этих металлов, абсорбирующихся отрицательно заряженной поверхностью бактерий. При этом изменяется проницаемость цитоплазматической мембраны, нарушается питание и размножение.
Спирты, илиалкоголи(этанол, изопропанол и др.). как антисептики, наиболее эффективны в виде 60–70 % водных растворов. Спирты осаждают белки и вымывают из клеточной стенки липиды. при правильном применении эффективны в отношении вегетативных форм большинства бактерий. Споры бактерий и грибов, а также вирусы к ним резистентны.
Галогены и галогеносодержащие препараты (препараты йода и хлора) широко применяют как дезинфектанты и антисептики. препараты взаимодействуют с гидроксильными группами белков, нарушая их структуру.
Как антисептики применяют йодсодержащие препараты – спиртовой раствор йода (5 % в этаноле); йодинол (1 % водный раствор содержит 0,1 % йода, 0,3 % калия йодида и 0,9 % поливинилового спирта, замедляющего выделение йода); йодонат (водный раствор комплекса поверхностно-активного вещества с йодом); повидон-йод (комплекс йода с поливинилпирролидоном) и раствор Люголя применяют для обработки слизистых оболочек.
Как дезинфектанты применяют хлорсодержащие препараты – газообразный хлор (взаимодействуя с водой, образует хлорноватистую кислоту; в присутствии органических веществ противомикробное действие уменьшается); хлорную известь (5,25 % NaClO, также образующую при растворении хлорноватистую кислоту); хлорамин Б (содержит 25–29 % активного хлора; для обеззараживания питьевой воды применяют в виде таблеток, содержащих 3 мг активного хлора).
Альдегидыалкилируют сульфгидрильные, карбоксильные и аминогруппы белков и других органических соединений, вызывая гибель микроорганизмов. Альдегиды широко применяют какконсерванты. Наиболее известные – формальдегид (8 %) и глутаральдегид (2–2,5 %) – проявляют раздражающие действие (особенно пары), ограничивающие их широкое применение.
Раствор формальдегидаобладает дезинфицирующим и дезодорирующим эффектами. Применяют для мытья рук, дезинфекции. Входит в состав препаратов (формидрон, мазь формалиновая). Мыльный раствор формальдегида (лизоформ) применяют для спринцеваний в гинекологической практике, для дезинфекции рук и помещений.
Уротропин (гексаметилентетрамин) в кислой среде организма расщепляется с выделением формальдегида; последний, выделяясь с мочой, оказывает антисептическое действие. Применяют при инфекционных процессах мочевыводящих и желчевыводящих путей, кожных заболеваниях. Входит в состав комбинированных препаратов (кальцекс, уробесал).
Кислоты и щелочи применяют как антисептики. Среди кислот наиболее известны борная, бензойная, уксусная и салициловая. Применяют для лечения поражений, вызванных патогенными грибами и бактериями. Наиболее распространена салициловая кислота, применяемая в спиртовых растворах (1–2 %), присыпках, мазях, пастах (например, для лечения дерматомикозов в областях, подверженных трению); оказывает также в зависимости от концентрации отвлекающее, раздражающее и кератолитическое действие. Из щелочей наиболее распространен раствор аммиака, применяемый для обработки рук хирурга (0,5 % раствор).
Металлы. Антимикробный эффект основан на способности осаждать белки и другие органические соединения. В качестве антисептиков широко применяют нитрат серебра (ляпис), сульфат меди (медный купарос) и хромат ртути (мербромин). Соединение металлов (особенно свинца, мышьяка и ртути) не рекомендуют применять для дезинфекции и антисептики, поскольку они способны накапливаться в организме.
Поверхностно-активные вещества (ПВА) (этоний, роккал, циригель) оказывают бактерицидное действие за счет нарушения проницаемости ЦПМ осмотического равновесия микробной клетки, что приводит к ее гибели. ПАВ являются соединениями четвертичных аммонийных оснований и используются в основном для обработки рук хирурга.
Бактериофаги
Бактериофагами называют вирусы бактерий. Явление бактериофагии изучали Н.Ф. Гамалея (1898), Ф. Творт (1915), Ф. д’Эрелль (1917). В результате агент, разрушающий бактерии, был назван бактериофагом (от греч. р hagos – пожирающий).
Бактериофаг способен инфицировать бактериальную клетку, репродуцироваться в ней, образуя многочисленное потомство, и вызывать ее лизис, сопровождающийся выходом фаговых частиц в среду обитания бактерий (рис. 34).
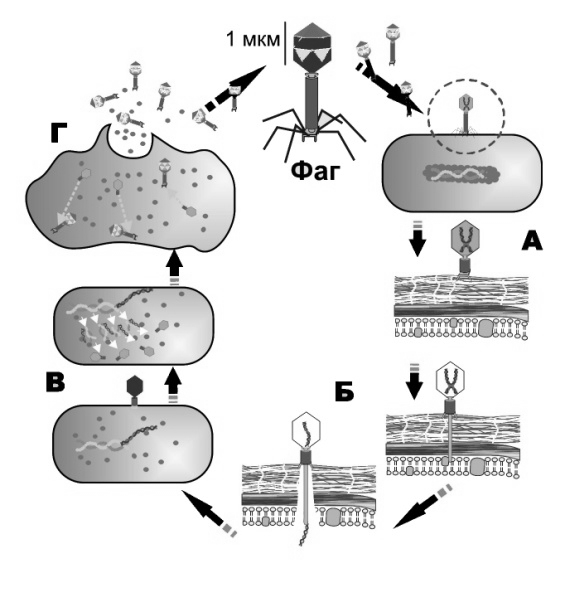
Рис. 34. Цикл развития бактериофага: а – адсорбция на бактерии, б – впрыскивание собственной ДНК внутрь бактерии, в – изменение наследственного кода бактерии и синтез бактериофагов, г – лизис бактерии и выход бактериофагов наружу
Бактериофаги широко распространены в почве, воде, экскрементах больных и здоровых животных, человека и обнаружены более чем у 100 видов бактерий.
Хозяевами бактериофагов являются ешерихии и сальмонеллы, стафилококки и стрептококки, микобактерии, листерии, коринебактерии и другие микроорганизмы. Процесс взаимодействия фага с клеткой протекает по типу продуктивной инфекции, или лизогении. В зависимости от этого различают вирулентные и умеренные фаги. Вирулентные фаги при проникновении в клетку бактерий размножаются в ней и вызывают лизис; умеренные фаги не вызывают лизиса, а остаются в состоянии лизогении.
По степени специфичности фаги разделяют на три группы: полифаги – лизируют родственные бактерии, монофаги – бактерии одного вида, а фаговары – только определенные варианты данного вида бактерий.
При контакте умеренного бактериофага с микробной клеткой последняя не лизируется и становится носителем бактериофага. Это явление получило название лизогении, а бактериальные культуры, обладающие этим свойством, называются лизогенными. Различают монолизогенность и полилизогенность.
Бактериальная культура, образующая один вид фага, является монолизогенной. Бактериальная культура, образующая несколько видов фагов, называется полилизогенной. Фаг способный лизогенировать клетку – хозяина, называется умеренным. При лизогении бактериофаг находится в состоянии профага, при котором бактериальная клетка не погибает. Профаг представляет собой геном вируса, ассоциированный с бактериальной хромосомой. Профаг в отличии от генома вирулентного фгага воспроизводится как часть бактериальной ДНК и синхронно с ней реплицируется.
Изменение свойств бактериальной культуры под влиянием фага получило название конверсии. Данный феномен заключается в приобретении лизогенными бактериями способности продуцировать токсины, изменять морфологию бактерий или их антигенные свойства. Наиболее изучена фаговая конверсия при образовании соматических антигенов у штаммов Salmonella.
В микробиологической практике бактериофаги используют для дифференциации бактериальных культур (сибиреязвенных, стафилококковых, рожистых, сальмонеллезных, колибактериозных и др.).
С помощью фага возможна также индикация патогенных бактерий во внешней среде (вода, выделения животных, пищевые продукты и другие субстраты) с помощью реакции нарастания титра фага.
Биологическая промышленность выпускает в жидкой форме коли-гертнерфаг против сальмонеллеза и колибактериоза телят, сибиреязвенные бактериофаги, фаг-гамму, фаг ВИЭВ и др.
Дата добавления: 2019-09-13; просмотров: 395; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
