Опыт 3. Дегидратация этанола.
В первую пробирку поместите 8 капель концентрированной серной кислоты, 10-12 капель этанола и несколько крупинок оксида алюминия. Закройте пробирку пробкой с газоотводной трубкой и конец трубки опустите во вторую пробирку с 4 каплями бромной воды. Нагревайте первую пробирку над пламенем спиртовки. Как только бромная вода начнет обесцвечиваться, немедленно опустите конец газоотводной трубки в заранее приготовленную третью пробирку с 1 каплей 2% раствора перманганата калия и 5 каплями воды. Продолжайте нагревание первой пробирки до обесцвечивания раствора КмпО4 в третьей пробирке. Затем удалите третью пробирку и подожгите у конца газоотводной трубки выделяющийся газ (горит светящимся пламенем).
Схема реакции:


Вопросы:
1. Опишите по стадиям механизм реакции внутримолекулярной дегидратации этанола.
2. Прогнозируйте продукт, который образуется в результате конкурентной реакции межмолекулярной дегидратации этанола.
Опыт 4. Цветные реакции фенолов с хлоридом железа (III).
Возьмите 5 пробирок. В первую пробирку поместите 3 капли фенола, во вторую – 3 капли 1% раствора пирокатехина, в третью – 3 капли 1% раствора резорцина, в четвертую – 3 капли 1% раствора гидрохинона, в пятую – 3 капли 1% раствора пирогаллола. В каждую из пробирок прибавьте по 1 капле 0,1н FeCl3. В первой пробирке появляется сине-фиолетовое окрашивание, во второй – зеленое окрашивание, в третьей – фиолетовое, в четвертой – зеленое, очень быстро переходящее в желтое (окисление гидрохинона в хинон), и в пятой – красное.
|
|
|
Схема реакции фенола с Fе3+:
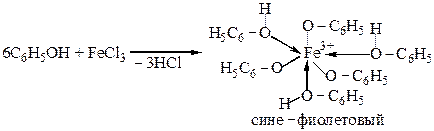
Вопросы:
1. Для каких целей используется данная реакция в качественном анализе?
2. Какие реакционные центры фенола участвуют в реакции фенола с хлоридом железа (III)?
Задачи для самостоятельного решения
1. Дайте систематическое название по заместительной номенклатуре IUРАС для каждого из приведенных соединений:

2. Напишите структурные формулы для каждого из следующих соединений:
а) 2-этоксипентан;
б) этилфениловый эфир;
в) N-метиламиноэтан;
г) трет.-бутиловый спирт;
д) пара-аминофенол;
е) диэтилсульфид.
3. Покажите графически распределение электронной плотности в молекулах пропанола, пропантиола, пропанамина. Сравните силу электрофильных центров пропанола и пропанамина. Приведите схему реакции взаимодействия с HCl наиболее активного из них. Опишите её механизм.
4. Сравните реакционную способность в реакциях SN1 и SN2 бутанола-1, бутанола-2 и 2-метилбутанола-2. Опишите для них механизмы реакций (SN1 и SN2), протекающих с галогеноводородами. Укажите стереохимические эффекты таких реакций.
5. Выделите реакционные центры в молекуле норадреналина и прогнозируйте продукты взаимодействия его с избытком НС1:
|
|
|

норадреналин
6. Этиловый спирт используют в промышленности для получения хлорэтана (средство для ингаляционного наркоза). Предложите реагент для такого превращения. Опишите механизм реакции.
7. Напишите схему превращения лимонной кислоты (3-гидрокси-3-карбоксипентандиовая кислота-1,5) в цис-аконитовую (3-карбоксипентен-2-диовая кислота-1,5). Предложите условия такого превращения. Опишите механизм реакции, объясните роль кислотного катализа.
8. В процессах метаболизма происходит ферментативное превращение яблочной кислоты (2-гидроксибутандиовая кислота) в фумаровую кислоту (транс-бутендиовая кислота). Напишите схему реакции и опишите её механизм.
9. В состав лекарственного препарата валидола входит ментол (2-изопропил-5-метилциклогексанол). Предложите продукты его превращения по схеме:
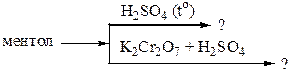
10. Цитраль используют в медицине для лечения заболеваний глаз. Его получают путем внутримолекулярной дегидратации 3,7-дигидрокси-3,7-диметилоктаналя. Напишите схему внутримолекулярной дегидратации, укажите условия реакции. Опишите механизм.
11. S-аденозилметионин (СН3 – SÅR1R2) является универсальным донором метильных групп для биосинтезов. С его участием происходит метилирование аминов. Предложите механизм метилирования коламина по схеме:
|
|
|
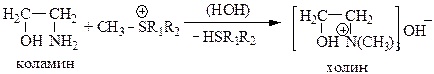
12. При b-окислении высших жирных кислот в организме протекают последовательно реакции гидратации и окисления по схеме:

Напишите схемы реакций, укажите продукты.
13. Гераниол, входящий в состав эфирных масел герани и розы при мягком окислении образует цитраль (гераниаль). Напишите схему реакции образования цитраля.

14. 3¢-фосфоаденозин-5¢-фосфосульфат (ФАФС или ФАФ-SO3H) является источником подвижных сульфатных групп, используемых для коньюгации природных соединений и ксенобиотиков с целью образования эфиров серной кислоты – растворимых продуктов метаболизма или нетоксичных и легко выводимых продуктов превращения лекарственных соединений. Сульфатной коньюгации подвергаются природные вещества (стероиды, токоферолы), эндогенные токсины, такие как фенолы, нафтахиноны. Прогнозируйте продукт сульфатной коньюгации стероидного андрогенного гормона андростерона:

15. Одним из путей метаболизма биогенных аминов – серотонина, гистамина и др. – является N-ацетилирование этих соединений с участием ацетилкофермента А. Прогнозируйте продукт N-ацетилирования гистамина, назовите реакционные центры, которые участвуют в этой реакции. Укажите тип и механизм реакции.
|
|
|

ЗАНЯТИЕ 7
РЕАКЦИОННАЯ СПОСОБНОСТЬ АЛЬДЕГИДОВ И КЕТОНОВ. РЕАКЦИИ AN И AN - E У ТРИГОНАЛЬНОГО АТОМА УГЛЕРОДА.
ЦЕЛЬ: Сформировать знания:
– электронного строения оксогруппы и реакционных центров альдегидов и кетонов;
– реакционной способности альдегидов и кетонов в реакциях нуклеофильного присоединения;
– механизма реакций AN и AN-E;
– реакций окисления.
Сформировать умения:
– выделять реакционные центры альдегидов и кетонов, исходя из взаимного влияния атомов;
– сравнивать реакционную способность альдегидов и кетонов в реакциях AN;
– писать по стадиям механизмы AN и AN-E;
– выполнять характерные и качественные реакции на альдегиды и кетоны.
ВОПРОСЫ ДЛЯ САМОПОДГОТОВКИ К ЗАНЯТИЮ:
1. Электронное строение оксогруппы. Реакционные центры альдегидов и кетонов.
2. Сравнение реакционной способности альдегидов и кетонов в реакциях нуклеофильного присоединения (AN). Механизм реакций нуклеофильного присоединения: гидратация, восстановление, реакция со спиртами (ацетализация) и тиолами. Гидролиз ацеталей, кислотный катализ.
3. Реакции присоединения – отщепления (AN-E). Взаимодействие альдегидов и кетонов с аммиаком, аминами. Гидролиз аминов.
4. Реакции с участием С-Н-кислотного центра: альдольное присоединение, голоформные реакции. Основной катализ. Альдольное расщепление. Биологическое значение этих процессов.
5. Окисление альдегидов, реакция диспропорционирования.
ЛИТЕРАТУРА
[1]. Тюкавкина Н.А., Биоорганическая химия. / Н.А.Тюкавкина, Ю.И. Бауков– М.: Медицина, 1991.– С. 181-194.
[2]. Гидранович Л.Г. Биоорганическая химия: Учеб. пособие. /Л.Г.Гидранович. – Витебск: ВГМУ, 2009.– С. 114-124.
[3]. Гидранович Л.Г. Лабораторные занятия по биоорганической химии.: Учеб. пособие / Л.Г.Гидранович. – Витебск: ВГМУ, 2012.– С. 49-56.
[4]. Гидранович Л.Г. Курс лекций по биоорганической химии.– Витебск.– 2003.– С. 94-103.
Дата добавления: 2019-09-13; просмотров: 917; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
