Изменения ядерного индекса
Ядерный индекс – это важнейший гематологический показатель, отражающий соотношение количества НФ разной степени зрелости, оцененное по структуре их ядер. Он рассчитывается как отношение всех незрелых форм к сегментоядерным НФ и колеблется от 0,06 и 0,1. Увеличение числа молодых нейтрофилов, когда индекс более 0,1, называется ядерным сдвигом влево. Преобладание сегментоядерных нейтрофилов (ядерный индекс менее 0,06) – сдвиг влево.
Лейкемические сдвиги влево:
1. Простой (гипорегенераторный) сдвиг влево – умеренное повышение в крови количества палочкоядерных НФ при сохранении баланса лейкоцитарной формулы. Причина: начальные стадии (или умеренное течение) гнойных инфекций;
2. Регенеративный сдвиг влево – в крови появляются метамиелоциты, лейкоцитоз (12-25). Прогноз всё еще благоприятен, потому что у ККМ достаточно резервов для новой мобилизации. Причина: тяжелые и относительно тяжелые бактериальные инфекции;
3. Гиперрегенеративный сдвиг влево – крайняя стадия гранулопоэтического ответа, с дисбалансом лейкоцитарной формулы, относительной моноцитопенией и лимфопенией (и абсолютным лимфоцитозом). В крови более половины незрелых форм, появляются миелоциты. Причина: тяжелые затяжные септические инфекции.
4. Регенеративно-дегенеративный сдвиг влево – это продолжение стимуляции миелопоэза на фоне истощения его ресурсов. Последние молодые формы дозревают до палочко- и сегментоядерных и покидают лейкоцитарную формулу. Весь гранулоцитопоэз уходит на производство нейтрофилов, наблюдается глубокая относительная и абсолютная агранулоцитопения. Причина: длительные и тяжелые инфекционные процессы.
|
|
|
5. Дегенеративный сдвиг влево – полное истощение миелопоэтического ростка. На фоне отсутствия молодых форм падает количество зрелых, в оставшихся наблюдаются дегенеративные изменения ядер и цитоплазмы. Причина: тяжелые, зачастую терминальные стадии длительных инфекционных процессов.
Лейкемические сдвиги вправо:
Это снижение относительного содержания палочкоядерных НФ по сравнению с нормой. Отличием от сдвигов влево здесь будет отсутствие длительной стимуляции миелопоэза и вариабельное количество сегментоядерных НФ. Причина: первичная недостаточность гранулоцитопоэза или первичная костномозговая недостаточность, а конкретнее – апластические анемии, мегалобластозы и т.п.
Билет№ 183
Лейкозы. Этиология и патогенез. Роль онкогенов. Факторы, способствующие анормальной экспрессии онкогенов. Принципы классификации лейкозов. Экспериментальные модели лейкозов.
Лейкозы – опухолевые заболевания кроветворной и лимфоидной ткани, представляющие собой новообразования первично костномозгового происхождения.
Являются заболеваниями клонального происхождения: лейкозные клетки представляют клон — потомство одной первоначально трансформированной кроветворной клетки.
|
|
|
Этиология
Лейкозыявляются полиэтиологическими заболеваниями.
- Ионизирующее излучение
Установлена связь между радиационным поражением и развитием острого и хронического миелолейкоза, острого эритромиелолейкоза и острого лимфобластного лейкоза у детей.
В клетках появляется кольцевидная хромосома - цитогенетический маркер радиационного поражения.
- Химические канцерогены
Бензол, использование цитостатических препаратов(мелфалан, азатиоприн, лейкеран, миелосан, левомицетин) может приводить к возникновению острого и хронического миелолейкоза, острого миеломонобластного лейкоза и эритромиелоза.
- Вирусы
вирус Эпштейна-Барра - лимфома Беркитта
«вирус T-лимфоцитарного лейкоза - лимфомы человека», полученного из Т-клеток грибовидного микоза.
В большинстве же случаев внедрение вирусных онкогенов в клетку вызывает ее иммортализацию (бессмертие), это способствует дальнейшим перестройкам генома, ведущим к злокачественной трансформации.
|
|
|
Патогенез
- Инициация
первоначальное изменение генома: хромосомные нарушения, в результате которых протоонкоген становится онкогеном. - Промоция
инициация стимулирует последующие накопления онкогенов в клетке, приводящее к трансформации (так называемый многоступенчатый канцерогенез).
Нестабильность генома лейкозных клеток, появление новых генетических дефектов, приводит к появлению в первоначальном опухолевом клоне новых субклонов, наиболее устойчивых к условиям среды при метастазировании и лечению. Этим объясняют необратимый характер течения лейкозов, генерализацию процесса, что и составляет суть опухолевой прогрессии, свойственной злокачественному росту.
Перестройки хромосом и формы лейкоза:
- транслокации (8; 21) и (6; 9) встречаются при миелобластном лейкозе
- t(15; 17) — при промиелоцитарном
- t(9; 11) — при монобластном
- t(4; 11) — при лимфобластном лейкозе
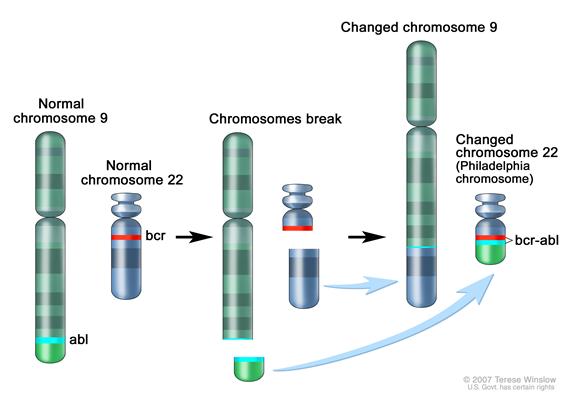
- t (9;22) - Филадельфийская хромосома (Ph'):
результат соединяющей протоонкоген abl хромосомы 9 с последовательностью bcr на хромосоме 22 - образуется новый ген-гибрид, белковый продукт которого обладает тирозинкиназной активностью.
В результате синтезируется одна из двух bcr-abl аномальных тирозинкиназ – р210 (при хроническом миелолейкозе) или р190 (при остром лимфобластном лейкозе взрослых).
|
- Опухолевая ткань первоначально разрастается в костном мозге, постепенно замещая нормальные ростки кроветворения:
- анемия
- тромбоцитопения
- лимфопения
- гранулоцитопения. - Метастазирование в различные органы: печень, селезенка, лимфатические узлы и др.
Инфильтрирование лейкозными клетками - обтурация сосудов - инфаркты, язвенно-некротические осложнения.
Клиника
Одинакова для всех типов острых лейкозов:
Начало заболевания - внезапное.
Состояние больного – тяжелое (интоксикация, геморрагический синдромом, дыхательная недостаточность - увеличение лимфоузлов – сдавливание дыхательных путей).
Возможно и постепенное развитие заболевания:
потеря аппетита, снижение трудоспособности, боли в костях, суставах, опухолевидные образования в области шеи, подмышечных впадинах (обусловленные увеличением лимфатических узлов).
Дата добавления: 2016-01-04; просмотров: 31; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!