Комплексообразующие реагенты.
Основные принципы поиска комплексобразующих реагентов – те же что и в аналитической химии.
Используют промышленно только 3 реагента: ИМ-50 - смесь гидроксамовых и карбоновых кислот С7-С9. Применяют при флотации руд редких металлов, и оловянных. Содержит не менее 75% гидроксамовых кислот, и не более 10% карбоновых. Гидроксамовые кислоты – слабые (рК=9,65-9,67), существуют в двух таутомерных формах:

С катионами железа гидроксамовые кислоты образуют прочные поверхностно-активные комплексы окрашенные в ярко-красный цвет.
Аспарал-Ф – реагент для флотации касситерита, флюорита. Это тетранатриевачя соль N-октадецил-N-сульфосукциониласпарагиновой кислоты:

Аспарал-Ф получают в виде 35%-ного раствора (выход 94-95%) из гексадециламина С16Н37NH2 и диэтилмалоната.
Флотол 7,9 – селективный собиратель при флотации оловосодержащих руд и плавикового шпата из бедных кварцево-оловяных и полевошпатовых руд при рН =3-5. 50-60%-ный водный раствор динатриевых солей смеси 1-оксиалкилен-1,1-дифосфоновых кислот С7-С9:

Получается из фракции синтетических жирных кислот С7-С9 и РCl3.
Был испытан и показал хорошие результаты при флотации фосфорсодержащих руд. Отрицательные стороны – нестабильность процесса получения, токсичное вещество.
Фофоновые кислоты – используют дляфлотации олова зарубежом, например, стирилфосфоновая кислота.
В отличие от гидроксамовых и жирных кислот фосфоновые кислоты – двухосновные, и значительно более сильные. Связи Р-О легче поляризуются, чем С-О. В полярной группе содержатся два отрицательнозаряженных атома кислорода, вседствие этого фосфоновые кислоты образуют более прочные комплексы с катионами железа и германия и высокозарядными катионами (олово, редкоземельные металлы). С щелочноземельными элементами они дают значительно более слабые комплексы. Стирилфосфоновая кислота не образут труднорастворимых икомплексных солей с ионами кальция и магния в разбавленных растворах.
|
|
|
МИГ-4Э – собиратель, имеющий в молекуле ацетиленовую группировку. Этинилвинилбутиловыйэфир был применен при флотации медно-молибденовых руд.
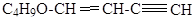
В качестве комплексообразующих собирателей целесобразно использовать вещества, образующие труднорастворимые комплексные соединения. Это могут быть внутрикомплексные соединения – неэлектролиты и электролиты. Последние – это комплексные ионы. Например,
внутрикомплексное незаряженное соединение меди:
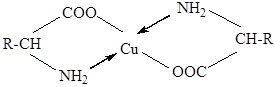
Химическая стабильность внутрикомплексных соединенйи определяется рядом факторов: электронным строением комплексообразующего иона, сторением и химической природой лиганда, количеством циклов, напряженностью циклических структур.
|
|
|
На рисунке изображены 3-х, 4-х, 5-ти и 6-ти членные циклы.
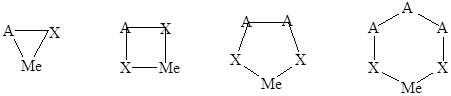
Х – замещающая группа – лиганд (обычно анион или нейтральная молекула);
А – молекулярный остаток;
Ме – ион металла.
Ион – комплексобразователь – акцептор электронов от лиганда должен иметь недостроенную электронную оболочку или 18—электронные внешние оболочки (наибольшая тенденция к комплексообразованию).
Стереохимия атома, т.е. направленность ковалетных связей зависит от числа связывающих и неподеленных пар на валентной оболочке. Шесть связей имеют отаэдрическую напрвленность. Четыре – тетраэдрическую направленность, три – пирамида или плоскость.Для большинства комплексообразующих ионов координационное число является переменным, зависит от природы этих ионов и лигадов. Некоторые характеризуются постоянным координационным число: КЧ=6 максимальное и наболее часто встречающееся.
При образовании внутрикомплексных соединеий должны быть соблюдены правила для лиганда:
Атом, связывающийся с металлом должен иметь по крайней мере одну пару электронов, которую он отдаст металлу. Практически эту роль могут играть только азот, кислород и сера.
|
|
|
Комплексообразование имеет место лишь в тех случаях, когда лиганд находится вблизи катиона и образует цикл. Максимум устойчивости у пяти-шестичленных циклов. В результате больших напряжений 3,4-членные циклы не устойчивы, а для больших циклов трудность в том, что уменьшается вероятность столкновения групп между собой с образованием цикла.
Существуют полидентатные лиганды. Чем больше циклов образуется, тем больше выигрыш энергии.
Комплексные соединения характеризуются константой устойчивости или нестойкости.
Органические вещества, способные образовывать внутрикомплексные соединения должны отвечать следующим требованиям:
В молекуле должны одновременно присутствовать солеобоазующая и комплексообразующая группы.
Взаимное расположение этих групп должно быть таково, чтобы имелась возможность образования 5,6-членых циклов.
Молекула реактива должна иметь большую молекулярную массу и обладать легкой деформируемостью электронных оболочек.
РЕАГЕНТЫ-ПЕНООБРАЗОВАТЕЛИ
Основным назначением реагентов-пенообразователей является увеличение дисперсности и стабилизации пузырьков воздуха в пульпе и повышение устойчивости пены, насыщенной частицами флотируемого минерала. Кроме основного действия пенообразователи замедляют всплывание пузырьков, а иногда влияют на собирательное действие реагентов и прочность прилипания частиц к пузырькам.
|
|
|
Дата добавления: 2018-10-26; просмотров: 684; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
