Молекулярная физика и термодинамика
Базовые понятия, законы и определения физических величин
Абсолютная влажность – количество водяных паров (в граммах), содержащихся в 1 м3 воздуха.
Влажность воздуха – содержание водяного пара в воздухе, определяющее характеристики погоды и климата.
Внутренняя энергия системы – это энергия системы, которая однозначно определяется ее термодинамическим состоянием. Внутренняя энергия системы включает в себя энергию хаотического движения всех микрочастиц системы и потенциальную энергию их взаимодействия. Во внутреннюю энергию системы не входит кинетическая энергия движения системы как целого и ее потенциальная энергия во внешнем силовом поле.
Изменение внутренней энергии 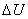 при переходе системы из состояния 1 в состояние 2 не зависит от вида процесса и равно
при переходе системы из состояния 1 в состояние 2 не зависит от вида процесса и равно 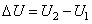 .
.
Второй закон термодинамики – закон возрастания энтропии, определяет направление происходящих в природе процессов и утверждает: в замкнутой системе энтропия либо остается неизменной (если в системе протекают равновесные обратимые процессы), либо возрастает (при неравновесных процессах) и в состоянии равновесия достигает максимума. Другие формулировки утверждают:
1.невозможен переход теплоты от тела менее холодного к телу более нагретому без каких-либо изменений в системе или в окружающей среде;
2.невозможно создать периодически действующую машину, единственным результатом работы которой было бы поднятие груза и охлаждение теплового резервуара.
|
|
|
Второй постулат термодинамики ("нулевое начало термодинамики") утверждает существование температуры как особой функции состояния равновесной системы.
Давление Лапласа – давление, обусловленное существованием сил поверхностного натяжения и искривленной поверхностью жидкости.
Диаграмма состояния – графическое изображение соотношения между параметрами состояния термодинамической равновесной системы. Обычно применяют проекции диаграммы состояния на одну из координатных плоскостей при постоянном значении остальных параметров.
Замкнутым процессом, или циклом называется такой процесс, по завершении которого система возвращается в исходное состояние.
Идеальная газовая шкала температур (шкала Кельвина) – шкала, установленная на основании уравнения Клапейрона–Менделеева. В качестве термометрического тела берется идеальный газ, а в качестве температурного параметра – произведение давления на объем. Согласно уравнению состояния идеального газа при температуре Т = –273,16 °С это произведение должно быть равно нулю. Эта температура есть абсолютный нуль температуры. Шкала, по которой отсчет температуры ведется от абсолютного нуля, называется идеально-газовой абсолютной шкалой. По определению этой шкалы существование температуры ниже абсолютного нуля невозможно. При абсолютном нуле тела и частицы, из которых они построены, обладают наименьшей возможной энергией. Это означает, что кинетическая энергия равна нулю, а потенциальная имеет наименьшее возможное значение.
|
|
|
Изопроцессы – термодинамические процессы, протекающие при неизменном значении какого-либо параметра состояния.
Испарение – процесс парообразования, происходящий со свободной поверхности жидкости.
Карно цикл– это прямой круговой равновесный процесс, состоящий из двух изотерм и двух адиабат. Как цикл тепловой машины, он обладает оптимальными свойствами и наибольшим значением КПД в заданном интервале температур нагревателя и холодильника.
Кипение – процесс интенсивного испарения жидкости не только с ее свободной поверхности, но и по всему объему жидкости внутрь образующихся при этом пузырьков пара.
Количество теплоты определяет изменение состояния термодинамической системы, происходящее в процессе теплообмена между системой и внешними телами. Количество энергии, переданное системой (системе) в процессе теплообмена, называется количеством теплоты. Теплота считается положительной, если она передается от внешних тел системе, и отрицательной, если она передается от системы внешним телам.
|
|
|
Коэффициент поверхностного натяжения равен:
1. силе поверхностного натяжения, действующей на единицу длины контура, ограничивающего поверхность жидкости;
2. работе, которую нужно совершить для создания единицы площади поверхностного слоя в изотермических условиях.
Коэффициент полезного действия теплового двигателя есть отношение работы А, совершенной рабочим телом в рассматриваемом прямом круговом процессе, к количеству теплоты 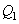 , сообщенной при этом рабочему телу нагревателем
, сообщенной при этом рабочему телу нагревателем 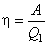 .
.
Краевой угол – угол между смоченной поверхностью твердого тела и касательной к поверхности мениска.
Мениск – искривленная поверхность жидкости внутри капиллярной трубочки или между двумя близко расположенными твердыми стенками.
Нагреватель – тело, сообщающее рассматриваемой термодинамической системе энергию в форме теплоты.
Насыщенный пар – пар, находящийся в термодинамическом равновесии с жидкостью или твердым телом.
Необратимый термодинамический процесс – это процесс, не допускающий возможность возвращения системы в первоначальное состояние без того, чтобы в окружающей среде остались какие-либо изменения.
|
|
|
Несмачивание – поверхностное явление, возникающее при соприкосновении жидкости с твердым телом и проявляющееся в стремлении жидкости сократить поверхность ее соприкосновения с твердым телом, что приводит к появлению на несмачиваемой поверхности твердого тела капель жидкости.
Обратимый термодинамический процесс – это процесс, допускающий возможность возвращения системы в первоначальное состояние без того, чтобы в окружающей среде остались какие-либо изменения.
Обратный цикл – круговой процесс, в котором рабочее тело переносит теплоту от холодного тела к более нагретому. Устройства, предназначенные для этого, называют холодильными машинами или холодильниками.
Относительная влажность воздуха определяется отношением плотности водяного пара при данной температуре к плотности насыщенного пара при той же температуре.
Первый закон термодинамики: изменение внутренней энергии термодинамической системы равно сумме работы, совершаемой над системой внешними телами, и количества теплоты, сообщенного системе 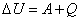 .
.
Первый постулат термодинамики – у изолированной системы существует состояние термодинамического равновесия, в которое она приходит с течением времени и никогда самопроизвольно выйти из него не может.
Перпетуум мобиле (вечный двигатель II рода) – воображаемый двигатель, который бы мог работать, не вступая в теплообмен с телами различной температуры. Одна из формулировок второго закона термодинамики утверждает: вечный двигатель второго рода невозможен.
Плавление – переход твердого кристаллического вещества в жидкое состояние. При постоянном внешнем давлении плавление чистого вещества происходит при постоянной температуре – температуре плавления.
Поверхностно-активные вещества – примеси, адсорбирующиеся на поверхности жидкости и уменьшающие энергию поверхностного слоя.
Принцип эквивалентности теплоты и работы (в формулировке Клаузиуса): во всех случаях, когда из теплоты появляется работа, тратится пропорциональное полученной работе количество тепла, и, наоборот, при затрате той или иной работы получится то же количество тепла.
Процесс– переход системы из одного состояния в другое, сопровождающийся изменением ее термодинамических параметров.
Прямой цикл – круговой процесс, в котором система получает от нагревателя количество теплоты 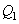 , отдает холодильнику количество теплоты
, отдает холодильнику количество теплоты 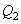 и совершает работу
и совершает работу 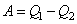 .
.
Работа – один из способов изменения состояния термодинамической системы, обусловленный изменением относительного расположения системы и внешних взаимодействующих с ней тел. Работа определяется количеством энергии, переданным системе в ходе изменения ее состояния, то есть в ходе процесса, поэтому работа есть функция процесса. Работу принято считать положительной, если она совершается системой. Если же работа совершается над системой внешними силами, то работу принято считать отрицательной.
Рабочее тело – термодинамическая система, совершающая круговой процесс в тепловой установке.
Равновесное состояние (состояние термодинамического равновесия) – это такое состояние, в котором не только все параметры системы постоянны во времени, но и нет никаких стационарных потоков за счет действия каких-либо внешних источников.
Смачивание – поверхностное явление, возникающее при соприкосновении жидкости с твердым телом и проявляющееся в растекании жидкости по твердой поверхности.
Статистические закономерности – это закономерности, которым подчиняются массовые явления.
Стационарное состояние системы – это такое ее состояние, при котором все параметры состояния не изменяются со временем.
Температура – статистический параметр состояния термодинамически равновесной системы, характеризующий степень нагретости тела. В условиях термодинамического равновесия температура всех тел, входящих в систему, одинакова. Температура характеризует внутреннее состояние системы и определяется средним значением кинетической энергии входящих в ее состав молекул. Температуру нельзя измерить непосредственно. Значение температуры определяют по изменению какого-либо свойства вещества, которое можно непосредственно измерить (объем, электросопротивление).
Теплоемкость тела С есть отношение количества теплоты Q, сообщенное телу в каком-либо процессе, к соответствующему изменению температуры тела 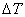 :
: 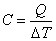 .
.
Теплоемкость есть функция процесса. Различают теплоемкость при постоянном объеме 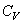 и при постоянном давлении
и при постоянном давлении 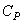 . Теплоемкость единицы массы вещества принято определять как удельную теплоемкость, теплоемкость вещества в количестве одного моля – как молярную теплоемкость.
. Теплоемкость единицы массы вещества принято определять как удельную теплоемкость, теплоемкость вещества в количестве одного моля – как молярную теплоемкость.
Термодинамическая система – совокупность макроскопических объектов (тел и полей), обменивающихся энергией в форме работы и в форме теплоты как друг с другом, так и с внешней средой.
Термодинамическая шкала температур – шкала, установленная на основании теоремы Карно. Температура, отсчитываемая по этой шкале, не зависит от свойств вещества, как это присуще эмпирической температуре. Термодинамическая шкала температур совпадает с идеально-газовой шкалой при равенстве величины градусов. Абсолютная термодинамическая шкала температур называется шкалой Кельвина. За основную единицу температуры по этой шкале берется Кельвин. Кельвин – это 1/273,16 часть термодинамической температуры тройной точки воды.
Точка кипения– температура жидкости, при которой давление ее насыщенного пара равно внешнему давлению.
Точка росы – температура, при которой пар вследствие изохорического охлаждения становится насыщенным. Относительная влажность воздуха при этой температуре равна ста процентам.
Удельная теплота парообразования– теплота, необходимая для испарения единицы массы жидкости, нагретой до температуры кипения.
Упругая деформация – деформация, которая исчезает после прекращения действия вызывающей ее силы.
Фаза – макроскопическая физически однородная часть вещества, отделенная от остальных частей системы границей раздела, так что она может быть извлечена из системы механическим путем.
Фазовый переход – переход вещества из одной фазы в другую. Различают два типа фазовых переходов: фазовые переходы первого рода и фазовые переходы второго рода.
Фазовыми переходами второго рода называются фазовые превращения, происходящие без поглощения или выделения тепла и изменения удельного объема. При фазовых переходах второго рода скачкообразно изменяются теплоемкость, коэффициент объемного расширения и некоторые другие характеристики вещества.
Фазовыми переходами первого рода называются фазовые превращения, сопровождающиеся поглощением или выделением тепла и изменением удельного объема.
Холодильник – тело, получающее от рассматриваемой термодинамической системы энергию в форме теплоты.
Основные формулы
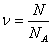
| Количество вещества, 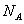 – постоянная Авогадро – постоянная Авогадро
|
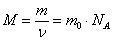
| Молярная масса, 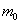 – масса молекулы – масса молекулы
|
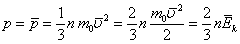
| Основное уравнение МКТ идеального газа |

| Давление идеального газа на стенки сосуда, k – постоянная Больцмана |
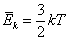
| Средняя кинетическая энергия поступательного движения молекул |
| p = p1 + p2 + p3 + ... = (n1 + n2 + n3 + ...)kT | Закон Дальтона |
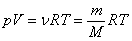
| Уравнение состояния идеального газа, R = kNA – универсальная газовая постоянная |
| pV = const при T = const | Изотермический процесс (закон Бойля–Мариотта) |
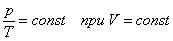
| Изохорный процесс (закон Шарля) |
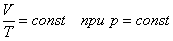
| Изобарный процесс (закон Гей-Люссака) |
| Ep = σS | Потенциальная энергия свободной поверхности жидкости, σ – коэффициент поверхностного натяжения |
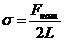
| σ – коэффициент поверхностного натяжения, Fнат. – сила поверхностного натяжения,L- длина линии соприкосновения |
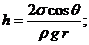
| Высота подъема смачивающей жидкости в капилляре. q - краевой угол, r - плотность жидкости |
| T = (t °C + 273,15) К | Абсолютная температура |
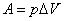 при р = const при р = const
| Работа газа при расширении (сжатии) |
| ΔU = Q – A; Q = ΔU + A | Первый закон термодинамики |
| A = CV(T2 – T1) | Работа газа в адиабатическом процессе |
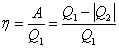
| КПД теплового двигателя |
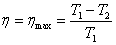
| КПД идеальной тепловой машины, работающей по циклу Карно |
| l = l0 (1 + αΔT); V = V0 (1 + βΔT); β ≈ 3α | Тепловое расширение тел |
Дата добавления: 2018-06-27; просмотров: 487; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
