Резистивные модели гемодинамики при изменении параметров сосудистой системы
Лекция№16 Математические модели кровотока
Математические модели течения крови по жестким и эластичным сосудам
В 1899 г. немецкий физиолог О. Франк теоретически развил идею о том, что артерии “запасают” кровь во время систолы и выталкивают ее в мелкие сосуды во время диастолы.
Поставим цель: рассчитать изменение гемодинамических показателей (например давления) во времени в некоторой точке х крупного сосуда (произвольность выбора точки обусловлена малостью коэффициента затухания пульсовой волны вдоль крупных сосудов).
На рис. 6 схематично показаны экспериментальные данные изменения давления Р в полости левого желудочка и в аорте, а также объемная скорость Qc поступления крови из сердца в аорту. Видно, что Р и Qc нелинейно изменяются во времени.

Рис. 6. Изменение гемодинамических показателей при сокращении сердца: а - давление крови в аорте (штриховая линия) и давление в левом желудочке сердца (сплошная); б - объемная скорость QС поступления крови в аорту во время систолы. Кривые F соответствуют первому сокращению, R - повторение процесса; точки 1 и 1’ соответствуют моментам открытия аортального клапана, точка 3 - его закрытию, точка 2 - момент времени, когда Qc достигает максимального значения
Для удобства рассмотрения вьделим две фазы кровотока в системе “левый желудочек сердца крупные сосуды мелкие сосуды” (рис.6):
1 фаза фаза притока крови в аорту из сердца с момента открытия аортального клапана до его закрытия (рис. 6 , т. 1à2à3).
2 фаза - фаза изгнания крови из крупных сосудов в мелкие после закрытия аортального клапана (рис. 6, т. Зà1’ ).
В модели Франка сделаны следующие допущения.
Все крупные сосуды объединены в один резервуар с эластичными стенками, объем которого пропорционален давлению. Они (а следовательно, и резервуар) обладают
Высокой эластичностью; гидравлическим сопротивлением резервуара пренебрегают.
Система микрососудов представлена как жесткая трубка. Гидравлическое сопротивление жесткой трубки велико; эластичностью мелких сосудов пренебрегают.
Эластичность и сопротивление для каждой группы сосудов постоянны во времени и по пространству.
Не рассматриваются переходные процессы установления движения Крови.
Существует “внешний механизм” закрытия и открытия аортального клапана, определяемый активной деятельностью сердца.
При поступлении крови из сердца часть ее размещается в крупных сосудах, растягивая их, а часть избытка крови протекает в мелкие сосуды. Можно записать уравнение баланса объема крови;
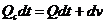 (9)
(9)
где Qc(t) - объемная скорость поступления крови из сердца (рис. 6б), Q(t) - объемная скорость кровотока в начале мелких сосудёв, dv — изменение объема крупных сосудов.
Предполагаем, что изменение объема резервуара линейно зависит от изменения давления в нем dP
 (10)
(10)
где С — эластичность - коэффициент пропорциональности между давлением и объемом,  .
.
Условно считая давление Р0 на выходе из жесткой трубки равным 0 и применяя для течения крови по ней закон Пуазейля, получим, что
 (11)
(11)
где Р(t) давление в крупных сосудах (в том числе на входе в мелкие), W - гидравлическое сопротивление мелких сосудов.
Систему уравнений (9, 10, 11) можно решить относительно Р(t) , Q(t) или v(t). Решим систему относительно Р(t).
Фаза
С учетом 9, 10, 11 получим уравнение
 (12)
(12)
Это неоднородное линейное дифференциальное уравнение, решение которого определяется видом функции Qc(t).
Будем считать Qc равной ее среднему значению Q0 за время между открытием и закрытием аортального клапана. Тогда уравнение (12) запишется:

Считая, что при t=0 давление Р = Рд, получим:

В результате находим закон повышения Р(t) в крупных сосудах с момента открытия и до закрытия аортального клапана:
 (13)
(13)
Считаем, что через время tc срабатывает механизм закрытия аортального клапана, при этом давление крови в крупных сосудах достигнет некоторого значения Рс:
 (14)
(14)
В зависимости (14) аргументом является не текущее время как в(13), а время систолы tc.
Примечание. Зависимость (13) получена в предположени постоянной скорости поступления крови из сердца в течение tc.
Qc=Q0 . Для расширения границ применимости модели необходимо учитывать не только собственные параметры W и С определяющие релаксационные процессы в системе сосуд–кровь, но и конкретный вид временной зависимости внешнего воздействия на систему, а именно Qc(t). Учет зависимости скорости поступления крови из сердца в аорту, представленной на рис. 6б, приведет к несколько другому закону нарасталня давления крови в моменты времени 1à2, когда Qc(t) возрастает до максимального значения, а также позволит найти зависимость падения давления крови в аорте в моменты времени 2à3, когда Qc падает до нуля.
Фаза
Вторая фаза начинается с момента закрытия аортального клапана (т.3 на рис. 6б). Именно этот момент будем считать начальным для 2 фазы. Модель Франка позволяет аналитически найти зависимость падения давления Р(t) в крупном сосуде после закрытия аортального клапана.
Поскольку кровь уже не поступает из сердца, то Qc=0 . Тогда уравнение (9) превращается в:
 (15)
(15)
Знак минус отражает уменьшение объема крупного сосуда с течением времени.
С учетом (10),

С учетом (11) получаем дифференциальное уравнение:
 (16)
(16)
Начальное условие : при t=0 (соответствует закрытию клапана) считаем давление Р=Рс. (В данной модели не учитываем различие давлений в т. 2 и 3, считая давление в т. 3 равным систолическому). В результате получаем закон изменения давления в крупных сосудах с момента закрытия аортального клапана:
 (17)
(17)
На рис. 7 приведена зависимость спада давления в крупных сосудах после закрытия аортального клапана.

Рис 7 Зависимость давления крови от времени в крупном сосуде после закрытия аортального клапана
Через некоторое время (tд) давление упадет до диастолического

После чего открывается клапан, тем самым закичивается фаза 2 и начинается опять фаза 1.
зависимость (17) качественно описывает экспериментальную зависимость Р(t) в аорте, приведенную на рис. 6а в т. 3à1’.
Резистивные модели гемодинамики при изменении параметров сосудистой системы
( в этой модели гидродинамические величины заменятся сопротивлениями и другими электрическими характеристиками)
Модель Франка учитывала гидравлическое сопротивление и эластичность сосудов (в электрическом аналоге емкость конденсатора). В ряде случаев можно упростить модель и не учитывать эластичность сосудов. Используя чисто резистивные модели, рассмотрим изменения гемодинамических показателей системы при:
1) сужении просвета сосуда, предшествующего разветвленному участку, например при образовании в нем тромба;
2) сужении просвета сосуда (образовании тромба) в одном из мелких сосудов разветвленного отдела кровеносной системы;
3) изменении вязкости крови.
Как при этом изменяются гемодинамические параметры вдоль сосудов?
Для математического описания распределения давления и скорости кровотока. в этих случаях необходимо упростить систему. Поэтому введем следующие допущеним:
а) параметры системы не изменяются во времени;
6) эластичность сосудов не учитывается;
в) не учитываются пульсации давления в различные фазы сердечного цикла, речь будет идти о среднем давлении;
г) течение жидкости ламинарное;
Для исследования поведения системы используем электрические чисто резистивные модели, то есть аналоговые модели, учитывающие только стационарные режимы течения и не учитывающие переходные процессы (процессы установления течения). В этом случае течение крови по сосудам будет моделироваться электрическим током в цепи из активных сопротивлений.
Введем электрические величины в резистивной модели для описаия гидродинамических величин кроветока (рис. 8):
Дата добавления: 2018-06-01; просмотров: 1407; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
