Основные законы идеальных газов
Все газы, в том числе природный газ подчиняются определенным законам. Но следует отметить, что эти законы в строгой форме справедливы только для идеальных газов. Реальные же газы имеют отклонение от законов для идеальных газов. Однако эти отклонения заметны только при давлениях более 0,5 МПа. Так как в городском газоснабжении, как правило, используют давления, не превышающие указанных пределов, то без каких-либо погрешностей можно пользоваться законами идеальных газов.
Закон Бойля— Мариоттаопределяет зависимость между давлением и объемом при постоянной температуре:
P0 V0 = P1 V1 = PV
PV - const,
где: Ро, Р1 Р— абсолютные давления;
Vo, V1 , V— объемы газа при давлениях Ро, Р1, Р. Отсюда, если объем Vo газа, имеющего температуру То и абсолютное давление Ро, увеличить при неизменной температуре То до объема V, то абсолютное давление этого газа изменится обратно пропорционально его объему:
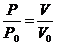
Этот закон, как мы увидим далее, обязательно учитывается при расчете газопроводов среднего, и высокого давления, распределительных газовых сетей, а также при подсчете количества газа, поданного по трубопроводам или находящегося в каких-либо емкостях или газгольдерах.
Закон Гей-Люссакаопределяет зависимость объема газа при постоянном давлении от температуры. Он выражается следующей формулой:
V=V0(1+αt),
где: Vo — объем газа при температуре, равной 0°С;
α — тепловой коэффициент расширения:
|
|
|
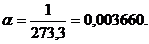
Изменение давления газа при постоянном объеме в зависимости от температуры подчиняется тому же закону:
P=P0(1+αt),
где: Ро — давление газа при 0° С;
α—коэффициент изменения давления, численно равный коэффициенту расширения.
Если в уравнениях V и Р подставить численное значение коэффициента α и вместо t подставить абсолютную температуру Т = t° С + 273, то получим:
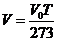
и соответственно
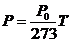
При другой температуре Т1 объем газа V1 также будет другим. Он будет равен:
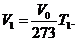
Если разделим V1 на V, то получим следующую зависимость:
 ,
,
т. е. при постоянном давлении объем газа пропорционален абсолютной температуре.
Общее уравнение состояния газов связывает три основные величины, характеризующие состояние газа: давление Р, температуру Т и объем V.
Эта связь представляется в следующем виде:
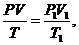 или
или 
Если это уравнение отнести к одному молю, то постоянная величина будет иметь одно и то же значение для всех газов R. уравнение газового состояния примет следующий вид:
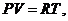
где: Т—абсолютная температура газа;
V—объем моля газа;
R — универсальная газовая постоянная.
|
|
|
При нормальных условиях объемы 1 кг моля различных идеальных газов одинаковы и равны 22,4 нм3/кг моль. Отсюда величина и размерность газовой постоянной зависят от того, в каких величинах выражены давление и объем газа. Если давление газа Р = 10330 кг/м2 и температура Т = 273° К, то
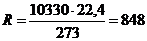 кгм/ град.
кгм/ град.
 Для любого простого газа удельная характеристическая газовая постоянная Ryd равна универсальной газовой постоянной R, деленной на молекулярный вес этого газа М:
Для любого простого газа удельная характеристическая газовая постоянная Ryd равна универсальной газовой постоянной R, деленной на молекулярный вес этого газа М:
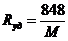 кгм/кг град.
кгм/кг град.
Дата добавления: 2018-06-27; просмотров: 790; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
